医用硅酮疤痕凝胶贴微生物限度检查方法学验证
辽宁省医疗器械检验检测院 (辽宁沈阳 110171)
内容提要: 目的:建立医用硅酮疤痕凝胶贴的微生物限度检查方法。方法:根据《中华人民共和国药典》(2015年版 四部),通过3次独立的平行试验,分别计算各试验菌每次试验的回收率。结果:在对需氧菌总数、霉菌和酵母菌总数方法验证的3次独立平行试验中,供试液对照组的菌回收率均大于70%;在对控制菌检查方法验证的3次独立平行试验中,阴性对照组无菌生长,实验组检出阳性试验菌。结论:通过方法学验证说明建立的微生物限度检查方法适用于医用硅酮疤痕凝胶贴的微生物限度检查,保证微生物限度检查方法的有效性。
医用硅酮凝胶具有改善疤痕表皮结构的作用,减轻毛细血管充血和胶原纤维增生,改善疤痕组织代谢和营养供给,从而防止增生性疤痕的形成。近年,在美容医疗产品中的应用越来越多,如医用硅酮疤痕凝胶贴、硅酮凝胶膏、硅酮凝胶喷雾剂等[1]。目前,对于硅酮疤痕凝胶贴的微生物限度检查法鲜有报道,本文结合2015年版《中华人民共和国药典》,建立了医用硅酮疤痕凝胶贴微生物限度检查的方法。
1.材料与方法
1.1 一般材料
仪器:集菌仪(HTY-2000A)(杭州高得医疗器械有限公司);薄膜过滤器(杭州泰林生物技术设备有限公司);多用生化培养箱(SP-530)(沈阳市伟明医疗设备厂);生物安全柜(HFsafe-1200)(上海力申科学仪器有限公司);全自动立式灭菌锅(LMQ.C-80C)(山东新华医疗器械股份有限公司);电子天平(XP2003S DR)(梅特勒-托利多仪器有限公司)。
供试品:医用硅酮疤痕凝胶贴,规格:8cm×6cm,批号:20180401,由企业提供。
实验菌种:铜绿假单胞菌[CMCC(B)10104]、金黄色葡萄球菌[CMCC(B)26003]、枯草芽孢杆菌[CMCC(B)63501]、白色念珠菌[CMCC(F)98001]、黑曲霉[CMCC(F)98003]均来自中国药品生物制品检定研究院医学菌种保藏中心。
培养基及试剂:甘露醇氯化钠琼脂培养基、沙氏葡萄糖琼脂(SDA)、胰酪大豆胨琼脂(TSA)、胰酪大豆胨肉汤(TSB)、溴化十六烷基三甲铵琼脂、吐温80(国药集团化学试剂有限公司);生理盐水(沈阳志鹰药业有限公司)。
1.2 方法
1.2.1 供试液制备
取供试品10g,放入90m生理盐水(含0.05%吐温80)中,振荡30min,作为1:10的供试液备用。
1.2.2 菌液制备[2]
分别挑取金黄色葡萄球菌、枯草芽孢杆菌、铜绿假单胞菌、白色念珠菌适量,用生理盐水稀释至0~100cfu/mL的菌悬液。取黑曲霉适量,加含0.05%吐温80的生理盐水5mL,洗下黑曲霉孢子作为原液,用含0.05%吐温80的生理盐水稀释至含菌数0~100cfu/mL的菌悬液。
1.2.3 采用薄膜过滤法进行验证试验
1.2.3.1 微生物限度计数适用性试验
需实验组操作:①氧菌总数:分别取供试液10mL,加到100m生理盐水中,薄膜过滤,用生理盐水300mL分次冲洗,100mL/次,在最后一次冲洗液中分别加入1mL(<100cfu)金黄色葡萄球菌、铜绿假单胞菌、枯草芽孢杆菌、白色念珠菌、黑曲霉菌。取出滤膜,菌面朝上贴于TSA上,33°C培养3d观察结果。②霉菌和酵母菌总数:分别取供试液10mL,加到100m生理盐水中,薄膜过滤,用生理盐水300mL分次冲洗,100mL/次,在最后一次冲洗液中分别加入1mL(<100cfu)白色念珠菌、黑曲霉菌。取出滤膜,菌面朝上贴于TSA上,23°C培养5d观察结果。
菌液组:以稀释液替代供试液,按试验组操作加入<100cfu/mL的菌液1mL,方法同试验组。
供试液对照组:取制备好的供试液,以稀释液代替菌液同试验组操作。
阴性对照组:取稀释液10mL,按试验组操作,进行相应培养及计数。
微生物的回收率:回收率=(试验组平均菌落数-供试液对照组平均菌落数)/菌液组菌落数×100%。
1.2.3.2 控制菌检查方法适用性试验
根据产品技术要求,对金黄色葡萄球菌和铜绿假单胞菌进行控制菌检查方法适用性试验。
金黄色葡萄球菌检查:取供试液10mL,加到100m生理盐水中,薄膜过滤,用生理盐水300mL分次冲洗,100mL/次,取滤膜加入至100mLTSB培养基中,向其中加入<100cfu的金黄色葡萄球菌,33°C培养24h。取上述培养物接种于甘露醇氯化钠琼脂培养基上,33°C培养24h。
铜绿假单胞菌检查:取滤膜加入至100mLTSB培养基中,向其中加入<100cfu的铜绿假单胞菌,33°C培养24h。取上述培养物接种于溴化十六烷基三甲铵琼脂培养基上,33°C培养24h。
阳性对照组:取相应菌液各1mL(<100cfu),分别接种于100mL相应的培养基中,培养及检查方法同试验组。
阴性对照组:取稀释液10mL,分别接种于100mL相应的培养基中,培养及检查方法同试验组。
供试液组:取制备好的供试液,不加菌液,同试验组操作。
所有验证均进行3次独立的平行试验。
2.结果
菌落计数及回收率测定三次独立的平行试验结果见表1。
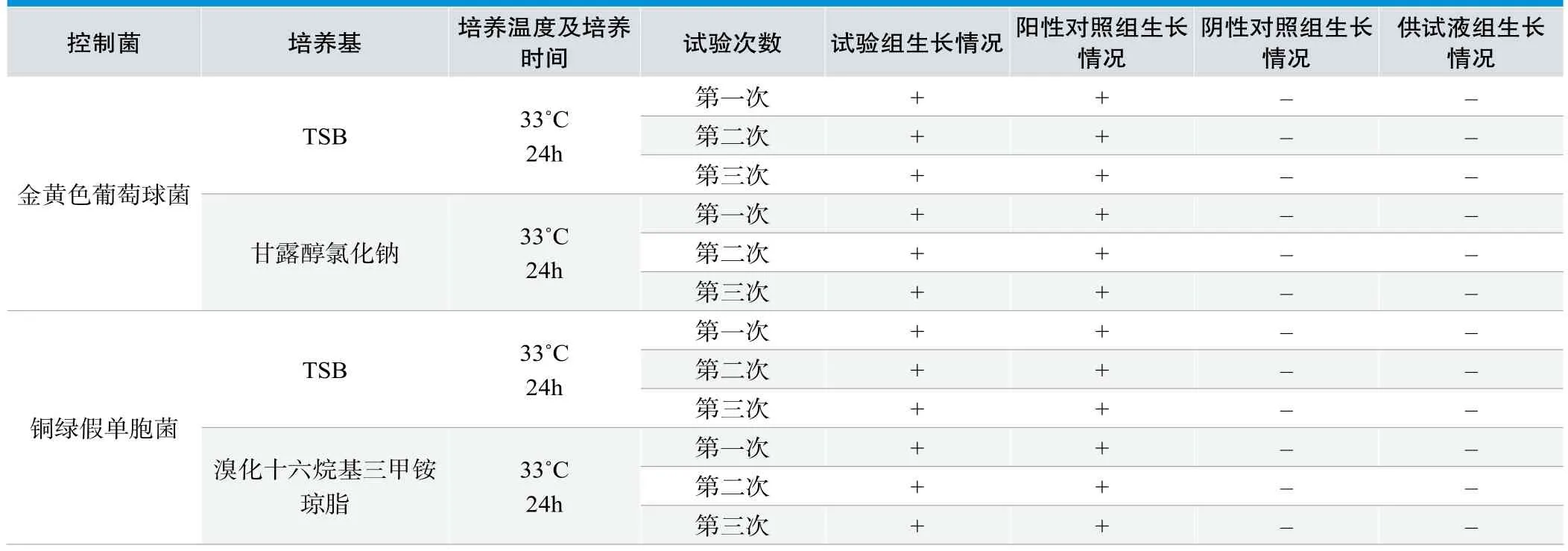
表2. 控制菌检查验证三次试验结果
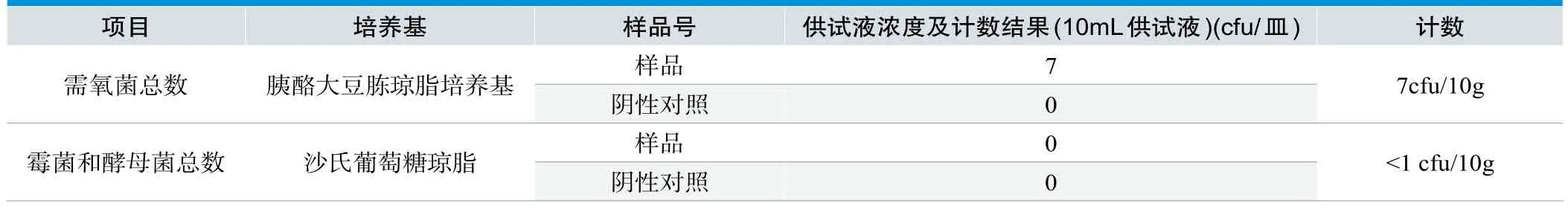
表3. 样品菌落计数结果
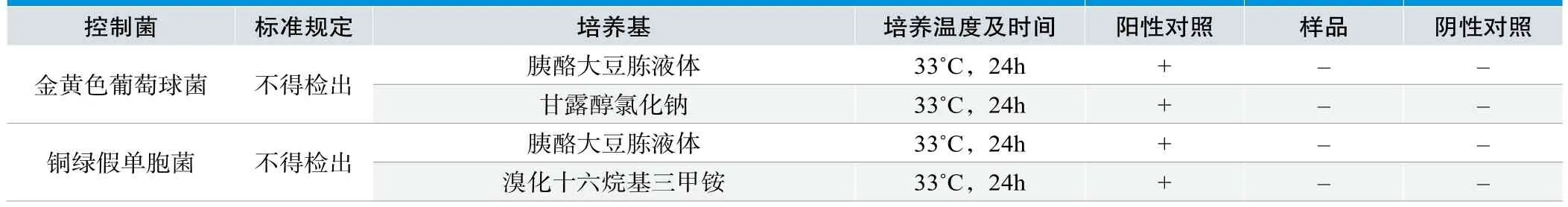
表4. 样品控制菌检查结果
控制菌检查验证三次独立的平行试验结果见表2。
样品菌落计数、控制菌检查结果见表3、表4。
3.讨论
对需氧菌总数、霉菌和酵母菌总数方法验证的3次独立平行试验中,供试液对照组的菌回收率均大于70%;在对控制菌检查方法验证的3次独立平行试验中,阴性对照组无菌检出,实验组检出阳性试验菌,故可根据此方法测定医用硅酮疤痕凝胶贴的需氧菌总数、霉菌和酵母菌总数和控制菌检查。
伴随中国药典2015版的发布,对于微生物的检验要求有了进一步的提高,我国食品、药品、医疗器械的微生物检验、管理控制体系与国际标准进一步接轨,微生物限度检查的方法学建立是非常必要的。

