医疗器械不良事件监测上报情况分析与思考
雷硕 林锦穗
1 福建医科大学附属第一医院医用材料与设备服务中心 (福建 福州 350005)
2 福建医科大学附属第一医院手术室 (福建 福州 350005)
内容提要: 目的:提高医院医疗器械不良事件上报质量,提升临床医护人员发现医疗器械不良事件的能力。方法:结合福建省与本院2017年和2018年医疗器械不良事件统计数据分析对比,做出针对性的改进方案。结果:本院来源于医务人员的医疗器械不良事件上报数量已经超过了临床工程师所上报的数量,医务人员对医疗器械不良事件监测工作的了解更加透彻。结论:医院作为医疗器械不良事件监测的重要环节,需要重视医疗器械不良事件监测上报政策的贯彻落实。
福建医科大学附属第一医院(以下简称本院)是一所具有50多年办学历史的教学医院,同时也是福建省医疗器械不良事件监测工作的哨点医院。医疗器械不良事件监测上报工作是本院医用材料与设备服务中心(以下简称中心)一项工作制度并一直作为工作中的重点。中心有二名高级工程师、一名工程师入选福州市药械化不良反应/事件监测评价专家委员会成员名单。本文对福建省和本院2017年和2018年医疗器械不良事件上报数据进行分类分析,从医疗器械不良事件监测工作存在的问题与对策方面进行思考。
1.本院医疗器械不良事件监测上报情况与分析
1.1 总体数据
根据2017年和2018年福建省三级医院上报医疗器械不良事件统计数据,本院报告数量分别为106例排名第4、110例排名第5;严重伤害事件报告数分别为92例,105例;医疗器械不良事件器械种类数分别为56种和55种;严重伤害报告数构成比均为最高,严重伤害报告数量均排名全省第1,为排查医疗器械临床使用安全风险提供了有利的信息[1,2]。
1.2 按管理类别统计
按照管理类别分析(见表1):2017年度、2018年度,本院与福建省统计数据差距不大,本院Ⅲ类不良事件比重略高,符合本院上报医疗器械不良事件器械种类数较多的实际情况;本院所有出入库的医疗器械均经过严格的准入审核,医疗器械不良事件均经过现场核实,不存在不详类别的医疗器械不良事件。
1.3 按事件后果统计
按事件后果分析(见表2):2017年度、2018年度,本院医疗器械不良事件严重伤害报告数占总报告数比显著高于同期省内平均水平。本院所上报的医疗器械不良事件质量高,种类多,数量多,不拘泥于常见重复性的案例。所有汇总至中心的医疗器械不良事件,均经过中心专家团队严格筛查,剔除重复,无价值的案例,上报的案例均力求真实、准确、高价值,能够充分反馈医疗器械不良事件的客观性。
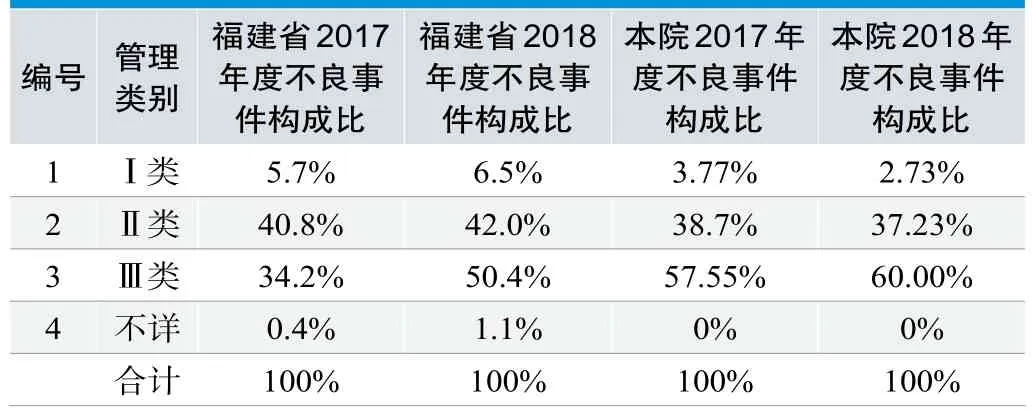
表1.2017年度、2018年度福建省与本院医疗器械不良事件按管理类别统计表
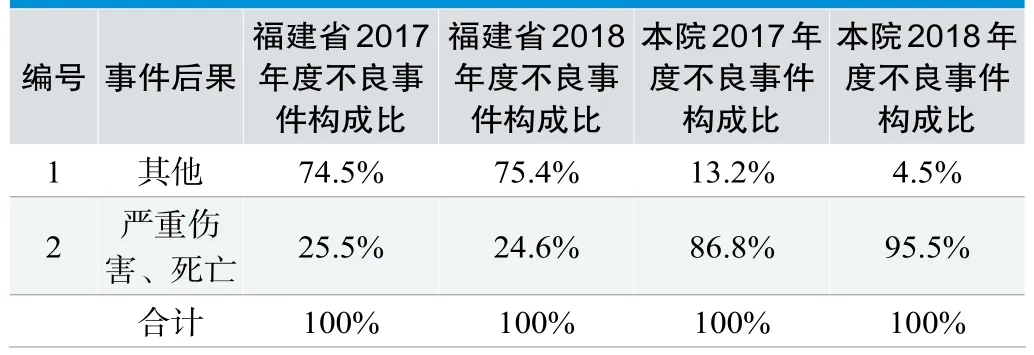
表2.2017年度、2018年度福建省与本院医疗器械不良事件按事件后果统计表
1.4 按报告人类别统计
按报告人类别分析(见表3):2017年度、2018年度,本院与福建省各项统计数据差距较大,报告人分布不均匀,本院医疗器械不良事件主要由临床工程师收集。
本中心由一名从事医疗设备维护和管理实践多年,经验丰富的工程师总负责医疗器械不良事件监测上报工作,各临床工程师长期工作于临床工程一线,熟练掌握各种医疗器械使用流程、工作原理,可以对医疗器械不良事件尤其是可疑医疗器械不良事件的发生情况做科学与客观性的分析预判[3]。临床工程师队伍规模大,为医疗器械不良事件监测工作的开展奠定了坚实的人员基础,临床工程师技术力量强,往往能敏锐地在医疗器械不良事件监测和再评价过程中发现优秀案例,明确描述事件发生过程,从而使得医疗器械在使用过程中能够最大限度降低风险[4]。
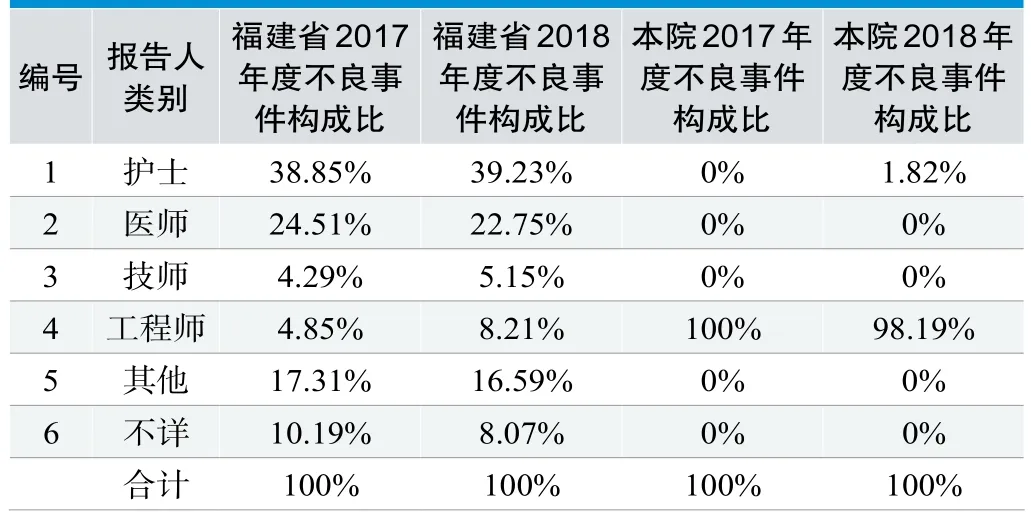
表3.2017年度、2018年度福建省与本院医疗器械不良事件按报告人类别统计表
2.存在的问题
2.1 临床科室不支持
2.1.1 缺乏培训
目前各级食品药品监督管理局举办的医疗器械不良事件培训班的培训对象是各级医院的设备管理部门,而仅仅依靠设备管理部门无法做到对医院临床医护人员的有效培训,培训效果未能主动在院内延伸到更大的范围。根据相关调查,临床医护人员反馈最多的问题是难以判断医疗器械故障是否属于医疗器械不良事件[5]。
2.1.2 担心追责
因为没有接受培训或者培训效果不好,大部分临床医护人员没有意识到医疗器械不良事件监测上报的重要性,担心上报医疗器械不良事件会给自身带来影响,引起患者投诉引发追责等不必要的麻烦。
2.2 报告人类别来源单一
本院医疗器械不良事件主要由临床工程师巡检、维修、保养过程中发现,临床科室不支持医疗器械不良事件监测工作加剧了本院医疗器械不良事件上报人类别来源较为单一的现实情况。
2.3 监管部门不够专业化
医疗器械不良事件上报后,食品药品监督管理局市场监管监测服务中心审核人员缺乏医疗器械不良事件监测的实践经验,大部分审核人员没有看到过医疗器械不良事件现场资料,部分上报的优质案例被盲目退回。尤其值得关注的是各级监管部门对医疗器械不良事件的培训重视程度不够,缺乏对医疗机构培训需求前期调查,形式单一,内容宽泛,缺乏系统性、直观性、可操作性[6]。
3.对策
3.1 培训与宣教
参加培训。积极组织临床工程师参加各级各类医疗器械不良事件培训班,同时要求参会临床工程师在中心例会上传达培训班学习内容,将培训班的课件分享至医院公共平台以供随时参阅学习。
交流互动。不定期邀请省市两级授课人员到中心授课,要求一线临床工程师都能准确掌握医疗器械不良事件基本概念,了解典型案例,熟悉收集上报流程,做到积极收集现场资料。与兄弟医院加强交流,互相分享案例,了解更多类型的医疗器械不良事件。
主动作为。中心主动与护理部,医务部联系,坚持开展院内一线科室医疗器械不良事件收集上报培训课,由中心专家与一线的医护人员直接沟通,解答疑问,解除顾虑。提高医疗器械不良事件监测人员队伍尤其是急诊科、手术室等重点科室监测人员对医疗器械不良事件的认识水平。
特色宣教。展开富有本院特色的宣教模式,针对常规培训效率低,培训内容针对性不强,概念过多难以消化的现状,中心以一线临床工程师多年积累的丰富翔实的图片、视频素材为主题,通过强烈的视觉听觉冲击,将医疗器械不良事件的内涵意义直观地传递给培训人员,培养临床医护人员发现判断和上报医疗器械不良事件的能力。
3.2 医院制度改进与激励
改进流程。本院建立了建立包括医疗器械不良事件在内的全院性医疗不良事件平台,患者情况、上报时间等客观事务性信息可以同步导入,尽量为上报人员提供便利,减少上报工作量。
制度保障。医院层面建立《医疗器械不良事件监测员制度》《医疗器械不良事件报告制度》《医疗器械不良事件上报表》《可疑医疗器械不良事件上报流程》,从制度上对临床科室医疗器械不良事件进行统一规范[7]。
3.3 主管部门引导
加强互动。各级行政主管部门应加强与医疗机构尤其是三级医院设备管理部门的联系,指导医疗器械不良事件监测工作开展,及时掌握监测动态,了解医疗机构医疗器械不良事件监测过程中存在的问题和需求,制定出相对应的管理计划并以此改进培训方案和内容,学习并了解临床工作人员尤其是临床工程师在事件分析上的专业判断,促进审核人员积累经验。
改进上报系统。积极向国家食品药品监督管理总局反馈医疗机构医疗器械不良事件上报过程中存在的困难,改进医疗器械不良事件上报系统,修改不切合实际情况的选项和要求,减少上报工作量。
4.效果
通过对策的实施,2019年度本院医务人员上报医疗器械不良事件的数量大幅增长,质量稳步提升。临床医务人员能够积极主动上报医疗器械不良事件,数量已经超过了临床工程师所上报数量,医务人员对医疗器械不良事件监测工作的了解更加透彻,医疗器械的使用风险得到了较好地控制。同时通过医疗器械不良事件监测工作,临床工程师能够进一步提升自身的知识水平,优化知识结构,不断发现并创新医疗器械维护和保养方法,通过分析医疗器械不良事件的发生原因,突破惯性思维,发现乃至改进维修思路,节约了大量的维修经费。
5.小结
本院医疗器械不良事件监测与上报工作有上报数量多质量高的特色,也存在着上报者较为单一的不足。重视医疗器械不良事件监测上报工作可以提升临床工程师分析解决问题的能力,提高设备部门医疗器械维护水平进而节约更多的维修经费。医疗器械不良事件上报制度赋予了使用单位更多的话语权,有利于促进医院的建设和发展,应予以高度的重视。

