抗VEGF联合复合式小梁切除术治疗新生血管性青光眼
孙曹毓,刘 驰,周 晶,王 辉
0引言
新生血管性青光眼(neovascular glaucoma,NVG)主要是由于视网膜发生缺血、缺氧损伤,刺激新生血管生成,累及前房角,造成眼压升高,从而导致严重的视神经、视功能损伤的一类疾病,常继发于糖尿病性视网膜病变、视网膜静脉阻塞、反复发生的视网膜脱离、炎症、外伤等,属于难治性青光眼,是临床治疗中极其棘手的疾病[1]。新生血管性青光眼主要的临床表现有急剧视力下降,剧烈眼痛、畏光,可伴头痛、恶心、呕吐,眼压可高达60mmHg以上,眼部查体表现为混合充血,常伴角膜雾状水肿,虹膜新生血管,部分可见瞳孔缘色素外翻,房角镜检查前房角可见不同程度的周边前粘连。目前,NVG的主要治疗方法有药物、手术两种,其中药物治疗主要采用β肾上腺素受体阻滞剂、α肾上腺素受体激动剂和碳酸酐酶抑制剂。手术方法有小梁切除术、引流阀植入术、睫状体光凝术等。关于NVG的治疗尚无最佳方案,根据既往临床观察发现,单一治疗方法治疗NVG,术后效果欠佳,易复发,存在较多并发症。因此,需要寻求一种可行、安全、有效、低痛苦的治疗方法,可以在长期有效控制眼压的基础上,尽可能挽救或保留患者视功能。
1对象和方法
1.1对象选取2017-01/2019-06于沈阳市第四人民医院眼科青光眼组就诊并收入院治疗的新生血管性青光眼患者为研究对象。入组标准:(1)受试者均知情同意,能够定期复查;(2)年龄30~70岁;(3)存在光感及以上视力;(4)联合应用三种局部降压药物眼压仍控制不良(IOP>28mmHg),或联合全身用药眼压控制不良(IOP>21mmHg);(5)屈光间质尚清,可窥及眼底。排除标准:(1)妊娠或哺乳期妇女;(2)伴有严重肝、肾、心血管疾病或凝血功能异常患者,血糖控制不稳定的糖尿病患者(空腹血糖连续测量3d以上>8.3mmol/L);(3)既往曾行抗青光眼手术的患者;(4)结、角膜急性炎症,虹膜角膜内皮综合征,严重玻璃体积血,视网膜脱离等合并其他眼病患者。依据上述标准选择后,共入组42例43眼,其中男25例26眼,女17例17眼。年龄36~68(平均51.72±10.75)岁。本研究已得到医院伦理委员会的批准。
1.2方法入院后予全身及局部联合降眼压治疗。术前均进行血常规、尿常规、心电图、视力、屈光状态、眼压、眼前节照相、房角镜、眼底(根据屈光间质状态完善)等检查。经检查入组后均给予常规治疗,包括左氧氟沙星滴眼液滴术眼,每日4次,每次1滴;根据术前眼压情况行局部或(和)全身降眼压对症治疗;术前清除睫毛根部油性分泌物、皮碎等,聚维酮碘及生理盐水冲洗结膜囊。
入院第3d患者术眼行抗VEGF治疗,根据患者自主选择予玻璃体腔注射雷珠单抗或康柏西普0.05mL,分为雷珠单抗组和康柏西普组;注药72h后行复合式小梁切除术,做以角膜缘为基底的巩膜瓣,术中局部应用氟尿嘧啶浸润,根据患者年龄、结膜厚度及巩膜瓣厚度放置2~5min,术中应用TVG房角镜头,镜下分离粘连关闭的前房角,巩膜瓣两角做固定缝线,两侧依据滤过情况酌情应用可调节缝线缝合。术后常规给予抗生素及类固醇激素滴眼液(左氧氟沙星滴眼液、醋酸泼尼松龙滴眼液),每天4次,共3wk。术后1~14d内根据前房深度、滤过泡弥散情况酌情拆除可调节缝线。之后随访期间根据眼压及滤过泡情况酌情应用激光切断固定缝线并教授患者每日2~3次行眼球按摩维护滤过泡畅通。根据屈光间质、荧光造影检查结果,对眼底进行相应的视网膜激光光凝治疗。术后随访6mo,观察时间节点设为术后1d,1、2wk,1、2、3、6mo,统计每个时间点视力、眼压数据。
疗效评定标准:根据虹膜新生血管消退情况、眼压、视力变化,制定疗效评定标准。虹膜新生血管消退程度:术前检查并记录虹膜新生血管分布情况,(1)显效:瞳孔缘新生血管消退;(2)有效:赤道部新生血管消退;(3)无效:血管消退范围达不到以上标准。眼压:(1)显效:眼压下降幅度≥30%;(2)有效:眼压10~21mmHg;(3)无效:达不到以上标准或眼压>21mmHg。视力:(1)显效:视力提高标准对数视力表2行及以上;(2)有效:视力提高标准对数视力表1行;(3)无效:达不到以上标准或视力下降者。有效率=(显效眼数+有效眼数)/总眼数×100%。
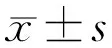
2结果
2.1分组情况及一般资料比较根据患者自主选择予玻璃体腔注射雷珠单抗或康柏西普后分组,其中雷珠单抗组18例18眼,康柏西普组24例25眼。两组性别与年龄差异均无统计学意义(χ2=0.312,P=0.576;t=0.906,P=0.370)。
2.2新生血管消退情况术后24h起,两组患者术眼虹膜表面新生血管开始逐渐减少。48h~7d,雷珠单抗组15眼及康柏西普组23眼术眼赤道部及瞳孔缘新生血管均消退,另外雷珠单抗组3眼及康柏西普组2眼赤道部新生血管消退,瞳孔缘部分粗大新生血管未消退(图1、2)。两组有效率均达到100%。

图1 术前虹膜表面及瞳孔缘可见新生血管。

图2 抗VEGF术后第7d虹膜表面及瞳孔缘新生血管已消退。
2.3眼压控制情况入院时测量眼压,抗VEGF治疗(玻璃体腔注药)后72h行复合式小梁切除术,小梁切除术后各观察时间点测量眼压,所得平均眼压见表1。多个时间点康柏西普组眼压数值略低于雷珠单抗组,但两组间差异无统计学意义(F组间=0.260,P组间=0.612)。两组时间和组别的交互效应无统计学意义(F组间×时间=0.997,P组间×时间=0.443)。在各时间点监测到的眼压值,差异有统计学意义(F时间=202.684,P时间<0.001)。术后1d,1、2wk,1、2、3、6mo眼压与术前眼压比较均显著降低,差异有统计学意义(均P<0.001)。术后第1d眼压显著降低,与其他时间点比较,差异有统计学意义(均P<0.001)。之后有回升趋势,术后第1wk眼压与之后时间点相比,差异有统计学意义(均P<0.001)。术后第2wk至术后第6mo,眼压趋于平稳,差异无统计学意义(均P>0.05)。42例43眼中,眼压均得到良好控制,其中显效12眼,有效27眼,有效率91%。

表1 入院时及术后1d,1、2wk,1、2、3、6mo两组测量所得眼压
2.4视力改善情况本研究中患者入院时测量视力,其中21眼视力为光感至指数/50cm,不足标准对数视力表可测得的最低视力0.02,无法以计量资料统计,故针对视力这一观察指标设定新的行数计量标准:光感=0行,眼前手动=0.5行,指数/10cm=1行,指数/30cm=1.5行,指数/50cm=2行,0.02=3行,0.04=4行,0.06=5行,0.08=6行,0.1=7行,之后按标准对数视力表行数计算,每增加1行均+1。应用标准对数视力表测量入院时视力,并按新设定行数记录。抗VEGF治疗(玻璃体腔注药)后行复合式小梁切除术,术后各节点测量视力,比较视力变化情况。两组间视力变化差异无统计学意义(F组间=0.089,P组间=0.879);两组时间和组别的交互效应无统计学意义(F组间×时间=0.367,P组间×时间=0.916);术后6mo视力略优于入院时,但在各时间点监测到的视力差别无统计学意义(F时间=2.039和,P时间=0.078),见表2。42例43眼中,共12眼视力不同程度提高,其中显效3眼,有效9眼,有效率28%。
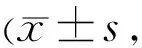
表2 入院时及小梁切除术后1d,1、2wk,1、2、3、6mo测量两组所得视力(按研究设定新的行数标准记录) 行)
3讨论
新生血管性青光眼为众多眼底疾病的终末期表现,其病因多种多样,97%来源于缺血性视网膜病变,其中视网膜静脉阻塞(36.1%)、糖尿病视网膜病变(32.2%)、颈动脉阻塞性疾病引起的眼部缺血(12.9%)较为常见,3%来源于其他原因,可见于放射性视网膜病变、眼部肿瘤(脉络膜血管瘤、脉络膜黑色素瘤、视网膜母细胞瘤、转移性恶性淋巴瘤等)、葡萄膜炎(Crohn病、Behcet病等)和其他情况(Coats病、Eales病、眼外伤、眼部手术等),本病预后极差[2]。
关于新生血管性青光眼发病机制的研究颇多,目前认为眼部新生血管的形成主要是由于促血管生长因子与抗血管生成因子的表达发生失衡,其中血管内皮生长因子(vascular endothelial growth factor,VEGF)上调起重要作用[3]。VEGF是Ferrara等[4]于1989首次提出的概念,主要作用是促进血管内皮细胞有丝分裂,在人体组织内表达具有明显的靶细胞选择性,在晶状体上皮细胞和角膜内皮细胞等组织几乎无表达。周浩川等[5]的研究发现,正常眼中的玻璃体中含有VEGF,其含量为0.18~0.60ng/mL,平均约为0.35ng/mL。Pe’er等[6-7]曾对23例因NVG失明后而摘除的眼球进行了分析,结果显示NVG眼内VEGF表达主要集中于视网膜神经节细胞层、内核层及外核层。视网膜缺血、缺氧可引起眼内VEGF水平上调,促进新生血管形成,分布于虹膜表面及房角[8]。万新顺等[9]的研究证实NVG患者房水、玻璃体中VEGF浓度显著增高,可达正常值的7.5~8倍。谭蔚[10]的研究也得到相似结论,NVG患者血清中的VEGF浓度是白内障组的2.9倍,房水中的VEGF浓度是白内障组6倍。国内外近年来的研究表明,抗VEGF已经成为辅助NVG治疗的首选方法[11]。
新生血管形成的早期,房角可见细小新生血管,此时尚未影响小梁的滤过功能,患者眼压不高,属于青光眼前期:随着缺血缺氧的加重、病程延长,新生血管长入小梁网,影响小梁滤过功能,患者眼压升高,虽房角可见大量新生血管,但此时患者房角仍大部分开放,即为开角型青光眼期,此时用药控制眼压,积极治疗原发病,有机会控制新生血管的形成及疾病进展;当虹膜及小梁表面新生血管的纤维血管膜收缩时,使得周边虹膜逐渐发生前粘连,房水流出通道被破坏,进入闭角型青光眼期,顽固性眼压升高,患者视力急剧下降,疼痛明显[12]。此时单纯药物治疗效果甚微,治疗方案的选择当综合考虑患者的个体差异、自身综合条件及治疗诉求,若患者仍有视力或有挽救视功能的需求,首选行抗VEGF联合复合式小梁切除术。
经本临床研究结果证实,玻璃体腔注射抗VEGF药后虹膜表面新生血管明显消退,我国现广泛应用于临床的抗VEGF药物(康柏西普眼内注射液及雷珠单抗眼内注射液)均可有效消退患者虹膜及前房角的新生血管,减少术中出血及术后前房积血的发生。待新生血管消退后行小梁切除术,术中分离已经粘连的房角,有助于恢复部分房角功能。本研究还发现,复合式小梁切除术后第1d眼压显著下降,此时可调节缝线可有效预防手术早期浅前房的发生;术后第1~2wk,即瘢痕愈合期,眼压开始逐渐回升,术中联合的抗代谢药物,逐渐拆除可调节缝线,有助于维持滤过泡功能,之后随访期间根据眼压及滤过泡情况酌情应用激光切断固定缝线并教授患者每日2~3次行眼球按摩维护滤过泡畅通,术后第2wk~第6mo眼压趋势平稳。本研究中,抗VEGF治疗联合复合式小梁切除术,术中分离房角,滤过泡局限时联合激光断线,教授患者学会有效的眼球按摩以维持功能滤过泡,综合运用多种手段,有效减轻瘢痕化导致的滤过道阻塞,防止复发,维持远期滤过泡的功能。随访至术后6mo对眼压控制的有效率可达91%,眼压的有效控制为积极治疗原发性疾病提供有力条件。
新生血管性青光眼大多继发于缺血性眼底病,陈荣[13]的研究发现,DR患者行全视网膜光凝(panretinal photocoagulation,PRP)后房水VEGF含量显著降低,因此,屈光间质状态及患者自身条件允许时,还应行PRP或联合玻璃体切割术,积极治疗原发病,改善眼底缺血、缺氧状态,从根本抑制新生血管形成。
本研究中,42例43眼中1眼术后第1d时发生I°浅前房(发生率2%),属滤过过强,经加压包扎3d后好转,未见脉络膜脱离及滤过泡漏;2眼术中前房穿刺眼压降低时前房出血(发生率5%),冲洗前房,无活动性出血后结束手术,术后观察均未见形成3mm以上液平的前房积血及玻璃体内活动性出血,并发症发生率7%,低于类似研究中约10%~20%的并发症发生率[14-16]。随访至术后6mo时,4眼滤过泡局限(9%),眼压升高,联合药物控制,此前眼压升高的病程均达到3mo以上,且未规律用药,血糖控制不稳,未系统监测眼压变化及坚持按摩。视力提高的12眼,均发病即来院就诊,且具有较好依从性,药物控制不良时及时手术治疗。因此,“早发现、早治疗”的原则在NVG的治疗中十分重要,患者发病时及时就医,并在治疗中具有良好的依从性,术后的密切随访,这些都可为视功能的恢复及远期效果提供保障。
目前NVG的治疗多种多样,因其预后极差的视力,仍为眼科的棘手疾病,究其根本是要以保留视功能为核心、以完成PRP为目标、以抗VEGF治疗和抗青光眼手术为关键手段,达到最大限度地挽救患者视功能的宗旨[17]。关于NVG这一难治性青光眼的攻克,尚需多中心、大样本、随机对照、长期随访的临床试验,为NVG患者寻求解除痛苦且可提高视功能的治疗方法。

