壳聚糖交联β-环糊精聚合物对Cu2+的吸附研究
梁远远, 厉捷, 陈静怡, 李银涛, 肖厚荣
(1.合肥学院 生物食品与环境学院, 合肥 230601; 2.威立雅(中国)环境服务有限公司, 上海 200041)
随着现代工业的发展, 水中重金属污染的现象也越来越严重, 有效治理重金属水体污染显得十分必要和紧迫[1-2]。 目前, 水体中重金属污染的处理方法一般包括化学沉淀法、 吸附法、 离子交换法、氧化还原法和生物法等[3]。 然而, 这些方法存在一定的缺点, 如成本较高、 去除效果不理想和可能会对环境产生二次污染等[4]。 吸附法的原理是利用吸附剂多孔结构且具有较大表面积的物理性质来吸附水中的污染物, 以达到去除水体中重金属的目的,目前经常使用的吸附剂有活性炭、 沸石等[5]。
壳聚糖是甲壳素的N-脱乙酰形式, 具有氨基和甲壳素结构, 可生物降解, 是一种环境友好型吸附材料。 壳聚糖具有氨基和羟基等活性基团, 易与金属离子形成络合物, 因此被广泛应用于水体中重金属的吸附[6-8]。 β-环糊精是环糊精葡萄糖基转移酶作用于淀粉的产物, 含有空腔结构可以包埋尺寸合适的化合物[9-10]。 利用交联剂将壳聚糖与β-环糊精交联, 得到的产物可以用于水处理, 一方面是利用壳聚糖分子上面的氨基依靠静电引力吸附金属离子, 交联剂柠檬酸中的剩余的羧基也可以螯合金属离子; 另一方面, β-环糊精的空腔结构的阻力易包埋金属离子。 因此, 将壳聚糖与β-环糊精交联形成的聚合物可以增强对金属离子吸附能力[11-12]。 本研究以壳聚糖和β-环糊精为原料, 以柠檬酸为交联剂, 采用溶液聚合法[13]合成壳聚糖/β-环糊精聚合物, 并探讨不同试验条件对Cu2+吸附效果的影响。
1 材料与方法
1.1 试剂与仪器
试剂: 壳聚糖(脱乙酰度≥90%), β-环糊精,十二烷基硫酸钠(SDS), 冰乙酸, 氢氧化钠, 二水合氯化铜, 柠檬酸, 甲醇, 三羟甲基氨基甲烷, 磷酸二氢钠, 二甲基亚砜, 无水乙醇。 以上均为分析纯。
仪器: pH 3C 酸度计, 集热式恒温加热磁力搅拌器, 真空干燥箱, 傅里叶红外光谱仪, 水浴恒温振荡器, 压片机, FAZ104 型电子天平, 扫描电子仪, 紫外可见分光光度计。
1.2 壳聚糖与壳聚糖/β-环糊精聚合物的制备
将2 g 的壳聚糖放进1%的冰乙酸溶液中, 充分搅拌至完全溶解, 然后将其缓慢地滴入1% 的十二烷基硫酸钠(SDS)溶液中, 磁力搅拌4 h, 采用氢氧化钠调节溶液pH 值至中性, 蒸馏水冲洗干燥后得到氨基被保护的SDS-壳聚糖。
将1 g SDS-壳聚糖溶于二甲基亚砜溶液中, 3 g β-环糊精溶于蒸馏水中, 在搅拌作用下, 将β-环糊精溶液溶于SDS-壳聚糖溶液中, 搅拌一定时间, 加入柠檬酸和磷酸二氢钠搅拌反应一定时间, 反应液用三羟甲基氨基甲烷/甲醇溶液沉淀, 脱去SDS 保护, 最后依次通过蒸馏水、 无水乙醇洗涤沉淀, 真空干燥, 粉碎得到壳聚糖/β-环糊精聚合物。
1.3 壳聚糖/β-环糊精聚合物吸附性能的测定
配制200 mL 的氯化铜溶液于烧杯中, 分别加入一定量的壳聚糖/β-环糊精聚合物和壳聚糖, 在30 ℃的恒温振荡器中振荡一定时间后对溶液进行离心操作, 取上层离心液, 稀释100 倍后经过分光光度计检测Cu2+浓度, 考察pH 值、 吸附时间、 初始浓度和温度对吸附效果的影响。
1.4 分析方法
试验采用2,9-二甲基-1,10-菲啰啉分光光度法[14]测定上清液中Cu2+浓度。 再按照公式(1)计算吸附剂对Cu2+的吸附容量。
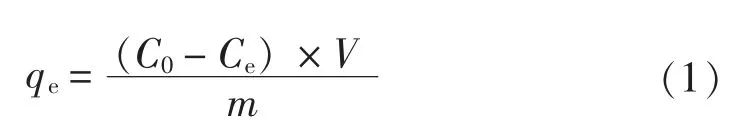
式中: qe为吸附材料的平衡吸附容量, mg/g;C0为初始Cu2+的 质量浓 度, mg/L; Ce为吸 附 后Cu2+的质量浓度, mg/L; V 为溶液的体积, mL; m为吸附材料的质量, mg。
2 结果与讨论
2.1 微观形貌分析
壳聚糖与壳聚糖/β-环糊精聚合物扫描电镜照片如图1 所示。

图1 扫描电镜照片Fig.1 SEM photographs
由图1 可知, 壳聚糖和壳聚糖/β-环糊精聚合物呈现出不规则结构, 壳聚糖的表面是光滑的颗粒状固体; 壳聚糖/β-环糊精聚合物表面粗糙、 凹凸不平, 并且还有一些空腔结构。 当金属离子进入壳聚糖/β-环糊精聚合物的空腔中后, 由于空腔阻力的存在, 使得金属离子难以摆脱束缚, 从而提高了该聚合物对重金属离子的吸附和包埋作用, 有利于增加吸附容量[15]。
2.2 红外光谱分析
对壳聚糖和壳聚糖/β-环糊精的结构进行表征,并将两者的红外光谱进行对比, 结果如图2 所示。
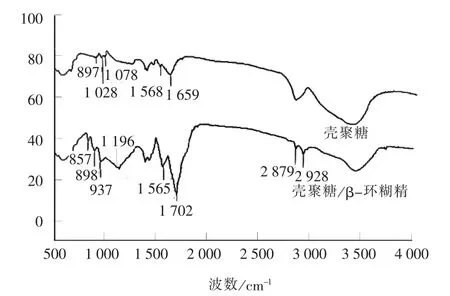
图2 壳聚糖和壳聚糖/β-环糊精聚合物扫描电镜Fig.2 Infrared spectroscopy of CTS and CTS/β-cyclodextrin
在壳聚糖的红外光谱中, 897 cm-1处发现了β-(1,4)糖苷键的特征峰, 1 028 cm-1和1 078 cm-1处分别出现了C6—OH 以及C3—OH 的伸缩振动, 1 568 cm-1和1 659 cm-1出现了NHCOCH3中N—H 的弯曲振动以及C—O 的伸缩振动。 在壳聚糖/β-环糊精聚合物红外光谱中, 在857 cm-1和937 cm-1处出现了属于β-环糊精的α-(1,4)吡喃葡萄糖和α-(1,4)糖苷键结构特征峰, 在1 028 cm-1和1 078 cm-1峰消失, 1 196 cm-1和1 702 cm-1处分别出现了酯基中的C—O 和C==O 结构特征峰, 1 565 cm-1保留了氨基的结构特征峰, 2 879 cm-1和2 928 cm-1处出现了原本分别属于壳聚糖 和β-环糊精的C—H 振动峰, 说明壳聚糖和β-环糊精通过交联剂柠檬酸发生了交联聚合[16]。
2.3 pH 值对吸附性能的影响
分别取0.2 g 壳聚糖与壳聚糖/β-环糊精聚合物加入200 mL 质量浓度为200 mg/L 的氯化铜溶液中, 调节pH 值为2 ~6, 在30 ℃恒温振荡器中振荡180 min, 考察pH 值对其吸附性能的影响, 结果如图3 所示。
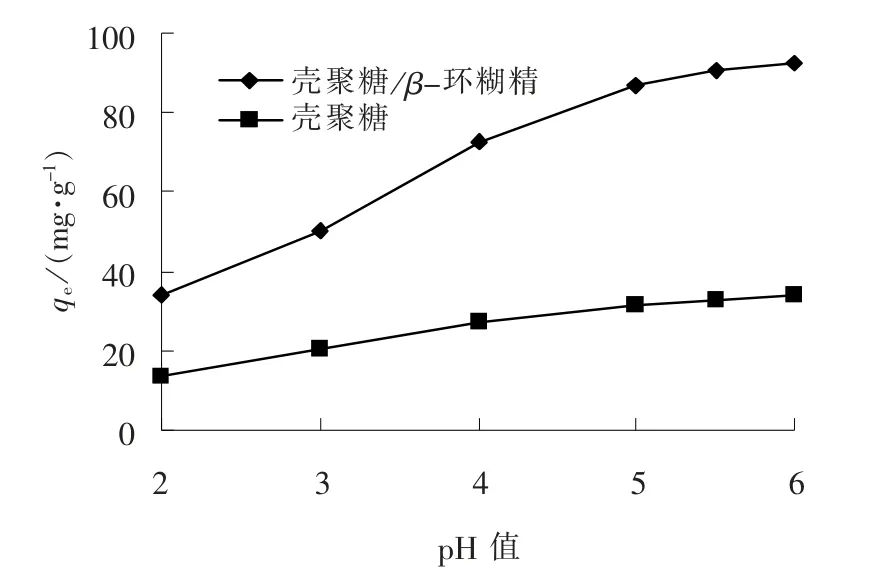
图3 pH 值对吸附性能的影响Fig.3 Effect of pH value on adsorption performance
由图3 可知, 壳聚糖/β-环糊精聚合物和壳聚糖对Cu2+的吸附量随着pH 值的上升而增加, 在pH 值为6 时, 达到最大值。 这是因为壳聚糖/β-环糊精聚合物中含有羟基、 羧基、 氨基等活性基团,对溶液中的重金属离子具有螯合作用, 可吸附重金属离子。 在强酸溶液中, H+和Cu2+竞争吸附, 占据聚合物中更多的吸附位点, 导致Cu2+与聚合物的螯合作用减弱, 吸附量降低。 当溶液中pH 值上升, 氨基等活性中心被重新释放出来, 与Cu2+发生配位作用, 增加了对Cu2+的吸附[17]。
2.4 吸附时间对吸附性能的影响
分别取0.2 g 壳聚糖和壳聚糖/β-环糊精聚合物加入到200 mL 质量浓度为200 mg/L、 pH 值为6的Cu2+溶液中, 在30 ℃下恒温振荡一定时间, 考察吸附时间对吸附性能的影响, 结果如图4 所示。
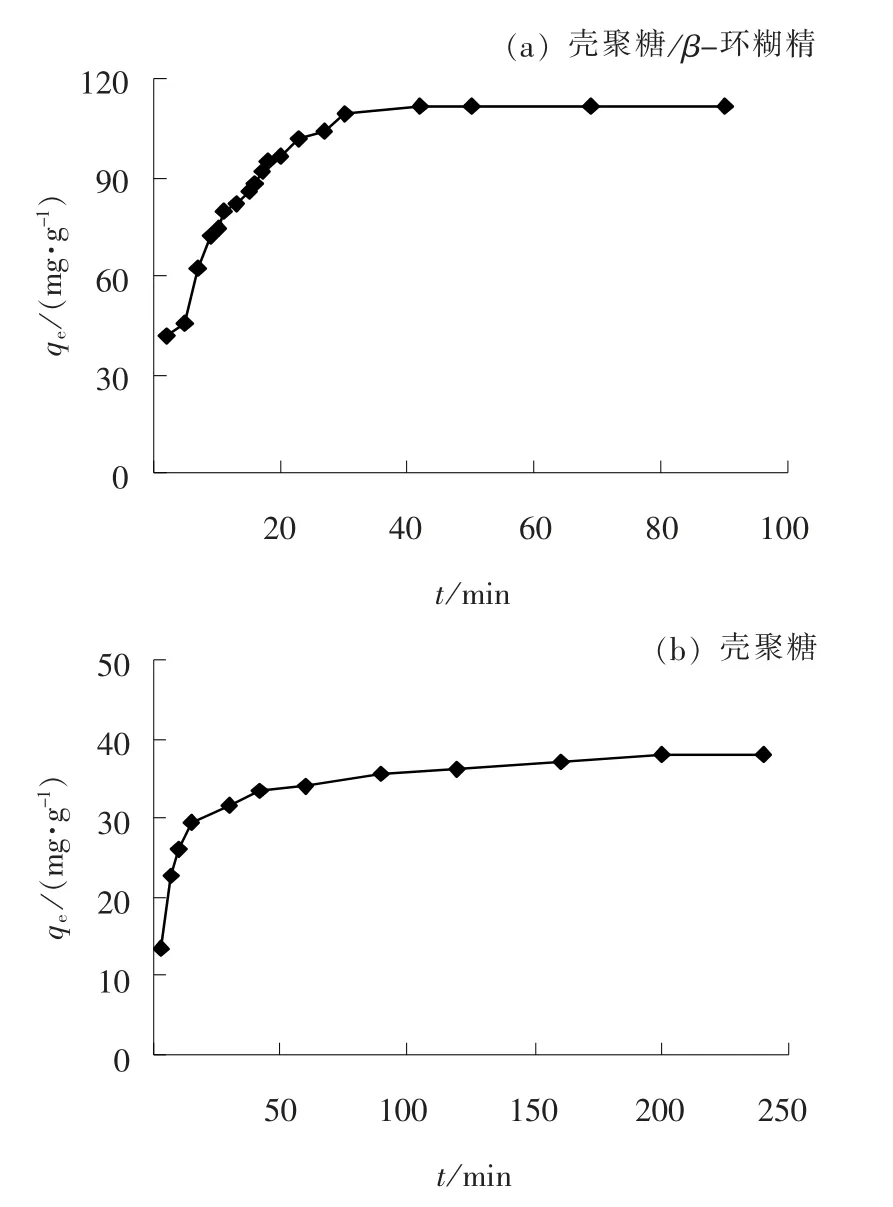
图4 吸附时间对吸附性能的影响Fig.4 Effect of adsorption time on adsorption performance
由图4 可知, 在0 ~15 min 内, 壳聚糖/β-环糊精聚合物对溶液中Cu2+的吸附量快速增加, 到40 min 逐渐达到吸附平衡。 对于壳聚糖而言, 在0 ~30 min 内, Cu2+的吸附量快速增加, 在210 min 才逐渐达到吸附平衡。 这是因为Cu2+吸附初期主要是以表面扩散为主[18], 该时期的吸附速率较快; 当表面吸附达到饱和时, 吸附过程开始向内部进行, 由于该阶段溶液中Cu2+浓度降低, 吸附过程中阻力开始变大, 因此吸附量增加缓慢直至吸附平衡。 壳聚糖/β-环糊精聚合物的吸附量大于壳聚糖, 这是因为该聚合物含有氨基、 羧基、 羟基等活性基团,这些基团能与Cu2+发生静电吸引、 离子交换、 络合等作用。 同时, 聚合物中保留了β-环糊精的空腔结构, 能够包埋Cu2+, 使其难逃脱束缚, 为吸附Cu2+提供了更多的吸附位点。 另外, 壳聚糖/β-环糊精聚合物的表面粗糙多孔, 也有利于吸附Cu2+。
通过拟一级和二级动力学模型对吸附过程进行拟合, 结果见表1。
由表1 可知, 壳聚糖/β-环糊精和壳聚糖对Cu2+的吸附过程更适用于拟二级动力学模型, 吸附过程主要是以化学吸附为主。
2.5 Cu2+初始浓度对吸附性能的影响
分别称取0.2 g 壳聚糖与壳聚糖/β-环糊精聚合物加入200 mL Cu2+溶液中, 在30 ℃下恒温振荡40 min, 考察Cu2+初始浓度对吸附性能的影响, 结果如图5 所示。
由图5 可知, 随着Cu2+浓度的增加, 壳聚糖/β-环糊精聚合物和壳聚糖的吸附量均呈现出逐渐增加的趋势, Cu2+浓度较低时壳聚糖/β-环糊精聚合物和壳聚糖对其吸附量增加较快, 这是因为此时吸附过程主要以表面扩散为主, 能对Cu2+建立起吸引作用, 可以快速地将Cu2+吸附在其表面。 当Cu2+浓度继续增加时, 壳聚糖/β-环糊精聚合物和壳聚糖的吸附位点被填满, 并达到平衡, 因此随着溶液中Cu2+的浓度增大, 壳聚糖/β-环糊精聚合物对Cu2+的吸附量逐渐变大直至饱和[19]。
利用Langmuir 和Freundlich 等温吸附模型对结果进行拟合分析, 结果如表2 所示。
由表2 可知, 壳聚糖和壳聚糖/β-环糊精的吸附过程更适用于Langmuir 等温吸附模型来拟合分析, 以单分子层吸附为主, 同时也进一步说明壳聚糖/β-环糊精和壳聚糖是依靠其活性基团吸附Cu2+。壳聚糖/β-环糊精的最大吸附量为209.58 mg/g, 大于壳聚糖的最大吸附量102.16 mg/g。 同时, 由于KL小于1, 说明壳聚糖/β-环糊精易于吸附Cu2+。

表1 吸附动力学参数Tab. 1 Adsorption kinetic parameters
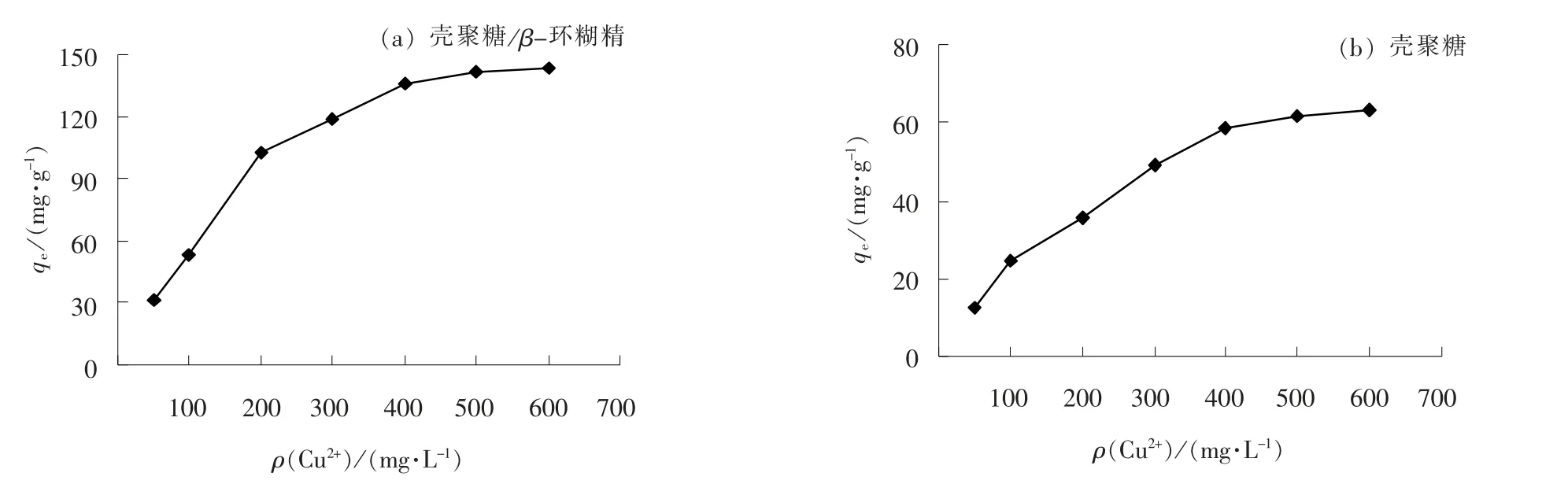
图5 Cu2+ 初始浓度对吸附性能的影响Fig.5 Effect of initial concentration of Cu2+on adsorption performance
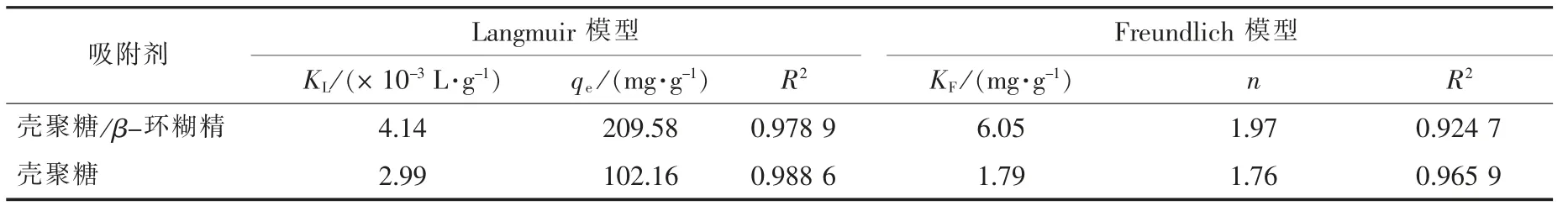
表2 壳聚糖与壳聚糖/β-环糊精对Cu2+ 的等温吸附模型Tab. 2 Isothermal adsorption models parameters of Cu2+by CTS and CTS/β-cyclodextrin
2.6 温度对吸附性能的影响
分别称取0.2 g 壳聚糖与壳聚糖/β-环糊精聚合物于250 mL 的锥形瓶中, 加入200 mL 质量浓度为100 mg/L Cu2+溶液, 在恒温振荡器中振荡40 min,考察温度对其吸附性能的影响, 结果如图6 所示。
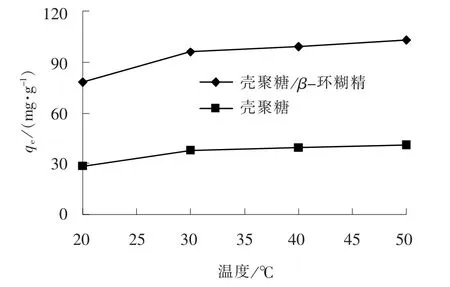
图6 温度对吸附性能的影响Fig.6 Effect of temperature on adsorption performance
由图6 可知, 随着温度的升高, 吸附到壳聚糖和壳聚糖/β-环糊精表面的Cu2+运动加剧, 增大了Cu2+与壳聚糖和壳聚糖/β-环糊精吸附位点的接触几率, 使得Cu2+的吸附量增大[20]。 因此, 温度升高有利于吸附过程的进行。 当温度超过30 ℃后,吸附量增加并不明显, 因此最佳温度为30 ℃。
3 结论
(1) 扫描电镜仪和红外光谱仪分析表明, β-环糊精和壳聚糖的羟基分别与柠檬酸的羧基发生反应,得到了壳聚糖/β-环糊精聚合物, 其比表面积大于壳聚糖的比表面积, 且具有空腔结构, 使得壳聚糖/β-环糊精聚合物的吸附能力优于壳聚糖。
(2) 在pH 值为6, 温度为30 ℃, Cu2+初始质量浓度为500 mg/L, 吸附时间为40 min, 投加量为0.2 g 的条件下, 壳聚糖/β-环糊精聚合物的吸附效果最好, 吸附量为141.90 mg/g。
(3) 壳聚糖/β-环糊精吸附过程更符合拟二级动力学模型和Langmuir 等温吸附模型, 表明该聚合物容易与Cu2+发生单层化学吸附。

