紫花地丁全草化学成分研究
崔 雪,郑重飞,李 莹,喻 琨,王 悦,姚庆强*
•化学成分 •
紫花地丁全草化学成分研究
崔 雪1,郑重飞1,李 莹1,喻 琨2,王 悦1,姚庆强1*
1. 山东省医学科学院药物研究所,山东第一医科大学,山东 济南 250000 2. 青岛大学纺织服装学院智能穿戴技术研究中心,山东 青岛 266071
研究紫花地丁全草的化学成分。采用硅胶、ODS、Sephadex LH-20凝胶和半制备型高效液相等柱色谱方法进行分离纯化,通过理化性质结合NMR、MS等谱学数据分析鉴定化合物结构。从紫花地丁95%乙醇提取物中分离得到21个化合物,分别鉴定为秦皮乙素-6--β--呋喃芹糖基-(1→2)-β--吡喃葡萄糖苷(1)、吲哚-3-甲酸乙酯(2)、脱氢地芰普内酯(3)、滨蒿内酯(4)、蒲公英苦素(5)、水杨苷(6)、丁香苷(7)、4-羟基-4-[3′-(β--葡萄糖基)亚丁基]-3,5,5-三甲基-2-环己烯-1-醇(8)、柑橘苷A(9)、(7,8)-二氢去氢二松柏醇-9--β--吡喃葡萄糖苷(10)、山柰素- 3--α--(4--乙酰基)鼠李糖基-7--α--鼠李糖苷(11)、山柰酚-7--α--鼠李糖苷(12)、山柰酚-3--α--鼠李糖苷(13)、山柰酚-3--α--鼠李糖基-7--α--鼠李糖苷(14)、山柰酚-3--β--葡萄糖苷(15)、芹菜素(16)、(+)-异地芰普内酯(17)、尿苷(18)、腺苷(19)、6-羟基-香豆素-7--α--鼠李糖基-(1→6)--β--葡萄糖苷(20)、(7,8)-二氢去氢二松柏醇-4--β--吡喃葡萄糖苷(21)。化合物1为新化合物,命名为紫丁葡芹苷,2为新天然产物,5~11和18为首次从堇菜属中分离得到,12和21为首次从紫花地丁中分离得到。
堇菜属;紫花地丁;香豆素苷;黄酮氧苷;秦皮乙素-6--β--呋喃芹糖基-(1→2)-β--吡喃葡萄糖苷;吲哚-3-甲酸乙酯;紫丁葡芹苷;蒲公英苦素;柑橘苷A
紫花地丁Makino为堇菜科堇菜属植物,是一种多年生草本植物,具有清热解毒、凉血消肿的功效,主要用于治疗疔疮肿毒、痈疽发背、丹毒、毒蛇咬伤等症状[1]。其用药历史悠久,始载于《千金方》。现代药理研究表明,紫花地丁具有抗炎、抗氧化、抗病毒、抗菌、抗肿瘤、抗凝血等作用[2-4]。目前,已从该植物中发现香豆素、黄酮、木脂素、萜类、甾体、生物碱等类化学成分[5-9]。但关于紫花地丁活性成分的研究报道还较少,为进一步丰富紫花地丁的化学结构类型,完善其物质基础,探寻活性较好的化合物,本实验对紫花地丁全草95%乙醇水提取物的化学成分进行系统研究,从中分离得到21个化合物,分别鉴定为秦皮乙素- 6--β--呋喃芹糖基-(1→2)-β--吡喃葡萄糖苷[aesculetin-6--β--apiofuranosyl-(1→2)-β--gluco-pyranoside,1]、吲哚-3-甲酸乙酯(ethyl indole-3- carboxylate,2)、脱氢地芰普内酯(dehydrololiolide,3)、滨蒿内酯(scoparone,4)、蒲公英苦素(taraxacin,5)、水杨苷(salicin,6)、丁香苷(syringin,7)、4-羟基-4-[3′-(β--葡萄糖基)亚丁基]-3,5,5-三甲基-2-环己烯-1-醇(()-4-hydroxy-4-[3′-(β--glucopyra- nosyloxy)butylidene]-3,5,5-trimethyl-2-cyclohexen-l- one,8)、柑橘苷A(citroside A,9)、(7,8)-二氢去氢松柏醇-9--β--吡喃葡萄糖苷[(7,8)-dihydro- dehydrodiconiferyl alcohol-9--β--glucopyranoside,10]、山柰素-3--α--(4--乙酰基)鼠李糖基-7--α--鼠李糖苷[kaempferol-3--α--(4--acetyl) rhamno-pyranoside-7--α--rhamnopyranoside,11]、山柰酚- 7--α--鼠李糖苷(kaempferol-7--α--rhamno- pyranoside,12)、山柰酚-3--α--鼠李糖苷(kaempferol-3--α--rhamnopyranoside,13)、山柰酚-3--α--鼠李糖基-7--α--鼠李糖苷(kaempferitrin,14)、山柰酚-3--β--葡萄糖苷(kaempferol 3--β--glucopyranoside,15)、芹菜素(apigenin,16)、(+)-异地芰普内酯 [(+)- isololiolide,17]、尿苷(uridine,18)、腺苷(β-adenosine,19)、6-羟基-香豆素-7--α--鼠李糖基-(1→6)--β--葡萄糖苷[6-hydroxy coumarin-7--α--rhamnosyl- (1→6)--β--glucoside,20]、(7,8)-二氢去氢松柏醇-4--β--吡喃葡萄糖苷[(7,8)-dihydrodehydro- diconiferyl alcohol 4--β--glucopyranoside,21]。其中,化合物1为新化合物,2为新天然产物,5~11和18为首次从堇菜属中分离得到,12和20为首次从该植物中分离得到。
1 仪器与材料
UltiMate 3000型高效液相色谱仪(美国Thermo Fisher公司),LC-20AR型制备液相色谱仪(日本Shimadzu公司),Avance 600型核磁共振仪(瑞士Bruker公司,TMS内标),X500 QTOF型高分辨质谱仪(美国AB Sciex公司)。柱色谱硅胶(60~100、300~400,目青岛海洋化工厂),柱色谱硅胶(200~300目,北京伊诺凯有限公司),薄层色谱硅胶预制板(烟台市化学工业研究所),LH-20型羟丙基葡聚糖凝胶(Sephadex LH-20,40~63 μm,德国Merck公司),ODS柱色谱填料(ODS-A-HG,50 μm,YMC公司)。实验所用色谱甲醇为美国Tedia公司,其他提取分离试剂均为分析纯(天津市富宇精细化工有限公司)。
紫花地丁全草于2018年3月采购于湖北聚瑞中药饮片有限公司,原产地为河南省平顶山市,经山东中医药大学王厚伟副教授鉴定为堇菜科植物紫花地丁Makino的干燥全草。
2 提取与分离
取紫花地丁干燥全草5 kg,用95%乙醇水回流提取3次,每次2 h,提取液合并后滤过,将滤液减压浓缩得总浸膏600 g。总浸膏经硅胶柱色谱(60~100目)分离,以石油醚、二氯甲烷、二氯甲烷-甲醇(50∶1)、二氯甲烷-甲醇(10∶1)、二氯甲烷-甲醇(5∶1)、二氯甲烷-甲醇(2∶1)、甲醇作为流动相梯度洗脱,共得到7个流分Fr. A~G。
Fr. B经硅胶柱色谱(200~300目)分离,以石油醚-二氯甲烷-甲醇(100∶0∶0、20∶1∶0、10∶1∶0、5∶1∶0、2∶1∶0、1∶1∶0、0∶100∶0、0∶10∶1、0∶2∶1、0∶0∶100)梯度洗脱,得到7个组分Fr. B-1~B-7。Fr. B-2经Sephadex LH-20柱色谱分离,得到4个组分Fr. B-2-1~B-2-4。Fr. B-2-3经Sephadex LH-20和ODS柱色谱分离,得到9个组分Fr. B-2-3-1~B-2-3-9。Fr. B-2-3-1经半制备型HPLC分离,以甲醇-水(30∶70)洗脱,得到化合物3(R=65 min,14.8 mg)。Fr. B-2-3-2经半制备型HPLC分离,以甲醇-水(35∶75)洗脱,得到化合物4(R=75 min,1.9 mg)。Fr. B-2-3-5经半制备型HPLC分离,以甲醇-水(50∶50)洗脱,得到化合物5(R=65 min,5.6 mg)。Fr. B-2-4经300~400目硅胶柱色谱分离,再经半制备型HPLC分离,以甲醇-水(60∶40)洗脱,得到化合物2(R=49 min,1.7 mg)。Fr. B-7经硅胶柱色谱(300~400目)分离,以二氯甲烷-甲醇(100∶0、100∶1、50∶1、20∶1、10∶1、5∶1、2∶1、0∶100)梯度洗脱,经薄层色谱(TLC)分析合并洗脱液,得到15个组分Fr. B-7-1~B-7-15。Fr. B-7-5经Sephadex LH-20和ODS柱色谱分离,再经半制备型HPLC分离,以甲醇-水(29∶71)洗脱,得到化合物17(R=37 min,22.7 mg)。
Fr. C经200~300目硅胶柱色谱分离,以二氯甲烷-甲醇(100∶0、500∶1、50∶1、20∶1、10∶1、5∶1、2∶1、0∶100)梯度洗脱,得到9个组分Fr. C-1~C-9。Fr. C-2经Sephadex LH-20柱色谱以及半制备型HPLC分离,以甲醇-水(60∶40)洗脱,得到化合物16(R=50 min,7.8 mg)。
Fr. D经硅胶柱色谱(200~300目)分离,以二氯甲烷-甲醇(50∶1、20∶1、10∶1、7∶1、5∶1、1∶1、0∶100)梯度洗脱,得到9个组分Fr. D-1~D-9。Fr. D-7经Sephadex LH-20和ODS柱色谱分离,得到15个组分Fr. D-7-1~D-7-15。Fr. D-7-2经半制备型HPLC分离,以甲醇-水(10∶90)洗脱,得到化合物19(R=70 min,34.4 mg)和6(R=90 min,15.8 mg)。Fr. D-7-3经半制备型HPLC分离,以甲醇-水(20∶80)洗脱,得到化合物7(R=60 min,6.8 mg)。Fr. D-7-5经半制备型HPLC分离,以甲醇-水(30∶70)洗脱,得到化合物8(R=47 min,6.0 mg)和9(R=50 min,15.2 mg)。Fr. D-7-7经半制备型HPLC分离,以甲醇-水(37∶63)洗脱,得到化合物10(R=71 min,2.9 mg)。Fr. D-7-9经半制备型HPLC分离,以甲醇-水(40∶60)洗脱,得到化合物15(R=100 min,2.8 mg)。Fr. D-7-10经半制备型HPLC分离,以甲醇-水(48∶52)洗脱,得到化合物13(R=56 min,5.0 mg)。Fr. D-7-13经半制备型HPLC分离,以甲醇-水(50∶50)洗脱,得到化合物11(R=60 min,11.2 mg)。Fr. D-7经Sephadex LH-20柱色谱和反复ODS柱色谱分离,最后经Sephadex LH-20柱色谱纯化,得到化合物14(18.5 mg)。
Fr. E经200~300目硅胶柱色谱分离,以二氯甲烷-甲醇(100∶0、100∶1、50∶1、20∶1、10∶1、5∶1、2∶1、1∶1、0∶100)梯度洗脱,得到8个组分Fr. E-1~E-8。Fr. E-3经Sephadex LH-20柱色谱分离,重结晶纯化得到化合物12(22.9 mg)。Fr. E-5经Sephadex LH-20和ODS柱色谱分离,得到12个组分Fr. E-5-1~E-5-12。Fr. E-5-2经半制备型HPLC分离,以甲醇-水(9∶91)洗脱,得到化合物18(R=23 min,13.4 mg)。Fr. E-5-4经半制备型HPLC分离,以甲醇-水(20∶80)洗脱,得到化合物20(R=59 min,7.7 mg)。Fr. E-5-5经半制备型HPLC分离,以甲醇-水(20∶80)洗脱,得到化合物1(R=77 min,8.9 mg)。Fr. E-5-8经半制备型HPLC分离,以甲醇-水(35∶65)洗脱,得到化合物21(R=46 min,6.5 mg)。
3 结构鉴定
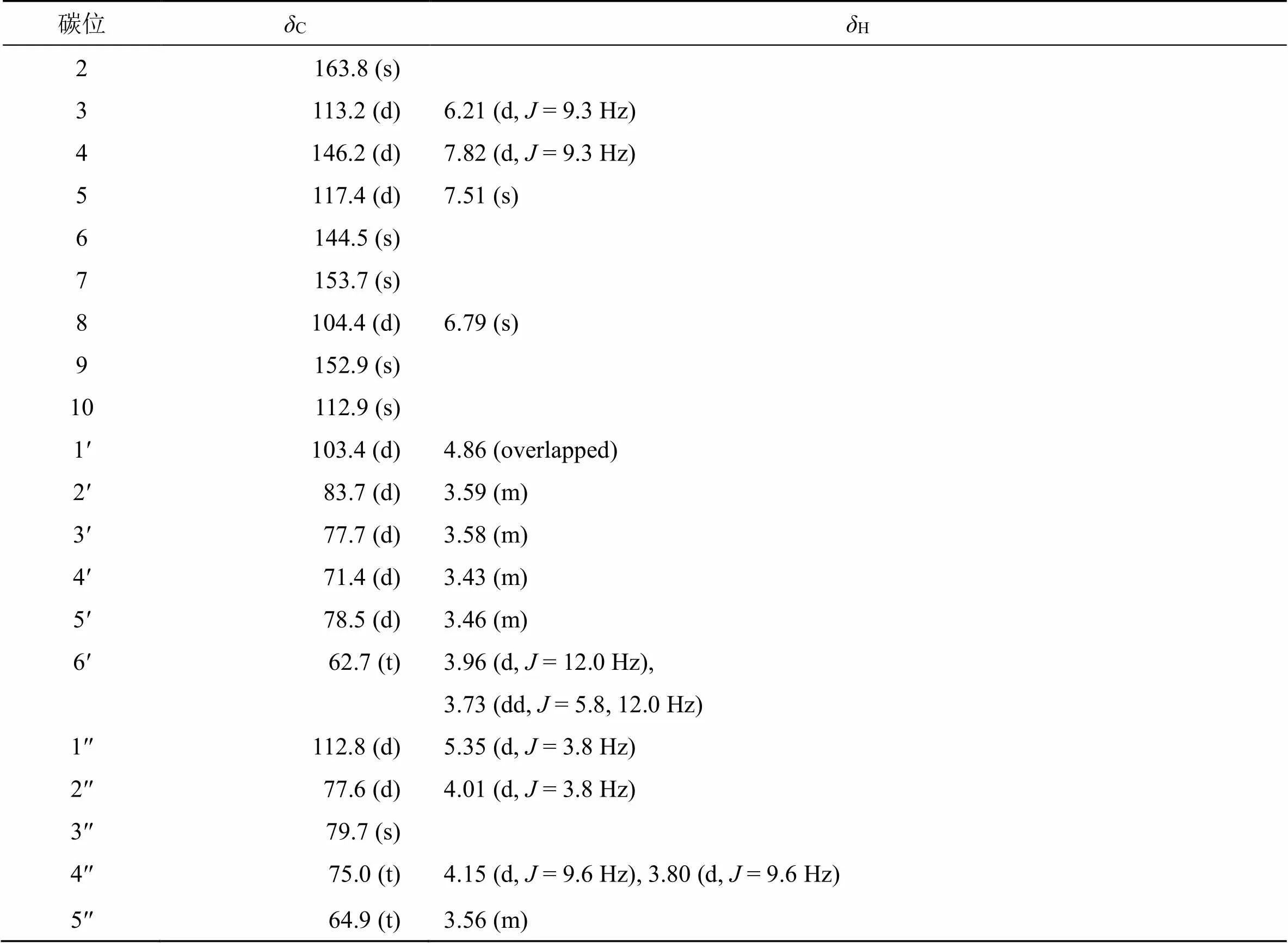
表1 化合物1的1H-、13C-NMR的波谱数据 (600/150 MHz, CD3OD)

化合物2:白色固体。ESI-MS/: 190.08 [M+H]+, 212.06 [M+Na]+。1H-NMR (600 MHz, CDCl3): 8.58 (1H, s, NH), 8.19~8.15 (1H, m, H-2), 7.91 (1H, d,= 3.0 Hz, H-4), 7.41~7.39 (1H, m, H-7), 7.26~7.25 (2H, m, H-5, 6), 4.38 (2H, q,= 7.1 Hz, H-9), 1.41 (3H, t,= 7.1 Hz, H-10);13C-NMR (150 MHz, CDCl3): 165.5 (C-8), 136.3 (C-7a), 131.1 (C-2), 126.0 (C-3a), 123.4 (C-6), 122.2 (C-4), 121.8 (C-5), 111.7 (C-7), 109.4 (C-3), 60.0 (C-9), 14.8 (C-10)。经SciFinder检索,化合物2在文献中通过合成得到[11],因此其作为1个天然产物首次从植物中分离得到,是新的天然产物,结构鉴定为吲哚-3-甲酸乙酯。
化合物3:黄色油状物。ESI-MS/: 195.10 [M+H]+, 217.08 [M+Na]+。1H-NMR (600 MHz, CDCl3): 5.89 (1H, s, H-7), 2.92 (1H, dd,= 13.6, 1.8 Hz, H-4a), 2.64 (1H, d,= 13.6 Hz, H-2a), 2.44 (1H, dd,= 14.3, 1.9 Hz, H-4b), 2.39 (1H, d,= 14.3 Hz, H-2b), 1.55 (3H, s, H-11), 1.39 (3H, s, H-9), 1.26 (3H, s, H-10);13C-NMR (150 MHz, CDCl3): 204.7 (C-3), 178.5 (C-8), 170.9 (C-6), 114.7 (C-7), 86.3 (C-5), 54.2 (C-4), 53.8 (C-2), 36.0 (C-1), 29.9 (C-11), 26.9 (C-9), 26.2 (C-10)。以上数据与文献报道一致[12],故鉴定化合物3为脱氢地芰普内酯。
化合物4:无色针状结晶(甲醇)。ESI-MS/: 207.06 [M+H]+, 229.04 [M+Na]+。1H-NMR (600 MHz, CDCl3): 7.60 (1H, d,= 9.4 Hz, H-4), 6.83 (1H, s, H-5), 6.82 (1H, s, H-8), 6.26 (1H, d,= 9.4 Hz, H-3), 3.93 (3H, s, 6-OCH3), 3.90 (3H, s, 7-OCH3);13C-NMR (150 MHz, CDCl3): 161.6 (C-2), 153.1 (C-7), 150.2 (C-9), 146.6 (C-6), 143.5 (C-4), 113.8 (C-3), 111.6 (C-10), 108.2 (C-5), 100.2 (C-8), 56.6 (6-OCH3), 56.6 (7-OCH3)。以上数据与文献报道一致[13],故鉴定化合物4为滨蒿内酯。
化合物5:黄色粉末。ESI-MS/: 243.09 [M+H]+, 265.08 [M+Na]+。1H-NMR (600 MHz, CDCl3): 6.50 (1H, s, H-6), 6.25 (1H, s, H-3), 5.06 (1H, dd,= 12.7, 3.3 Hz, H-8), 2.96 (1H, dd,= 16.8, 3.3 Hz, H-9a), 2.77 (1H, dd,= 16.8, 12.7 Hz, H-9b), 2.50 (3H, s, H-14), 2.24 (3H, s, H-15), 1.99 (3H, s, H-13);13C-NMR (150 MHz, CDCl3): 194.4 (C-2), 173.7 (C-12), 161.7 (C-5), 154.9 (C-7), 147.6 (C-10), 144.0 (C-4), 134.5 (C-3), 128.6 (C-1), 124.5 (C-11), 111.3 (C-6), 77.2 (C-8), 41.5 (C-9), 22.3 (C-14), 14.4 (C-15), 9.1 (C-13)。以上数据与文献报道一致[14],故鉴定化合物5为蒲公英苦素。
化合物6:黄色结晶(甲醇)。ESI-MS/: 309.09 [M+Na]+。1H-NMR (600 MHz, CD3OD): 7.35 (1H, dd,= 7.5, 1.5 Hz, H-6), 7.29 (1H, dt,= 7.5, 1.5 Hz, H-4), 7.20 (1H, d,= 7.5 Hz, H-3), 7.06 (1H, dt,= 7.5, 0.9 Hz, H-5), 4.93 (1H, d,= 7.4 Hz , H-1′), 4.76 (1H, d,= 12.9 Hz, H-7b), 4.60 (1H, d,= 12.9 Hz, H-7a), 3.90 (1H, dd,= 12.2, 2.1 Hz, H-6′b), 3.72 (1H, dd,= 12.2, 5.4 Hz, H-6′a), 3.56~3.42 (4H, m, H-2′~5′);13C-NMR (150 MHz, CD3OD): 156.9 (C-2), 131.9 (C-1), 130.3 (C-6), 130.2 (C-4), 124.0 (C-5), 117.0 (C-3), 103.0 (C-1′), 78.1 (C-3′), 77.7 (C-5′), 74.9 (C-2′), 71.3 (C-4′), 62.4 (C-6′), 60.9 (C-7)。以上数据与文献报道一致[15],故鉴定化合物6为水杨苷。
化合物7:白色结晶(甲醇)。ESI-MS/: 395.13 [M+Na]+。1H-NMR (600 MHz, CD3OD): 6.77 (2H, s, H-3, 5), 6.56 (1H, d,= 15.8 Hz, H-7), 6.35 (1H, dt,= 15.8, 5.6 Hz, H-8), 4.89 (1H, d,= 7.7 Hz, H-1), 4.24 (2H, dd,= 5.6, 1.4 Hz, H-9), 3.87 (6H, s, 2×OCH3), 3.80 (1H, dd,= 12.0, 2.4 Hz, H-6′b), 3.68 (1H, dd,= 12.0, 5.2 Hz, H-6′a), 3.21~3.50 (4H, m, H-2′~5′);13C-NMR (150 MHz, CD3OD): 154.5 (C-2, 6), 136.0 (C-1), 135.4 (C-4), 131.4 (C-7), 130.2 (C-8), 105.6 (C-1′), 105.5 (C-3, 5), 78.5 (C-3′), 78.0 (C-5′), 75.9 (C-2′), 71.5 (C-4′), 63.7 (C-9), 62.7 (C-6′), 57.2 (2×OCH3)。以上数据与文献报道一致[16],故鉴定化合物7为丁香苷。
化合物8:黄色油状物。ESI-MS/: 387.18 [M+H]+, 409.16 [M+Na]+。1H-NMR (600 MHz, CD3OD): 5.86 (3H, m, H-2, 7, 8), 4.42 (1H, m, H-9), 4.34 (1H, d,= 7.8 Hz, H-1′), 3.85 (1H, dd,= 11.7, 1.9 Hz, H-6′a), 3.62 (1H, dd,= 11.7, 5.5 Hz, H-6′b), 3.23~3.35 (3H, m, H-3′~5′), 3.17 (1H, m, H-2′), 2.52 (1H, d,= 17.0 Hz, H-6b), 2.15 (1H, d,= 16.9 Hz, H-6a), 1.92 (3H, s, H-13), 1.29 (3H, d,= 6.4 Hz, H-10), 1.04 (6H, d,= 3.7 Hz, H-11, 12);13C-NMR (150 MHz, CD3OD): 201.3 (C-1), 167.4 (C-3), 135.4 (C-8), 131.7 (C-7), 127.3 (C-2), 102.9 (C-1′), 80.2 (C-4), 78.3 (C-5′), 78.2 (C-3′), 77.4 (C-9), 75.4 (C-4′), 71.8 (C-2′), 63.0 (C-6′), 50.8 (C-6), 42.6 (C-5), 24.8 (C-12), 23.6 (C-11), 21.3 (C-10), 19.7 (C-13)。以上数据与文献报道一致[17],故鉴定化合物8为4-羟基- 4-[3′-(β--葡萄糖基)亚丁基]-3,5,5-三甲基-2-环己烯-1-醇。
化合物9:黄色油状物。ESI-MS/: 409.16 [M+Na]+。1H-NMR (600 MHz, CD3OD): 5.89 (1H, s, H-8), 4.52 (1H, d,= 7.8 Hz, H-1′), 4.32 (1H, m, H-3), 2.20 (3H, s, H-10), 1.47 (3H, s, H-12), 1.38 (3H, s, H-13), 1.16 (3H, s, H-11);13C-NMR (150 MHz, CD3OD): 213.1 (C-7), 200.9 (C-9), 119.2 (C-6), 101.5 (C-8), 98.8 (C-1′), 78.9 (C-5), 78.7 (C-3′), 77.9 (C-5′), 75.4 (C-2′), 71.8 (C-4′), 63.9 (C-3), 63.0 (C-6′), 50.0 (C-2), 48.2 (C-4), 37.2 (C-1), 32.7 (C-11), 30.2 (C-13), 26.8 (C-10), 26.8 (C-12)。以上数据与文献报道一致[18],故鉴定化合物9为柑橘苷A。
化合物11:黄色粉末。ESI-MS/: 621.13 [M+H]+, 643.11 [M+Na]+。1H-NMR (600 MHz, CD3OD): 7.77 (2H, d,= 8.7 Hz, H-2′, 6′), 6.96 (2H, d,= 8.7 Hz, H-3′, 5′), 6.73 (1H, d,= 2.0 Hz, H-8), 6.47 (1H, d,= 2.0 Hz, H-6), 5.56 (1H, s, H-1′′′), 5.53 (1H, br s, H-1′′), 4.83 (1H, t,= 2.0 Hz, H-4′′), 4.21 (1H, br s, H-2′′), 4.02 (1H, s, H-2′′′), 3.84 (2H, m, H-3′′, 5′′′), 3.60 (1H, m, H-3′′′), 3.47 (1H, d,= 9.5 Hz, H-4′′′), 3.26 (1H, m, H-5′′), 2.04 (3H, s, COCH3), 1.27 (3H, d,= 6.2 Hz, H-6′′′), 0.79 (3H, d,= 6.3 Hz, H-6′′);13C-NMR (150 MHz, CD3OD): 179.8 (C-4), 172.5 (COCH3-4′′), 163.7 (C-7), 163.2 (C-5), 162.0 (C-4′), 160.1 (C-2), 158.3 (C-9), 136.0 (C-3), 132.2 (C-2′, 6′), 122.5 (C-1′), 116.7 (C-3′, 5′), 107.7 (C-1′′), 102.7 (C-10), 100.8 (C-6), 100.0 (C-1′′′), 95.8 (C-8), 75.0 (C-4′′), 73.7 (C-4′′′), 72.2 (C-5′′′), 71.9 (C-2′′), 71.8 (C-2′′′), 71.5 (C-3′′′), 70.2 (C-3′′), 69.8 (C-5′′), 21.1 (4′′-COCH3), 18.2 (C-6′′′), 17.7 (C-6′′)。以上数据与文献报道一致[20],故鉴定化合物11为山柰素- 3--α-L-(4--乙酰基)鼠李糖基-7--α-L-鼠李糖苷。
化合物12:黄色针状结晶(甲醇)。ESI-MS/: 433.07 [M+H]+, 455.05 [M+Na]+。1H-NMR(600 MHz, DMSO-6): 12.47 (1H, s, 5-OH), 10.15 (1H, s, 4′-OH), 9.53 (1H, s, 3-OH), 8.08 (2H, d,= 9.0 Hz, H-2′, 6′), 6.93 (2H, d,= 9.0 Hz, H-3′, 5′), 6.82 (1H, d,= 2.1 Hz, H-8), 6.42 (1H, d,= 2.1 Hz, H-6), 5.54 (1H, d,= 1.5 Hz, H-1′′), 1.13 (3H, d,= 6.2 Hz, rha-CH3);13C-NMR (150 MHz, DMSO-6): 176.1 (C-4), 161.4 (C-7), 160.4 (C-5), 159.4 (C-4′), 155.8 (C-9), 147.5 (C-2), 136.1 (C-3), 129.7 (C-2′, 6′), 121.6 (C-1′), 115.5 (C-3′, 5′), 104.7 (C-10), 98.9 (C-6), 98.4 (C-1′′), 94.4 (C-8), 71.6 (C-4′′), 70.3 (C-3′′), 70.1 (C-2′′), 69.9 (C-5′′), 18.0 (C-6′′)。以上数据与文献报道一致[21-22],故鉴定化合物12为山柰酚-7--α--鼠李糖苷。
化合物13:黄色结晶(甲醇)。ESI-MS/: 433.08 [M+H]+,455.06 [M+Na]+。1H-NMR (600 MHz, CD3OD): 7.77 (2H, d,= 8.8 Hz, H-2′, 6′), 6.94 (2H, d,= 8.8 Hz, H-3′, 5′), 6.38 (1H, d,= 1.9 Hz, H-8), 6.21 (1H, d,= 2.0 Hz, H-6), 5.38 (1H, d,= 1.6 Hz, H-1′′′), 4.22 (1H, dd,= 3.4, 1.6 Hz, H-2′′), 3.71 (1H, dd,= 9.1, 3.4 Hz, H-3′′), 3.34 (2H, m, H-4′′, 5′′), 0.92 (3H, d,= 5.7 Hz, H-6′′);13C-NMR (150 MHz, CD3OD): 179.8 (C-4), 166.2 (C-7), 163.4 (C-5), 161.8 (C-4′), 159.4 (C-2), 158.7 (C-9), 136.4 (C-3), 132.0 (C-2′, 6′), 122.8 (C-1′), 116.7 (C-3′, 5′), 106.0 (C-10), 103.7 (C-1′′), 100.0 (C-6), 94.9 (C-8), 73.3 (C-4′′), 72.3 (C-3′′), 72.2 (C-5′′), 72.1 (C-2′′), 17.8 (C-6′′)。以上数据与文献报道一致[23],故鉴定化合物13为山柰酚-3--α--鼠李糖苷。
化合物14:黄色粉末。ESI-MS/: 579.14 [M+H]+, 601.12 [M+Na]+。1H-NMR (600 MHz, CD3OD): 7.81 (2H, d,= 8.7 Hz, H-2′, 6′), 6.95 (2H, d,= 8.7 Hz, H-3′, 5′), 6.74 (1H, d,= 2.1 Hz, H-8), 6.48 (1H, d,= 2.1 Hz, H-6), 5.56 (1H, s, H-1′′′), 5.40 (1H, s, H-1′′), 1.26 (3H, d,= 6.2 Hz, H-6′′′), 0.94 (3H, d,= 5.7 Hz, H-6′′);13C-NMR (150 MHz, CD3OD): 180.0 (C-4), 163.7 (C-7), 163.2 (C-5), 161.9 (C-4′), 160.0 (C-2), 158.3 (C-9), 136.6 (C-3), 132.2 (C-2′, 6′), 122.6 (C-1′), 116.7 (C-3′, 5′), 107.7 (C-1′′), 103.7 (C-10), 100.7 (C-6), 100.0 (C-1′′′), 95.8 (C-8), 73.7 (C-4′′′), 73.3 (C-4′′), 72.3 (C-5′′′), 72.3 (C-2′′), 72.2 (C-3′′), 72.1 (C-5′′), 71.9 (C-2′′′) , 71.5 (C-3′′′), 18.2 (C-6′′′), 17.8 (C-6′′)。以上数据与文献报道一致[24],故鉴定化合物14为山柰酚-3--α--鼠李糖基-7--α--鼠李糖苷。
化合物15:黄色针状结晶(甲醇)。ESI-MS/: 449.10 [M+H]+, 471.08 [M+Na]+。1H-NMR (600 MHz, CD3OD): 8.05 (2H, d,= 8.7 Hz, H-2′, 6′), 6.89 (2H, d,= 8.7 Hz, H-3′, 5′), 6.39 (1H, s, H-8), 6.19 (1H, s, H-6), 5.24 (1H, d,= 7.4 Hz, H-1′′);13C-NMR (150 MHz, CD3OD): 179.6 (C-4), 167.0 (C-7), 163.2 (C-5), 161.7 (C-4′), 159.1 (C-2), 158.7 (C-9), 135.6 (C-3), 132.4 (C-2′, 6′), 123.0 (C-1′), 116.2 (C-3′, 5′), 105.6 (C-10), 104.3 (C-1′′), 100.3 (C-6), 95.1 (C-8), 78.6 (C-5′′), 78.2 (C-3′′), 75.9 (C-2′′), 71.5 (C-4′′), 62.8 (C-6′′)。以上数据与文献报道一致[25],故鉴定化合物15为山柰酚-3--β--葡萄糖苷。
化合物16:黄色粉末。ESI-MS/: 271.04 [M+H]+, 293.02 [M+Na]+。1H-NMR (600 MHz, DMSO-6): 12.95 (1H, s, 5-OH), 7.92 (2H, d,= 8.8 Hz, H-2′, 6′), 6.92 (2H, d,= 8.8 Hz, H-3′, 5′), 6.76 (1H, s, H-3), 6.48 (1H, d,= 2.0 Hz, H-8), 6.19 (1H, d,= 2.0 Hz, H-6);13C-NMR (150 MHz, DMSO-6): 181.7 (C-4), 164.2 (C-7), 163.7 (C-2), 161.4 (C-4′), 161.2 (C-5), 157.3 (C-9), 128.4 (C-2′, 6′), 121.2 (C-1′), 116.0 (C-3′, 5′), 103.7 (C-10), 102.8 (C-3), 98.9 (C-6), 94.0 (C-8)。以上数据与文献报道一致[26],故鉴定化合物16为芹菜素。
化合物18:白色粉末。ESI-MS/: 267.05 [M+Na]+。1H-NMR (600 MHz, CD3OD): 8.04 (1H, d,= 8.1 Hz, H-6), 5.94 (1H, d,= 4.7 Hz, H-1′), 5.78 (1H, d,= 8.1 Hz, H-5), 4.25 (1H, t,= 5.0 Hz, H-3′), 4.21 (1H, t,= 5.0 Hz, H-2′), 4.07 (1H, m, H-4′), 3.89 (1H, dd,= 12.3, 2.7 Hz, H-5′b), 3.79 (1H, dd,= 12.3, 3.2 Hz, H-5′a);13C-NMR (150 MHz, CD3OD): 166.3 (C-4), 152.5 (C-2), 142.8 (C-6), 102.8 (C-5), 90.7 (C-1′), 86.3 (C-4′), 75.7 (C-3′), 71.3 (C-2′), 62.3 (C-5′)。以上数据与文献报道一致[28-29],故鉴定化合物18为尿苷。
化合物19:白色粉末。ESI-MS/: 268.09 [M+H]+, 290.07 [M+Na]+。1H-NMR (600 MHz, DMSO-6): 8.34 (1H, s, H-8), 8.13 (1H, s, H-2), 7.34 (2H, s, 6-NH2), 5.87 (1H, d,= 6.2 Hz, H-1′), 5.43 (2H, m, 2′, 5′-OH), 5.19 (1H, s, 3′-OH), 4.60 (1H, m, H-2′), 4.14 (1H, s, H-3′), 3.96 (1H, q,= 3.4 Hz, H-4′), 3.67 (1H, dt,= 12.1, 3.4 Hz, H-5′a), 3.55 (1H, m, H-5′b);13C-NMR (150 MHz, DMSO-6): 156.2 (C-6), 152.4 (C-2), 149.0 (C-4), 139.9 (C-8), 119.4 (C-5), 87.9 (C-1′), 85.9 (C-4′), 73.4 (C-2′), 70.7 (C-3′), 61.7 (C-5′)。以上数据与文献报道一致[30],故鉴定化合物19为腺苷。
化合物20:白色粉末。ESI-MS/: 487.12 [M+H]+, 509.10 [M+Na]+。1H-NMR (600 MHz, CD3OD): 7.86 (1H, d,= 9.5 Hz, H-4), 7.35 (1H, s, H-8), 7.04 (1H, s, H-5), 6.31 (1H, d,= 9.5 Hz, H-3), 4.90 (1H, d,= 7.8 Hz, H-1′), 4.73 (1H, brs, H-1′′), 1.26 (3H, d,= 6.2 Hz, H-6′′);13C-NMR (150 MHz, CD3OD): 164.5 (C-2), 150.9 (C-7), 149.5 (C-9), 146.2 (C-6), 146.0 (C-4), 115.5 (C-10), 114.6 (C-3), 114.0 (C-5), 105.8 (C-8), 103.5 (C-1′), 102.1 (C-1′′), 77.9 (C-3′), 77.5 (C-5′), 74.9 (C-2′), 73.8 (C-4′′), 72.6 (C-3′′), 72.2 (C-2′′), 72.1 (C-4′), 70.0 (C-5′′), 68.0 (C-6′), 18.2 (C-6′′)。以上数据与文献报道一致[31-32],故鉴定化合物20为6-羟基-香豆素-7--α--鼠李糖基-(1→6)--β--葡萄糖苷。
利益冲突 所有作者均声明不存在利益冲突
[1] 中国药典 [S]. 一部. 2020: 352.
[2] 宋妍. 紫花地丁药理作用的研究现状 [J]. 中医临床研究, 2017, 9(12): 136-137.
[3] Wang Y L, Zhang L, Li M Y,. Lignans, flavonoids and coumarins fromand their α-glucosidase and HCV protease inhibitory activities [J]., 2019, 33(11): 1550-1555.
[4] Zhou H Y, Hong J L, Shu P,. A new dicoumarin and anticoagulant activity fromMakino [J]., 2009, 80(5): 283-285.
[5] Xie C, Veitch N C, Houghton P J,. Flavone C-glycosides fromMakino [J]., 2003, 51(10): 1204-1207.
[6] 黄霁秋, 杨敬芝, 薛清春, 等. 紫花地丁化学成分研究 [J]. 中国中药杂志, 2009, 34(9): 1114-1116.
[7] Du D S, Cheng Z H, Chen D F. Anti-complement sesquiterpenes from[J]., 2015, 101: 73-79.
[8] 肖永庆, 毕俊英, 刘晓宏, 等. 地丁化学成分的研究 [J]. 植物学报, 1987, 29(5): 532-536.
[9] 徐金钟, 曾珊珊, 瞿海斌. 紫花地丁化学成分研究 [J]. 中草药, 2010, 41(9): 1423-1425.
[10] Matsuda N, Kikuchi M. A coumarin glycoside fromvar.[J]., 1995, 38(3): 803-804.
[11] Lee K Y, Lee H S, Kim J N. Synthesis of indoles and benzisoxazolines from baylis—Hillman adducts of 2-nitrobenzaldehydes [J]., 2007, 28(2): 333-335.
[12] Zeng Q, Ye J, Ren J,. Chemical constituents from[J]., 2013, 49(3): 486-492.
[13] Wu S H, Luo X D, Ma Y B,. Two new germacranolides from[J]., 2001, 3(2): 95-102.
[14] Ahmad V U, Yasmeen S, Ali Z,. Taraxacin, a new guaianolide fromwallichii [J]., 2000, 63(7): 1010-1011.
[15] 邓可众, 熊英, 高文远. 半边莲的化学成分研究 [J]. 中草药, 2009, 40(8): 1198-1201.
[16] Kiem P V, Minn C V, Dat N T,. Two new phenylpropanoid glycosides from the stem bark of[J]., 2003, 26(12): 1014-1017.
[17] 孟江, 董晓萍, 周毅生, 等. 鲜鱼腥草酚类化学成分的研究 [J]. 中国中药杂志, 2007, 32(10): 929-931.
[18] 郭蓉, 王跃虎, 石亚娜, 等. 云南金钱槭茎化学成分 [J]. 天然产物研究与开发, 2012, 24(8): 1007-1013.
[19] Su D M, Tang W Z, Hu Y C,. Lignan glycosides from[J]., 2008, 71(5): 784-788.
[20] 栾欣, 王皓, 温远影. 狗脊化学成分研究 [J]. 热带亚热带植物学报, 2002, 10(4): 361-365.
[21] Lee M W, Lee Y A, Park H M,. Antioxidative phenolic compounds from the roots ofsachalinensis A. Bor [J]., 2000, 23(5): 455-458.
[22] 杨秀伟, 张建业, 钱忠明. 罗汉果中新的天然皂苷[J]. 中草药, 2008, 39(6): 810-814.
[23] 谭俊杰, 蒋山好, 朱大元. 天山棱子芹化学成分的研究 [J]. 天然产物研究与开发, 2005, 17(3): 267-271.
[24] 袁琳, 黄文忠, 梁德强, 等. 合柄铁线莲中黄酮苷类化学成分研究 [J]. 中国药学杂志, 2015, 50(6): 497-501.
[25] 冯卫生, 郝志友, 郑晓珂, 等. 哥兰叶化学成分的研究 [J]. 药学学报, 2007, 42(6): 625-630.
[26] 白丽明, 高鸿悦, 马玉坤, 等. 鼠曲草化学成分及其抗氧化活性研究 [J]. 中草药, 2016, 47(4): 549-553.
[27] 霍立娜, 王威, 刘洋, 等. 紫苏叶化学成分研究 [J]. 中草药, 2016, 47(1): 26-31.
[28] 胡小燕, 窦德强, 裴玉萍, 等. 猫爪草中化学成分的研究 [J]. 中国药学: 英文版, 2006, 15(2): 127-129.
[29] Ma Y T, Qiao L R, Shi W Q,. Metabolites produced by an endophyteisolated from[J]., 2010, 46(3): 504-506.
[30] 吴斌, 林文辉. 昙花化学成分的研究 [J]. 中国药学杂志, 2010, 45(7): 496-499.
[31] Sarker S D, Waterman P G, Armstrong J A. Coumarin glycosides from two species of[J]., 1995, 58(7): 1109-1115.
[32] 柳航, 胡巍, 方芸. 紫花地丁乙酸乙酯部位的化学成分研究 [J]. 安徽医药, 2015, 19(6): 1068-1071.
[33] Matsuda N, Sato H, Yaoita Y,. Studies on the constiuents ofspecies. part XIII. isolation and absolute structures of the neolignan glycosides with the enantiometric aglycones from the leaves ofawabuki K. KOCH [J]., 1996, 44(5): 1122-1123.
Chemical constituents from whole herbs of
CUI Xue1, ZHENG Zhong-fei1, LI Ying1, YU Kun2, WANG Yue1, YAO Qing-qiang1
1. Institute of Materia Medica, Shandong First Medical University &Shandong Academy of Medical Sciences, Jinan 250000, China 2. Research Center for Intelligent and Wearable Technology, College of Textiles and Clothing, Qingdao University, Qingdao 266071, China
To investigate the chemical constituents from whole herbs of.The chemical constituents were isolated and purified by silica gel, ODS column chromatography, Sephadex LH-20 column chromatography and semi-preparative HPLC. The structures of the isolated compounds were identified by physicochemical properties, NMR and MS spectroscopic methods.A total of 21 compounds were isolated from the 95% ethanol extract of, and their structures were identified as aesculetin 6--β--apiofuranosyl-(1→2)-β--glucopyranoside (1), ethyl indole-3-carboxylate (2), dehydrololiolide (3), scoparone (4), taraxacin (5), salicin(6), syringin (7), ()-4-hydroxy-4-[3′-(β--glucopyranosyloxy) butylidene]-3,5,5-trimethyl-2-cyclohexen-l-one (8), citroside A (9), (7,8)-dihydrodehydrodiconiferyl alcohol-9--β-- glucopyranoside (10), 3--α-L-(4--acetyl)rhamnopyranosyl kaempferol 7--α-L-rhamnopyranoside (11), kaempferol-7--α-- rhamnopyranoside (12), kaempferol-3--α-L-rhamnopyranoside (13), kaempferitrin (14), kaempferol-3--β--glucopyranoside (15), apigenin (16), (+)-isololiolide (17), uridine (18), β-adenosine (19), 6-hydroxycoumarin-7--α--rhamnosyl-(1→6)--β--glucoside (20), and (7,8)-dihydrodehydrodiconiferyl alcohol 4--β--glucopyranoside (21).Compound 1 is obtained as a new compound, named as vioyegluapiside and compound 2 as a new natural product, with compounds 5-11 and 18 isolating from the genus Viola for the first time and with compounds 12 and 21 from plantfor the first time.
genus Viola;Makino; coumarin glycoside; flavone-glycosides; aesculetin-6--β--apiofuranosyl-(1→2)-β--glucopyranoside; ethyl indole-3-carboxylate; vioyegluapiside; taraxacin; citroside A
R284.1
A
0253 - 2670(2021)04 - 0917 - 08
10.7501/j.issn.0253-2670.2021.04.002
2020-11-28
山东省重点研发计划(鲁渝科技协作)项目(2019LYXZ026);山东省农业科技园区产业提升工程项目(2019YQ033);山东第一医科大学学术提升计划(2019LJ003)
崔 雪,女,硕士研究生,从事天然药物化学研究。E-mail: cuixue_sunny@163.com
姚庆强,男,博士,博士生导师。Tel: (0531)82595867 E-mail: yao_imm@163.com
[责任编辑 王文倩]

