宰后猪肉pH值、骨架蛋白表达水平和持水性之间的关系
李华健,陈 韬,杨波若,李 霞,李燕清,王博文,卞健科,舒国涛
(云南农业大学食品科学技术学院,云南 昆明 650201)
持水性会影响猪肉的加工特性、感官品质和盈利能力,是猪肉最重要的品质之一[1-3]。肉畜屠宰后,由于汁液流失造成的质量损失一般在1%~10%之间[4],过高的汁液流失易导致PSE(pale, soft, exudative)肉或RSE(reddish-pink,soft, exudative)肉,给肉类行业造成巨大的经济损失[5]。因此,研究宰后猪肉持水性的影响因素具有直接的经济价值和现实意义。
目前,国内外学者[6-7]主要应用相关性分析探讨pH值、骨架蛋白变化与持水性的关系,其存在一定的局限性,因为相关性分析虽然能反映各变量与因变量的相关程度,但并不能完全反映出各变量对因变量的相对重要性,偏最小二乘回归(partial least squares regression,PLSR)分析则能对数据进行分解和筛选,克服变量多重相关性的影响,提取对因变量解释性最强的变量,从而更好地反映出变量对因变量的相对重要性[8],弥补相关性分析的不足。另外,研究者普遍认为:细胞膜骨架蛋白整联蛋白(integrin)的降解有助于汁液流失通道的形成,增加汁液流失[9-10]。然而,肌细胞膜骨架蛋白不仅包含跨膜的整联蛋白,还包含与膜相连的蛋白,如踝蛋白(talin)、黏着斑蛋白(vinculin)、抗肌营养不良蛋白(dystrophin)等,这些蛋白通过肋小节(costameres)将肌原纤维和细胞外基质间接地联结起来[11]。整联蛋白-踝蛋白、黏着斑蛋白复合物是肋小节中介导细胞-细胞和细胞-基质相互作用的主要受体复合物,其中整联蛋白贯穿于肌细胞膜,外联肌细胞外基质内接踝蛋白,黏着斑蛋白和踝蛋白相互作用调节整联蛋白黏着斑的形成,对细胞彼此之间的附着十分重要[12-14]。由于踝蛋白、黏着斑蛋白与整联蛋白在细胞中的位置和功能存在不同,可能会对持水性产生不同的影响[7]:Kristensen等[15]的研究表明猪肉宰后成熟过程中,黏着斑蛋白的缓慢降解和踝蛋白的快速降解与持水性的增加有关;Schäfer等[16]研究认为黏着斑蛋白的降解与持水性无关;Bee等[6]的研究表明猪肉宰后48、72 h和120 h的踝蛋白表达水平与贮藏损失率呈显著正相关(P<0.05),宰后48 h的黏着斑蛋白表达水平与贮藏损失率呈显著负相关(P<0.05);Di Luca等[17]通过蛋白组学研究发现汁液流失率低的肉样黏着斑蛋白表达量更高。由此可见,踝蛋白和黏着斑蛋白与持水性的关系依然还存有争议。近年,Puolanne等[18]提出肉的持水机理还不清楚,肌细胞膜骨架蛋白与持水性的关系应结合pH值、不同离子和蛋白质变性等进一步研究。因此,本研究主要运用相关性分析和PLSR分析探讨pH值及整联蛋白、踝蛋白、黏着斑蛋白变化与持水性之间的关系,以期为持水性的改善及预测宰后猪肉的汁液流失率提供一定的理论依据。
1 材料与方法
1.1 材料与试剂
在曲靖市某商业屠宰场,选择6.5 月龄、饲养条件相同、体质量相近((105±5)kg)的20 头去势三元杂交猪(大河乌猪×约克夏×长白猪),按照GB/T 17236—2019《畜禽屠宰操作规程 生猪》[19]进行屠宰,热分割、胴体四分体后取13肋至最后腰椎处的背最长肌(带皮、脂肪和骨),用塑料薄膜包裹,放在0~4 ℃冷库中,在宰后不同时间点测定相关指标,并在各时间点取样,用自封袋排气封存于-80 ℃冰箱备用。根据宰后45 min的pH值经聚类分析,将样品分为高pH组和低pH组。
β-巯基乙醇、十二烷基硫酸钠(sodium dodecyl sulfate,SDS)、Tris、N,N’-双-亚甲基丙烯酰胺、溴酚兰、N,N,N’,N’-四甲基乙二胺(N,N,N’,N’-tetramethylethylenediamine,TEMED)(分析纯)、丙烯酰胺(超级纯) 美国Amresco公司;过硫酸胺(ammonium persulfate,APS)、乙二胺四乙酸(ethylenediaminetetraacetic acid,EDTA) 天津市风船化学试剂科技有限公司;BCA蛋白浓度测定试剂盒 北京索莱宝科技有限公司;预染Marker 美国Thermo公司;牛血清白蛋白(albumin from bovine serum,BSA)、clone 8D4踝蛋白一抗 美国Sigma公司;MAB1900整联蛋白一抗、MAB3574黏着斑蛋白一抗、AP181P二抗和0.45 μm的疏水性聚偏氟乙烯(poly(vinylidene fluoride),PVDF)转印膜 美国Millipore公司;特超敏化学发光检测试剂盒美国Everbright公司。
1.2 仪器与设备
HI9025C便携式pH计 意大利哈纳公司;全自动酶标仪 北京普朗新技术有限公司;通用电泳仪电源、小型垂直电泳系统、槽式转印系统、ChemiDoc MP全能型成像系统 美国Bio-Rad公司。
1.3 方法
1.3.1 pH值的测定
采用王娟等[20]的方法,用便携式pH计测定宰后45 min和3、9、12、24 h猪背最长肌的pH值。每组样品平行测量3 次取平均值。
1.3.2 汁液流失率的测定
参照Honikel[21]的方法测定汁液流失率,并稍作修改。于宰后24 h取2.5 cm厚背最长肌一片,用万分之一天平称质量(m1/g)。用铁丝钩住肉条的一端,使肌纤维垂直向下,悬挂于塑料袋中,充气(肉样不能和塑料袋接触),扎紧袋口,在4 ℃条件下吊挂24 h,取出称质量(m2/g)。汁液流失率按下式计算。
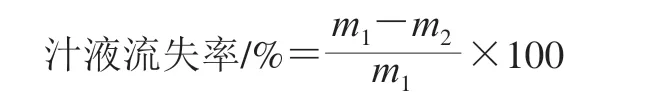
1.3.3 细胞骨架蛋白表达水平测定
采用Western blot技术测定踝蛋白(分子质量225 kDa)、整联蛋白(分子质量116 kDa)和黏着斑蛋白(分子质量120 kDa)在不同时间点(宰后45 min和3、9、12、24 h)的降解情况。SDS-聚丙烯酰胺凝胶电泳(polyacrylamide gel electrophoresis,PAGE)全肌肉蛋白样品的制备参照Lonergan等[22]的方法并稍作修改。称取0.8 g切碎的背最长肌肉样,加入10 mL全肌肉蛋白提取液(10 mmol/L pH 7.0磷酸钠、2 g/100 mL SDS),6 500 r/min匀浆30 s后在20 ℃、离心力1 500×g条件下离心20 min,取上清液,使用BCA蛋白浓度测定试剂盒测定蛋白质量浓度,用双蒸水将质量浓度调至6.4 mg/mL。取1 mL 6.4 mg/mL蛋白质上清液与0.5 mL上样缓冲液(30 mmol/L Tris-HCl、3 mmol/L EDTA、3 g/100 mL SDS、体积分数30%甘油、0.002 g/100 mL溴酚蓝,pH 8.0)混合后加入0.1 mLβ-巯基乙醇(最终蛋白质浓度为4 mg/mL)。50 ℃水浴加热20 min,冷却至室温,存放于-80 ℃冰箱备用。
SDS-PAGE:踝蛋白、整联蛋白和黏着斑蛋白分别使用质量分数8%、10%、10%的分离胶,浓缩胶都使用质量分数5%的凝胶。待胶凝聚后,向电泳槽中加入电泳缓冲液(25 mmol/L Tris、192 mmol/L甘氨酸、2 mmol/L EDTA和0.1 g/100 mL SDS),对准胶孔注入蛋白质样品。整联蛋白、黏着斑蛋白和踝蛋白每个泳道上样量分别为80、80、120 μg全肌肉蛋白样液。按照Bee等[6]的方法从左至右依次加入5 μL预染Marker、参比蛋白样品和宰后45 min~24 h的蛋白样品(参比蛋白样液由宰后45 min,高pH组中汁液流失率最小的样品制备)。设定浓缩胶电压80 V、30 min,分离胶电压120 V、1 h,进行电泳。
转膜:电泳结束后将凝胶转移至PVDF膜。整联蛋白和黏着斑蛋白在200 mA下转印1.5 h,踝蛋白在220 mA下转印2 h,整个过程在0 ℃下进行。转印缓冲液由25 mmol/L Tris、192 mmol/L甘氨酸、2 mmol/L EDTA和体积分数15%甲醇组成。
Western blotting:转印后,将膜置于含有5 g/100 mL BSA的TBST缓冲液(含20 mmol/L Tris-HCl、100 mmol/L NaCl、体积分数0.05% Tween 20,pH 7.5)中室温封闭1 h,再置于一抗中4 ℃孵育过夜。一抗孵育完成后,在室温下用TBST缓冲液洗膜3 次(10 min/次)。将洗过的膜置于二抗中室温孵育1 h。二抗孵育完成后在室温下用TBST缓冲液洗膜3 次(10 min/次)。将洗净后的膜用化学发光试剂盒显影,于暗室曝光。用ImageJ软件分析完整的目标蛋白条带灰度值,按照Bee等[6]的方法分别以蛋白条带上5 个时间点所测的灰度值与每块凝胶上加载的参比样品灰度值之比(即相对灰度值),表示完整的目标蛋白表达水平。每张膜重复定量3 次求平均值。
一抗和二抗稀释液都使用含3 g/100 mL BSA的TBST缓冲液。整联蛋白和黏着斑蛋白的一抗稀释比为1∶800(V/V,下同),踝蛋白一抗稀释比为1∶500。整联蛋白和黏着斑蛋白的二抗稀释比为1∶8 000,踝蛋白的二抗稀释比为1∶6 000。
1.4 数据统计与分析
采用SPSS 19.0软件计算数据的平均值和标准差,并进行Duncan’s多重比较、独立性T检验和相关性分析(由于pH值数据不服从正态分布,因此pH值与骨架蛋白表达水平的相关性采用Spearman相关性分析)。鉴于PLSR法可以解决样本量少、变量不服从正态分布等问题[23-24],各变量与汁液流失率的关系采用Unscrambler 9.7软件进行PLS1回归分析。采用Origin 2018软件进行绘图。P<0.05认为具有统计学意义。
2 结果与分析
2.1 聚类分析结果
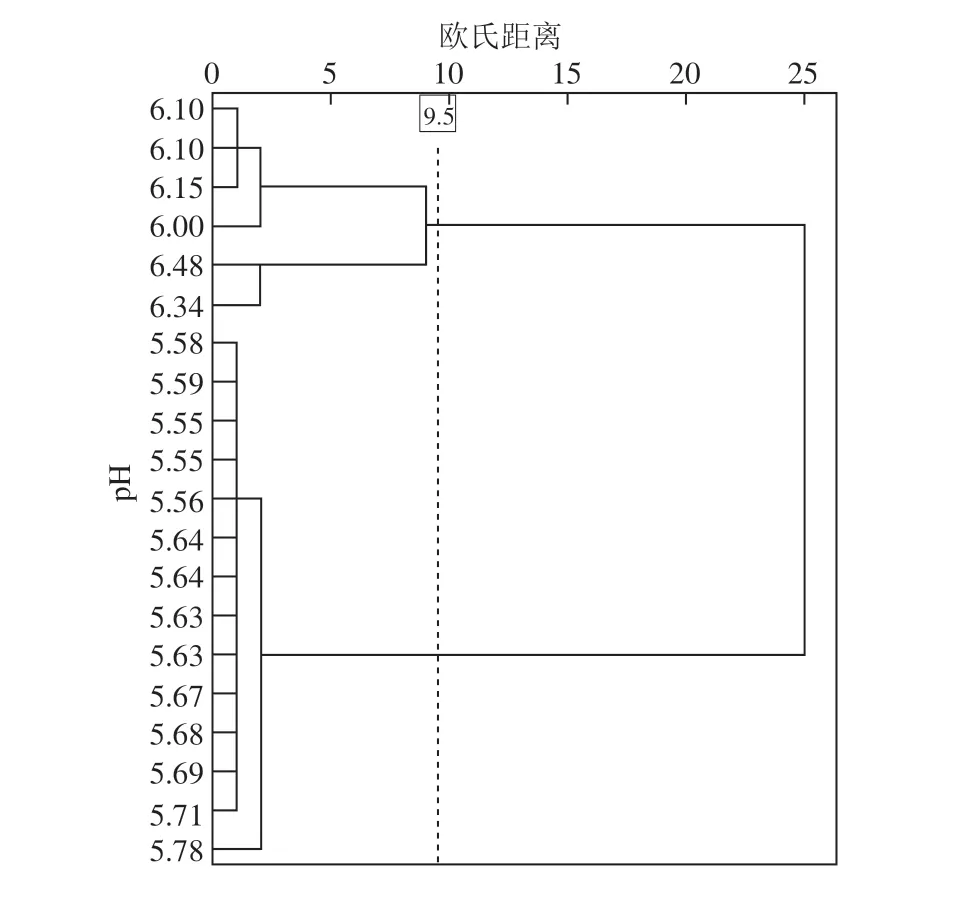
图1 宰后45 min样品的pH值聚类分析树状图Fig.1 Dendrogram of cluster analysis for pH of pork samples at 45 min postmortem
根据宰后45 min样品pH值的大小进行聚类分析,结果如图1所示。当欧氏距离增至9.5时,可将20 个样品分成高pH组(pH45min≥6.00,n=6)和低pH组(pH45min≤5.78,n=14)。分组后,高pH组的汁液流失率极显著低于低pH组(P<0.01)(图2)。此结果与Bee[6]、Zhang Muhan[25]等的研究结果一致。王娟等[20,26]的研究也表明,与杂交猪相比,具有较高持水性的梅山猪宰后45 min的pH值明显更高(P<0.05)。
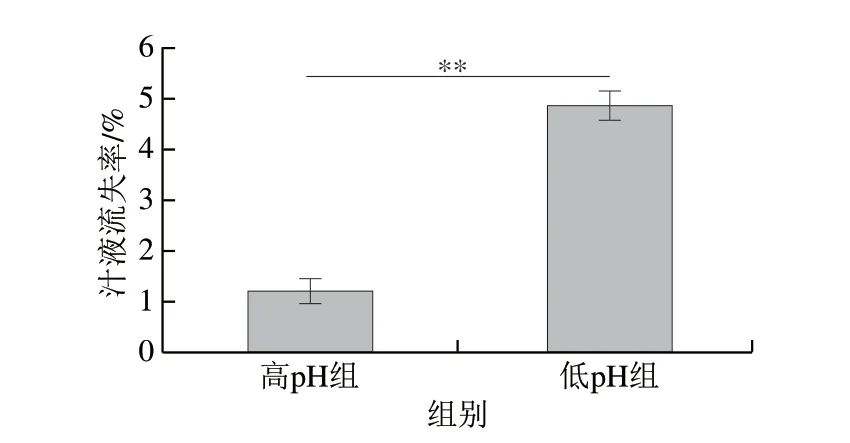
图2 不同pH值组肉样的汁液流失率Fig.2 Drip loss of pork samples with different pH values
2.2 不同组别pH值和骨架蛋白的表达水平分析结果
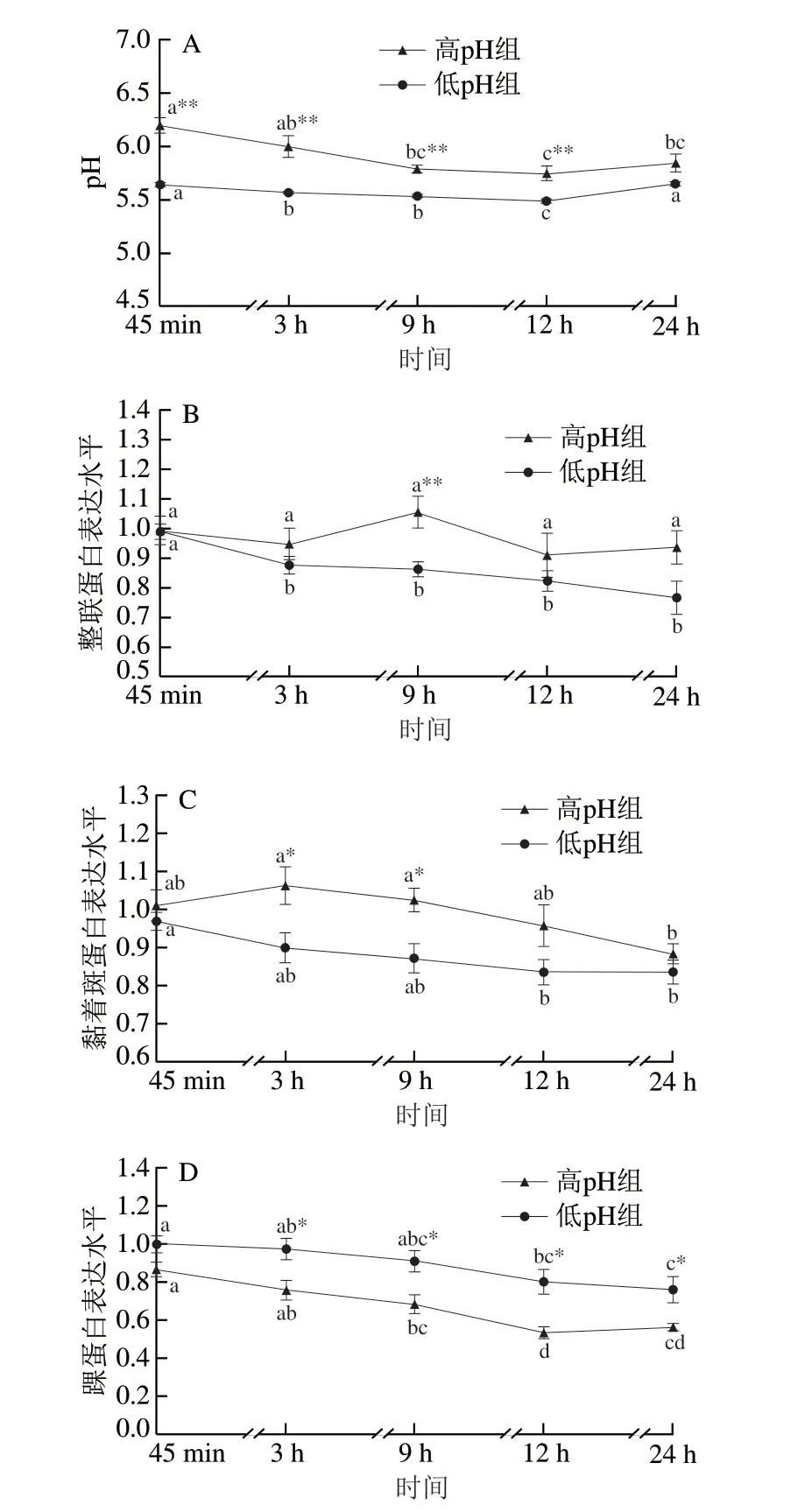
图3 宰后不同pH组样品的pH值(A)和整联蛋白(B)、黏着斑蛋白(C)、踝蛋白(D)表达水平的变化Fig.3 Changes in pH (A), and expression levels of integrin (B),vinculin (C), and talin (D) in pork samples with different pH values during postmortem aging
如图3所示,高、低pH组之间的pH值和完整的骨架蛋白表达水平存在一定的差异。高pH组的pH值在宰后45 min和3、9、12 h都极显著高于低pH组(P<0.01),整联蛋白表达水平在宰后9 h 极显著高于低p H 组(P<0.01),黏着斑蛋白表达水平在宰后3 h和9 h显著高于低pH组(P<0.05),踝蛋白表达水平在宰后3、9、12、24 h都显著低于低pH组(P<0.05)。
与宰后45 min相比,高pH组的pH值到宰后9 h显著降低(P<0.05),而低pH组到宰后3 h就显著降低(P<0.05),在宰后12~24 h两组肉样的pH值都有上升的趋势,低pH组出现显著上升(P<0.05)。整联蛋白在高pH组中未见显著降解(P>0.05),而低pH组在宰后3 h较宰后45 min出现显著降解(P<0.05)。高pH组宰后24 h的黏着斑蛋白较宰后3 h出现显著降解(P<0.05),低pH组宰后12 h的黏着斑蛋白较宰后45 min出现显著降解(P<0.05)。相对于宰后45 min,高pH组的踝蛋白在宰后9 h出现显著降解(P<0.05),低pH组在宰后12 h才出现显著降解(P<0.05)。说明pH值的降低可能会影响骨架蛋白的降解。何凡等[27]对宰后羊肉品质的研究也表明:在宰后45 min,低滴水损失组的pH值显著高于高滴水损失组(P<0.05),且pH值的下降会导致蛋白质降解,造成较高的汁液流失率。
2.3 pH值与骨架蛋白表达水平的相关性分析结果
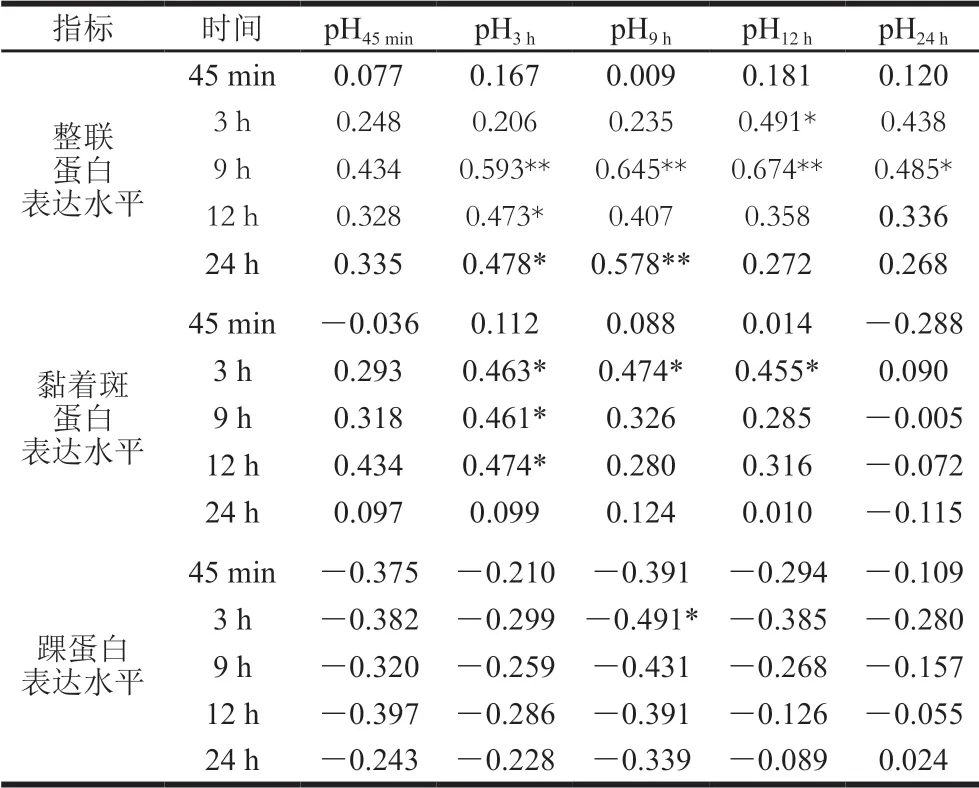
表1 pH值与骨架蛋白表达水平的相关性分析结果Table 1 Correlation analysis between pH and expression levels of cytoskeletal proteins
如表1所示,在各时间点,整联蛋白和黏着斑蛋白表达水平与pH值整体呈正相关性,踝蛋白与之相反。整联蛋白表达水平在宰后3 h与宰后12 h的pH值呈显著正相关(P<0.05),在宰后9 h与宰后3、9、12 h的pH值呈极显著正相关(P<0.01),与宰后24 h的pH值呈显著正相关(P<0.05),在宰后12 h与宰后3 h的pH值呈显著正相关(P<0.05),在宰后24 h与宰后3 h和9 h的pH值分别呈显著(P<0.05)和极显著(P<0.01)正相关。黏着斑蛋白表达水平在宰后3 h与宰后3、9、12 h的pH值呈显著正相关(P<0.05),在宰后9 h和12 h与宰后3 h的pH值呈显著正相关(P<0.05);宰后3 h的踝蛋白表达水平与宰后9 h的pH值呈显著负相关(P<0.05)。
2.4 PLSR分析结果
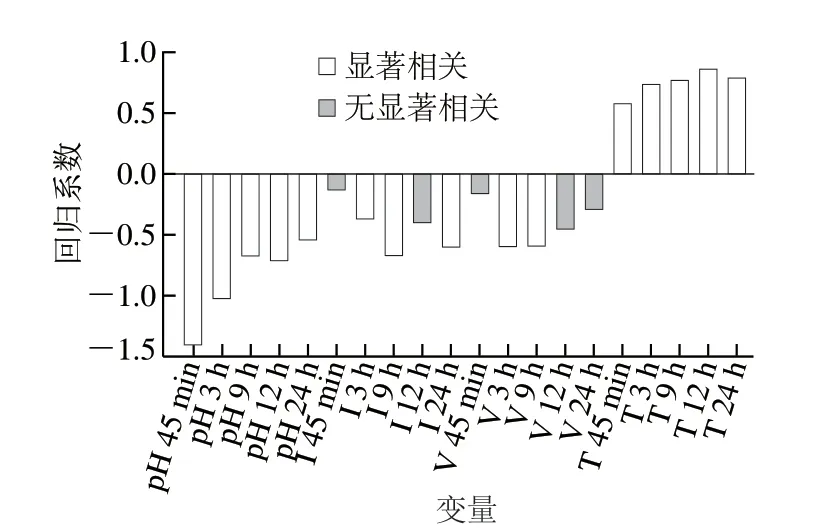
图4 pH值和整联蛋白、黏着斑蛋白和踝蛋白表达水平与汁液流失率的PLS1模型分析Fig.4 Regression coefficient of the PLS1 model explaining variance in drip loss versus pH and expression levels of integrin, vinculin and talin
为探究pH值和骨架蛋白与汁液流失率的关系,将各时间点的pH值和骨架蛋白表达水平与汁液流失率建立PLS1回归模型。如图4所示,汁液流失率与各时间点的pH值都呈显著负相关,与宰后3、9 h和24 h的整联蛋白表达水平呈显著负相关,与宰后3 h和9 h的黏着斑蛋白表达水平呈显著负相关,与宰后45 min~24 h 的踝蛋白表达水平呈显著正相关(P<0.05)。说明宰后猪肉中pH值的降低、整联蛋白和黏着斑蛋白的降解会增加汁液流失,而踝蛋白的降解有利于减少汁液流失。Brewer[2]也认为,高持水性的肉具有较高的pH值,pH值的变化以及整联蛋白、黏着斑蛋白和踝蛋白等骨架蛋白的降解会对持水性产生影响;Zhang Wangang等[28]的研究表明宰后1 d的整联蛋白表达水平与汁液流失率呈显著负相关(P<0.05);Bee等[6]的研究表明,pH值与汁液流失率呈负相关(宰后45 min和6 h的pH值与汁液流失率的相关系数分别为-0.49和-0.56),在宰后24 h,黏着斑蛋白表达水平与汁液流失率呈显著负相关,踝蛋白表达水平与汁液流失率呈显著正相关(P<0.05),且pH值的降低会影响踝蛋白的降解,与本研究结果一致。
对变量与汁液流失率进行PLSR分析,可以简单得到变量对汁液流失率的直接贡献。如表2所示,分别对pH值、骨架蛋白表达水平与汁液流失率建立PLS1回归模型。结果显示:pH值(模型1)、整联蛋白表达水平(模型3)、黏着斑蛋白表达水平(模型4)和踝蛋白表达水平(模型5)分别占汁液流失率变异的77%、41%、44%和34%。
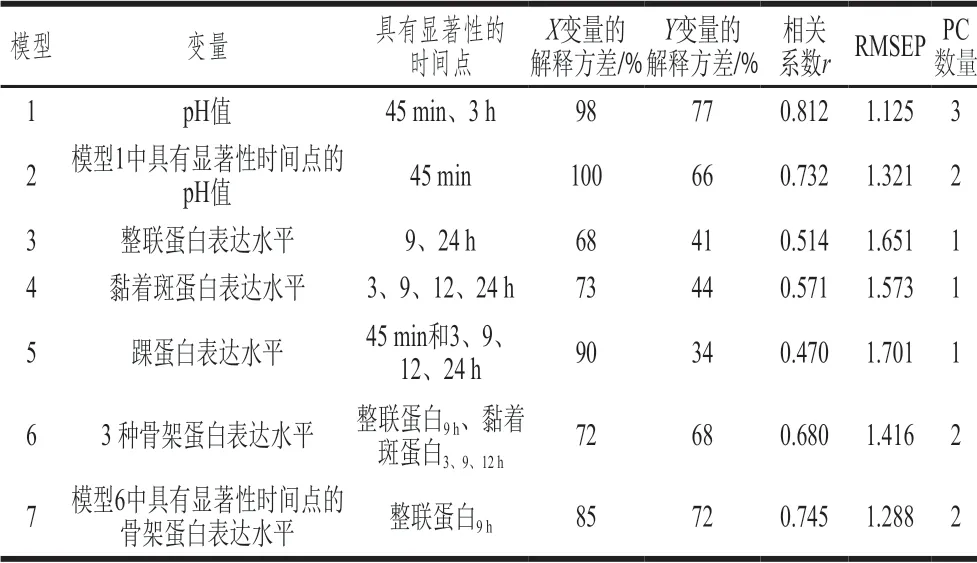
表2 测量参数(X变量)分别解释汁液流失率(Y变量)方差的PLS1模型Table 2 Figures of merit of PLS1 models for each independent variable to explain variance in drip loss
为进一步明晰pH值和3 种骨架蛋白在何时对汁液流失率的直接贡献较大,将各时间点的pH值与汁液流失率建立PLS1回归模型1,排除不显著变量后继续建立PLS1回归模型2,该模型主要由宰后45 min的pH值控制,且占汁液流失率变异的66%,说明宰后45 min的pH值对汁液流失率的影响较大;将3 种骨架蛋白表达水平与汁液流失率建立PLS1回归模型6,排除不显著变量后继续建立PLS1回归模型7,该模型主要由宰后9 h的整联蛋白表达水平控制,且占汁液流失率变异的72%,说明在3 种骨架蛋白中,宰后9 h的整联蛋白表达水平对汁液流失率的影响较大。
3 讨 论
基于宰后45 min猪背最长肌的pH值对其进行分组后,高pH组的pH值在宰后12 h内极显著高于低pH组(P<0.01)(图3A);高pH组的汁液流失率极显著小于低pH组(P<0.01)(图2);宰后45 min~24 h的pH值与汁液流失率呈显著负相关(P<0.05)(图4)。说明pH值越低,猪肉的持水性越差。此结果与谢华等[29]的研究一致。魏心如等[30]通过相关性分析也发现宰后24 h的pH值与压榨损失率和滴水损失率均呈显著负相关(P<0.05),指出提高pH值有助于保持冷却鸡肉的持水性。最近Watanabe等[31]的研究也表明pH值是影响猪肉持水性最重要的因素之一,与汁液流失率呈极显著负相关(P<0.01)。
在宰后45 min~24 h,高pH组的整联蛋白和黏着斑蛋白表达水平高于低pH组,踝蛋白表达水平低于低pH组,且高pH组的整联蛋白和黏着斑蛋白降解速率较低pH组慢,踝蛋白降解速率较低pH组快(图3B~D)。pH值与整联蛋白和黏着斑蛋白表达水平整体呈正相关性,与踝蛋白表达水平整体呈负相关性(表1)。说明pH值降低越快,整联蛋白和黏着斑蛋白的降解越多,踝蛋白降解越少。Brewer[2]和Lonergan[32]等也认为pH值会通过调节钙蛋白酶的活性从而影响骨架蛋白降解。
在所研究的骨架蛋白中,9 h的整联蛋白表达水平对汁液流失率的影响最大(表2,模型7)。这可以从Lawson[9]和Zhang Wangang[28]等的研究中得到解释:由于整联蛋白的特殊位置,当整联蛋白降解时,膜和黏附结构被破坏,肌细胞/膜之间的相互作用减弱,形成汁液流失通道,增加汁液流失。因此,完整的整联蛋白能起到阻止汁液流失通道开放、减少宰后猪肉汁液流失的作用。但pH值的降低比骨架蛋白降解对持水性的影响更大。因为pH值的变化会影响骨架蛋白的降解,且在图4多变量模型中各时间点的pH值都对汁液流失率产生较大的负作用,并单独解释了汁液流失率变异的77%(表2,模型1),大于骨架蛋白对汁液流失率的贡献。考虑到简单实用性和预测准确性,宰后45 min的pH值可以作为宰后猪肉汁液流失率的预测指标。因为单独对pH值与汁液流失率进行PLS1回归分析,剔除不显著变量后只有宰后45 min的pH值对汁液流失率有显著影响(表2,模型2)。Hamoen等[33]的研究也表明pH值是预测宰后肉品质的可靠指标。Schäfer等[16]的研究表明pH值可以解释汁液流失率变异的85%,宰后2 h内的pH值可以用于预测汁液流失率。
综上,宰后猪肉中pH值的高低会通过影响细胞骨架完整性,进而影响最终产品的持水性。pH值的降低对猪肉持水性的影响较骨架蛋白降解影响更大,且宰后45 min的pH值可以用于预测宰后猪肉汁液流失率。

