营养素、肠道菌群与健康
梁玉慧 郑钜圣
肠道菌群存在于我们每个人的肠道中,虽然看不见也摸不着,却时刻在发挥重要的作用。虽然它们是“菌”,却可以与人类和平相处。它们受到基因、饮食营养、药物、生活方式等各种环境因素的影响,同时也对我们的健康起着重要的调节作用。
肠道菌群与健康
我们的肠道里生活着数万亿的微生物,包括细菌、真菌、病毒和其他单细胞生物等,统称为肠道菌群。它们是人体内环境的重要组成部分,重量可达1~2公斤,被视为人体的另一个“器官”。肠道内数量庞大的微生物与宿主之间存在着重要的相互作用。近年来,随着测序技术的发展和多组学检测的深入,人们对肠道微生物的了解也越来越具体。目前已经发现,肠道菌群不仅会影响人体对食物的消化和对营养的吸收,同时也在人类各种疾病,包括肥胖症、心血管疾病、2型糖尿病、癌症和阿尔茨海默病等神经系统疾病中扮演着重要的角色。自2013年至今,有超过3万篇科学论文涉及肠道菌群,足以证明它对于人类健康的重要性[1]。
肠道菌群从婴儿出生便开始逐渐建立,母亲的阴道、母乳、产房的环境等都会影响肠道菌群的定植。随着婴儿慢慢地生长发育和多样化辅食的添加,人体内肠道菌群的多样性和丰富度逐渐增加并趋于相对稳定。然而,肠道菌群由于受到人类宿主生活方式和饮食习惯的影响仍处于动态变化中,并且饮食营养逐渐成为影响肠道菌群最重要的因素之一。世界上不存在相同的两片树叶,同样也不存在两个相同的肠道菌群个体。事实上,即使是年龄和人体特征相仿的健康个体,其肠道菌群也有很大的差异,这就导致至今对于“健康”的肠道菌群仍然没有一个很明确的定义。通常,人们认为存在较少的致病菌、同时具有较高多样性和丰富度的肠道菌群是相对健康的。
肠道菌群的多样性和丰富度与人体健康之间存在着密切的关系。在不同的研究中均发现,与健康对照组相比,患炎症性肠病、克罗恩病、2型糖尿病、肥胖癥、湿疹和阿尔茨海默病等人群的肠道菌群多样性较低,而且具有与健康对照组不同的肠道菌群组成。目前已有大量以疾病为中心的研究,试图找到特定的微生物或者微生物群作为生物标记物用于疾病的诊断。饮食作为肠道菌群结构组成的决定因素之一,与身体健康密切相关,也已成为人们关注的热点。
营养素与肠道菌群
营养素主要是指为了维持人体生长发育、繁殖等一切自然生命活动和过程而需要从食物中摄取的物质。人体对营养素的消化和吸收主要发生在胃肠道。而大多数微生物居住在消化道较远端的地方,在那里每克生物量就有超过1011个细胞。在大部分营养物质(宿主能消化的)被吸收后,大多数的肠道微生物就会暴露在剩余食物中,包括宿主无法消化的膳食纤维和其他食物残渣。肠道菌群再进一步利用这些营养物质合成部分维生素、必需氨基酸以及短链脂肪酸等重要的代谢副产品,以促进宿主的身体健康。而短链脂肪酸的副产物,如丁酸盐、丙酸盐和乙酸盐等又可以作为肠上皮细胞的主要能量来源。
蛋白质、脂质、碳水化合物、维生素、矿物质等作为主要的营养素,是维持机体正常生命活动的基础,同时对肠道菌群的结构组成和功能也有着重要的影响。饮食中所包含的营养素的种类和数量不仅会直接影响宿主体内肠道菌群的组成,同时也会通过影响宿主的新陈代谢和免疫系统,间接地塑造肠道菌群。
膳食蛋白可被蛋白酶和肽酶水解,在肠道中生成氨基酸、二肽和三肽,这些消化产物会被某些微生物利用或被小肠的肠细胞吸收。微生物群和宿主之间的氨基酸交换可能是双向的,肠道菌群在膳食蛋白的消化吸收和氮循环过程中扮演着重要的角色。而未被消化的氨基酸通常不被结肠细胞吸收,而是通过肠道菌群发酵成大量的细菌代谢物或其他终产物,如短链脂肪酸、硫酸氢和氨等。在一项以职业橄榄球运动员和普通健康男性作为对照的观察研究中发现,蛋白质的摄入量与肠道菌群多样性呈正相关。另外一项研究比较了欧洲儿童和非洲农村儿童的肠道菌群,结果发现摄入更多动物蛋白(肉、蛋、奶酪等)的欧洲儿童肠道中拟杆菌属和另枝菌属的细菌丰度更高。同样在一项对成年人进行饮食干预的研究中也发现,富含动物蛋白的饮食模式会导致肠道菌群中拟杆菌属和嗜胆菌属的丰度也有所增加,而罗斯拜瑞氏菌、直肠真杆菌和布氏瘤胃球菌的丰度却有所减少[2]。此外,多项临床研究发现,炎症性肠病患者粪便中的直肠真杆菌丰度低于健康受试者。而在一项大规模的前瞻性研究中发现,高蛋白质,尤其是动物蛋白质的摄入量与炎症性肠病的发生率显著升高有关。这些研究证据表明蛋白质、肠道菌群和人体健康之间有着密切的关系。
食物中主要的脂肪类型是饱和脂肪和不饱和脂肪,大多数膳食油脂中都包含着不同比例的饱和脂肪和不饱和脂肪。研究发现,摄入较高的饱和脂肪和反式脂肪会升高血液中的总胆固醇和低密度脂蛋白含量,进而增加心血管疾病的患病风险。而有益健康的脂肪,如单不饱和脂肪和多不饱和脂肪则能够降低慢性疾病的患病风险。典型的西方饮食中饱和脂肪和反式脂肪含量高,单不饱和脂肪和多不饱和脂肪含量低,因此容易引发诸多健康问题。研究显示,高脂饮食会增加厌氧微生物总量以及拟杆菌属的细菌数量,而低脂饮食会在双歧杆菌丰度增加的同时,降低人体空腹血糖和总胆固醇含量。在一项为期6个月的干预研究中发现,低脂饮食与肠道菌群多样性增加有关,而高脂饮食与粪杆菌属的减少,以及另枝菌属和拟杆菌属的增加有关[3]。研究人员对饮食组成分别为高脂肪、低纤维与高纤维、低脂肪的受试者肠道菌群进行比较时,发现后者的肠道菌群中具有更丰富的普雷沃菌属,而目前的证据表明,这种细菌都是对人体健康有益的微生物。进一步通过前瞻性队列研究发现,主要来自食用油的n-6多不饱和脂肪酸与糖尿病患病风险呈正相关,与肠道菌群多样性呈负相关。因此,过多地摄入n-6不饱和脂肪酸很可能对肠道菌群的组成和功能产生不利影响,从而增加糖尿病的患病风险[4]。
碳水化合物是目前在肠道菌群相关研究中出现频率相对较高的营养素。它可以分成两类:可消化的和不可消化的。可消化的碳水化合物包括淀粉和糖,如葡萄糖、果糖、蔗糖和乳糖等,它们在小肠中被酶降解;不可消化的碳水化合物包括膳食纤维和抗性淀粉,在小肠中不能被酶降解,它们会到达大肠,在那里被微生物发酵。在我国蒙古族人群中开展了一项观察研究:第1周,志愿者先将小麦作为主食,研究人员发现其肠道中链状双歧杆菌、两歧双歧杆菌的数量显著增加。接下来的第2周和第3周,志愿者分别以大米和燕麦为主食,第2周后,发现其肠道中青春双歧杆菌、长双歧杆菌、魏斯氏菌和黏滑罗斯菌的丰度急剧下降,而第3周后却又急剧上升[5]。还有其他的研究表明,富含高纤维的饮食干预,包括全谷物、菊粉、低聚果糖混合纤维、可溶性玉米纤维及全麦面包等,不仅会增加肠道微生物的多样性,而且也会增加粪便中一些有益的微生物,如双歧杆菌、乳酸菌、艾克曼菌、普拉梭菌、罗斯拜瑞氏菌和普氏菌等的含量。而这些微生物能够发酵膳食纤维,从而生成乙酸盐、丙酸盐和丁酸盐等短链脂肪酸。这些短链脂肪酸不仅能够通过激活G偶联受体调控宿主代谢、改善胰岛素敏感性、促进葡萄糖稳态,同时还能与免疫因子相互作用,维持肠道免疫稳态。
除了以上提到的蛋白质、脂肪和碳水化合物等宏量营养素之外,维生素和矿物质等微量营养素对人体健康同样至关重要,科学家们也围绕着微量营养素与肠道菌群及人类健康的关系展开了一系列研究[6]。尽管有关营养素的研究对于理解饮食与健康具有重要的作用,在过去几十年里也取得了很好的进展,然而,当代营养学研究已经从对营养素的研究转为对膳食模式和食物本身的研究,因为没有营养素是孤立起作用的。因此,对于营养素与肠道菌群关系的研究也转为对饮食模式与菌群结构及健康关系的研究。如近几年不少证据表明地中海饮食模式能够通过改善肠道菌群,进一步促进机体代谢健康。该饮食模式以均衡地摄入水果、谷物、蔬菜以及单不饱和脂肪和多不饱和脂肪为基础。一项在肥胖人群中开展的研究发现,在坚持地中海饮食一年之后,受试者肠道内罗斯氏菌属和颤螺菌属的丰度增加,而这两种都是对人体相对有益的微生物。
营养素、肠道菌群与疾病:因果关系还是相关关系?
尽管有诸多基于模式生物开展的机理研究机制和探索证明了肠道菌群对人类疾病及健康的影响,然而大部分菌群与疾病的因果关系并没有在人类身上进行过验证。同样,关于营养素与肠道菌群的研究也没有源于人类的充分证据,以往小样本的人类干预试验往往局限于益生菌及益生元领域,没有很好的外推性。从证据等级的角度上看,基于人群的随机对照试验和前瞻性队列是最佳的研究方式,而这两种方式的应用在营养素与菌群领域仍然相当有限,也就是说,目前的研究证据等级相对较低,绝大部分相关研究有待进一步开展。
因此,有关营养素、肠道菌群与疾病的研究应该遵循三步走策略:一是积累更多大样本量的人群证据,比如利用横断面或病例对照的研究方式进行观察和探索;二是利用跟踪随访的方式,研究饮食营养的变化对肠道菌群的影响,以及肠道菌群随着时间的变化与疾病的关系;三是利用随机对照的方式,研究探索营养素对肠道菌群和疾病的影响,或者基于人群队列和孟德尔随机化分析研究营养素、肠道菌群和疾病三者之间的因果关系。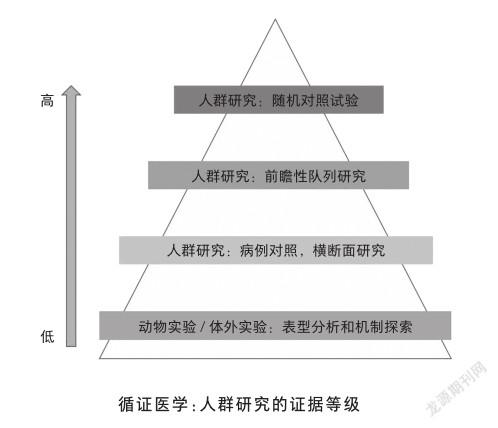
此外,当前有关肠道菌群与健康以及营养素与肠道菌群的研究绝大部分仍局限于肠道细菌范围,而细菌仅仅是肠道菌群的一个组成部分,因此,可将肠道中的病毒、真菌与人类健康作为未来的研究方向。比如真菌控生作用理论就提出了由真菌来调控肠道菌群和宿主生态的全新理论[7]。近年来,基于人群的关于肠道真菌组相应的描述性工作正在慢慢展开,关于肠道病毒组的越来越多的研究工作也在逐步开展。期待这些方向能进一步推动营养素、肠道菌群与疾病的研究发展,为营养学及其相关领域研究提供新的思路。[1]Valdes A M, Walter J, Segal E, et al. Role of the gut microbiota in nutrition and health. British Medical Journal. 2018, 361: k2179.
[2]Riaz M S, Shi J, Mehwish H M, et al. Interaction between diet composition and gut microbiota and its impact on gastrointestinal tract health. Food Science and Human Wellness, 2017, 6(3): 121-130.
[3]Wan Y, Wang F, Yuan J, et al. Eff ects of dietary fat on gut microbiota and faecal metabolites, and their relationship with cardiometabolic risk factors: a 6-month randomised controlled-feeding trial. Gut, 2019, 68(8): 1417-1429.
[4]Miao Z, Lin J S, Mao Y, et al. Erythrocyte n-6 polyunsaturated fatty acids, gut microbiota, and incident type 2 diabetes: A prospective cohort study. Diabetes Care, 2020, 43(10): 2435-2443.
[5]Li J, Hou Q, Zhang J, et al. Carbohydrate staple food modulates gut microbiota of mongolians in China. Front Microbiol, 2017, 8: 484.
[6]Yang Q, Liang Q, Balakrishnan B, et al. Role of dietary nutrients in the modulation of gut microbiota: A narrative review. Nutrients, 2020, 12(2).
[7]Zheng J S, Wahlqvist M L. Regulobiosis: A regulatory and food system-sensitive role for fungal symbionts in human evolution and ecobiology. Asia Pacifi c Journal of Clinical Nutrition, 2020, 29(1): 9-15.
關键词:肠道菌群 营养素 健康 ■

