基于美国FAERS数据库的托珠单抗不良事件信号挖掘
罗林 张佳颖 陈力 龙恩武
摘要目的:挖掘托珠单抗的不良事件(ADE)信号,为其临床安全合理使用提供参考。方法:收集美国FDA不良反应报告系统中2015 年第1 季度至2020 年第2 季度共22 个季度的托珠单抗相关ADE报告数据,经数据标准化后,采用比例失衡法进行ADE信号挖掘。结果:共提取以托珠单抗为首要怀疑药物的ADE报告163 718 份,涉及患者26 674 例。在26 674 例患者中,女性所占比例(73.69%)高于男性(19.04%),年龄以60~74 岁(21.19%)为主。在163 718 份ADE報告中,报告国家以美国(70.15%)、加拿大(15.95%)、日本(3.33%)、澳大利亚(3.05%)、巴西(1.43%)为主;消费者(31.35%)和医师(24.94%)是主要上报人群。共挖掘出托珠单抗ADE信号747 个,以类风湿性关节炎、关节痛、疼痛等较为常见,以残疾评估量表分数增加、残疾评估量表分数降低、舒张压异常、收缩压异常等信号较强;共发现托珠单抗药品说明书中未记录的ADE信号共33 种,以血氧饱和度降低、血压降低、心率异常等实验室指标异常为主。ADE主要累及的系统器官共27 个,涉及肌肉骨骼及结缔组织、全身性疾病以及给药部位各种反应、各类检查等。结论:临床应用托珠单抗时,除关注药品说明书中已提及的ADE外,还应密切关注血氧饱和度、血压、血常规等各项实验室指标,并在ADE发生时及早采取干预措施,以保证患者用药安全有效。
关键词托珠单抗;美国FDA不良事件报告系统;比例失衡法;不良事件;信号挖掘
ABSTRACT OBJECTIVE:To provide reference for clinical safe and rational drug use by mining adverse drug events(ADE)signals for tocilizumab. METHODS:Data of ADE reports related to tocilizumab in the first quarter of 2015 to second quarter of2020 were collected from US FDA adverse event reporting system. After data standardization,the proportional imbalance methodwas used for ADE signal mining. RESULTS:A total of 163 718 ADE reports were extracted,in which tocilizumab was primarysuspected drug,involving 26 674 patients. In 26 674 patients,the proportion of female(73.69%)was higher than that of male(19.04%),and the age was mainly 60-74 years old(21.19%). Among the 163 718 ADE reports,the main reporting countrieswere the United States (70.15%),Canada (15.95%),Japan (3.33%),Australia (3.05%) and Brazil (1.43%);consumers(31.35%) and doctors (24.94%) were the main reporting staff. A total of 747 ADE signals for tocilizumab were obtained,commonly rheumatoid arthritis,joint pain and pain;and the signals as the increase of disability assessment scale score,thedecrease of disability assessment scale score,abnormal diastolic blood pressure and abnormal systolic blood pressure were strong. Atotal of 33 kinds of ADE signals were found,which were not recorded in the instructions of tocilizumab,and mainly abnormallaboratory indicators such as decreased oxygen saturation,decreased blood pressure and abnormal heart rate. ADE mainly involved27 system organs,including musculoskeletal and connective tissue,various reactions of systemic diseases and drug delivery site,various examinations. CONCLUSIONS:In addition to the ADE mentioned in the drug instructions,when using tocilizumab inclinic,attention should also be paid close to blood oxygen saturation,blood pressure,blood routine indexes and other laboratoryindicators,and intervention measures should be taken earlywhen ADE occurs,so as to ensure the safety and effectivenessof drug use.
KEYWORDS Tocilizumab;US FDA adverse event reportingsystem;Proportional imbalance method;Adverse drug events;Signal mining
白细胞介素6(interleukin-6,IL-6)是一个多功能促炎细胞因子,与类风湿性关节炎(rheumatoid arthritis,RA)的发生密切相关[1]。托珠单抗(tocilizumab)是全球首个针对IL-6 受体的人源化单克隆抗体,可通过抑制IL-6 受体的活性来阻断IL-6 通路的信号转导,从而减轻患者的全身炎症,最终降低其疾病活动度,缓解相关症状并保护其关节[2]。自2008 年起,托珠单抗陆续在日本、美国和欧洲各国获批上市,并于2013 年首次获得国家食品药品监督管理总局批准在我国上市,用于治疗RA。2016 年,托珠单抗以豁免Ⅲ期临床试验的形式获批新适应证,成为我国首个获批用于全身型幼年特发性关节炎的生物制剂[3]。
2020 年3 月,国家卫生健康委发布《新型冠状病毒肺炎诊疗方案(试行第7 版)》,新增托珠单抗作为免疫治疗药物,用于双肺广泛病变及重型且实验室检查示IL-6水平升高的患者[4]。此次新增适应证的应用使托珠单抗临床用量倍增,也使其成为了相关临床研究的热点之一[5]。但针对该药新增适应证的相关临床研究才刚启动,前期临床研究数据十分有限,且目前尚未见基于相关数据库进行不良事件(adverse drug events,ADE)信号挖掘的研究。因此,为了提高ADE信号的检出能力,减少数据选择带来的偏倚,本文主要利用比例失衡法(measures of disproportionality)中常用的3 种方法[报告比值比法(reporting odds ratio,ROR)、比例报告比值法(proportional reporting ratio,PRR)和英国药品及保健品管理局(Medicines and Healthcare Products RegulatoryAgency,MHRA)的综合标准法(以下简称“MHRA法”)],对美国FDA 不良事件报告系统(FDA adverse events reportingsystem,FAERS)收集的托珠单抗相关数据进行挖掘和筛选,分析托珠单抗可疑的ADE信号,以期为该药的临床安全合理应用提供参考。
1 资料与方法
1.1 数据来源
本研究所用数据库为FAERS(https://fis.fda.gov/extensions/FPD-QDE-FAERS/FPD-QDE-FAERS.html)。FAERS 的数据来源为自发呈报系统(spontaneous reportingsystem,SRS),即由报告者(卫生健康从业人员或患者)自发报告的ADE信息[6]。收集FAERS数据库中2015年第1 季度至2020 年第2 季度共22 個季度的相关数据,提取患者基本信息、药品使用信息、ADE、预后情况、报告来源、日期和报告国家/地区等信息。笔者以美国FDA官网批准和维基百科上所有关于托珠单抗的商品名及通用名为关键词,从FAERS数据库下载对应季度的美国信息互换标准代码(American standard code for informationinterchange,ASCII)数据包,导入MySQL5.7 数据库,经过核对个人信息记录(demo)去重,筛选“drugname”项符合“托珠单抗”的ADE。
1.2 数据标准化
本研究采用国际医学科学组织理事会国际医学用语词典(Medical Dictionary for Regulatory Activities,MedDRA)中药物不良反应术语集的首选系统器官分类(system organ class,SOC)和首选术语(preferred term,PT)对ADE 进行分类和描述;使用MedDRA 23.0 软件进行PT、高位语(high level term,HLT)、高位组语(highlevel group term,HLGT)、SOC编码及中英文映射。
1.3 数据挖掘方法
目前,国内外用于药品ADE信号检测的数据挖掘方法主要是比例失衡法[7]。该法的原理是比较目标药物-事件的出现频率与背景频率的差异,即在1 个包含所有药物事件报告的数据库中,当目标药物-事件组合的出现频率明显高于整个数据库的背景频率,并且达到了设定的阈值,就认为产生了1 个信号[8]。
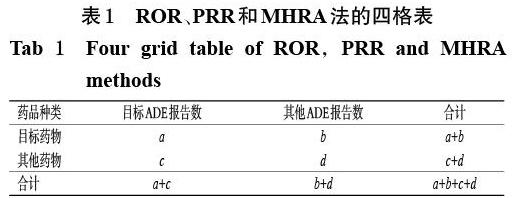
本研究同时应用ROR、PRR 和MHRA法进行信号挖掘[9-11]。3 种方法均基于四格表(表1),通过比较目标药物(托珠单抗)的ADE报告数和其他所有药物的ADE报告数(背景数据)来判断是否“失衡”,以此挖掘潜在的ADE信号[12];同时,3 种方法联用可以降低假阳性和假阴性信号的数量,提高结果的可靠性[13]。
1.4 数据的计算与筛选
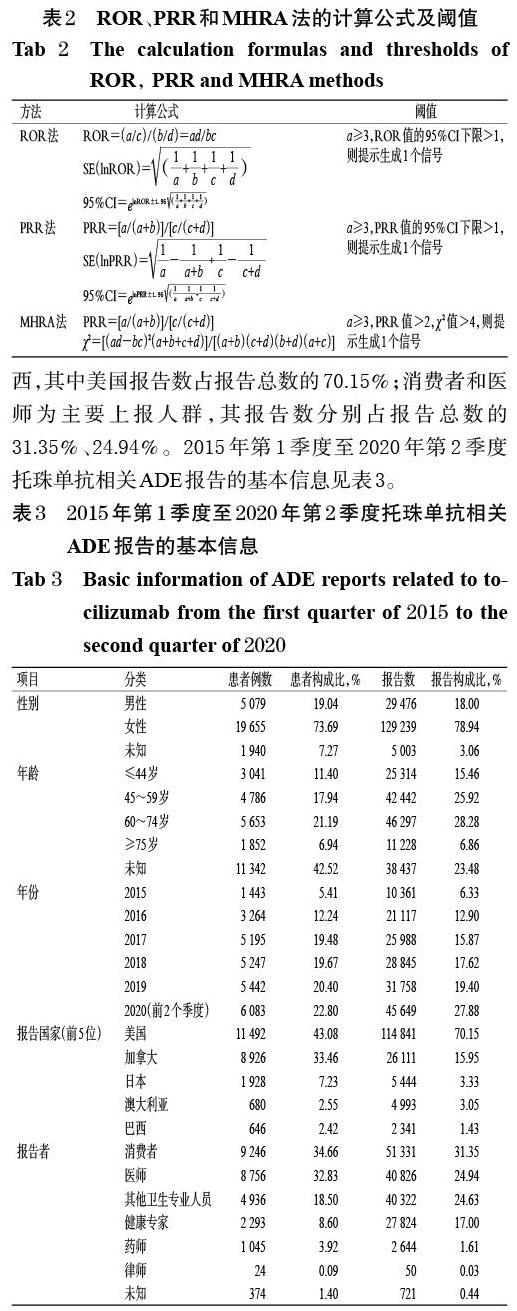
对上述标准化后的术语进行统计,筛选出报告数大于3 例的数据。根据上述四格表(表1),计算出对应的ROR值、PRR 值、χ2值和相应的95%置信区间(CI)下限并统计信号数,排除不满足阈值要求的报告。其中,ROR值的95%CI 下限越大,信号就越强,说明目标药物与目标ADE 之间的联系就越强[14 - 15]。ROR、PRR 和MHRA法的计算公式及阈值[16]见表2。
2 结果
2.1 ADE报告的基本信息
2015-2020 年共22 个季度的ADE 背景信号共有24 359 117 个,从中筛选出“drug name”项为“托珠单抗”且为首要怀疑药物的报告共163 718 份,涉及ADE种类共3 953 种、患者共26 674 例。在26 674 例患者的报告中,女性所占比例(73.69%)高于男性(19.04%),年龄主要集中于60~74 岁(21.19%);2015-2020 年ADE报告分别涉及1 443、3 264、5 195、5 247、5 442、6 083 例患者,呈逐年递增的趋势。在163 718 份ADE报告中,报告数据前5 位的国家分别是美国、加拿大、日本、澳大利亚、巴西,其中美国报告数占报告总数的70.15%;消费者和医师为主要上报人群,其报告数分别占报告总数的31.35%、24.94%。2015 年第1 季度至2020 年第2 季度托珠单抗相关ADE报告的基本信息见表3。
2.2 ADE信号挖掘结果
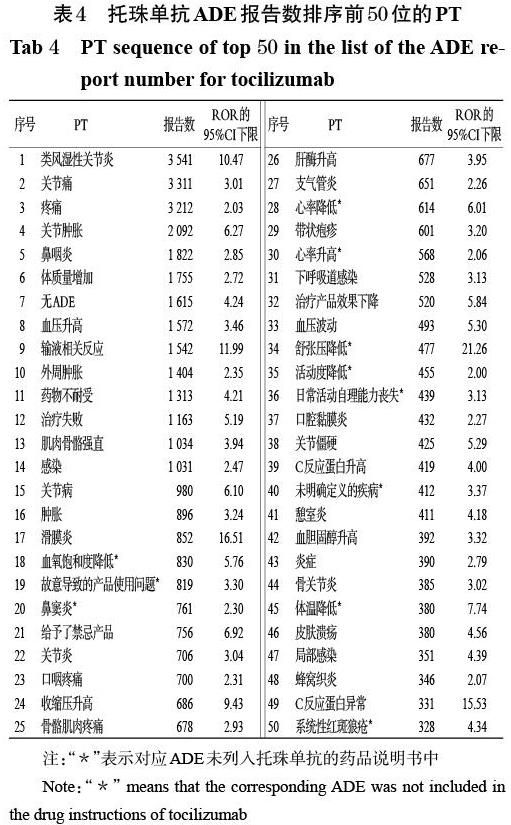
对以托珠单抗为首要怀疑药物的ADE信号进行筛查,经ROR、PPR和MHRA法筛选最终获得信号747 个,PT报告总数为71 301 个。在有信号的PT中,以ROR法为例(ROR、PRR和MHRA法在特异度和信号检测能力上具有很好的一致性,且ROR法的灵敏度较高[14]),ROR值及其95%CI 下限越大,说明信号强度越大[14-15],分别按该ADE的报告数(a 值)和信号强度(ROR值的95%CI下限)的前50 位进行PT 排序,结果见表4、表5。其中,较常见的ADE为类风湿性关节炎、关节痛、疼痛等;而相关性较高(即信号较强)的ADE为残疾评估量表分数增加、残疾评估量表分数降低、舒张压异常、收缩压异常等。此外,也挖掘出了未列入其药品说明书的一些ADE信号,共33种,如心率降低/升高、舒张压降低等。
2.3 ADE累及的系统器官
根据MedDRA对有信号的PT 进行SOC分类排序,结果发现有信号的SOC共27 个,分类后各SOC的信号数、ADE报告数及其构成比情况见表6。在71 301 份报告中,各种累及肌肉骨骼及结缔组织的疾病的ADE报告数最多(如类风湿性关节炎、关节痛、关节肿胀等),共计18 114 份,占25.41%。此外,报告数较多的SOC还有全身性疾病及给药部位各种反应(如疼痛、外周肿胀、药物不耐受等)、各类检查(如体质量增加、血压升高、血氧饱和度降低等)、感染及侵染类疾病(鼻咽炎、感染、鼻窦炎)等,分别为12 602、12 402、10 550 份。
3 讨论
本研究所得到的托珠单抗ADE信号与已知的安全性信息基本一致[17],其ADE主要集中于感染、用药部位反应、实验室检查异常和胃肠道、呼吸、皮肤疾病等方面,包括带状疱疹、外周肿胀、胃炎、血压异常、间质性肺疾病、皮肤溃疡等。这些ADE与药品说明书收录基本相同,也与一些文献分析、临床研究的结果相似[18-19],证明了本研究方法的可行性及结果的可靠性。
3.1 托珠单抗致ADE发生的人群特点
本研究共纳入托珠单抗导致的ADE报告71 301 份,共涉及26 674 例患者。在报告中,女性发生ADE的例数远远多于男性,男女比例为1 ∶3.87。有文献报道,性别在RA发病率上有极显著差异,女性发病率高于男性(约高出3 倍)[20]。因此,女性使用托珠单抗治疗的机会增加,发生ADE的概率也就随之升高。在已知年龄的患者中,各个年龄段都有ADE的发生,其中60~74 岁人群占比略高,且报告数也较大,可能与老年患者身体机能下降和日常联合用药较多有所关联[21]。2015 年第1 季度至2020 年第2 季度ADE报告数逐年递增,其中2020 年仅2个季度的ADE 报告数就多于2015-2019 年的总报告数,其原因主要是突发新型冠状病毒肺炎疫情造成托珠单抗临床需求快速增长,故临床和公众对该药的安全性更为关注。ADE的报告国家中,美国、加拿大报告数占比较高(分别为70.15%、15.95%),可能与白种人RA发病率较其他人种更高有关[22],但目前尚未有直接的证据表明RA发病率与种族的关系,其关联性有待进一步研究。此外,我国尚未建立ADE数据库,缺乏相应的研究数据,故借助FAERS为我国患者合理使用托珠单抗提供客观资料,可有助于降低用药风险。消费者和医师为主要上报人群,其上报的报告数分别占报告总数的31.35%、24.94%。可见,通过临床工作者和患者上报ADE是药物上市后ADE监测的主要形式之一,其监测范围较广,并有助于提高数据的可利用性[23]。
3.2 托珠单抗的ADE信号
3.2.1 ADE 信号累及的系统器官本研究经过ROR、PRR 和MHRA法分析发现,托珠单抗较强的ADE信号是各种肌肉骨骼、结缔组织疾病和全身性疾病及给药部位各种反应,但由于该药主要适用于关节炎患者人群的临床治疗,因此患者出现的骨骼肌肉疼痛肿胀、行动不便等症状可能与病情本身相关,暂无法判断相关ADE是否是由药品直接产生的[24]。此外,托珠单抗作为生物制剂,其免疫原性是其主要的安全性问题之一,可能会引发患者免疫反应、皮肤反应等,若患者出现上述几方面的损害时,临床应优先考虑与托珠单抗有关并提高警惕[25]。同时,ADE 信号较强的还有各类实验室检查异常、胃肠系统疾病,其中包括血压升高、胆固醇升高、肝功能异常、血常规异常、胃肠穿孔等,与药品说明书中托珠单抗常见的ADE一致,提示临床医务工作者应对使用托珠单抗治疗的患者进行定期监测,一旦出现相关ADE时应及时予以干预。另外,生物制剂相关的免疫反应还包括全身炎症反应、感染及侵染类疾病,上述疾病也是托珠单抗较强的安全信号之一。有研究显示,接受托珠单抗治疗的患者会发生因细菌、侵袭性真菌、病毒等病原体引起的严重感染,且严重感染的发生率较高[26]。因此,若患者合并有高龄、多种基础疾病、免疫力低下等使感染风险加剧的因素时,临床应慎用托珠单抗[27]。
3.2.2 新的ADE信號本研究发现了未列入托珠单抗药品说明书的ADE信号共33 种。其中,在ADE发生频次排序前50 位的PT中新的ADE信号有11 种(33.33%,11/33),在信号强度排序前50 位的PT 中新的ADE信号有22 种(66.67%,22/33)。值得关注的是,实验室检查指标异常有13 种(39.39%,13/33),主要包含血氧饱和度降低、血压降低、体温降低、心率异常、身高低于正常、凝血异常等,均是其药品说明书未提及的内容;同时,上述ADE信号较强,与托珠单抗的相关性亦较强,提示临床在使用托珠单抗时应注意对患者进行相关指标的监测,并重点关注用药后患者各种实验室检查数据的异常情况。除此之外,产品的储存错误及使用问题也是该药的ADE信号之一。有研究显示,托珠单抗的输液反应发生率为6.9%,若储存条件不当或装置材料浑浊都可增加该ADE出现的概率[28]。根据托珠单抗注射液药品说明书,其应在2~8 ℃的冰箱中避光保存,且应现配现用[29]。因此,临床医务工作者在托珠单抗应用过程中应严格遵循其药品说明书的要求,同时应加强对相关产品储存知识的了解,以保障患者用药安全。
3.3 本研究的局限性
本研究为上市后ADE信号研究,数据来源于真实世界且样本量大,是评价药品安全风险的关键方法[30]。但本研究仍存在一定的局限性:首先,FAERS数据库的数据大多来源于欧美人群,来源于亚洲人群的较少,因此研究结果可能与我国实际情况有所差异;其次,FAERS数据库的部分数据存在缺失、错误、质量不高等情况,可能会使研究结果出现误差。另外,为了减少遗漏的信号、降低假阳性和假阴性信号的数量,本研究联用了比例失衡法中的ROR、PRR和MHRA法。其中,ROR法的主要优点是计算简单,可分析药品交互作用导致的ADE;其缺点在于当目标药物仅引发目标ADE 而未见其他ADE 的情况下,不能计算ROR 值[31]。PRR 法的分析原理与ROR法类似,但在报告数较少的情况下不易分析、解释结果,且易出现假阳性信号[32],加之该法受限于相关报告数量,故常与其他数据挖掘方法联合使用。
MHRA法是在PRR法的基础上综合考虑了多个指标,方法更为严谨[33]。本文虽然采用多种方法进行综合评价,并以ROR值及其95%CI 下限进行结果展示,但若要在实际临床中判断目标药物与目标ADE是否具有关联性,仍需要进一步的评估。
4 结语
本研究基于美国FAERS数据库,利用比例失衡法对托珠单抗上市后的不良事件进行挖掘分析,所得到的结果与其药品说明书较为一致,如感染、用药部位反应、实验室检查异常和胃肠道、呼吸、皮肤疾病ADE发生率较高;同时,本研究也发现了一些新的ADE信号,如血氧饱和度、体温、心率、凝血方面的异常。临床在使用托珠单抗时,除关注药品说明书中已提及的ADE外,还应密切监测患者的上述各项实验室指标,并在ADE发生时及早采取干预措施,以保证患者用药安全有效、降低用药风险。托珠单抗作为免疫抑制剂,其安全性备受关注,本研究在一定程度上弥补了药品上市前临床样本的不足,也可为临床合理用药提供参考。
参考文献
[ 1 ] 姜楠,费允云,赵岩.白细胞介素-6 阻断剂在类风湿关节炎的治疗应用[J].中华临床免疫和变态反应杂志,2012,6(3):232-236.
[ 2 ] 杨兆文,曹金,张立民,等.托珠单抗在类风湿关节炎中的研究进展[J].世界临床药物,2014,35(9):523-526,546.
[ 3 ] 李永柏,刘婧,胡坚,等.生物制剂在全身型幼年特发性关节炎治疗中的应用[J].中国实用儿科杂志,2017,32(4):308-313.
[ 4 ] 国家卫生健康委.关于印发新型冠状病毒肺炎诊疗方案(试行第七版)的通知:国卫办医函〔2020〕184 号[EB/OL].(2020-03-03)[2021-01-20]. http://www.nhc.gov.cn/xcs/zhengcwj/202003/46c9294a7dfe4cef80dc7f5912eb1989.shtml.
[ 5 ] 张建红,朱立勤,刘子艳,等.托珠单抗在新型冠状病毒治疗中的临床药学指引[J].中国医院药学杂志,2020,40(10):1077-1080.
[ 6 ] 李苑雅,张艳,沈爱宗.基于自发呈报系统药品不良反应信号检测方法的研究进展[J].安徽医药,2015,19(7):1233-1236.
[ 7 ] EGBERTSAC G,MEYBOOMR H B,VAN PUIJENBROEKE P. Use of measures of disproportionality in pharmacovigilance:three Dutch examples[J]. Drug Saf,2002,25(6):453-458.
[ 8 ] 管晓东,史录文,焦立公,等.数据挖掘方法检测药品不良反应信号的应用研究[J].药物不良反应杂志,2016,18(6):412-416.
[ 9 ] 代菲,舒丽芯,储藏,等.简述分析几种信号监测方法在药物不良事件中的应用[J].药学实践杂志,2012,30(5):380-383.
[10] SUBEESH V,MAHESWARI E,SINGH H,et al. Noveladverse events of iloperidone:a disproportionality analysisin US Food and Drug Administration adverse event reportingsystem (FAERS) database[J]. Curr Drug Saf,2019,14(1):21-26.
[11] BATE A,EVANS S J W. Quantitative signal detectionusing spontaneous ADR reporting[J]. PharmacoepidemiolDrug Saf,2009,18(6):427-436.
[12] 陳炯华,魏永越,谢雁鸣.基于SRS的中药上市后安全性信号检测方法介绍[J].中成药,2010,32(6):1036-1039.
[13] 张婧媛,白羽霞,韩晟,等.数据挖掘方法检测药品不良反应信号的应用研究[J].药物不良反应杂志,2016,18(6):412-416.
[14] 陈友生,缪健,梁义敏,等.常用药品不良反应信号检测方法研究进展[J].中国药物依赖性杂志,2014,23(2):89-92.
[15] 陈力,李海龙,刘迅,等.基于美国FDA不良事件报告系统数据库的洛匹那韦/利托那韦风险信号挖掘研究[J].药物不良反应杂志,2020,22(3):180-187.
[16] SAKAEDA T,TAMON A,KADOYAMA K,et al. Datamining of the public version of the FDA adverse event reportingsystem[J]. Int J Med Sci,2013,10(7):796-803.
[17] 温晓娜,刘文生,孟舒献.托珠单抗致不良反应的文献分析[J].现代药物与临床,2020,35(8):1688-1693.
[18] 左玮,刘容吉,许秀丽,等.托珠单抗不良反应研究进展[J].临床药物治疗杂志,2020,18(3):16-20.
[19] JUSTET A,NEUKIRCH C,POUBEAU P,et al. Successfulrapid tocilizumab desensitization in a patient with stilldisease[J]. J Allergy Clin Immunol Pract,2014,2(5):631-632.
[20] 孙林梅.类风湿性关节炎常见体质类型调查及相关问题的研究[D].咸阳:陕西中医学院,2006.
[21] RASCH E K,HIRSCH R,PAULOSE-RAM R,et al. Prevalenceof rheumatoid arthritis in persons 60 years of ageand older in the United States:effect of different methodsof case classification[J]. Arthritis Rheum,2010,48(4):917-926.
[22] ENGEL A,BURCH T A. Chronic arthritis in the UnitedStates health examination survey[J]. Arthritis Rheum,2010,10(1):61-62.
[23] 张亮,付文焕.美国卫生系统药师协会药品不良反应监测及报告指南[J].中国药物警戒,2009,6(3):177-179.
[24] 苏哲,张宁.托珠单抗治疗中重度类风湿关节炎的临床研究[J].实用药物与临床,2019,22(5):526-529.
[25] 刘雪梅,王江滨,庄建阳.类风湿关节炎患者托珠单抗生物治疗所致不良反应的预防与护理[J].护理学报,2015,22(4):31-33.
[26] YOKOTA S,IMAGAWA T,MORI M,et al. Longtermsafety and effectiveness of the anti-interleukin-6 receptormonoclonal antibody tolicizumab inpatients with systemicjuvenile idiopathic arthritis in Japan[J]. J Rheumatol,2014,41(4):759-767.
[27] 吴丹纯,方蘅英,謝园园,等.托珠单抗治疗类风湿关节炎不良反应的预防护理[J].现代临床护理,2014,13(7):49-51.
[28] DE BENEDETTI F,BRUNNER H I,RUPERTO N,et al.Randomized trial of tocilizumab in systemic juvenile idiopathicarthritis[J]. N Engl J Med,2015,367(25):2385-2389.
[29] 黄天马,洪忠芹.全身型幼年特发性关节炎患儿输注托珠单抗不良反应的预防与护理[J]. 全科护理,2019,17(23):2862-2864.
[30] 郭晓昕,杜晓曦.药品风险信号的发现与上市后研究[J].中国临床药理学杂志,2011,27(8):634-641.
[31] 磨国鑫.国内药物警戒中比值失衡测定法研究与实践的回顾[J].中国药物评价,2015,32(2):118-121.
[32] 汤榕,李林贵,孙维红,等.药品不良反应报告常用信号检测方法应用研究[J].中国药房,2012,23(14):1309-1311.
[33] 任经天,王胜锋,侯永芳,等.常用药品不良反应信号检测方法比较研究[J].中国药物警戒,2011,8(5):294-298.
(收稿日期:2021-02-01 修回日期:2021-06-23)
(编辑:张元媛)

