3D打印生物活性玻璃/羟基磷灰石骨修复材料的理化性能研究
王 鑫,赵 帆,甄 平
(1.宁夏医科大学,银川 750004;2.甘肃省人民医院,兰州 730000;3.西北民族大学,兰州 730030;4.中国人民解放军联勤保障部队第九四〇医院,兰州 730000)
骨修复材料的最优解是自体骨移植,但由于其数量有限及异体骨存在排异反应,因此临床上尝试采用生物材料替代自体骨移植。多种材料均可用于制备骨修复材料,包括可降解金属材料如铁-锰支架[1]、镁合金支架[2]、多孔镁支架[3]等;与天然骨具有相似矿物成分的材料如羟基磷灰石[4]、β-磷酸三钙(β-TCP)[5]、生物活性玻璃[6]等;有机高分子材料如聚乳酸-羟基乙酸共聚物(PLGA)[7]等。这些材料在机械强度、成骨性、可降解性方面分别具有出色表现,但难以实现多方面优势的整合。羟基磷灰石因其本身为人体骨组织的主要无机物成分,作为人工骨支架修复材料已应用于临床多年[8]。研究[9-11]已证实,羟基磷灰石具有一定成骨性及生物相容性,可通过加入其他材料解决降解性较差的问题。生物活性玻璃可与人体骨组织发生键合[12-13],将生物活性玻璃加入传统陶瓷材料中有望提高其降解性能[14],但传统制作工艺如冷冻干燥法、添加造孔法无法实现材料的多孔特点[15],会对移植后的代谢、血供产生影响[16],而使用3D打印技术可解决孔隙率及孔径不可控的问题[17]。本研究设计了复合材料模型,通过3D打印技术完成生物活性玻璃/羟基磷灰石复合支架的制备,分析测试其表面形貌特征,检测其力学性能、孔隙率及降解性能,以期为骨修复材料的选择提供新的可能。
1 材料与方法
1.1 仪器与试剂
主要试剂:羟基磷灰石(中国昆山)、生物活性玻璃(北京有机化学厂);主要仪器:3D打印机(德国Envision TEC公司)、LGJ冷冻干燥机(解放军军事医学科学院实验仪器厂)、扫描电镜(Zeiss Gemini Ultra-55)、紫外分光光度仪(G1115A,美国HP公司)、万能材料力学试验机(日本SHimadzu公司)、超声破碎仪(中国上海)。
1.2 方法
1.2.1 生物活性玻璃/羟基磷灰石复合支架的制备 采用生物活性玻璃(BG%)/羟基磷灰石(HA%)BG0/HA100、BG10/HA90、BG20/HA80、BG30/HA70、BG40/HA60、BG50/HA50、BG100/HA0的配比混合液作为打印墨水。利用三周期极小曲面(triply periodic minimal surfaces,TPMS)(一种在三维空间中三个独立方向均呈周期性的极小曲面)可以制造具有复杂功能梯度的多孔结构,螺旋曲面(gyroid,G单元)为TPMS孔隙单元中的一种。应用Wolfram Mathematica 9.0软件进行建模,设计的G单元多孔结构如图1所示,结构外形为圆柱形,将数据导出为STL格式,以便进一步的分层切片处理,保存到DLP打印机中制备复合支架,进行成型工艺研究。

图1 多孔结构支架模型
1.2.2 生物活性玻璃/羟基磷灰石复合支架的形貌结构观察 将不同配比组成的生物活性玻璃/羟基磷灰石复合支架置于光学显微镜下对其表面微观形象及内部孔隙结构进行观察,并连接电脑进行支架材料打印线条及孔隙尺寸测量;实验前置于喷金铜台上40 s,利用场发射扫描电子显微镜观测多孔结构孔隙特征、表面微观形貌。
1.2.3 测量生物活性玻璃/羟基磷灰石复合支架的孔隙率 采用阿基米德排水法测量,孔隙率p=(m3-m1)/(m3-m2)×100%(m1为支架质量,m2为支架在沸水中的质量,m3为支架湿重)。
1.2.4 生物活性玻璃/羟基磷灰石复合支架的力学分析 将各组支架的标准样件在室温下应用微机控制电子万能试验机进行静态压缩力学测试,压缩加载速度为0.5 mm·min-1,力值调零,逐渐加力,直至支架材料屈服,记录数值。
1.2.5 生物活性玻璃/羟基磷灰石复合支架的降解实验 将各组支架的标准样件放入去离子水中,超声波震荡洗涤30 min,确保孔隙内无杂质后放入75%乙醇中浸泡30 min,然后在真空干燥箱内80℃条件下干燥12 h。试样冷却后在天平上称重,放入烧杯中,按照样件质量1 g放入100 mL溶液的比例添加SBF溶液。密封后放入温度设定为36.8℃的水浴震荡箱中进行14 d降解实验:(1)样件失重检测分别测量样件在第0、3、7、14天时的质量,计算失重比;(2)形貌和矿化检测分别在第0、3、7、14天观察样件的表观形貌变化。
1.3 统计学方法
采用SPSS 19.0统计学软件进行数据分析。计量资料以均数±标准差(±s)表示,组间比较采用t检验。P≤0.05为差异有统计学意义。
2 结果
2.1 生物活性玻璃/羟基磷灰石复合支架的外观结构、显微结构及孔隙率
复合支架的宏观照片如图2所示,显示其为圆柱体支架结构,理论孔隙直径与实际基本相符均为500μm。通过扫描电镜观察,BG20/HA80的复合支架微观孔隙结构最为均匀,而BG30/HA70、BG40/HA60、BG50/HA50配比的复合支架表面开始出现裂痕,见图3。通过EDS测试复合支架表面钙磷元素分布及钙磷比,显示其复合支架钙磷元素分布均匀,钙磷比接近天然骨组织,见图4、图5。

图2 复合支架的宏观照片

图3 各比例复合支架扫描电镜图(×10K)

图4 复合支架EDS分层图像(×100)
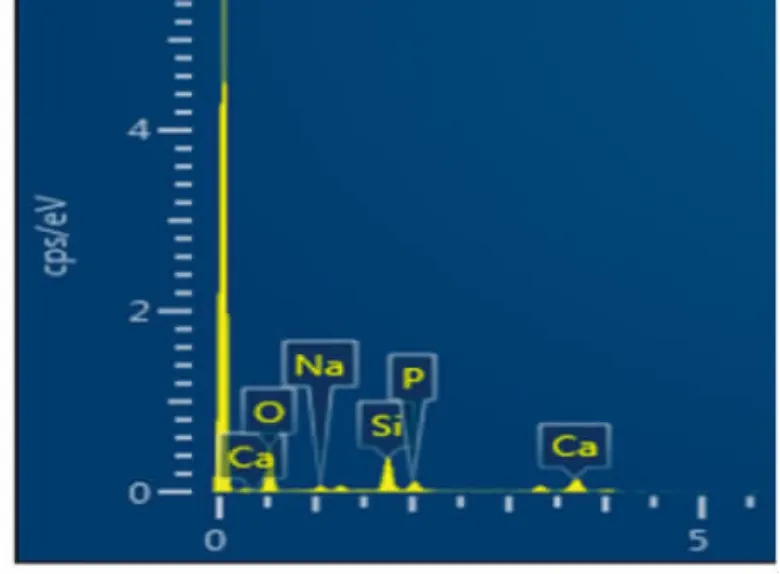
图5 EDS检测复合支架钙磷比
对不同配比的复合支架进行阿基米德排水法测得孔隙率分别为BG0/HA100组(68.29±0.39)%、BG10/HA90组(68.21±0.59)%、BG20/HA80组(65.71±2.22)%、BG30/HA70组(59.37±1.19)%、BG40/HA60组(55.17±2.08)%、BG50/HA50(52.54±1.79)%和BG100/HA0组(46.5±1.48)%,除BG100/HA0组外,各组复合支架孔隙率均达到50%以上,符合人工骨材料孔隙率要求;BG20/HA80组与BG100/HA0组孔隙率差异有统计学意义(t=3.375,P=0.027 9),见图6。

图6 不同配比复合支架的孔隙率比较
2.2 生物活性玻璃/羟基磷灰石复合支架力学分析结果
通过万能生物力学实验机对不同配比复合支架以0.5 mm·min-1速率进行抗压强度测试,BG20/HA80、BG30/HA70、BG40/HA60、BG50/HA50、BG100/HA0抗压强度均在2 MPa以上,见图7。最大抗压强度满足人体松质骨的应力要求。
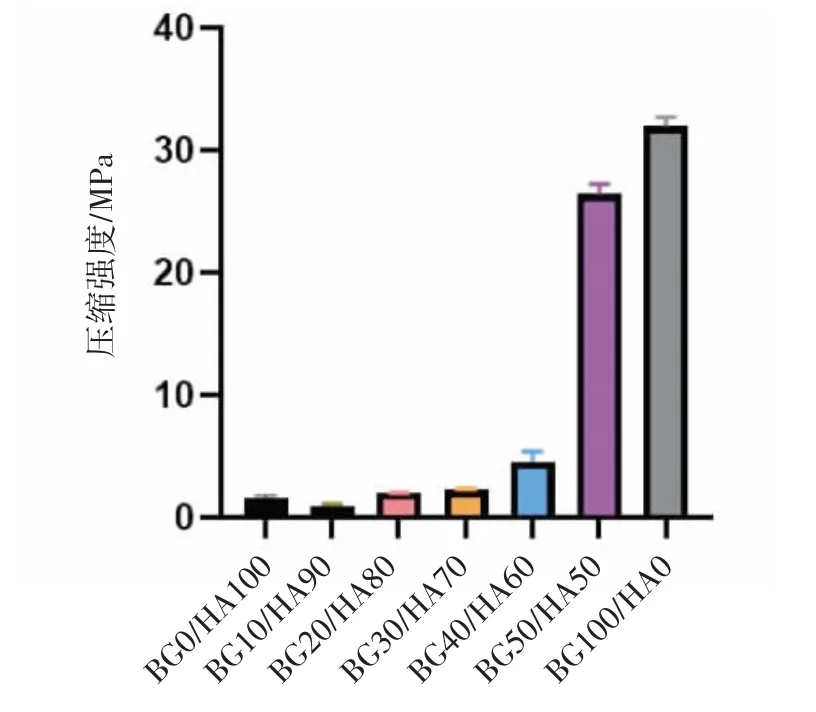
图7 不同配比复合支架抗压强度比较
2.3 生物活性玻璃/羟基磷灰石复合支架的降解性能测试
将复合支架浸泡于缓冲液,计算不同浸泡时间后复合支架的质量损失,得到质量变化曲线,见图8。加入生物活性玻璃的复合支架表现出更好的降解性能,在缓冲液中浸泡2周后,复合支架失重率分别为BG0/HA100组(2.85±0.29)%、BG10/HA90组(2.91±0.10)%、BG20/HA80组(7.55±0.79)%、BG30/HA70组(10.58±1.21)%、BG40/HA60组(11.53±1.33)%、BG50/HA50(10.41±1.29)%、BG100/HA0组(14.50±0.71)%。其中BG20/HA80组2周后的失重率为BG0/HA100组的2.7倍。

图8 不同配比复合支架体外降解时间-比例曲线
3 讨论
羟基磷灰石是人体和大多数动物骨骼的主要无机成分,含有可与机体组织键合的羟基且钙磷比为1.67,接近人体骨[18],在体内具有良好生物相容性,但纯羟基磷灰石在实际应用中受降解性、硬度、脆性、柔韧性的限制[19];生物活性玻璃作为一种人工合成的可降解无机材料,具有良好的生物活性且能与宿主骨组织亲密地键合,通过羟基磷灰石来诱导骨组织再生,不足之处在于其脆性大、机械性能不足及对较大骨缺损修复效果不佳,限制了其在受力部位及大尺寸骨缺损修复中的应用[20]。研究[21]表明,在人工骨支架材料中添加生物活性玻璃可提高其降解性,添加20%生物活性玻璃可以使PCL支架的力学性能明显上升[22]。若将二者以一定的比例经过相关技术制备成一种新的骨修复材料,在骨修复过程中平衡各材料的优劣势将各组分优势最大化,以期达到骨修复材料理想的参数指标。本研究通过设计多孔支架模型,将生物活性玻璃与羟基磷灰石材料结合3D打印制作出不同材料配比的骨修复支架,通过宏微观的支架形貌观察,发现生物活性玻璃的加入可使支架具有孔洞特性,当其含量为20%时孔径分布较宽,互相连接的孔径适合细胞增殖[23]、血管再生[24]、营养代谢及运输[25];证实了生物活性玻璃的加入与复合材料的抗压强度呈正相关,未添加生物活性玻璃的羟基磷灰石支架抗压强度不能满足人体骨组织的机械性能要求[26-27];反映了生物活性玻璃的加入比例越高,降解性能也随之增加,但加入过高比例的生物活性玻璃会使支架在浸泡1 d后即发生明显的降解,容易使支架溃散,因此选择降解曲线相对平缓且降解率较高的复合支架配比最为合适。本研究从生物活性玻璃/羟基磷灰石骨修复材料设计、制备的基础出发,介绍其结构以及成分比例不同组别之间的区别,梳理其理化性能方面的优缺点,选择符合较高骨修复材料要求的生物活性玻璃/羟基磷灰石复合支架作为最优组。
临床转化应用方面,临床上人工骨修复材料应同时具备较高的孔隙率[28]、较强的机械性能以及良好的降解性能。通过3D技术打印满足临床上个体化差异的骨修复材料,负载不同药物治疗、不同病因引起的骨缺损,例如设计、使用适宜复合支架负载万古霉素缓释微球治疗金葡菌引起的感染性骨缺损等,更好地促进骨组织的修复重建以治疗相关疾病。在本实验制备生物活性玻璃/羟基磷灰石复合支架的过程中,虽然生物活性玻璃因其良好的生物活性、生物安全性及性能可调控性,具有良好的医学应用前景,但目前商品化的生物活性玻璃材料还很有限,同样的情况也出现在羟基磷灰石材料上。尽管二者作为新型材料已经取得许多令人瞩目的研究成果,但在临床应用中的可行性仍需进一步研究和证实。本实验的不足之处在于未能完成各项细胞、体内实验,以测试复合材料的生物性能,以及载药后治疗感染性骨缺损的相关研究,这也是接下来研究的方向。
综上所述,通过3D技术打印不同配比的生物活性玻璃/羟基磷灰石支架,对比不同配比复合支架的各项性能,在平衡优化各性能条件下,本实验选出BG20/HA80组,其具备良好的宏微观结构、孔隙率、力学性能及降解性。不同配比的复合支架材料表现出不同的性能,提示可通过调整配比来满足不同性能的需求,为骨缺损治疗材料的研究提供的新思路。促进骨修复材料向功能健全骨组织的转化是骨修复材料后续研究的重要方向。

