罗欧咳祖帕复方的血清药物化学研究
陈悦,闫俊林,刘佳倪,李莉,康金森(新疆医科大学药学院,乌鲁木齐 830011)
罗欧咳祖帕是用于治疗哮喘的经典药方,具有温肺平喘、止咳化痰作用。该方由神香草、鸢尾根组成,目前的研究集中在罗欧咳祖帕复方中的单味药材的物质基础,其中神香草(Hyssopus cuspidatusBoriss)化学成分包括挥发油[1-3]、黄酮类[4-5]、萜类及酚酸类等[6-8],鸢尾根(Iris halophilaPall)化学成分包括黄酮类和挥发油等[9-11],这些成分具有抗氧化活性[10]、抗炎作用[11-14]、抗菌、降血脂、降血压[14]等作用。但缺乏对于复方本身的物质基础的系统研究,中药复方成分多且复杂,有些化学成分在体外药理活性强,但是生物利用度低,在体内很难达到有效治疗浓度,有些成分则经过肠内菌或者肝脏代谢以代谢产物发挥作用[15]。因此,为探究罗欧咳祖帕复方在体内的潜在活性成分,采用血清药物化学研究方法,利用UHPLC-QE-MS技术,对罗欧咳祖帕复方后的血中移行成分进行鉴定,为罗欧咳祖帕复方进一步研究开发提供实验依据。
1 材料
1.1 仪器
超高效液相 1290 UPHLC(Agilent);高分辨质谱Q Exactive Focus、离心机Heraeus Fresco17(Thermo Fisher Scientific);天 平BSA124S-CW(Sartorius);研磨仪JXFSTPRP-24(上海净信科技有限公司);纯水仪明澈 D24 UV(Merck Millipore);超声仪YM-080S(深圳市方奥微电子有限公司);色谱柱ACQUITY UPLC BEH C18(2.1 mm×100 mm,1.7 μm)(Waters)。
1.2 试药
神香草药材(新疆维吾尔药业有限责任公司,批号:Y1911044),鸢尾根药材(新疆恩萨尔维吾尔医药饮片药业有限公司,批号:190523),神香草药材经新疆医科大学天然药物教研室帕丽达·阿不力孜教授鉴定为唇形科神香草属植物硬尖神香草的全草,喜碱鸢尾根药材经新疆医科大学天然药物教研室丛媛媛教授鉴定为鸢尾科鸢尾属植物喜碱鸢尾的根部,标本现均存于新疆医科大学中心实验室;甲醇(批号:67-56-1)、乙腈(批号:75-05-8)、甲酸(批号:64-18-6)(CNW Technologies);L-2-氯苯丙氨酸(批号:103616-89-3,上海恒柏生物科技有限公司)。
1.3 实验动物
SPF级雄性SD大鼠,体质量 180~220 g [新疆医科大学动物实验中心,实验动物生产许可证号:SCXK(新)2018-0002]。
2 方法
2.1 罗欧咳祖帕复方提取物样品的制备
按照临床用药的配伍比例(具体比例保密),采用水煎煮法制备复方罗欧咳祖帕粗提物,加入乙醇至含醇量为70%,室温下静置,将提取液过滤减压浓缩成浸膏,干燥后获得罗欧咳祖帕复方提取物粉末[16]。称取100 mg样本,加入500 μL提取液[甲醇∶水=4∶1,内标(L-2-氯苯丙氨酸)质量浓度为10 μg·mL-1]以及两个小钢珠;涡旋30 s后45 Hz研磨240 s,冰水浴超声1 h;-40℃静置1 h后,将样本4℃、12 000 r·min-1离心15 min;取出上清液过0.22 μm滤膜至进样瓶中检测。
2.2 含药血清样品的制备
取SD大鼠10只,适应性喂养1周后,随机分成空白组和给药组,空白组4只,给药组6只。给药前12 h禁食、自由饮水,给药组大鼠灌胃罗欧咳祖帕复方提取物药液(生药3.185 g·kg-1),空白组大鼠灌胃等量蒸馏水,给药量均为1 mL/100 g,连续给药3 d,早、晚各给药1次。末次给药1 h 后,腹主动脉取血,静置2 h,4℃、3000 r·min-1离心10 min,收集血清得到空白血清和含药血清样品,取400 μL血清样本,加入40 μL盐酸(2 mol·L-1);涡旋1 min,4℃ 静置15 min;重复涡旋静置4次后,加入1.6 mL乙腈;涡旋5 min,12 000 r·min-1离心5 min,取上清液1800 μL氮吹干;加入150 μL 80%甲醇(内标质量浓度为10 μg·mL-1)复溶,涡旋5 min,12 000 r·min-1(离心力13 800 g,半径8.6 cm)离心5 min;取120 μL上清液到进样瓶中检测[17]。
2.3 分析条件
2.3.1 色谱条件 采用UPHLC进行分析。柱温为55℃,流速为500 μL·min-1,进样体积为5 μL。流动相0.1%甲酸水溶液(A)-0.1%甲酸乙腈水溶液(B)梯度洗脱(0~11 min,15%~75%B;11~12 min,15%~98%B;12~14 min,98%B;14~14.1 min,98%~15%B;14.1~16 min,15%B;18~25 min,100%B;25~30 min,5%B)。
2.3.2 质谱条件 鞘气:45 Arb,辅助气:15 Arb,离子传输管温度:400℃,Full MS分辨率:70 000,MS/MS 分辨率:17 500,NCE模式时,所用碰撞能为阶梯能量:15、30、45 eV,喷雾电压:4.0 kV(正离子模式)或-3.6 kV(负离子模式)。
2.4 数据处理
使用XCMS软件将质谱原始数据导入,进行保留时间矫正、峰识别、峰提取、峰积分、峰对齐等,利用自建二级质谱数据库及相应裂解规律匹配法对含有MS/MS数据的峰进行物质鉴定。使用SIMCA软件对数据进行对数(LOG)转换加UV格式化处理。
3 结果与讨论
3.1 成分分析
比较相同色谱、质谱条件下罗欧咳祖帕复方提取物、罗欧祖帕复方含药血清、空白血清的图谱(见图1~2),发现在正、负离子同时扫描的模式下,从罗欧咳祖帕复方含药血清中共检测比对出385个主要入血化学成分。

图1 罗欧咳祖帕正离子模式TIC图Fig 1 TIC diagram of positive ion mode of Loki zupa

图2 罗欧咳祖帕负离子模式TIC图Fig 2 TIC diagram of negative ion mode of Loki zupa
3.2 正交偏最小二乘法-判别分析(OPLS-DA)
采用OPLS-DA法[18]进行分析,结果见图3~4。可以看出,两组样本区分非常显著,样本全部处于95%置信区间内。

图3 复方含药血清组(F)对复方提取物组(T)的OPLS-DA分析Fig 3 OPLS-DA analysis of compound medicated serum group(F)to compound extract group(T)

图4 复方含药血清组(F)对空白血清组(K)的OPLS-DA分析Fig 4 OPLS-DA analysis of compound medicated serum group(F)to blank serum group(K)
3.3 置换检验分析
置换检验结果如图所示(见图5~6)。原模型R2Y非常接近1,说明建立的模型符合样本数据的真实情况;原模型Q2非常接近1,说明如果有新样本加入模型,会得到近似的分布情况;置换检验随机模型的Q2值均小于原模型的Q2值;Q2的回归线与纵轴的截距小于零;同时随着置换保留度逐渐降低,置换的Y变量比例增大,随机模型的Q2逐渐下降,说明原模型可以明确解释两组样本之间的差异,具有良好的稳健性(复方含药血清组对复方提取物组R2Y=0.91,Q2=-0.68;复方含药血清组对空白血清组R2Y=0.97,Q2=-0.2),不存在过拟合现象。

图5 复方含药血清组对复方提取物组的置换检验分析Fig 5 Replacement test of compound medicated serum group to compound extract group

图6 复方含药血清组对空白血清组的置换检验分析Fig 6 Replacement test analysis of compound medicated serum group to blank serum group
3.4 差异代谢物分析
采用多元变量统计方法进行分析[19]。
本研究选择的筛选标准为Student'st检验的P值小于0.05,同时OPLS-DA模型第一主成分的变量投影重要度大于1,以火山图可视化方式表示(见图7~8),蓝色代表下调差异代谢物,红色代表上调差异代谢物,灰色代表无显著变化代谢物。正离子模式下的复方含药血清组对复方提取物组共筛选到323个差异代谢物;其中45个上调差异代谢物,如deoxynivalenol、spermine、acetylcarnitine、alpha-linolenic acid、L-isoleucin、lysine等;278个下调差异代谢物,如一枝蒿甲素、三尖杉碱、滨蓟黄素、白射干素、京尼平苷、山柰酚等;正离子模式下的复方含药血清组对空白血清组共筛选到19个差异代谢物;其中12个上调差异代谢物,如12-羟基茉莉酸、pipecolic acid等;7个下调差异代谢物,如黄曲霉素B1、7,8-二羟基黄酮等;负离子模式下的复方含药血清组对复方提取物组共筛选到248个差异代谢物;其中56个上调差异代谢物,如香草酸、松香酸、云杉素等;192个下调差异代谢物,如乙酰丁香酮、香草醛、水杨酸甲酯等;负离子模式下的复方含药血清组对空白血清组共筛选到22个差异代谢物,其中17个上调差异代谢物,如高良姜素、棕矢车菊素、异鼠李素、柳穿鱼黄素、鸢尾黄酮乙素等。这些差异代谢物共33类:分别为miscellaneous(其他类)、flavonoids(黄酮类)、terpenoids(萜类)、alkaloids(生物碱)、iridoids(环烯醚萜类)、phenylpropanoids(苯丙素类)、lipids(脂质类)、steroids(甾体类)、amino acid derivatives(氨基酸衍生物)、sesquiterpenoids(倍半萜类)等。

图7 正离子模式(A)和负离子模式(B)下复方含药血清组对复方提取物组的差异代谢物分析火山图Fig 7 Analysis Volcano plot of differential metabolites between compound medicated serum group and compound extract group in positive ion mode(A)and negative ion mode(B)
3.5 入血成分分析
对代谢组的定性定量结果进行OPLS-DA分析、单变量统计分析和多元变量统计分析(multivariate analysis,MVA)后筛选出显著差异的代谢物,基于样本中物质碎裂产生的二级谱图同数据库谱图比对给出谱图相似度得分值,并对差异化合物进行筛选后初步鉴定罗欧咳祖帕复方中的主要入血成分(见表1及表2)。在正、负离子同时扫描的模式下从罗欧咳祖帕复方含药血清中共鉴定出28个主要入血化学成分,其中18个为原形成分,包括高良姜素、棕矢车菊素、异鼠李素、4-羟基苯甲酸酯、双氢青蒿素、鸢尾黄酮乙素、癸二酸、亚油酸、中亚阿魏二醇香草酸酯、苯丙酮酸、pipecolic acid、testolactone、7-hydroxy-3-(3-hydroxy-4-methoxyphenyl)-6-methoxychromen-4-one、(3E)-4-(1,2,4-trihydroxy-2,6,6-trimethylcyclohexyl)-3-buten-2-one、azuleno(5,6-c)furan-1(3H)-one,4,4a,5,6,7,7a,8,9-octahydro-3,4,8-trihydroxy-6,6,8-trimethyl-、5-hydroxy-2-(3-hydroxy-4-methoxyphenyl)-7-[3,4,5-trihydroxy-6-[(3,4,5-trihydroxy-6-methyloxan-2-yl)oxymethyl]oxan-2-yl]oxychromen-4-one、牡荆苷、海柯皂苷元,10个为代谢产物,包括柳穿鱼黄素、异棕榈酸、petunidin-3-O-betaglucopyranoside、(-)-茉莉酸、12-羟基茉莉酸、肌酸、白坚木卡品、(2S,3S,4S,5R,6S)-3,4,5-trihydroxy-6-[5-hydroxy-2-(4-hydroxyphenyl)-6-methoxy-4-oxochromen-7-yl]oxyoxane-2-carboxylic acid、kaempferol-3-O-glucuronoside、tricin。

表1 正离子模式下化学成分 Tab 1 Chemical composition in positive ion mode

表2 负离子模式下化学成分 Tab 2 Chemical composition in negative ion mode
4 讨论
本实验建立了UHPLC-QE-MS法对罗欧咳祖帕复方含药血清进行检测,具有离子传输效率高、灵敏度高、重复性高等优点。
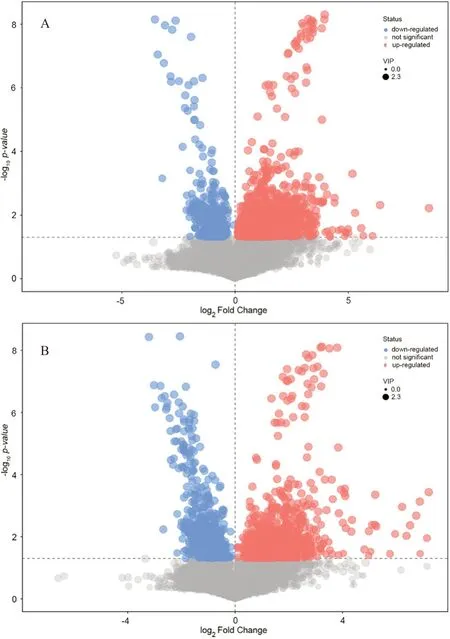
图8 正离子模式(A)和负离子模式(B)下复方含药血清组对空白血清组的差异代谢物分析火山图Fig 8 Analysis Volcano plot of differential metabolites between compound medicated serum group and blank serum group in positive ion mode(A)and negative ion mode(B)
本实验在建立 UHPLC-QE-MS法的基础上,采用XCMS及SIMCA软件进行数据采集和化合物谱库比较鉴定,可对中药复方复杂化学体系进行快速筛选鉴定,通过对罗欧咳祖帕复方提取物、含药血清、空白血清的质谱信息、保留时间、精确相对分子量以及自建二级质谱数据库比对初步检测出主要成分,并且通过OPLS-DA分析、单变量统计分析和多元变量统计分析统计代谢组化合物信息,筛选出差异化合物。上述方法共初步鉴定出18种原形入血成分,10种代谢产物,主要包括黄酮类、萜类、生物碱类等成分,这些化合物种类分布广泛,具有多种生物活性及丰富的药用价值,是研究天然产物和开发新药的重要来源。
然而基于QE的非靶标代谢组学并不能最终确定复方中的入血成分,还需进一步采用对照品比对来明确复方药效物质,其次本实验结果是在正常动物体内的表现,其于疾病动物体内的表现是否有差异,需开展进一步的研究。但上述入血成分也初步揭示其可能为罗欧咳祖帕复方在体内发挥药效的物质基础,可为其后续研究开发提供实验依据。

