磁性甲壳素多孔碳球的制备及对姜黄素的吸附
刘帅,陈慧洁,李文婷,李中天,卢言辉,彭海龙
(南昌大学化学化工学院,江西 南昌 330031)
姜黄素是传统中药姜黄中一种天然多酚类化合物(图1),具有抗炎、抗菌、抗癌、抗氧化等多种药理作用[1-2],姜黄素在医药和食品领域具有广泛的应用。但是,姜黄素溶解性差、生物利用度低、稳定性差、代谢快等缺点严重阻碍了其应用[3]。许多包埋策略,如纳米颗粒、脂质体、胶束、微纳米乳液和固体分散体等,对姜黄素进行包埋,进而提高其稳定性和生物利用度[3]。但是,这些包埋方法在包埋过程中往往涉及有机溶剂,其残留对人体健康具有一定毒副作用[4]。
甲壳素是仅次于纤维素的天然氨基多糖,因其无毒、生物可再生、生物相容性和生物可降解性等优点而受到越来越多的关注[5]。甲壳素可用来制备螯合剂、药物载体、伤口愈合剂、膜等功能性材料[6]。近年来,甲壳素在尿素/氢氧化钠溶液中,通过循环冻融方法将其溶解,利用乳化法制备甲壳素纤维多孔微球(chitin nanofiberous microspheres,CNMs)[7]。CNMs具有多级孔结构和高比表面积等优点[8],研究人员利用CNMs作为吸附剂和药物递送载体进行了报道[9]。
多孔碳材料具有比表面积大、密度低、孔容大、轻质、选择性好等优点,是一种常用的新型吸附剂包埋体系,在水的净化、催化剂载体和药物传递等领域[10-11]具有广泛的应用和良好的前景。甲壳素中含有丰富的氮乙酰基,炭化后可以产生高质量的氮掺杂碳骨架。利用CNMs可制备具有多级孔结构和高比表面积的氮掺杂甲壳素纳米纤维碳微球(N-doped chitin nanofiberous carbonized microspheres,N-CNCMs)[12-13]。然而,N-CNCMs作为药物载体来吸附和包覆活性分子的报道较少。由于其独特的磁响应性、生物分离和药物传递方面的潜力,Fe3O4纳米粒受到了广泛的关注和研究[14]。在N-CNCMs中引入Fe3O4纳米粒不仅解决了分离缺陷,还提高了传递性能,提升了它的应用潜能,更加拓宽了它的应用前景。
本文利用甲壳素为原材料,通过环境友好的方法设计了一种新型功能材料磁性氮掺杂甲壳素多孔碳球(magnetic nitrogen-doped chitin microspheres,MNCMs),并且作为包埋载体来吸附包埋姜黄素。MNCMs表现出优异的吸附性能、易分离和回收、高比表面积和多孔机框架结构等特点。吸附过程在乙醇溶液中进行,避免了有机溶剂残留毒副作用。同时,本文对MNCMs的理化性能和吸附机制进行了详细探讨。
1 实验部分
1.1 实验药品
甲壳素购自中国浙江金壳生化有限公司,实验之前按照之前的报道[7]进行纯化。四氧化三铁纳米微粒购自Sigma公司。司盘-85、异辛烷和吐温-85均购自中国上海阿拉丁公司。姜黄素(分析纯:99.00%)购自四川成都西雅试剂。
1.2 磁性氮掺杂甲壳素多孔碳球(MNCMs)的制备
6 g纯化甲壳素粉末分散到含有11 g氢氧化钠、4 g尿素和85 g去离子水的混合溶液中,以1 000 r·min-1搅拌10 min,冻融3次后得到透明甲壳素溶液(水相)。在0 ℃下将4.4 g司盘-85和100 g异辛烷加入三颈烧瓶混合30 min(油相)。0.6 g Fe3O4纳米粒均匀分散到水相中,并迅速注入到油相,以1 000 r·min-1搅拌乳化60 min。将2.4 g吐温-85加入乳液悬浮液中,搅拌60 min,将其转移到60 ℃水浴锅继续搅拌5 min形成磁性CNMs。用10%盐酸溶液将pH调至7,静置分离异辛烷。利用磁铁将磁性CNMs分离,用水和乙醇各洗涤3次,叔丁醇浸泡6 h后冻干备用。得到的磁性CNMs在管式炉中650 ℃条件下煅烧4 h,黑色的产品为磁性氮掺杂碳化甲壳素微球(MNCMs)。
1.3 MNCMs的表征
MNCMs样品用扫描电子显微镜(SEM,JSM-6701F)进行形貌分析。采用X射线衍射仪(XRD,D8-ADVANCE X,德国Bruker公司)对姜黄素的晶体变化进行分析。利用傅里叶红外光谱(FTIR,Nicolel5700,美国Thermo Nicolet公司)分析姜黄素与MNCMs之间相互作用。全自动比表面积及孔径分析仪(BET,Autosorb-2,美国康塔公司)测量MNCMs比表面积。同步热分析仪(TGA-DSC,SDT-Q-600,美国TA公司)测定姜黄素热稳定性。振动样品磁强计(VSM7407,美国Lake Shore公司)研究N-NCMs磁性能。
1.4 吸附实验
将10 mg MNCMs样品加入到不同质量浓度的姜黄素-乙醇溶液(5,10,20,30,40,50 mg·L-1)中,充分搅拌吸附12 h。使用磁铁将MNCMs样品进行分离,UV-vis在420 nm波长下测定上清液中未被吸附姜黄素的含量。根据以下公式计算了MNCMs吸附效率η[15-16]:
(1)
式中:mi为姜黄素的初始质量,g;mn为未被吸附姜黄素的质量,g;η为MNCMs的吸附效率,%。
为进一步研究MNCNs的吸附机制,对MNCMs动态和静态吸附进行了详细研究,将10 mg MNCMs样品加入到50 mL质量浓度为10 mg·L-1的姜黄素溶液,25 ℃下搅拌,在预定时间下(15,30,60,120,210,300,420,540,720 min)取出5 mL溶液,UV-vis在420 nm处测定姜黄素质量浓度。将10 mg MNCMs样品加入到50 mL姜黄素溶液(10 mg·L-1)中,在不同温度下(25,35,45 ℃)搅拌吸附12 h,取出5 mL溶液,UV-vis在420 nm处测定姜黄素质量浓度。
2 结果与讨论
2.1 分析表征
2.1.1 形貌、结构和元素分析
利用SEM研究了姜黄素和MNCMs吸附前后形貌。如图2所示,MNCMs由纳米甲壳素碳纤维缠绕形成的球形,具有清晰可见的多孔结构(图2)。MNCMs内部呈现出相同的多孔结构和互连通道(图3),与之前文献[17]报道结果相似,此结构使姜黄素更容易进入其内部,到达快速吸附效果,进而提高其吸附性能。对MNCMs元素分析发现C,O,N和Fe元素均匀地分散在MNCMs样品中(图4)。
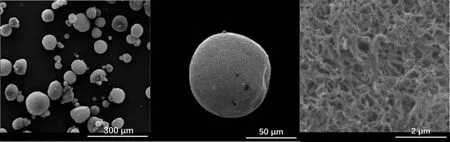
图2 吸附前MNCMs形貌图Fig.2 Morphology of MNCMs before adsorption

图3 吸附前MNCMs内部结构图Fig.3 Internal structure of MNCMs before adsorption

图4 吸附前MNCMs元素分析Fig.4 Elemental analysis of MNCMs before adsorption
从姜黄素的SEM图可以看出姜黄素具有良好晶型结构(图5)。吸附姜黄素后,MNCMs仍然保持与吸附前相似的形貌结构(图6),但是其碳纤维束表面变得更加粗糙。可见被MNCMs吸附后,姜黄素晶型由原来的结晶型转变为无定形,在微球表面有姜黄素颗粒出现。

图5 姜黄素形貌图Fig.5 Morphology of curcumin

图6 吸附后MNCMs形貌图Fig.6 Morphology of MNCMs after adsorption
2.1.2 磁性能分析
从图7可以看出,吸附前后MNCMs都表现出良好的磁滞行为,吸附姜黄素前后其磁饱和度(21.45 emu·g-1)基本保持不变。优异的磁性使得本文研究的多孔微球易分离回收。
2.1.3 XRD和DSC分析
MNCMs和姜黄素的XRD结果如图8所示。24.30°和43.21°峰分别对应(002)和(100)的反射信号,表明MNCMs为无定形状态和石墨结构[10]。在30.16°,35.46°,53.60°,57.05°和62.70°峰分别属于Fe3O4的(220)、(311)、(422)、(511)和(440)[18]。姜黄素在10°~30°范围内出现一系列尖峰,表明姜黄素具有良好的结晶性质。被MNCMs吸附后,姜黄素尖峰几乎消失了,表明吸附后姜黄素晶体变成了无定形结构。由DSC测定姜黄素的熔点为183.7 ℃(图9),而被MNCMs吸附后,姜黄素熔化峰消失,说明姜黄素以非晶态分散到N-CNCMs中,热稳定性得到了极大的提高。
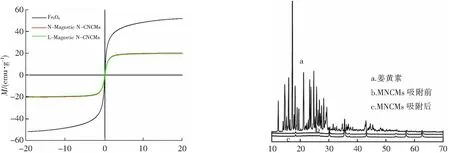
H/kG图7 吸附姜黄素前后MNCMs的磁性能图Fig.7 Magnetic properties of magnetic MNCMs before and after adsorption2θ/(°)图8 姜黄素、MNCMs吸附前后的XRD衍射图Fig.8 XRD spectrum of curcumin,MNCMs before adsorption,MNCMs after adsorption
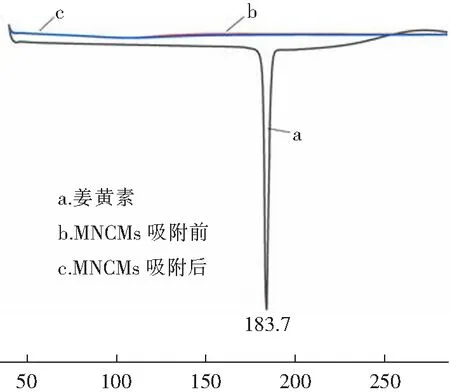
θ/℃图9 姜黄素、MNCMs吸附前、MNCMs吸附后的DSC图Fig.9 DSC of curcumin,MNCMs before adsorption,MNCMs after adsorption
2.1.4 比表面积分析
采用氮气吸附脱附的方法研究了MNCMs前后孔结构和比表面积。MNCMs吸附前后均呈现Ⅰ型H3滞回曲线(图10),由于它们具有相同的多级孔结构[8]。MNCMs的比表面积达418 m2·g-1,负载姜黄素后MNCMs的比表面积减小到241 m2·g-1,大量姜黄素分子吸附在纳米碳纤维表面,占据了MNCMs的孔隙,使得比表面积减小。孔径分布结果如图11所示,结果表明吸附前后MNCMs均呈现介孔/大孔结构,孔径呈延伸连续分布。
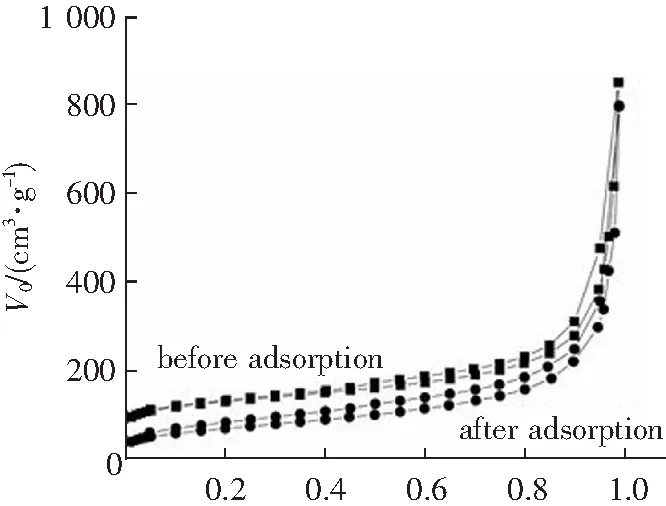
p/p0图10 吸附前后MNCMs比表面积Fig.10 Surface area of MNCMs
2.2 吸附条件优化
本文对姜黄素浓度、吸附温度和时间进行了优化。固定吸附剂用量(10 mg),姜黄素质量浓度(10 mg·L-1)和吸附温度(35 ℃),考察MNCMs在不同时间(15,30,60,120,210,300,420,540 min)对姜黄素吸附(图12),随着时间增加,吸附量迅速增加,在200 min后达到吸附平衡。固定吸附剂用量(10 mg),吸附时间(12 h)和吸附温度(35 ℃),姜黄素浓度为10 mg·L-1到50 mg·L-1,如图13所示,N-CNCMs吸附量随着姜黄素浓度增加而增加,当浓度达到50 mg·L-1时吸附量趋于稳定,这时MNCMs吸附位点几乎被姜黄素完全占据,吸附量不再增加。温度影响如图13所示,当温度在25~45 ℃变化时,MNCMs在35 ℃吸附能力最强。因此,MNCMs对姜黄素最佳吸附条件为:姜黄素浓度为50 mg·L-1时,MNCMs用量为10 mg,吸附时间为200 min,温度为35 ℃。

D/nm图11 吸附前后MNCMs的孔径分布Fig.11 Pores distribution of MNCMs

t/min图12 时间对MNCMs吸附量影响Fig.12 Effects of time on the adsorption capacity of magnetic MNCMs
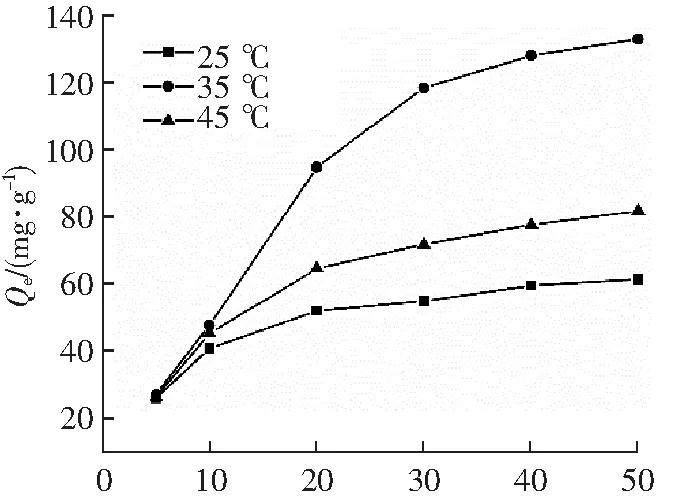
ρ/(mg·L-1)图13 温度和质量浓度对MNCMs吸附量影响Fig.13 Effects of temperature and mass concentration on the adsorption capacity of magnetic MNCMs
2.3 吸附动力学研究
采用准一级动力学模型、准二级动力学模型、Weber-Morris内扩散动力学模型对N-CNCMs动力学进行研究。准一级动力学模型如下[19]:

(2)
ln(Qe-Qt)=lnQe-k1t
(3)
式中:Qe为平衡时吸附量,mg·g-1;Qt为t时的吸附量,mg·g-1;k1为准一级模型吸附速率系数,min-1;t为吸附时间,min。准二级动力学模型如下[20]:

(4)
(5)
式中:Qe为平衡时的吸附量,mg·g-1;Qt为t时的吸附量,mg·g-1;k2为准二级模型的吸附速率系数,g·mg-1·h-1;t为吸附时间,min。Weber-Morris内扩散动力学模型如下[21]:
Qt=kwt0.5+C
(6)
式中:Qt为t时的吸附量,mg·g-1;kw为Weber-Morris内扩散动力学模型的吸附速率系数,g·mg-1·min-1;t为吸附时间,min;C为Weber-Morris内扩散动力学模型的吸附速率常数。
3种吸附动力学模型拟合结果见图14~图16和表1、表2,可以看出:准一级动力学模型的相关系数最小(R2=0.826 4),准二级动力学模型与实验数据的拟合程度最高(R2=0.999 7)。在表1和表2中,准二级动力学模型的拟合度最高,且实验所得吸附量与用准二级动力学模型所计算的理论值更为接近。因此,MNCMs对姜黄素的吸附符合准二级动力学机制。
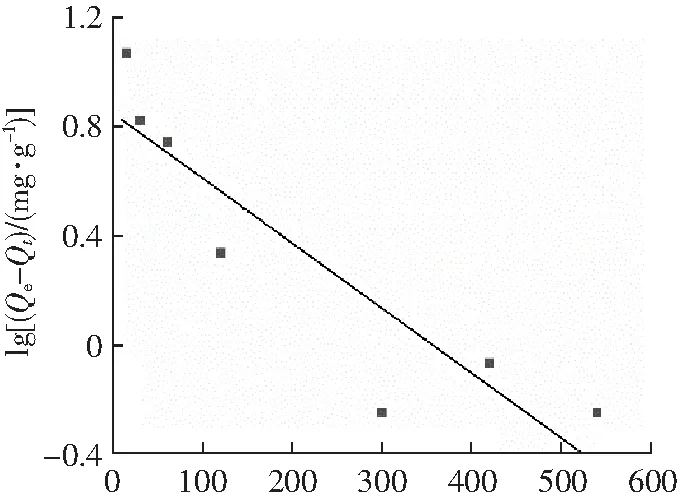
t/min图14 准一级动力学模型Fig.14 The first-order model
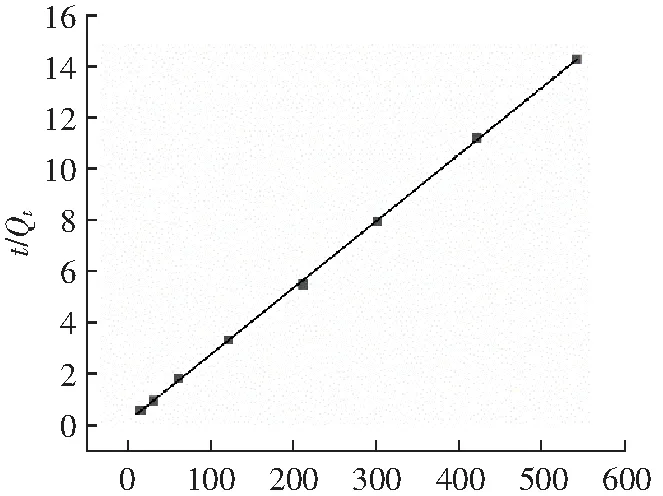
t/min图15 准二级动力学模型Fig.15 The second-order model
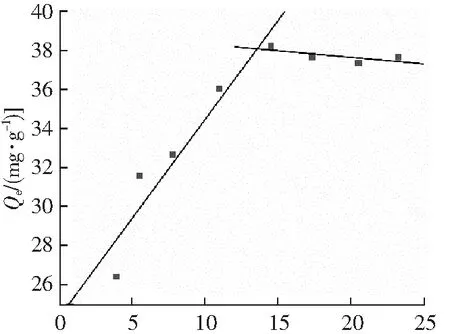
t1/2/min1/2图16 Weber-Morris内扩散动力学模型Fig.16 Weber-Morris model
2.4 等温平衡吸附研究
在不同温度(25,35,45 ℃)下对姜黄素进行吸附热力学研究,利用Langmuir和Freundlich模型进行了拟合。Langmuir等温吸附方程[22]为
式中:ρe为平衡时质量浓度,mg·L-1;Qm为最大吸附量,mg·g-1;Qe为平衡时对姜黄素的吸附量,mg·g-1;ρ0为平衡时质量浓度,mg·L-1;b为与吸附能力有关的Langmuir常数,L·mg-1。吸附难易程度以分离因子RL表示。Freundlich等温吸附方程[23]为
式中:kf为与吸附能力有关的Freundlich常数;n为与温度有关的常数。
从图17、图18和表3可以看出,Langmuir模型具有较好拟合结果,对Freundlich模型的拟合系数偏低。这说明MNCMs表面不均匀,与SEM所观察结果一致。

表1 准一级及准二级动力学模型参数Tab.1 Isothermal adsorption model parameters of the first-order and the second-order

表2 Weber-Morris内扩散动力学模型参数Tab.2 Isothermal adsorption model parameters of Weber-Morris model
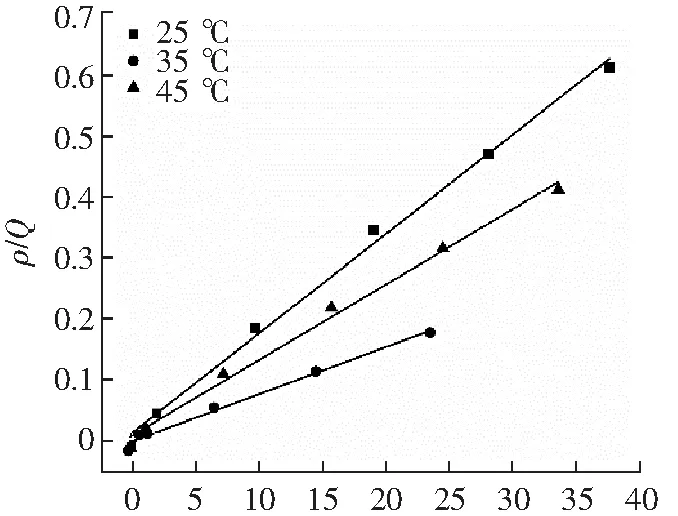
ρ/(mg·L-1)图17 Langmuir等温吸附模型Fig.17 Langmuir isothermal adsorption models
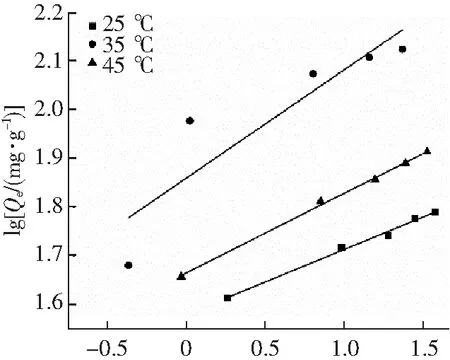
lg[ρ/(mg·L-1)]图18 Freundlich等温吸附模型Fig.18 Freundlich isothermal adsorption models
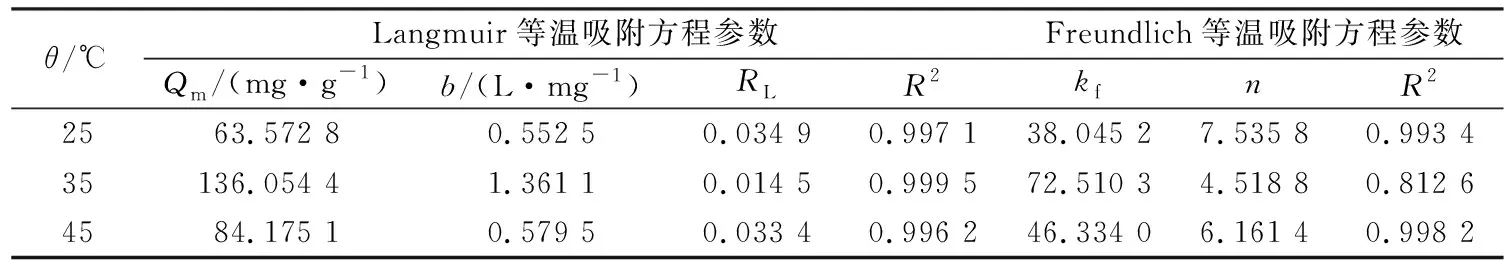
表3 Langmuir 和Freundlich等温吸附模型模型参数Tab.3 Isothermal adsorption model parameters of Langmuir and Freundlich
2.5 吸附对照实验
为了进一步说明MNCMs对姜黄素具有较高的吸附容量,实验设计以未煅烧的纯甲壳素、煅烧后的纯甲壳素微球、煅烧的磁性甲壳素微球和煅烧的磁性壳聚糖微球在相同条件下吸附相同浓度姜黄素。实验结果如图19所示,经煅烧的磁性甲壳素微球(MNCMs)吸附容量显著高于其余3种材料。
2.6 吸附机制探讨
MNCMs吸附机制主要包括以下几个方面:首先,MNCMs具有三维多孔结构、互联通孔道和高比表面积等特点,姜黄素可以很容易地进入MNCMs内部;其次,MNCMs具有氮掺杂碳的性质,在碳化纤维上形成了丰富的碱性位点(氮元素),姜黄素的两个苯环显示出一定的酸性,氮掺杂结构可以大大提高MNCMs对姜黄素的亲合性和吸附能力。此外,MNCMs的石墨结构可与姜黄素形成稳定的π-π键。因此,MNCMs对姜黄素具有良好吸附性能。
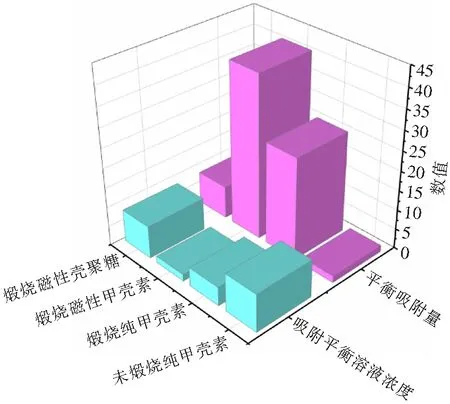
图19 不同材料对姜黄素的吸附容量Fig.19 Adsorption capacity of different materials for curcumin
3 结论
本文以生物可降解、天然无毒、生物相容性优良的甲壳素高分子材料制备新型吸附材料(MNCMs)。MNCMs由纳米碳纤维组成,具有三维多孔结构,比表面积高,同时具有良好的磁性。MNCMs碳纤维上分布一定的氮掺杂和石墨结构。基于上述特性,MNCMs对姜黄素具有良好的吸附效果,在外面磁场下能够快速分离回收。可将其他药物在磁性碳化甲壳素微球上进行物理负载并制备成靶向制剂,使其在人体经过外加磁场的引导而达到靶向和定点释放的效果。

