水力空化对大豆分离蛋白钙致凝胶行为的影响
李晓惠,任仙娥,杨锋,黄永春,黄承都,张昆明,刘纯友
(广西科技大学 生物与化学工程学院,广西糖资源绿色加工重点实验室,广西高校糖资源加工重点实验室,广西 柳州 545006)
大豆分离蛋白(soy protein isolate, SPI)以豆粕为原料,通过低温脱脂技术而制得,其蛋白质含量在90%以上,并含有将近20种氨基酸,不含胆固醇且营养丰富,具有很高的营养价值。大豆蛋白具有起泡性、溶解性、乳化性、凝胶性等优良的功能特性[1],其中凝胶性赋予大豆蛋白较高的黏弹性和可塑性,在产品应用中可以做水、糖、脂肪和一些功能因子的载体,使得大豆蛋白广泛应用于各种食品中,如豆腐及火腿肠[2]。大豆分离蛋白凝胶的形成主要是通过蛋白质分子的聚集来实现的。在蛋白质聚集过程中,当排斥力和吸引力达到平衡时,就形成了规则的三维网络结构。
硫酸钙,又称石膏,是目前使用较为广泛的凝固剂。Ca2+能够屏蔽蛋白质分子表面的负电荷,破坏蛋白质表面的水化层和双电层,与羧基上的H+发生交换作用形成钙桥。大豆蛋白通过静电相互作用、疏水相互作用以及钙桥相互聚集连接形成凝胶网络结构。硫酸盐类凝固剂溶解度比较低,凝胶的成胶速度会受到它的影响,它与蛋白反应较缓慢,使得其诱导形成的凝胶结构更加细腻致密,持水性较好[3]。
超声空化作为有效的物理改性手段已经广泛应用于蛋白质改性,而水力空化有着与超声空化相近的空化效应,而且相比超声空化,水力空化耗能低、能效高、处理量大,更易于工业化生产。水力空化是流动的液体经孔板、叶轮或转子时引起的巨大压差产生的,空化泡溃灭的瞬间会产生高温、高压和高剪切力等,可以修饰蛋白质的结构,改善蛋白质的功能特性[4]。基于此,本实验研究了SPI通过水力空化处理后其钙致凝胶行为的变化规律,为大豆蛋白凝胶制品品质的调控和新产品的开发提供了理论基础和技术支撑。
1 材料和方法
1.1 材料
大豆分离蛋白(SPI):山东禹王生态食品有限公司。
1.2 试剂
牛血清蛋白:上海源叶生物科技公司;硫酸钙、β-巯基乙醇、三氯乙酸、福林酚、氯化钠、碳酸钠、氢氧化钠、酒石酸钾钠、五水合硫酸铜、尿素等:均为分析纯。
1.3 主要仪器与设备
DF-101S集热式恒温加热磁力搅拌器 巩义市予华仪器有限责任公司;MCR T2流变仪 奥地利Anton Paar有限公司;TA-XT Plus质构分析仪 英国Stable Micro System公司;JXN-26冷冻高速离心机 贝克曼库尔特(美国)股份有限公司;UV-2600紫外可见分光光度计 岛津仪器(苏州)有限公司;Alpha 1-4 LD Plus真空冷冻干燥机 德国Christ公司;Phenom ProX扫描电子显微镜 上海复纳科学仪器有限公司;水力(涡流)空化实验装置由实验室自制,与课题组前期使用的装置相同[5]。
1.4 方法
1.4.1 水力空化处理SPI
用去离子水配制质量浓度为8 g/dL的SPI分散液,室温下用集热式恒温加热磁力搅拌器低速搅拌2 h使之充分溶解。取300 mL SPI分散液用作空白对照,剩余分散液倒入水力空化装置的分散液贮箱中,开启冷凝水,调节压力为0.4 MPa,进行水力空化(10,30,60 min)处理,处理后的SPI分散液用保鲜膜封口,放入冰箱4 ℃冷藏,备用。
1.4.2 钙致凝胶的制备
将SPI分散液放入水浴锅中加热至分散液达到90 ℃并保温30 min,冷却至35 ℃左右。加入硫酸钙凝固剂(加入量为0.35 g/dL)使之混合均匀,再放入恒温水浴锅中90 ℃保温20 min形成凝胶,冰水浴冷却至室温再放入冰箱中冷藏(4 ℃、24 h),待测。
1.4.3 凝胶强度的测定
将冷藏过夜盛有凝胶样品的玻璃瓶放置在质构分析仪的平台上进行穿刺测定,选择P/0.5的圆柱形探头,调整好样品的位置使探头对准瓶子中心,测定参数为:测前速度为5 mm/s,穿刺和测后速度均为1 mm/s,压缩距离为10 mm,触发力为5.0 g。凝胶强度为下压至 10 mm 时的最大力量。
1.4.4 凝胶持水性的测定
根据Yi Shumin等[6]的方法,使用分析天平准确称取不同处理时间的凝胶各5 g于离心管中,在台式高速离心机上离心,离心的速度设置为8000 r/min,离心20 min,取出离心管后将其倒扣在吸水纸上使水分排干,擦干离心管内外的残留液。以离心前后质量之差作为凝胶释放液体的质量。持水性(WHC)计算公式如下:
式中:Wt为样品中凝胶的总含水量(g);Wr为离心后释放的液体质量(g)。
1.4.5 凝胶分子间作用力的测定
参照任仙娥等的方法,稍作改动。将SPI凝胶样品用大蒜压制器压碎,各称取0.5 g于三角瓶中,分别加入SA 溶液(0.6 mol/L NaCl,pH 为7.0)、SB 溶液(0.6 mol/L NaCl+1.5 mol/L尿素,pH为7.0)、 SC溶液(0.6 mol/L NaCl+8 mol/L尿素,pH为7.0)和SD溶液(0.5 mol/L β-巯基乙醇+8 mol/L尿素,pH为7.0)各15 mL,充分溶解后,于10000 r/min离心10 min,向离心所得上清液中分别加入15 mL的20 g/dL三氯乙酸,于10000 r/min离心10 min,向所得沉淀中加入1 mL 1 mol/L NaOH溶液,溶解后取1 mL溶液,采用 Lowry 法测定蛋白质含量。其中离子键参与凝胶的贡献比例为 SA 溶液中溶解的蛋白质含量,氢键参与凝胶的贡献比例为 SB 与 SA 溶液中溶解的蛋白质含量之差,疏水相互作用参与凝胶的贡献比例为 SC 与 SB 溶液中溶解的蛋白质含量之差,二硫键参与凝胶的贡献比例为SD与SC溶液中溶解的蛋白质含量之差。
1.4.6 凝胶形成过程的流变学特性测定
采用赵城彬等[7]的实验方法,略作修改。取SPI分散液50 mL于烧杯中,放入水浴锅中加热至分散液达到90 ℃并保温30 min,冰浴冷却至35 ℃左右,加入0.35%的硫酸钙,迅速搅拌使其溶解,再吸取大约3 mL 的分散液于装载台上,使用直径为50 mm的平板进行实验,应变和频率分别设置为0.5%和1 Hz,在样品和平板边缘凹陷处滴加植物油,防止测试时间过长导致样品水分蒸发。实验中的温度扫描由升温阶段、保温阶段和冷却阶段组成,初始温度设置为25 ℃,以2 ℃/min的速率从25 ℃升温至90 ℃并保温20 min,再以2 ℃/min的速率从90 ℃降温至 25 ℃,测定储能模量(G′)、损耗模量(G″)随温度和时间的变化情况。随后在1~100 rad/s的频率范围内进行扫描,记录G′和G″随频率的变化情况。
1.4.7 扫描电子显微镜观察
使用Phenom ProX扫描电子显微镜进行凝胶微观结构观察,将凝胶样品切成1 cm的薄片后冷冻干燥24 h,观察前对干燥好的凝胶样品进行喷金,电压设置为10 kV,放大倍数为300倍[8]。
1.4.8 数据处理
实验中图表所示的数据均为3次以上重复平行实验取得,数据以平均值±标准差的形式表示,使用软件SPSS 26.0进行数据分析,用Duncan检验数据间的差异显著性,P<0.05表示差异显著,并使用OriginPro 9.1进行绘图。
2 结果与分析
2.1 水力空化处理对SPI钙致凝胶强度的影响
由图1可知,水力空化处理(10,30,60 min)可以显著(P<0.05)提高SPI钙致凝胶强度。未处理的SPI形成的钙致凝胶强度为(11.76±0.72) g,水力空化10 min后的SPI钙致凝胶强度显著(P<0.05)增加到(36.92±0.43) g,而后随着空化时间延长至30 min,凝胶强度进一步增强并达到最大值(46.22±0.74) g。这可能是因为水力空化使蛋白质分子粒径减小,提高了蛋白质的溶解度[9],使蛋白与凝固剂硫酸钙充分接触,Ca2+发挥盐桥作用,加强蛋白质分子间的交联,使得形成的凝胶的网络结构更为紧密均匀,导致凝胶的强度大大增强。刘冉等[10]研究发现功率超声处理可以为凝胶形成提供更多的作用位点,从而加速凝胶形成,提高其凝胶强度和凝胶结构的稳定性。但是SPI空化60 min相对空化30 min来说形成的钙致凝胶强度又有一定的下降,可能是因为在长时间的空化作用下蛋白变性聚合,开始形成蛋白聚合物,影响了凝胶的致密结构,以致于凝胶强度稍有下降。
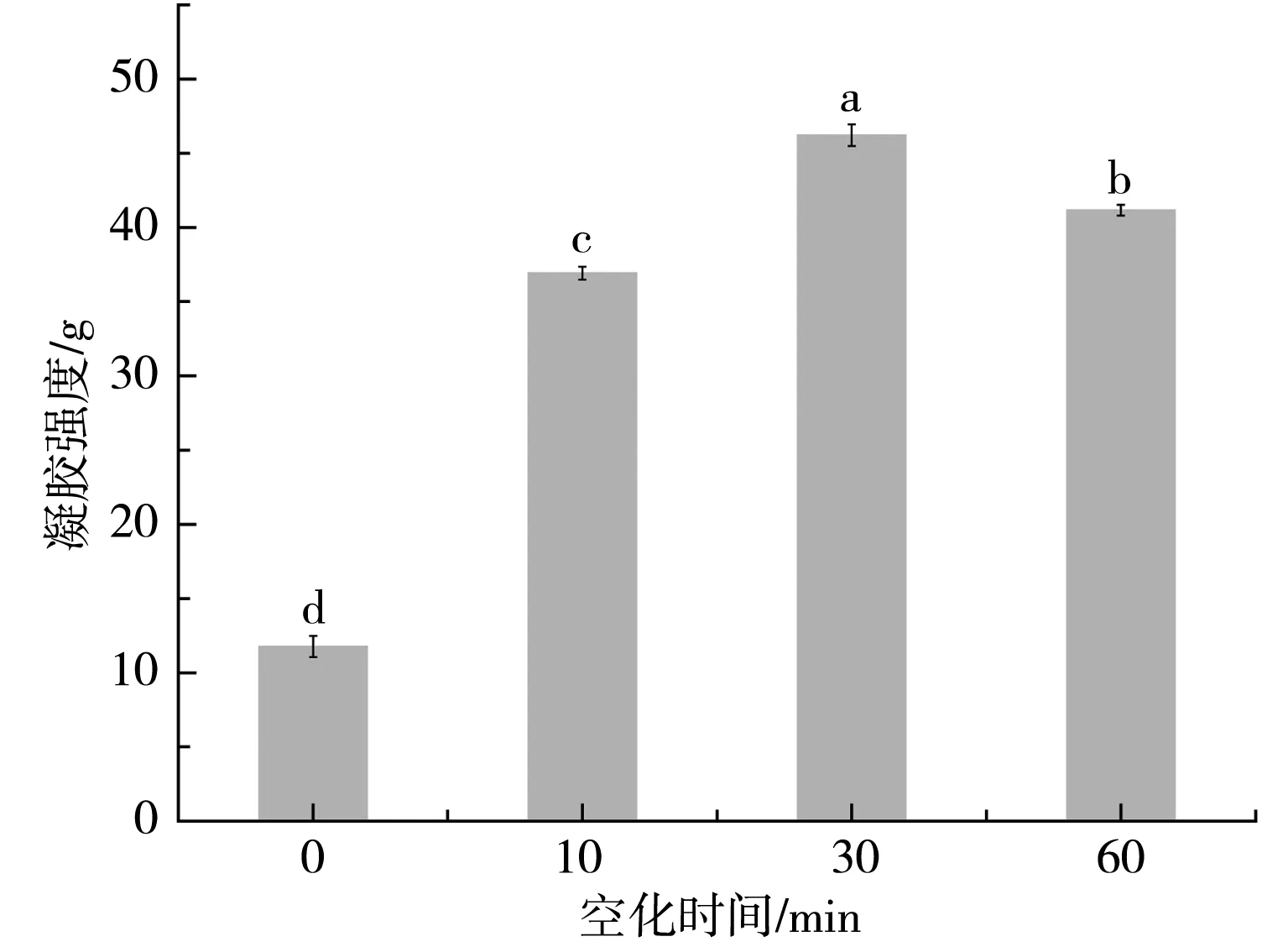
图1 水力空化处理对SPI钙致凝胶强度的影响Fig.1 Effect of HC treatment on calcium induced gel strength of SPI
2.2 水力空化处理对SPI钙致凝胶持水性的影响
持水性作为重要的凝胶特性之一,能间接地反映出凝胶空间网络结构的紧密程度。由图2可知,SPI经过水力空化处理后形成的钙致凝胶的持水性都有相应的增强。未处理的SPI形成的钙致凝胶持水性为(63.02±0.65)%,水力空化10,30,60 min后SPI形成的钙致凝胶持水性分别为(68.70±1.97)%、(89.76±0.76)%、(80.54±2.21)%。汪长青等[11]研究发现经过超声预处理形成的SPI凝胶持水性显著大于未处理样品,超声空化使蛋白质粒径分子减小,有助于形成均匀致密的凝胶网络,从而可以束缚住凝胶体系中的水,使凝胶具有较高的持水性。

图2 水力空化处理对SPI钙致凝胶持水性的影响Fig.2 Effect of HC treatment on water holding capacity of calcium induced gel of SPI
2.3 水力空化处理对SPI钙致凝胶流变学性质的影响
2.3.1 温度扫描
SPI分散液的钙致凝胶形成曲线随时间的变化见图3。

图3 水力空化处理对SPI钙致凝胶G′和 G″的影响Fig.3 Effect of HC treatment on G′ and G″ of calcium induced gel of SPI
由图3可知,在升温-保温-冷却的热循环过程中,SPI钙致凝胶样品的G′和G″随时间的变化基本呈现相同的变化趋势,均先下降再升高。初始升温阶段,与未处理的SPI相比,进行空化处理的SPI的G′和G″有所降低,使蛋白溶液体现出了更像液体的流变性。SPI分散液受到了外部应力的作用,破坏了分散液的黏弹结构,所以模量随着温度的升高而出现短期下降。当温度升高到一定的温度后,蛋白质分子去折叠,蛋白分子内部的疏水基团和巯基就会逐渐被暴露,在硫酸钙的作用下,蛋白分子发生了聚集,G′和G″开始增大。最开始G′小于G″,随着不断升温,G′快速增加,当G′=G″时,在此温度下,开始形成凝胶的空间网络结构。在交点过后,模量随着时间的延长不断增大,继续加热,蛋白分子间不断发生交联聚集,模量不断增加,在长时间高温的暴露下,疏水相互作用成为主要分子间作用力,凝胶的网络结构得到加强。在保温的过程中,G′和G″随时间的延长缓慢增大。在冷却的过程中,G′和G″迅速增加。这表明在升温和保温的过程中,SPI分散液逐渐从液态转变为固态特征行为的凝胶结构,在冷却过程中,钙致凝胶的空间网络得到增强。未进行空化处理的SPI在685.4 s时,G′=G″;水力空化处理10,30,60 min的SPI在1217,980.9,1040 s时,G′=G″。空化后的SPI成胶时间相对延后是因为水力空化降低了SPI的黏度。在冷却阶段结束后空化0,10,30,60 min的SPI最终形成凝胶的G′值分别为655.16,835.74,4723.60,1335.70 Pa。由此可见,水力空化可以显著提升SPI钙致凝胶的G′值,且水力空化30 min的SPI形成的凝胶最终G′值最大,进一步与前文凝胶强度结果相印证。秦新生[12]研究发现,超声处理30 min 时,SPI/WG蛋白酶致凝胶具有最高的G′值(2938 Pa),随后是40 min超声处理的凝胶(2698 Pa),均大于未经超声波处理的凝胶(2373 Pa)。
2.3.2 频率扫描
为了进一步检验水力空化处理后SPI钙致凝胶网络的形成情况,模拟凝胶后进行频率扫描。不同水力空化时间下对SPI形成凝胶的频率扫描见图4。

图4 最终形成的SPI钙致凝胶G′和G″随角频率变化的情况
由图4可知,钙致凝胶所有样品的G′值始终大于G″值,表明此时凝胶已经形成了较好的凝胶网络结构。在全频率扫描范围内,所有样品的G′和G″几乎不随着频率的增加发生变化,即G′和G″对振荡频率显示出较低的依赖性,这说明形成的凝胶网络结构稳定。通过频率扫描数据可以看出,水力空化可提高SPI钙致凝胶的G′值。
2.4 水力空化处理对SPI钙致凝胶分子间作用力的影响
由图5可知,经水力空化的SPI形成的钙致凝胶中离子键含量显著下降(P<0.05),空化30 min后的SPI凝胶的疏水相互作用和二硫键含量与未处理的相比显著增大(P<0.05),疏水相互作用和二硫键对分子构象的改变和蛋白分子聚集起主要作用,是凝胶形成的主要作用力。SPI钙致凝胶中氢键含量均小于2%,说明氢键对维持SPI凝胶结构的贡献较小。SPI经水力空化处理后分子内部的巯基和疏水基团暴露,导致在硫酸钙致使蛋白分子交联形成凝胶网络结构的同时,形成大量的二硫键,疏水相互作用增强,舒展的肽链通过二硫键和疏水相互作用构成蛋白聚集体进而形成均匀致密的凝胶网络结构[13]。

图5 水力空化对SPI钙致凝胶分子间作用力的影响Fig.5 Effect of HC on intermolecular forces of calcium induced gel of SPI
2.5 水力空化处理对SPI钙致凝胶微观结构的影响
由图6可知,未经水力空化处理的SPI形成的钙致凝胶微观结构多呈松散且无规则的粗糙鳞片状,经水力空化处理后的SPI形成的钙致凝胶网络结构相对紧凑致密,尤其水力空化处理30 min后形成了具有致密孔洞和均匀结构的凝胶网络结构。产生这种现象的原因是:一方面由于水力空化显著降低了蛋白粒径,增大了SPI的溶解度,使硫酸钙充分发挥了盐桥的作用,促进凝胶聚集体的形成。另一方面,水力空化导致游离巯基和疏水基团暴露于SPI蛋白分子的表面,有利于分子间疏水相互作用和二硫键的形成,形成致密稳定的凝胶结构。Hu Hao等[14]研究发现与未处理的SPI酸促凝胶相比,超声空化处理SPI形成的酸促凝胶具有更致密、更均匀的微观结构。李素云等[15]研究发现经超声预处理的小麦蛋白与壳聚糖复合物颗粒分布更加均匀,使复合物形成一种更致密的凝胶网络结构。由图6中d可知,延长水力空化时间到60 min,反而会形成较大的空洞结构,这种变化趋势与本文的凝胶强度、持水性和流变性质的实验结果相对应。

3 结论
对SPI分散液进行不同时间(10,30,60 min)的水力空化处理显著改善了钙致凝胶的凝胶性能。水力空化处理后的SPI形成的钙致凝胶中二硫键含量和疏水相互作用显著增加,成为凝胶形成的主要分子间作用力。SPI经水力空化处理后形成的钙致凝胶微观结构也变得更加致密均匀。水力空化处理还显著地增加了SPI钙致凝胶的凝胶强度、持水性和凝胶最终的G′值,而且水力空化30 min时均达到最大值,凝胶强度与未处理样品相比提高了3.9倍;持水性提升了26.7%;最终形成凝胶的G′值与未处理样品相比增大了7.2倍。可见,水力空化处理可作为食品蛋白质凝胶产业中加工的新技术。

