熊果酸固体分散体的制备与质量评价
张 领,段丽颖,武 倩
(河北省中药研究与开发重点实验室/ 承德医学院中药研究所,河北承德 067000)
熊果酸(ursolic acid,UA)别名乌索酸、乌苏酸,是从杜鹃花科熊果中提取的一种五环三萜类化合物,具有抗菌[1]、护肺[2]、保肝[3]、降血糖[4]、调血脂[5]等多种生理活性,和诱导胶质瘤细胞凋亡[6]、抗脑瘤[7]、抗癌[8]、治疗重症肌无力[9]、抗增殖活性[10]的作用。另外,UA具有明显的抗氧化功能[11],是一种较强的抗氧化剂,对人体的抗衰老、皮肤祛斑、祛色素都有积极作用。UA水溶性差,25℃时水中溶解度仅为7.16 μg/L[12],生物利用度低。现有的提高UA溶出度和提高生物利用度的制剂技术有自微乳冻干制剂[13]、纳米脂质体[14]、固体分散体等。其中固体分散体由于工艺简单,是常用于提高药物的溶出度和生物利用度的手段之一。文献报道有关熊果酸固体分散体(ursolic acid solid dispersions,UA-SD)的研究常采用载体如泊洛沙姆188[15]、PVP K30[16]等,近年来,随着科技的发展,出现了许多新的辅料,如聚乙烯已内酰胺-聚醋酸乙烯酯-聚乙二醇接枝共聚物(Soluplus)、维生素E聚乙二醇琥珀酸酯(TPGS)等,具有广泛的应用前景。其中,Soluplus具有良好的抑晶、增溶效果,为固体分散体的制备提供了更多选择。本课题优选新型载体材料,制备UA-SD,以提高药物的溶出度、生物利用度。
1 仪器与试剂
1.1 仪器
Agilent1260型高效液相色谱仪(美国安捷伦公司),AG-254电子分析天平(瑞士梅特勒-托利多公司),RC806溶出试验仪(天津天大天发公司),JA-2003电子天平(奥豪斯仪器有限公司),GT16-3型高速台式离心机(北京时代北利离心机有限公司),SHZ-DCZZZ循环水式真空泵(巩义市予华仪器有限责任公司),HZQ-C气浴恒温振荡器(天坛市天竟实验仪器厂),HF型热风循环干燥箱(吴江华飞电热设备有限公司),KQ2200DE型超声波清洗器(昆山市超声仪器有限公司),EYELA旋转蒸发仪(北京五洲东方科技发展有限公司),DSC250热分析仪(美国TA仪器),D8-Advance型X射线衍射仪(德国 Bruker公司),Nicolet380红外光谱仪(美国热电集团),Nano SEM430扫描电镜(美国FEI公司)
1.2 试剂
熊果酸原料药(宝鸡市金台区科瑞仪器经销部,批号:HU023144198),熊果酸对照品(成都普菲德生物技术有限公司,批号:19011506),Soluplus(北京凤礼精求医药股份有限公司),TPGS(湖北鸿运隆生物科技有限公司),PVP VA64(德国BASF公司),PEG 6000(北京凤礼精求医药股份有限公司),SDS(天津市光复精细化工研究),柠檬酸(天津市标准科技有限公司),磷酸氢二钠(天津欧博凯化工有限公司),磷酸二氢钾(天津市科密欧化学试剂有限公司),氢氧化钠(天津欧博凯化工有限公司),浓盐酸(北京化工厂),甲醇(色谱纯,Fisher Technology Inc,USA),磷酸(色谱纯,Fisher Technology Inc,USA),无水乙酸钠(天津市佳兴化工玻璃仪器工贸有限公司)
2 UA的含量测定方法
2.1 色谱条件
色谱柱:Kromasil 100-5-C18(150×4.6mm);流动相:甲醇-0.1%磷酸水(90:10),流速为1.0 ml/min;柱温:30℃;进样量:10μl;检测波长:210nm。
2.2 溶液的配制
对照品溶液的配制:精密称取UA对照品约3mg,置容量瓶中,加甲醇,超声,放冷,定容,即得。
供试品溶液的配制:取样品,加入甲醇,超声,放冷,定容,即制得供试品溶液。
2.3 标准曲线的绘制
精密量取对照品溶液,注入HPLC测定,以峰面积对UA浓度做图,得方程:Y= 4.2989X + 2.6741,R2= 0.9994,线性范围:8~102μg/ml。
2.4 回收率实验
精密吸取2.2项下UA对照品溶液,加入处方比例辅料,用适量甲醇稀释得低、中、高3种浓度,每个浓度平行实验3次,按2.1色谱条件进行测定,计算回收率。结果显示,UA样品的回收率均在95%~105%范围内,RSD值均小于2%,符合标准。见表1。
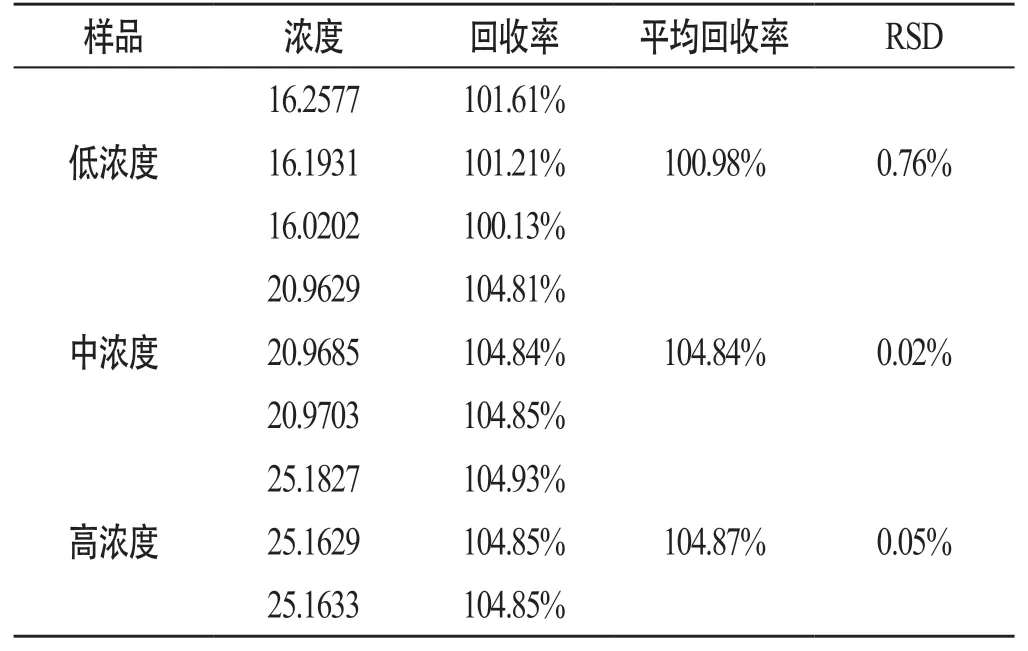
表1 UA样品回收率
3 结果
3.1 抑晶实验
3.1.1 实验条件 选用介质为0.2%十二烷基硫酸钠(sodium dodecyl sulfate, SDS)水溶液,900ml,温度37℃,转速50r/min,桨法。
3.1.2 实验方法 精密称取Soluplus、PVPVA64、TPGS三种辅料各360mg,置于900ml 0.2%SDS中。精密称取UA原料药34mg,用4ml甲醇超声溶解,制得UA原料药溶液。将UA原料药溶液加入溶出介质中,在水中形成超饱和溶液,于5、10、15、30、45、60、90、120min分别取样5ml,迅速补充同温空白介质5ml。样品过0.45μm微孔滤膜后,用HPLC检测,绘制不同载体对UA超饱和溶液析晶抑制效果曲线图。结果显示,三种载体对UA超饱和溶液的析晶均有一定抑制作用,但Soluplus的抑晶效果最为突出,故选用Soluplus制备UA-SD。见图1。
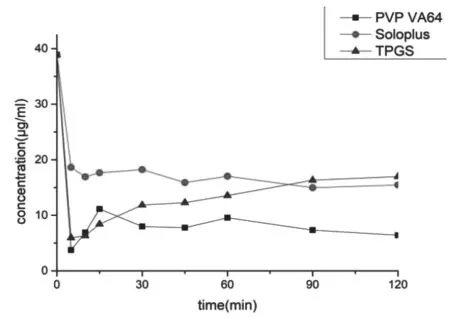
图1 不同载体对UA超饱和溶液析晶的抑制作用
3.2 UA-SD的制备
3.2.1 UA-SD制备方法 采用溶剂法制备UA-SD,按照1:3、1:5、1:7、1:9、1:11、1:15的比例,精密称取UA原料药与Soluplus,将UA原料药与载体分别溶于适量无水乙醇中,超声至完全溶解,将载体的乙醇溶液加入原料药的乙醇溶液中,超声10min,于50℃减压回收乙醇,得到白色固体后,置于干燥器内24h,取出,研细,即得到不同比例的UASD。
3.2.2 UA物理混合物的制备方法 精密称取适量UA原料药与Soluplus,采用搅拌的方法将2者混匀,制备载药比1:3、1:5、1:7、1:9、1:11、1:15的UA物理混合物。
3.3 溶出实验
参照《中国药典》四部,桨法,100r/min,37℃,溶出介质为0.2%SDS水溶液,900ml。样品分别为:UA原料药25mg、不同载药比的UA-SD、不同比例的物理混合物(含UA25mg)。于5、10、15、30、45、60、120min分别取样5ml,同时补充同温溶出介质5ml,0.45μm微孔滤膜后,注入HPLC检测,绘制溶出曲线。结果显示,120min时,UA原料药的累积溶出度为10.1%,UA-SD1:3时累积溶出度为36.5%、UA-SD1:5时累积溶出度为39.7%、UA-SD1:7时累积溶出度为48.6%、UA-SD1:9时累积溶出度为59.0%、UA-SD1:11时累积溶出度为102.7%、UA-SD1:15时累积溶出度为87%、PM1:3时累积溶出度为6.67%、PM1:5时累积溶出度为6.73%、PM1:7时累积溶出度为5.60%、PM1:9时累积溶出度为5.75%、PM1:11时累积溶出度为4.74%、PM1:15时累积溶出度为6.32%。与原料药相比,物理混合物在120 min时累积溶出度无明显增加,而UA-SD在120min累积溶出度明显增高,其中1:11和1:15的SD增加最为明显,故选择两个比例的样品进行表征。见图2。
可以组建营销团队,讲好朱家尖故事,围绕故事展开AR内容设计,让游客的行程更加有趣,在应用中充分考虑社交化,让口碑传播通过生动有趣的AR应用迅速且广泛传播。
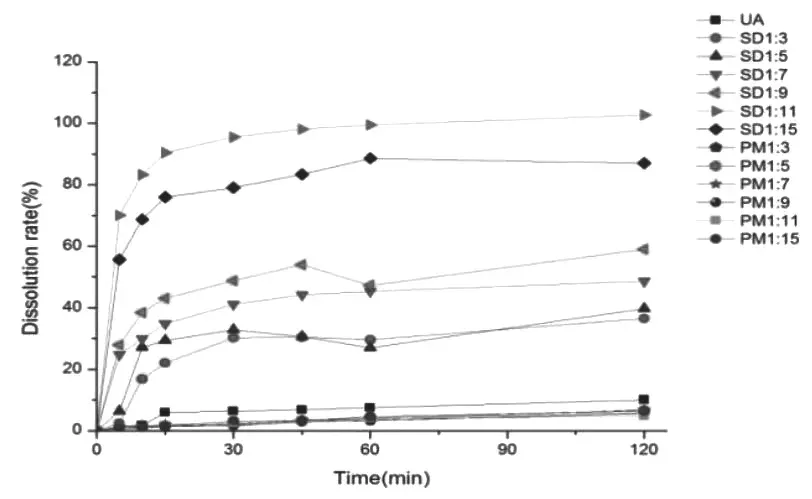
图2 不同样品的溶出曲线
3.4 溶解度实验
3.4.1 介质的配制 按照《中国药典》2015版溶液配制方法分别配制pH1.2、4.5、6.8、7.2的缓冲溶液,以及加入0.2%
SDS的 pH1.2、4.5、6.8、7.2缓冲溶液以及0.2% SDS水溶液。共10种介质。
3.4.2 溶解度实验 在6.1配制的10种介质中分别加入过量UA原料药、不同载药比UA-SD、物理混合物。将样品放入37℃恒温振荡箱中振荡48h,经13000r/min离心20min后,过0.45μm滤膜,注入HPLC进行检测。结果显示,介质中加入0.2%SDS可有效增加样品的溶解度,同时UA-SD在不同介质中的溶解度大于物理混合物的溶解度,并且随着载药比的不同,溶解度增加程度不同。见表2、图3。
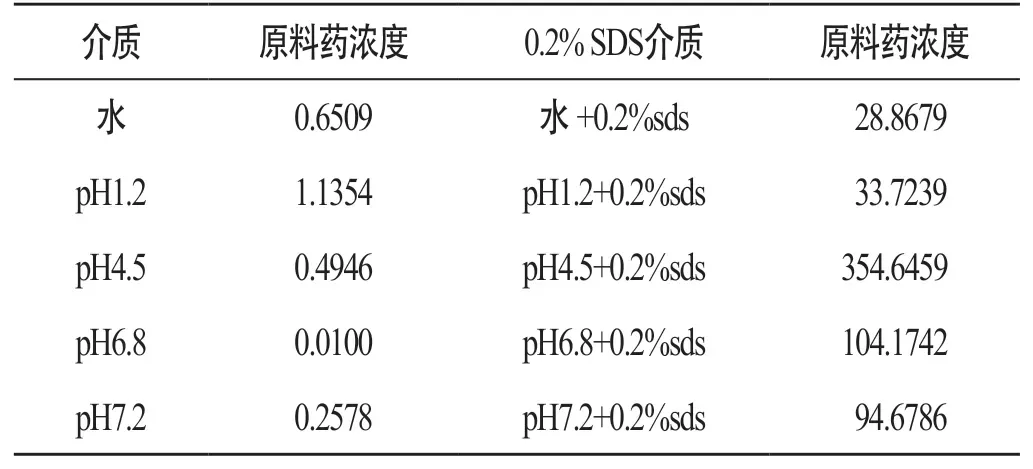
表2 UA原料药在水及0.2%SDS水中的溶解度(μg/ml)
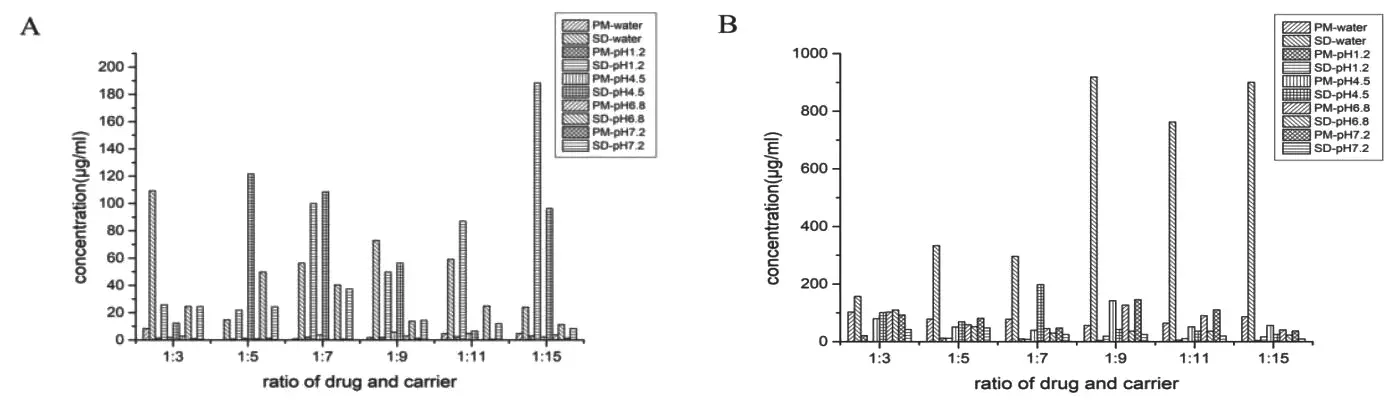
图3 不同载药比例UA-SD、物理混合物在不同介质中的溶解度
3.5 理化性质表征
3.5.1 扫描电镜法(scanning electron microscope, SEM) 取适量样品,用扫描电镜对样品进行分析。测试条件:电流10 mA,加速电压5.0 kV。将SEM图放大100倍时观察图像,见图4。

图4 SEM图谱
由图4A可知,UA原料药为不规则棱柱形晶体,由图4B可知,载体Soluplus近似球状,由图4C、4E可知,1:11、1:15的UA-SD为不规则的团块状,由图4D、4F可知,1:11、1:15的UA物理混合物为Soluplus球状载体上粘附有UA原料药。
3.5.2 差示扫描量热法(differential scanning calorimetry,DSC) 选用DSC250热分析仪进行分析。测试条件:扫描范围为25 ℃~300 ℃,升温速度为10 K/min,见图5。
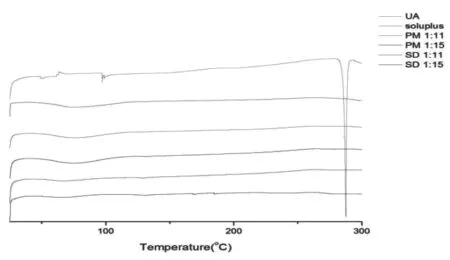
图5 DSC图谱
由图5可知,UA原料药的晶体特征吸热峰出现在285℃左右,载体Soluplus的吸热峰不明显,在75℃左右,为一宽、钝的吸热峰。而UA物理混合物中并未出现UA的吸热峰,仅存在载体的特征吸热峰,可能是载体融化时导致药物溶解在载体中,进而未出现UA的特征吸热峰。UA-SD中也仅有较弱的载体特征吸热峰,未出现UA的特征吸热峰。
3.5.3 X射线衍射法(X-Ray Diffraction, XRD) 取适量样品,进行X射线衍射分析。仪器工作电压:40kV,工作电流:40mA,Cu靶。实验条件:2θ扫描范围3~50度,步长0.02度/步,见图6。
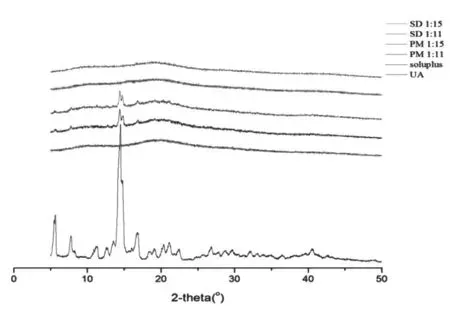
图6 XRD图谱
由图6可知,UA原料药5.47°、7.77°、10.87°、12.60°、13.52°、14.46°、16.76°、19.03°、20.35°、21.15°、22.48°、26.76°等处存在较明显的特征衍射峰,而载体Soluplus不存在上述衍射峰;UA物理混合物中,尽管UA的某些特征衍射峰被掩盖,但在7.77°、10.87°、14.46°、16.87°仍可观察到变弱的UA特征衍射峰的存在,表明UA被载体稀释,特征衍射峰减弱,但仍以晶体形式存在;而在UA-SD中UA的特征衍射峰则完全消失,表明UA在SD中可能以无定形形式存在。
3.5.4 傅里叶变换红外光谱法(fourier transform infrared spectroscopy, FT-IR) 取样品适量,与适量的KBr研磨、混合均匀后压片,在400~4000 cm-1波长范围内进行傅里叶红外光谱扫描,记录相应谱图,见图7。
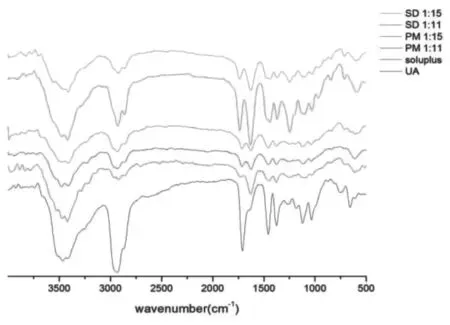
图7 FT-IR图谱
由图7可知,UA原料药中存在2个特征峰,3469cm-1处存在较强的-OH峰,1709cm-1处存在较强的C=O峰。载体Soluplus在1629cm-1处存在一较为明显的特征峰,可区别于UA原料药。UA-SD中,-OH峰由3469cm-1移向低频区3417cm-1,C=O峰由1709cm-1移向高频区1725cm-1,峰强度减弱,同时保留了Soluplus在1629cm-1处的特征峰,UA物理混合物中未出现新峰,可以认为是UA原料药与载体的简单加和。
3.6 工艺验证
根据3.2.1项下的实验方法,制备UA-SD,平行制备3份。根据3.3项下实验方法,对每份UA-SD进行溶出实验,平行3份。经HPLC检测,绘制累积溶出曲线,见图8。
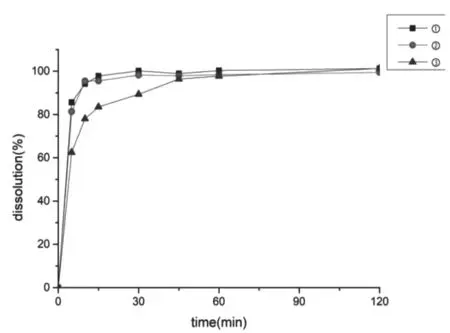
图8 工艺验证UA-SD(1:11)溶出曲线
由图8可知,3批UA-SD1:11累积溶出度在120min时分别达到101%、99%、101%,与3.3项溶出实验结果无较大差异,即可证明此工艺适用于本实验。
4 讨论
UA具有溶解度小、溶出速度慢的特点,故本研究用溶剂法将其制备成固体分散体以提高UA的溶解、溶出度。固体分散体中,载体抑制了被高度分散的粒子聚集趋势(抑晶性),且载体本身可促进药物的溶出。由于UA在无水乙醇中溶解度较好,可以减少实验中溶剂用量,且无水乙醇无毒性,本研究在固体分散体的制备过程中,选用了无水乙醇作为溶剂。实验操作过程中注意事项有:抑晶实验时,注意样品的保温,防止因温度变化导致药物析晶,影响检测结果;溶出度实验时,注意防止药物粘附在溶出杯壁及桨上,否则影响检测结果;溶解度实验时,注意观察不同pH缓冲液中是否出现析晶,以免影响实验结果。
由实验结果可以得出,UA-SD在120min时累积溶出度为102%,远远高于UA原料药及物理混合物的累积溶出度。可能因为UA原料药在SD中以无定形状态存在,分散度增加,故累积溶出度增加。在一定的范围内,固体分散体的累积溶出度随载药比的增大而增加。由此看出,固体分散体成功使原药物的溶解度大大提高,改善了其溶出速率。通过理化性质表征结果显示,FT-IR中峰形的变化提示UA与载体之间形成了氢键。UA原料药以无定形状态分布在载体中,UA原料药的晶体结构发生变化,故累积溶出度得到了提高。
综上所述,以Soluplus为载体制备UA-SD,可明显提高UA的体外溶出度。

