中药配方颗粒质量标准薄层鉴别与液相指纹图谱/特征图谱研究现状及对照提取物应用可行性探讨
饶丽芬 李泳雪 郭隆钢
1广州白云山奇星药业有限公司,广州 510530;2广东省药品检验所,广州 510663;3广州科曼生物科技有限公司,广州 510700
自2001 年12 月1 日配方颗粒纳入中药饮片管理范畴,从此配方颗粒正式开始了产业发展和使用的历史,并通过试点生产企业和试点医院的推行,积累了大量的质量和临床数据。多年来,国家药品监督管理局以及国务院不断对配方颗粒产业的发展和质量要求多次发文[1-4]。近3 年来,国家配方颗粒质量标准和地方标准也在不断发文和完善中[5-6]。2021 年《国家药监局国家中医药局国家卫生健康委国家医保局关于结束中药配方颗粒试点工作的公告》(以下简称《公告》)已正式发布,结束了长达20 年的中药配方颗粒试点工作[7]。并开始了各省地区地方标准制订的工作,使国家配方颗粒质量标准开展全国范围的标准制订工作有序进行。《公告》要求中药配方颗粒省级标准的制订应严格按照《中药配方颗粒质量控制与标准制订技术要求》执行,主要关注点包括:(1)研究用样品的代表性;(2)标准汤剂研究的标准性;(3)工艺研究的合理性;(4)质量标准研究的科学性、严谨性;(5)质量标准复核的重要性[8]。截止到本文撰写日,国家配方颗粒质量标准已经有196 个品种公布,各省地区也有多个质量标准发布,其中广东省发布最多,共256 个[9]。从标准内容来看,多数省份与广东省发布标准多个品种相同,这与广东省作为中药以及配方颗粒产业大省有密切关系。
目前,绝大多数配方颗粒质量标准都已经建立了薄层鉴别的方法,国家配方颗粒质量标准中,指纹图谱有部分应用,特征图谱有较多应用;在地方标准中,指纹图谱少数应用,特征图谱有较多应用。
国家配方颗粒质量标准中,黄柏配方颗粒[10]和枳壳配方颗粒[11]使用对照提取物作为薄层鉴别用标准物质;广东省配方颗粒质量标准中,盐巴戟天配方颗粒使用对照提取物用于薄层鉴别以及特征图谱分析。
配方颗粒质量标准薄层色谱鉴别方法的应用情况及问题
目前已公布的196 个国家标准配方颗粒品种中,全部都有薄层色谱鉴别方法,大多数沿用了目前中国药典相应药材标准的薄层鉴别方法,少数品种有新的鉴别方法。
从1990 年版《中国药典》开始,使用对照药材作为薄层鉴别的参照物得到了广泛应用,部分解决了当时中药鉴别使用化学对照品缺乏专属性的问题。薄层色谱亦得到了大范围的应用和技术提高,然而翻阅后续多个版本的中国药典,很多品种薄层鉴别方法并没有进行修订或提高,在2010 年版、2015 年版《中国药典》的薄层色谱图集中,一些新的薄层鉴别方法已经纳入其中,但并未在中国药典一部中进行修订[12-13]。配方颗粒质量标准中大多数沿用中国药典的薄层鉴别方法,已经有几十年未有修订,随着薄层色谱技术的发展和仪器、薄层板等耗材的不断进步,有些陈旧的方法已经不适应现有检测条件,前处理复杂、有毒试剂如氯仿等作为提取溶剂、显色剂不合理的情况时有出现,增加了配方颗粒质量标准应用时的操作难度以及安全隐患。相对液相指纹图谱/特征图谱来言,薄层鉴别的分离度相对较低,操作中实验者的人为因素影响较大,实验水平差异巨大,导致薄层色谱的技术和操作规范性的重视程度远远不够,这也是配方颗粒质量标准中薄层鉴别方法并无较大提高的原因之一。
如人参配方颗粒质量标准(国家药品标准YBZ-PFKL-2-21186)[14]薄层鉴别仍沿用中国药典中样品前处理方式:取本品0.2 g,研细,加水0.5 ml 搅拌湿润,加水饱和正丁醇10 ml,超声处理30 min,吸取上清液加3倍量氨试液,摇匀,放置分层,取上层液蒸干,残渣加甲醇1 ml使溶解,作为供试品溶液。另取人参对照药材1 g,加水50 ml,煎煮30 min,滤过,滤液浓缩至近干,加水饱和正丁醇10 ml,同法制成对照药材溶液。对照药材溶液的制备前处理复杂,且正丁醇沸点较高(117.25 ℃),导致整个前处理过程耗时较长,目前大多数国家配方颗粒标准或各省地方标准中薄层鉴别所使用对照药材做为参照物的制备方法中均需要先加水煎煮再进行前处理,大大增加了操作时间。
再如大青叶配方颗粒质量标准(国家药品标准YBZ-PFKL-2021033)[15]、杜仲配方颗粒质量标准(国家药品标准YBZ-PFKL-2021040)[16]、钩藤(钩藤)配方颗粒质量标准(国家药品标准YBZ-PFKL-2021052)[17]、浙贝母配方颗粒质量标准(粤PFKL0117)[18]多个品种中,薄层鉴别中供试品制备使用三氯甲烷作为提取溶剂,毒性较强。
再如炒白芍配方颗粒质量标准(国家药品标准YBZ-PFKL-2021016)[19]、赤芍(芍药)配方颗粒质量标准(国家药品标准 YBZ-PFKL-2021026)[20]薄层鉴别所用显色剂为5%香草醛硫酸溶液,酸枣仁配方颗粒质量标准(国家药品标准YBZ-PFKL-2021191)[21]薄层鉴别所用显色剂为1%香草醛硫酸溶液,其硫酸均为浓硫酸,腐蚀性强,在喷雾显色操作中需要有足够好的通风和保护条件,否则对于操作人员健康会造成伤害,且浓硫酸吸水性极强,导致在日常湿度较大的省份很容易在显色后吸水放热,整个薄层板面斑点有大量水印影响判断,可使用1%香草醛-10%硫酸甲醇(或乙醇)等显色剂更为合理。
现有大部分薄层鉴别方法的展开剂经过了多年的应用,基本可以满足鉴别的需求,供试品处理以及显色条件方面的改变,所需预实验难度远远低于展开剂的选择,希望这些沿用多年的方法可以做出更人性化的修订,从而提高检测的效率、安全性和可靠性。
配方颗粒质量标准指纹图谱/特征图谱方法的应用情况及问题
在国家及地方配方颗粒质量标准中,指纹图谱/特征图谱作为中药多成分质量分析的重要方法得到了广泛应用,将配方颗粒整体质量标准提高了一个档次,是配方颗粒质量标准乃至中药质量标准的重大进步,其涵盖范围远远超过目前2020 年版《中国药典》中的药材质量标准的应用数量。
在现行配方颗粒质量标准指纹图谱/特征图谱的方法中,大部分在参照物溶液部分使用了对照药材或对照饮片作为多成分的参照物,少部分使用化学对照品作为参照物,并以计算相对保留时间的方法作为分析判断的标准。
在标准起草及复核过程中,特征图谱的特征峰相对保留时间问题有较多争议和讨论。使用不同的色谱仪器以及色谱柱时,相对保留时间有个别超出标准制订的范围,但并不能作为判断其质量不合格的标准。使用对照药材作为随行对照,在一定程度上可以解决该问题,但由于对照药材/对照饮片与已经经过工业化生产的配方颗粒在很多品种上成分有着较大差异,为了解决此问题,参照物中对照药材/对照饮片的供试品溶液制备方法往往需要先使用水煎煮,再进行进一步的处理,大大增加了前处理难度,且实际应用中依然有部分品种无法通过使用对照药材/对照饮片做随行对照来解决相对保留时间的问题,这与对照药材/对照饮片本身或因不同批次或产地导致的内在成分差异相关。
解决此问题的备选方案中,使用配方颗粒对照提取物作为参照物是更为可行的方法。广东省配方颗粒质量标准中,盐巴戟天配方颗粒[22]的薄层鉴别以及特征图谱首先使用了对照提取物作为参照物,从技术角度来讲是一个进步,其特征图谱分析结果见图1、图2。
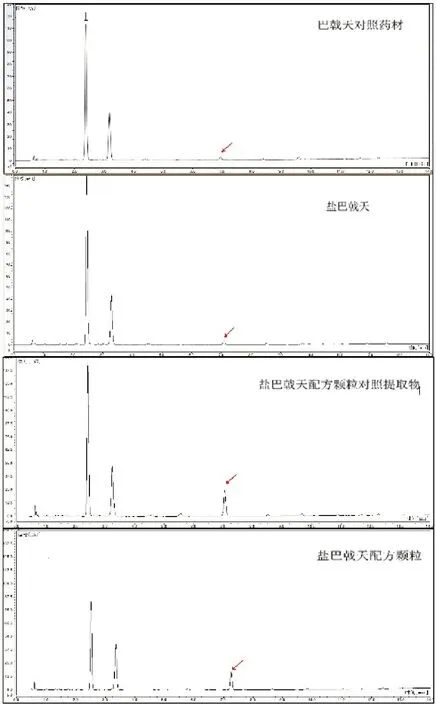
图1 盐巴戟天配方颗粒环烯醚萜类指纹图谱
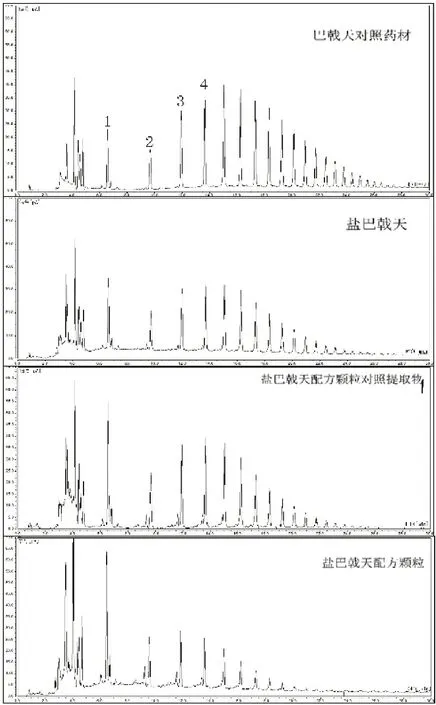
图2 盐巴戟天配方颗粒寡糖类特征图谱
将对照药材供试品制备方式按照水煎煮处理后进一步处理,所得到对照药材溶液特征图谱仍与饮片或者配方颗粒有较大不同。盐巴戟天为经过炮制(有蒸制这一步)的饮片,其中环烯醚萜类和寡糖类成分均会产生变化,故而使用巴戟天对照药材作为盐巴戟天配方颗粒质量标准的参照物不够合理。经过标准化制备的配方颗粒对照提取物则更加适合本品种特征图谱分析使用,其色谱行为与盐巴戟天饮片(按照标准汤剂制备方法制备样品)更为一致。
另有部分品种特征图谱色谱峰较多,多个特征峰保留时间很接近,给结果判定带来一定难度,如灵芝(赤芝)配方颗粒质量标准(国家药品标准YBZ-PFKL-2021086)[23],见图 3。
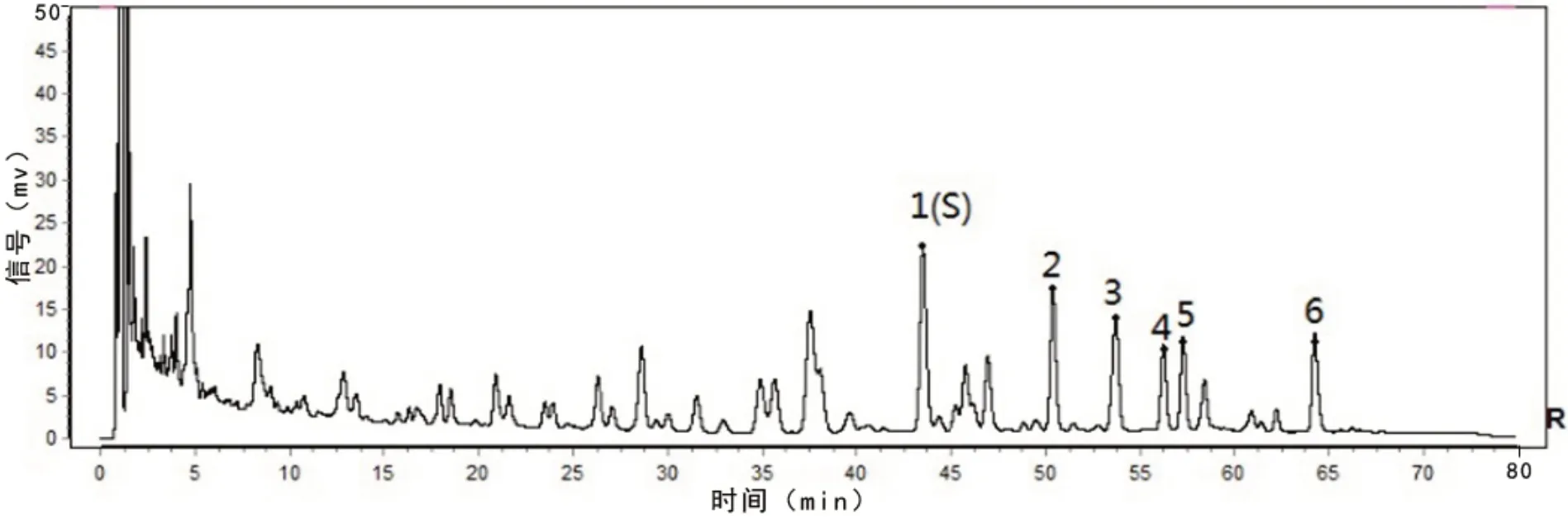
图3 国家药品标准YBZ-PFKL-2021086灵芝(赤芝)对照特征图谱
国内对照提取物生产厂家与欧洲药典会在关于赤芝质量标准标准物质、赤芝对照提取物应用于SST(系统适应性实验),实验讨论中所使用超高效液相色谱(UPLC)色谱分析方法多个色谱峰分离度较好,值得参考借鉴,见图4。

图4 欧洲药典会赤芝质量标准草案赤芝样品及对照提取物UPLC指纹图谱
对照提取物应用于配方颗粒质量标准的可行性探讨
1、研究背景介绍
对照提取物/标准提取物在近年来国内外质量标准的应用范围逐渐扩大,此技术方法在20 世纪90 年代德国银杏叶制剂中已经开始使用,使用标准提取物结合指纹图谱分析的方法,银杏叶制剂得到了有效的质量控制,从含量上有上下限的要求,从多个成分指认上使用色谱峰指纹图谱相似度来控制,此种手段还解决了当时国内银杏叶制剂质量的若干问题,如使用芦丁掺假以提高黄酮含量等[24-25]。
配方颗粒质量标准其核心离不开对于“标准汤剂”的研究,国家药监局配方颗粒质量标准指导原则中要求不得少于15 批原料制备得到“标准汤剂”,并进一步分析其出膏率、转移率、指纹图谱/特征图谱色谱峰指认等数据,此要求对于控制配方颗粒的质量稳定有着重要的指导意义。根据“标准汤剂”得到的指纹图谱/特征图谱为质量标准的标准图谱,而参考“标准汤剂”制备工艺经标准化制备的配方颗粒对照提取物,则可作为多成分的标准物质,数据化的标准图谱离不开标准物质的实体,并且随着分析手段的不断进步,标准图谱的优化可以使用对照提取物来进一步开发方法,使得标准的不断提高和图谱的不断进步一直有标准物质的实物作为参照,两者不可缺少。
2021 年中检院发布的《对照提取物技术指导原则》以及广东省药品检验所发布的《标准物质研制技术指导原则》中,对于对照提取物以及配方颗粒中对照提取物的研制规范有明确要求,要求基原明确,原料不得少于15 批,对于薄层鉴别以及特征图谱鉴别用的对照提取物其批间相似度不得低于0.95,对于指纹图谱分析用的对照提取物其批间相似度不得低于0.985。在实际执行中参照“标准汤剂”的要求以及相关指导原则的要求,对照提取物作为实验室规模可以制备的标准物质,可以较容易控制到与“标准汤剂”的一致性以及代表性。结合配方颗粒质量标准中薄层鉴别,指纹图谱/特征图谱分析的需求,对照提取物是更为合理的随性参照物。该标准物质具备比对照药材/对照饮片更为均一和批间一致性高的优势[26],前处理较简单,可减少实验人员的操作难度以及由此带来的操作误差。
2、对照提取物应用于配方颗粒质量标准部分品种的研究情况及所解决问题的讨论
2.1、枳壳对照提取物 使用枳壳对照提取物对7 批不同厂家生产的枳壳配方颗粒进行薄层色谱与高效液相指纹图谱色谱的分析,图谱见图5~8。
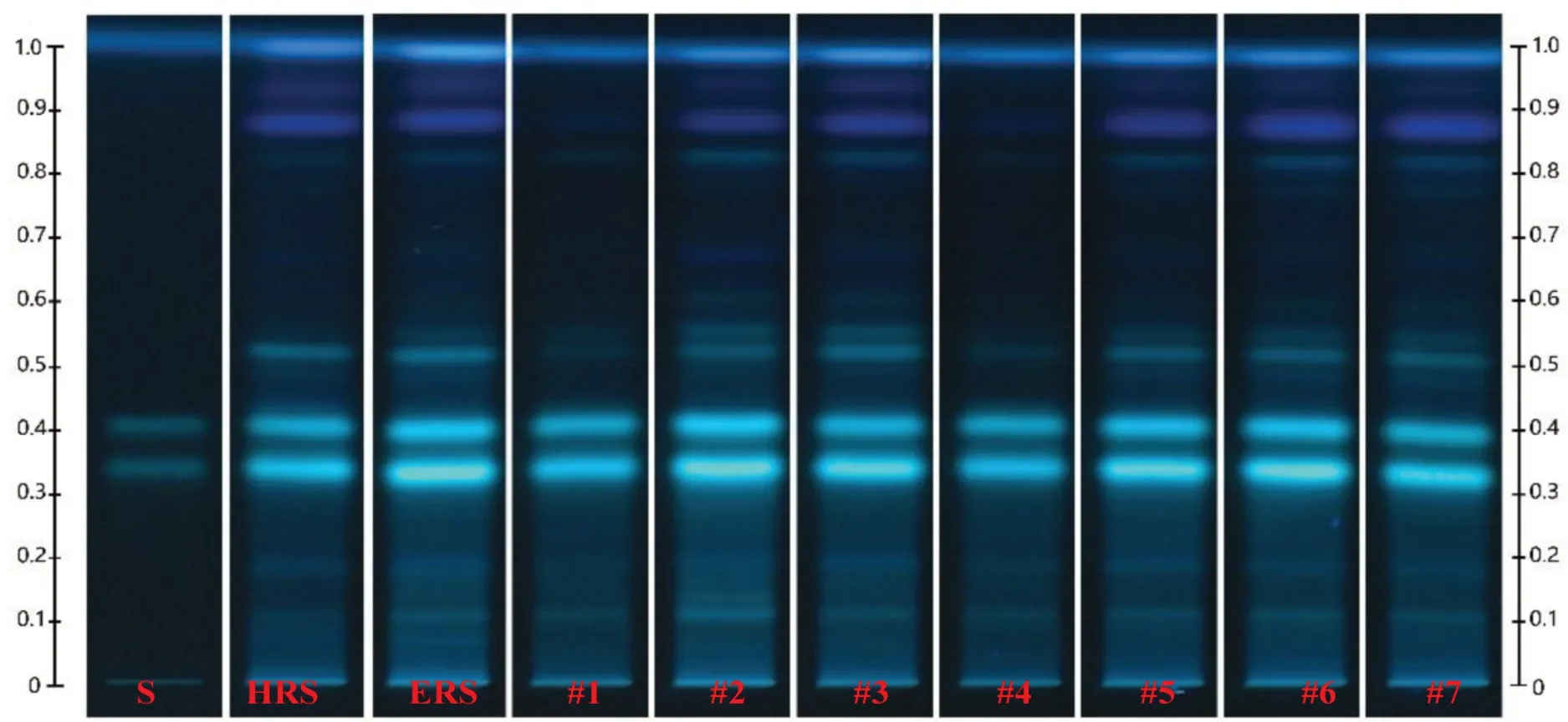
图5 枳壳ERS与枳壳颗粒TLC图谱(黄酮苷类)
现行标准中关于特征图谱色谱峰相对保留时间有明确规定,然而在使用相同粒径但不同柱长的色谱柱时,得到的色谱如图8。
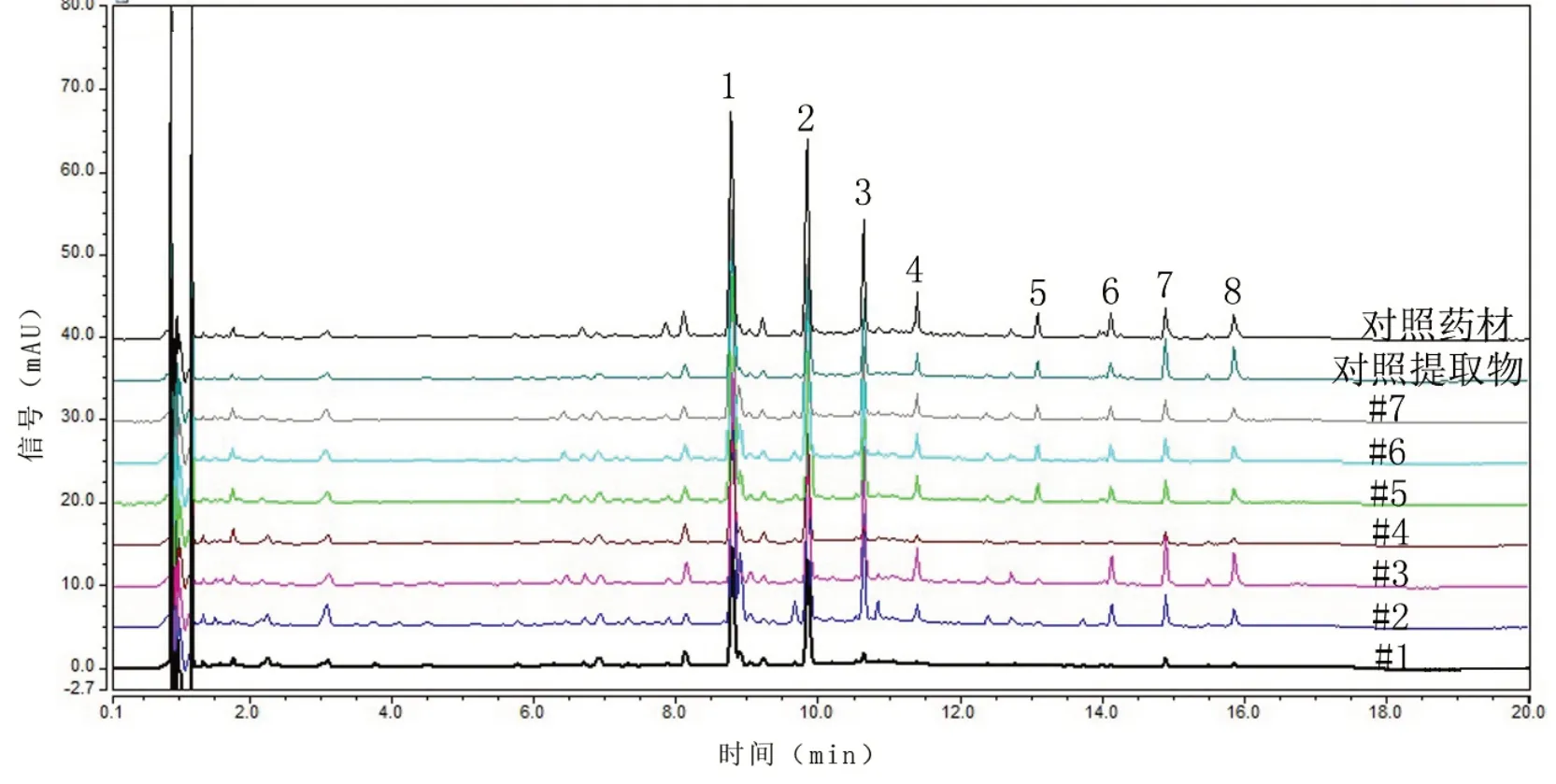
图8 枳壳配方颗粒指纹图谱分析
虽然各特征峰均有较高的分离度,但经计算多个色谱峰的相对保留时间不在公示质量标准范围内。若使用对照提取物计算色谱相似度,则样品#2、#3、#5、#6、#7 与对照提取物相似度>0.9,质量较好,其质量情况亦可以在薄层色谱中反映出同样的结果。使用对照提取物为参照物可以适用于枳壳配方颗粒指纹图谱分析,说明使用对照提取物可以解决部分靠单纯计算相对保留时间而引起的误判问题。
2.2、黄柏对照提取物 使用黄柏对照提取物对收集自中国台湾地区和大陆的14 批配方颗粒进行薄层色谱分析,结果见图9。

图9 黄柏对照提取物与黄柏配方颗粒TLC图谱
图谱显示不同厂家之间黄柏配方颗粒的质量有明显差异,大陆几家厂家的配方颗粒质量相对稳定,需要注意的是使用碘化铋钾对黄柏中生物碱类成分显色时,需喷以足够量的显色剂才可以得到清晰图谱,在实际操作中若不注意则待检测斑点颜色会较浅或者无法显示,薄层色谱操作的规范化对于实验结果的判断非常重要。
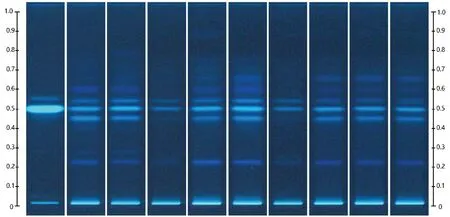
图6 枳壳ERS与枳壳颗粒TLC图谱(黄酮苷元类)
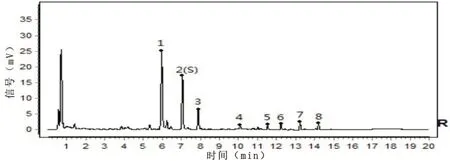
图7 枳壳配方颗粒国家标准对照特征图谱
2.3、黄芪(蒙古黄芪)配方颗粒质量标准特征图谱高效液相色谱/蒸发光散射检测器(HPLC-ELSD)结果分析 对一批黄芪(蒙古黄芪)配方颗粒进行特征图谱中HPLC-ELSD 分析,并对两批对照药材同步进行分析,得到的结果见图10。
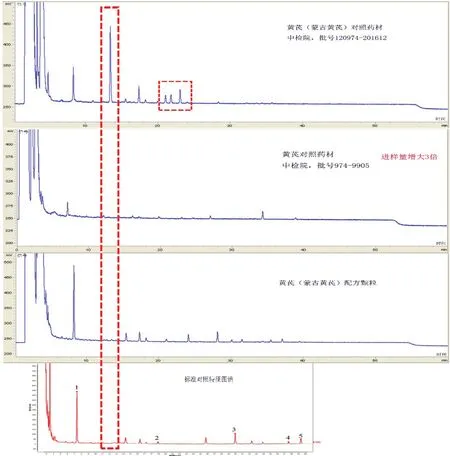
图10 黄芪(蒙古黄芪)配方颗粒及对照药材HPLC-ELSD图谱
所收集两批中检院的黄芪对照药材,其中现有批次为120974~201612,另一批时间较久,使用两者按照配方颗粒公布标准(国家药品标准YBZ-PFKL-2021065)特征图谱分析的方法分析,发现两批图谱差异巨大,可能跟批号974-9905 已过期有关,但现有批次成分与配方颗粒样品以及公布稿的对照特征图谱仍有较大差异,且在此条件下无法找到4 号峰及5 号峰。使用黄芪(蒙古黄芪)配方颗粒对照提取物作为参照物分析结果见图11。
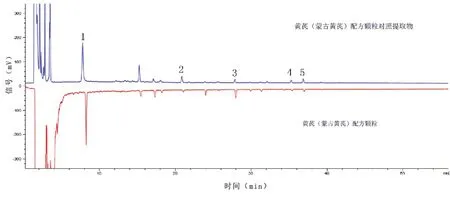
图11 黄芪(蒙古黄芪)配方颗粒及对照提取物HPLC-ELSD图谱
两者图谱中5 个色谱峰均对应一致,对照提取物可以作为配方颗粒特征图谱的随行对照参照物,经过标准化的制备,对照提取物极大减少标准物质的批间差异。
2.4、炒赤芍(芍药)配方颗粒对照提取物 在本品中对照提取物的研发过程中,收集样品阶段发现赤芍(芍药)样品目前存在有较多的掺伪情况,经进一步调查,发现伪品多为“山赤芍”(习称),从2016 年开始,在山西及西北地区有较多的“家种赤芍”,其饮片外观与传统的野生赤芍非常接近,然而经分析其成分含有较多的芍药内酯苷(图12),而正品野生赤芍(芍药)基本不含芍药内酯苷,白芍中此成分常见,猜测在种植过程中农户所使用种子有误。按照目前中国药典赤芍药材标准及地方标准中炒赤芍饮片标准,均无法对其进行有效区分,仅仅以芍药苷作为指标成分或仅仅使用部分特征峰指认,将无法对“山赤芍”进行辨认,在标准执行中可能会出现投料有误但无法检出的问题。希望相关部门和标准起草单位引起一定的重视。

图12 赤芍及“山赤芍”部分样品分析
总结
现行配方颗粒质量标准的优点:(1)针对每个基原有单独的质量标准,确保了原料基原的稳定。(2)制法有明确的量化数据,控制了生产工艺的稳定。(3)大量应用特征图谱分析方法并部分应用指纹图谱分析方法,做到了配方颗粒质量的整体控制。(4)指标成分含量设置上下限并确定了其规格相当于药材的比例,保证了配方颗粒质量的相对稳定。
存在的部分问题:(1)薄层色谱方法陈旧,条件待完善。(2)在省级质量标准制订中标准物质不足或难以找到法定标准物质,对质量标准的提升不利。(3)特征图谱/指纹图谱色谱峰指认对于仪器及色谱柱的要求苛刻。
对配方颗粒质量标准薄层鉴别与液相指纹图谱/特征图谱方法的几点建议:(1)建议对薄层色谱方法进行优化,尤其在前处理、显色剂方面进行简单优化,以方便实验操作。进一步针对配方颗粒专属性的成分开发薄层色谱鉴别方法。(2)建议在研究中逐步将特征图谱替换为指纹图谱分析,更能保障其质量稳定可控。(3)建议广泛应用配方颗粒对照提取物在薄层色谱鉴别、特征图谱/指纹图谱分析中。
利益冲突所有作者均声明不存在利益冲突

