阿奇霉素胶囊人体生物等效性研究
欧明洪,何海霞,贾旭明(1.四川达州市中心医院药学部,达州市 65000;2.重庆医科大学附属第一医院临床药理研究室,重庆市 400016;.四川达州市食品药品检验所,达州市 65000)
阿奇霉素(Azihromycin)[1]为半合成的十五元大环内酯类抗生素,其游离碱供口服,乳糖酸盐供注射。本品的抗菌谱与红霉素相近,作用较强,临床上用于敏感微生物所致的呼吸道、皮肤和软组织感染。为评价四川科创制药有限公司研制的2种规格的阿奇霉素胶囊在健康男性受试者的药动学特征及与杭州爱大制药有限公司生产的阿奇霉素胶囊是否等效,本文采用微生物法测定其血药浓度,并对其药动学和生物等效性进行了研究,现报道如下。
1 材料
指示菌:藤黄微球菌(编号:28001);受试制剂1:阿奇霉素胶囊(四川科创制药有限公司,规格:每粒0.25 g,批号:20030605,含量:99.83%);受试制剂2:阿奇霉素胶囊(四川科创制药有限公司,规格:每粒0.125g,批号:20030615,含量:92.8%);参比制剂:阿奇霉素胶囊(杭州爱大制药有限公司,规格:每粒0.25g,批号:040611;批准文号:国药准字H10970148);阿奇霉素标准品(中国药品生物制品检定所出品,购于重庆市药品检验所,批号:130352-200203,规格:946 IU·mg-1)。
2 方法
2.1 研究对象
21名男性健康志愿者,汉族,平均年龄(23.6±2.27)岁(21~30岁);平均体质量(60.2±5.80)kg(52~75 kg);平均身高(169.7±5.87)cm(160~182 cm)。试验前所有受试者肝功、肾功、血压、心电图检查均正常。本试验经四川达州市中心医院医学伦理委员会审批通过,受试者于充分了解试验内容后志愿签署知情同意书。
2.2 给药方案
将21名受试者采用拉丁方设计,随机分为A、B、C组,每组7人。试验前禁食12 h后,于次日晨8时,A、B、C组受试者分别交叉空腹吞服500 mg[2]受试制剂1、受试制剂2或参比制剂(200 mL温开水服药)。服药当日统一进标准餐。受试期间禁止大量活动,禁止吸烟、饮酒及含酒精、咖啡因类饮料,试验期间禁用一切非试验药物。
2.3 血样采集
A、B、C组受试者分别空腹吞服500 mg受试制剂1、受试制剂2或参比制剂(Ⅰ周期)后0.5、1.0、2.0、3.0、4.0、6.0、8.0、12、24、48、72、96、144 h时抽取前臂静脉血 3.0 mL,分离血清,低温保存(-20℃),待测。间隔2周后B、C、A组受试者分别空腹吞服500 mg受试制剂1、受试制剂2或参比制剂(Ⅱ周期),按上述方法采取静脉血。再间隔2周后,C、A、B组受试者分别空腹吞服500 mg受试制剂1、受试制剂2或参比制剂(Ⅲ周期),按上述方法采取静脉血(注:文献报道[2,3],本品tmax为2 h左右,t1/2为48 h左右,根据《中国药典》2005年版“药物制剂生物利用度和生物等效性试验指导原则”的要求,我们在达峰时间前取样3~4个点,在峰时间后取样8~10个点,取样持续到5个半衰期以上或终末浓度为峰浓度的10-1~20-1)。
2.4 血清样品检测(微生物杯碟法)
2.4.1 标准液的配制:准确称取阿奇霉素标准品,用无水乙醇溶解后加缓冲液(pH7.8)稀释成1 mg·mL-1标准贮备液,置-40℃储存备用。
2.4.2 指示菌 :选用藤黄微球菌(编号28001)[2,3]。
2.4.3 培养基Ⅱ号[4]:蛋白胨6 g,牛肉浸膏1.5 g,酵母浸膏6 g,葡萄糖1 g,琼脂20 g,蒸馏水1000 mL,调pH 7.8~8.0,在115℃灭菌30 min后备用。
2.4.4 测定方法:参照文献[5],将培养基Ⅱ号熔化后冷至约50℃,加入适量藤黄微球菌菌液,混匀,于超净工作台上倒入经高压灭菌的平皿中(12 mL/皿),冷凝后放入不锈钢小杯,每个血样分别加入2个小杯,同时另放2个小杯,内加标准液。静置相同时间后,置37℃孵育14~16 h,取出,以游标卡尺测量抑菌圈直径,按标准曲线计算血液标本中的药物浓度。
2.5 方法学研究[6]
2.5.1 标准曲线的制备及最低检测浓度:以正常人血清配制系列阿奇霉素标准液(浓度为 2.4、1.2、0.6、0.3、0.15、0.075、0.038、0.019、0.009和0.005 μg·mL-1),组间距1∶2,中心浓度为0.1 μg·mL-1,用磷酸盐缓冲液(pH 7.8)和正常人血清各半作为稀释液。测定抑菌圈,以血药浓度的对数为纵座标(Y),菌圈的直径为横座标(X)进行直线回归,得标准曲线方程Y=0.12657X-0.30464(r=9988))。结果表明,阿奇霉素检测浓度在0.005~2.4 μg·mL-1浓度范围内线性关系良好。本法最低检测浓度为0.005 μg·mL-1。
2.5.2 回收率试验:按照“2.5.1”项下方法,于空白血清中加入0.6、0.075、0.01875、0.005 μg·mL-14种浓度的阿奇霉素标准液,各配制若干份,按“2.4.4”项下方法操作,评价本法测定血清阿奇霉素含量的回收率。结果,4种浓度回收率分别为(109.29±9.44)%、(100.81±6.98)%、(110.06±3.24)%、(99.92±3.72)%。
2.5.3 精密度试验:按照“2.5.1”项下方法,于空白血清中加入0.6、0.075、0.01875、0.005 μg·mL-14种浓度的阿奇霉素标准液,各配制若干份,同日内按“2.4.4”项下方法分别测定其抑菌圈,得出日内相对标准差(RSD),并于日间按“2.4.4”项下方法测定并计算出日间RSD。精密度试验结果见表1。
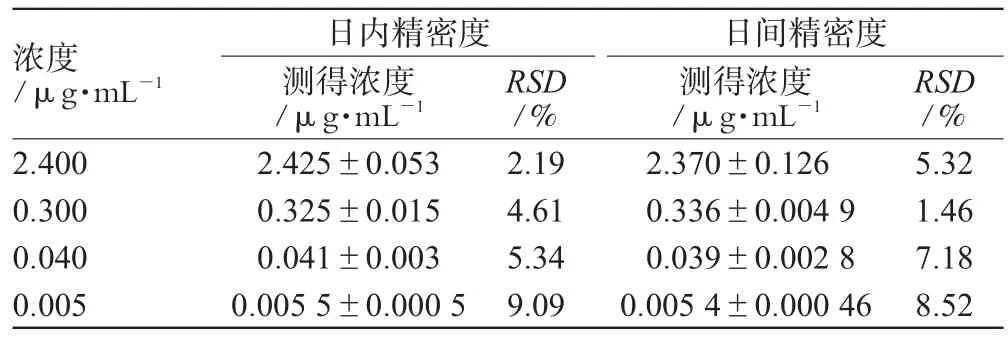
表1 精密度试验结果(n=6)Tab 1 Results of precision test(n=6)
2.5.4 冻融试验:将含药血清反复冷冻(-20℃)、溶解,1周内测定4次,结果见表2。

表2 冻融试验结果(n=4)Tab 2 The result of frozen-melt test(n=4)
3 结果
3.1 药-时曲线
21名受试者交叉口服受试制剂1、受试制剂2或参比制剂各500 mg后的平均药-时曲线见图1。
3.2 数据处理
采用三交叉试验设计生物利用度计算和生物等效性分析程序(BIO3)计算机软件,计算各个体的药动学参数,Cmax、tmax以实测值计算,AUC按梯形面积法计算。取值范围0~144 h。采用各受试者的受试制剂与参比制剂的AUC0~144分别计算相对生物利用度(F),有关药动学参数见表3。
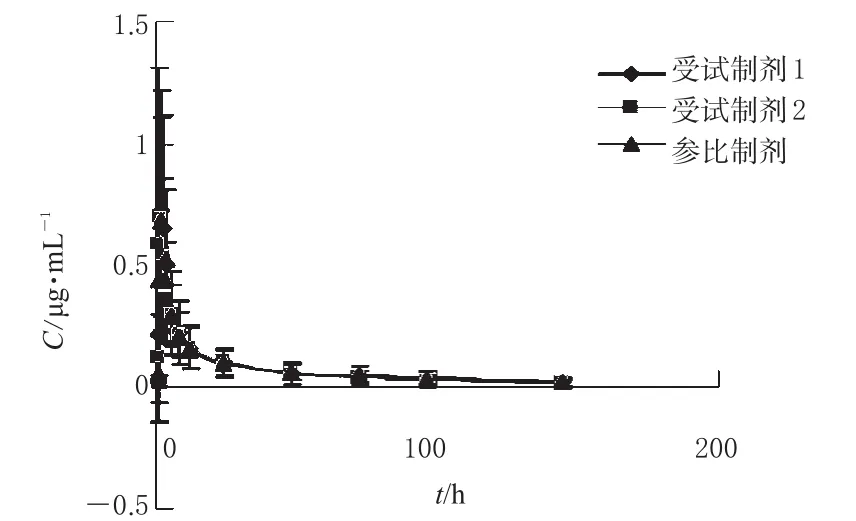
图1 受试者口服3种制剂后平均药-时曲线Fig 1 Mean plasma concentration-time curves of 3 kinds of preparations
3.3 生物等效性评价
对3组的AUC、Cmax数据均经对数转换后进行方差分析表明,受试制剂1、试制剂2、参比制剂间均无差异;90%置信区间见表4,并作出生物等效性判定。另用非参数统计Krus-kall-Wallis法,判定tmax均无差异。

表3 受试者口服3种制剂后的药动学参数(n=21)Tab 3 Comparison of pharmacokinetics parameters of three preparations(n=21)
由表4判定结果:(1)受试制剂1的AUC0~144、Cmax与参比制剂的 AUC0~144、Cmax均生物等效;(2)受试制剂 2 的AUC0~144、Cmax与参比制剂的AUC0~144、Cmax均生物等效。
4 讨论

表4 阿奇霉素胶囊拉丁方设计AUC、Cmax及其90%%置信区间Tab 4 AUC,Cmaxand their 90%%confidence interval of azihromycin capsule in Latin square design
阿奇霉素的体内测定方法已有文献报道[2,3,6],有高效液相色谱(HPLC)-紫外法、HPLC-安培电化学检测法、微生物法等。本文在现有试验条件下,以《中国药典》为依据,采用经典微生物法测定血清中阿奇霉素的浓度,经方法学研究验证,回收率、日内及日间精密度、灵敏度均能满足临床药动学及生物等效性研究的要求。
文献报道,阿奇霉素因在其配基上的9位引入了一个甲基化的氮原子,使之具有独特的药动学特点及广谱的抗菌活性,即组织选择性高、半衰期长、对酸稳定、口服比较容易吸收、生物利用度高,因此深受厂家、患者的青睐。本研究结果显示,21例受试者单剂量口服500 mg阿奇霉素胶囊后,2种规格的阿奇霉素胶囊与参比胶囊在人体内吸收、分布、消除较为一致,受试制剂1、受试制剂2相对于参比制剂的生物利用度分别为(102.73±15.63)%和(103.17±13.64)%,经统计学分析证明,两两间均无显著性差异(P>0.05),具有生物等效性。本试验为四川科创制药有限公司研制的2种规格的阿奇霉素胶囊临床应用提供了依据。
[1]陈新谦,金有豫,汤 光主编.新编药物学[M].第15版.北京:人民卫生出版社,2005:1、90.
[2]张 青,郭蓓宁,张婴元.阿奇霉素临床药代动力学研究[J].中国临床药理学杂志,1996,12(2):89.
[3]贾琳静,乔海灵,张莉蓉,等.阿奇霉素颗粒剂的健康人体药物动力学和相对生物利用度[J].河南医科大学学报,2001,36(6):712.
[4]国家药典委员会编.中华人民共和国药典(二部)[S].2005年版.北京:化学工业出版社,2005:79、附录Ⅺ.
[5]张治锬编著.抗生素药品检验[M].北京:人民卫生出版社,1987:34.
[6]关倩明,李子熊,张秋莲.HPLC法测定阿奇霉素的含量[J].药物分析杂志,1998,18(5):300.

