组胺检测试纸的研制
王 丽,吴 强,桑宏庆,刘贤进
(1.安徽科技学院食品药品学院,安徽凤阳233100;2.江苏省农业科学院农业部食品安全监控重点实验室,江苏南京210014;3.福建农林大学食品科学学院,福建福州350000)
组胺检测试纸的研制
王 丽1,2,吴 强3,桑宏庆1,刘贤进2,*
(1.安徽科技学院食品药品学院,安徽凤阳233100;2.江苏省农业科学院农业部食品安全监控重点实验室,江苏南京210014;3.福建农林大学食品科学学院,福建福州350000)
利用比色法的原理制备了组胺检测试纸,对显色体系进行了筛选,对试纸制备的条件进行了研究,并制备了标准比色卡,通过与国标法进行比较对试纸进行了评价。实验结果表明:最佳的显色体系为对氨基苯磺酸钠和亚硝酸钠溶液,两者的最佳浓度分别为40g/L和400g/L,两者的最佳体积比为10∶0.3,最佳试纸纸材为超厚滤纸,最佳浸泡时间为20min,最佳干燥条件为60℃在干燥箱中干燥,试纸的检出限为4μg/mL,试纸检测结果与国标法检测结果相吻合,数据的重现性较好。
试纸,组胺,检测
组胺(Histam ine,HA),又名组织胺,分子式C5H9N3,化学名 4(5)-(2-氨乙基) 咪唑[1]。组氨为一种生物胺,它的前体物质是组胺酸,组氨酸是蛋白质经过分解后的一种氨基酸。水产品中组胺主要是组氨酸在莫根氏变形杆菌、组胺无色杆菌等微生物和组氨酸脱羧酶的共同作用下发生脱羧反应产生的[2]。组胺有毒性,可以降低血压,当有机体摄入组胺超过100mg(或每千克体重1.5mg)时,即可引起过敏性食物中毒[3]。在生物胺引起的食品安全问题中,组胺对人类的健康的影响最大[4]。如2002年9月,中山市某公司2004年3月1日厦门市某公司的食堂曾发生过组胺食物中毒事件[5-6]。欧美及我国对部分食品中组胺含量做了限量要求:美国FDA要求进口水产品组胺不得超过50mg/kg;欧盟规定鲭科鱼类中组胺含量不得超过100mg/kg,其它食品中的组胺含量不得超过100~800mg/kg;我国规定鲐鱼中组胺含量不得超过 300mg/kg[5,7]。目前,国内外对组胺的测定方法有偶氮试剂比色法、荧光分光光度法、HPLC法、气相色谱法、薄层色谱法和生物学法等。这些方法所用试剂、器皿较多,操作繁琐、费时,大型仪器价格昂贵。试纸法是把化学反应从试管或化学器皿里移到滤纸上进行,利用迅速产生明显颜色的化学反应进行目视定性或半定量分析[8-9]。试纸法携带方便、操作简单、检测速度快、价格便宜、对操作员要求低、检测可在室温下顺利进行。目前亚硝酸盐检测试纸、重金属Al3+检测试纸、牛奶掺假检验试纸、碘盐中碘含量试纸、转基因农作物检测试纸、甲醛检测试纸已有报道[8,10,11-14]。但国内外组胺检验试纸尚未见报道,因此我们通过实验研制了检测组胺的试纸,快速检测食品尤其是水产品中组胺。

表1 不同显色体系的显色效果
1 材料与方法
1.1 材料与仪器
定性快速滤纸101、定性中速滤纸102、定性慢速滤纸103、定量快速滤纸201、定量快速滤纸202、定量慢速滤纸203、加厚滤纸、超厚滤纸 杭州富阳特种纸业有限公司;鱼 凤阳菜市场;对氨基苯磺酸纳、三氯乙酸、亚硝酸钠、正戊醇、氢氧化钠、盐酸、无水碳酸纳、对硝基苯胺 均为分析纯;磷酸组胺 生物试剂。
721 分光光度计 上海第三分析仪器厂;HH数显恒温水浴锅 金坛市金城国胜实验仪器厂;FC204电子分析天平 上海精科仪器厂;101C-3B电热鼓风干燥箱 上海市实验仪器总厂。
1.2 实验方法
1.2.1 显色体系的筛选 显色体系A:采用GB/T5009.45-1996 方法[15],使用的对硝基苯胺与亚硝酸钠为偶氮试剂,同时分别取 0.00、0.20、0.40、0.60、0.80、1.00m L 20μg/m L组胺标准溶液于10m L比色管中并用1mol/L HCl补足至1.0m L。各比色管中加15%碳酸钠溶液 3m L,偶氮试剂 3m L,加水至10.0m L,混匀。
显色体系B[16]:另外取一组上述同样的一系列组胺溶液,分别加入5g/L对氨基苯磺酸钠溶液5.0m L,0.3m L 50g/L亚硝酸钠溶液,混匀。
放置10m in后对比观察显色体系A和显色体系B在比色管中显色反应,在两者中选择显色速度快、显色稳定、色阶变化明显的作为试纸浸泡液。
1.2.2 试纸制备
1.2.2.1 基本实验方法 实验步骤:a.配制成显色剂溶液;b.将滤纸浸泡到盛有显色剂溶液的平皿中一定时间后取出;c.将吸附有显色剂的试纸干燥并剪裁成规格统一0.5×3cm长条。
1.2.2.2 试纸制备条件的选择 根据上述的基本实验方法,根据组胺在试纸上反应的速度、色阶变化、显色稳定性、均匀性等指标来确定最佳的试纸制备条件。根据其所显颜色深浅规定标准如下:
深红色:+++;浅红色:++;微红色:+;橙黄色:-;微黄色:- -。
1.2.3 标准比色卡的制备 将制作的试纸与系列浓度组胺溶液反应,根据反应颜色的深浅及色阶的变化印刷制作标准比色卡。1.2.4 试纸的评价
1.2.4.1 试纸检出限实验 将制作的试纸与系列浓度组胺溶液反应确定试纸的最低检测限度,对试纸作出评价。
1.2.4.2 试纸的校正性实验 试纸法同国标方法反复的检测同一样品来对试纸进行校正性实验。国标法测定样品参照 GB/T5009.45-1996[15]。
2 结果与讨论
2.1 显色体系的选择
将显色剂A和B分别与同一浓度组胺在比色管中进行反应,通过肉眼观察显色效果,结果如表1所示。
从表1可看出,显色体系A和显色体系B与组胺溶液反应显色速度都较快,但显色体系B颜色较深,色阶变化比较明显。因此确定对氨基苯磺酸钠和亚硝酸钠为试纸的浸泡溶液。
2.2 试纸制备条件的选择
2.2.1 显色剂浓度的选择 将定性中速滤纸浸泡在不同浓度的对氨基苯磺酸钠和亚硝酸钠的混合液中,两者体积比为10∶0.3,浸泡时间20min,室温晾干后与50μg/m L组胺溶液反应,通过观察在试纸上反应效果来确定浸泡试剂的最佳浓度,结果如表2所示。

表2 显色剂浓度对试纸效果的影响
实验发现1~3号试纸显色为橙黄色,4~5号显色为微红色,但4号显色速度、稳定性、均匀性均优于5号。所以选择40g/L的对氨基苯磺酸钠溶液和400g/L的亚硝酸钠溶液的混合液作为试纸的浸泡液。
2.2.2 显色剂最佳配比的选择 分别将40g/L的对氨基苯磺酸钠溶液和400g/L的亚硝酸钠溶液按体积比为 10∶0.1、10∶0.3、10∶0.6 混合,分别将定性中速滤纸在其中进行浸泡20m in,取出在室温条件晾干后与50μg/m L组胺溶液反应,结果如表3所示。

表3 显色剂配比对试纸的影响
实验可以看出三种不同配比溶液中浸泡的试纸与组胺显色反应速度均较快,但在配比为10∶0.3的混合液中浸泡的试纸显色程度明显,而另外两者与组胺反应的颜色暗淡,不容易辨别。所以两种显色剂体积比例为10∶0.3为宜。
2.2.3 试纸用纸的选择 将各类不同纸材的纸张分别浸泡到40g/L的对氨基苯磺酸钠溶液和400g/L的亚硝酸钠溶液的混合液中,两者体积比为10∶0.3,浸泡时间20m in,室温晾干后与50μg/m L组胺溶液反应,结果如表4所示。
由表4看出,在同一浸泡时间条件下,所有不同材质的纸张中,超厚滤纸显色速度最快,与加厚型滤纸显色均最明显,其中稿纸在显色速度、显色均匀程度、显色程度上均最差。所以选定超厚滤纸为检测组胺试纸的材料,其它的滤纸由于吸附能力较弱,故不予采用。

表4纸材对试纸效果的影响
试纸纸张的选择需要满足容易吸附显色剂,干燥时间短等要求,另外各种物质在不同试纸上的扩散速度、吸附程度是不同的[17]。实验证明用超厚滤纸作为组胺试纸的材料,因为该试纸材质致密,容易吸附显色剂,且吸附量较大而均匀,需要干燥时间短,显色稳定快速。而且在浸泡时间长的条件下不容易变形。而采用普通纸张,由于吸附能力较弱,纸质差,容易破碎,烘干后药品残留量低,使用后,其显色能力不明显。
2.2.4 浸泡时间的选择 将超厚滤纸浸泡到40g/L的对氨基苯磺酸钠溶液和400g/L的亚硝酸钠溶液的混合液中,两者体积比为10∶0.3,浸泡时间范围选择在10~30min,室温晾干后与50μg/m L组胺溶液反应,结果如表5所示。

表5 浸泡时间对试纸效果影响
由表5看出不同浸泡时间的试纸与组胺反应速度大体相同,但是显色程度有差异,浸泡时间在10m in左右时,显色效果不好,试纸上显色班驳不均匀;当浸泡时间为15m in时,试纸显色效果同样不好,但显色比较均匀;当浸泡20m in时显色各项指标均最佳;25m in以上,浸泡时间太长,纸张在平皿中不易取出,且纸张易破,不易晾干操作,并且晾干后试纸的形状保持不好。综合考虑,浸泡时间选择为20m in左右。
2.2.5 试纸干燥环境对试纸的影响 将超厚滤纸浸泡到40g/L的对氨基苯磺酸钠溶液和400g/L的亚硝酸钠溶液的混合液中,两者体积比为10∶0.3,浸泡20m in,不同干燥条件后与50μg/m L组胺溶液反应,结果如表6所示。
结果显示不同干燥条件的试纸的显色速度和显色程度差异不大,但室温、干燥器干燥所需时间均较长,而且有微黄底色。干燥箱30、40、50、60℃干燥的试纸均较好,且几乎没有微黄底色,但60℃干燥所需时间更短,所以干燥条件选择干燥箱60℃为宜。
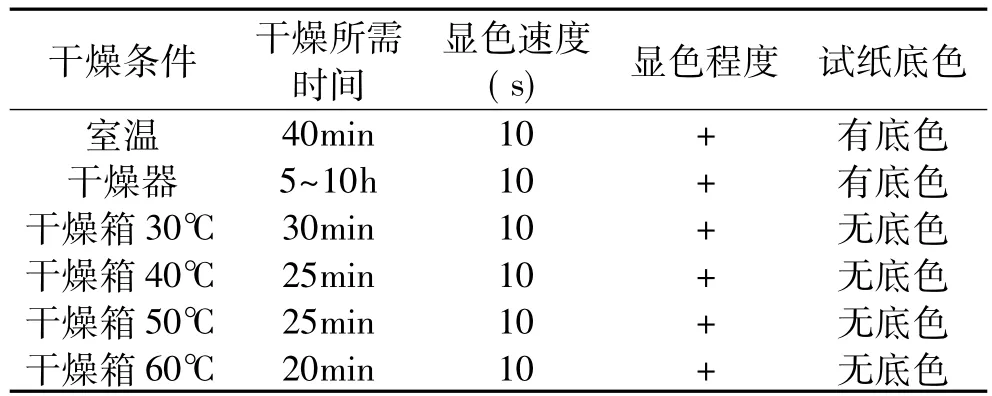
表6 干燥条件对试纸效果影响
2.2.6 显色条件对试纸的影响 在实验中,反应的酸碱度很重要。有文献记载重氮偶合反应需在酸性条件下进行,过量盐酸会使结果偏低,灵敏度降低,甚至检测不出来[9,18-19]。通过实验发现,试纸先浸泡到未加盐酸的显色体系中,临时用1mol/L盐酸把组胺溶液pH调至1~2后与试纸反应显色比较明显。同时发现,温度在反应过程中也很重要。在室温、30、40、50、60、70、80℃水浴后的组胺处理液调节 pH后与试纸反应,发现30℃水浴后的组胺处理液与试纸显色效果最佳。
2.3 标准比色卡的制备
将试纸分别与一系列浓度为 1、2、3、4、5、6、7、8、9、10、20、25、30、35、40、45、50、60、70、75、80、85、90、100、125、150、175、200μg/m L 的组胺溶液根据显色深浅、色阶的变化制作标准比色卡。
2.4 试纸的使用方法
将含有样品处理液于30℃水浴用1mol/L盐酸调节pH至1~2,用玻璃棒蘸取与试纸接触,反应便在试纸上进行。然后与标准比色卡进行对照,即可估计出样液中组胺的浓度。
2.5 试纸效果评价
2.5.1 试纸检出限的确定 将制作的试纸与系列浓度组胺溶液反应,确定试纸的最低检测限度,结果如表7所示。
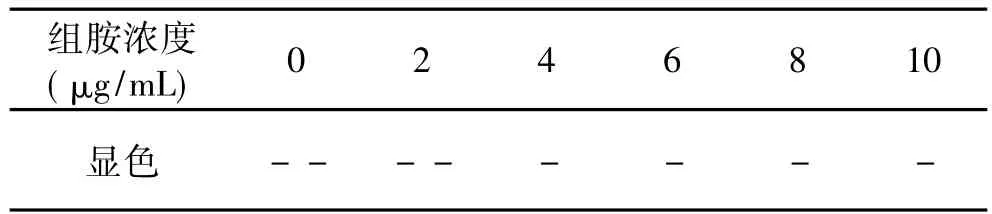
表7 组胺检测试纸最低限检测结果
由表7可见,当组胺达到4μg/m L时,试纸已经有显示,则试纸的检出限为4μg/m L。
2.5.2 试纸精确性校验 以冰箱中长期储藏的鱼进行应用实验。参照标准比色卡,用试纸测定样品中组胺,并与国标法测定相比较,结果如表8所示。

表8 样品中测定结果(μg/mL)
从实验结果看出,试纸的颜色所对应的浓度范围与真实浓度符合度较好。多次重复实验结果表明,数据的重现性较好,试纸检测的浓度范围与国标方法检测的精确浓度相吻合。
3 结论
3.1 显色体系筛选结果表明:对氨基苯磺酸钠和亚硝酸钠混合色阶变化明显,适合作为试纸制备的浸泡溶液。
3.2 试纸制备条件选择结果表明:显色剂为40g/L的对氨基苯磺酸钠溶液和400g/L的亚硝酸钠溶液,两者的最佳体积比为10∶0.3,最佳纸材是超厚滤纸,最佳浸泡时间是20min,最佳干燥条件是在60℃干燥箱中干燥。试纸在塑料袋内密封置于阴凉干燥处保存。
3.3 通过应用实验,确定试纸的检出限为4μg/m L,试纸检测结果与国标法检测结果相吻合。
[1]李伟荣,姚丽梅,王宁生.5-羟色胺、组胺检测方法概述[J].中西医结合心脑血管病杂志,2003,1(7):409-412.
[2]李立,李金强,钟响.反相分配离子对色谱法快速测定鱼肉中的 HA[J].检验检疫科学,2001,11(4):44-45.
[3]杨文军,马丹,张丽英,等.鱼粉中的有毒有害物质组胺HPLC 检测方法初探[J].饲料广角,2004(4):28-29.
[4]Bodmer S,Imark C,Kneubuhl M.Biogenic amnines in foods:Histamine and food processing[J].Inflammation Research,1999,48(2):296-300.
[5]李志军,吴永宁,薛长湖.生物胺与食品安全[J].食品与发酵工业,2004,30(10):84-91.
[6]徐金德.一起秋刀鱼引起组胺食物中毒事件的调查[J].海峡预防医学杂志,2004,10(5):41.
[7]Shalaby A R.Significance of biogenic amines to food safely and human health[J].Food Reaearch International,1996,29(7):675-690.
[8]周焕英,高志贤,崔晓亮.试纸法在食品、水质及其它快速检测中的应用[J].解放军预防医学杂志,2003,21(2):148-151.
[9]吴爱芳,曾丹.试纸对肉类熟食制品中亚硝酸盐的快速检测[J].中国食物与营养,2005(6):34-36.
[10]O Yu Nadzhafova,S V Lagodzinskaya,V V Sukhan.Test Paper for the Determination of Aluminum in Solution[J].Journal of Analytical Chemistry,2001,56(2):178-181.
[11]李喆,王诗哲,吴也平.牛奶掺假检验试纸的研制[J].高师理科学刊,2004,24(2):38-40.
[12]李珊,吴迪,徐伟,等.碘盐中碘含量检测试纸的制备与应用[J].河北省科学院学报,2003,20(4):240-242.
[13]袁铁琰,张大兵,王全喜.试纸条技术在转基因农作物检测中的应用[J].生物技术通报,2004(5):37-39.
[14]吴翠玲,肖凤英,徐金瑞.甲醛的试纸化测定研究[J].福建化工,2003(2):24-26.
[15]黄伟坤.食品检验与分析[M].北京:中国轻工业出版社,1995:501-502.
[16]郝宏兰.水产品中组胺的测定方法研究[J].食品科学,2000,21(8):46-49.
[17]屈智慧,邹东雷,张思相,等.亚硝酸根试纸的开发与研制[J].化学工程师,2005,7(7):1-4.
[18]王丽玲,白艳玲.水产品组胺测定中盐酸量对结果影响的探讨[J].现代科学仪器,2001(5):55.
[19]高鹤娟.食品卫生方法(理化部分注解)[M].北京:人民卫生出版社,1987:357.
Preparation for the detected paper of histam ine
WANG Li1,2,WU Qiang3,SANG Hong-qing1,LIU Xian-jin2,*
(1.College of Food and Medical Science,Anhui Science and Technology University,Fengyang 233100,China;2.Key Laboratory of Agro-food Safety and Quality Ministry of Agriculture,Jiangsu Academy of Agricultural Sciences,Nanjing 210014,China;3.College of Food Science,Fujian Agriculture and Forestry University,Fuzhou 350000,China)
This text introduced a new preparation m ethod of a detected paper for detecting the histam ine by the colorim etry princip les,screening the color system and researching the conditions of the papers.The standard color card was prepared.The detected paper was evaluated through com paring the national standard method.The results of the experiment showed that:the best color system was hybrid solution which was compsed by the sodium pam inobenzenesulfonate and sodium nitrite,the best concentration respectively was40g/L and 400g/L,the best volume ratio was 10∶0.3,the best paper m aterial was the thick filter paper,the best soaking time was 20m inutes,the best drying conditionswas 60℃ in the oven,the paper detected lim it was 4μg/m L.Practical experiment indicated that the detected resultsof the detected paper were in accordancew ith the detected results of the national standard method,the re-emergence of the date was better.
detected paper;histam ine;detection
TS201.2
A
1002-0306(2011)06-0410-04
2010-05-31 *通讯联系人
王丽(1977-),女,硕士,讲师,研究方向:食品安全与检测。
安徽科技学院自然科学研究项目(ZRC2010257);江苏省农业科技自主创新项目[CX(10)236]。

