RRM1蛋白表达与含吉西他滨方案一线治疗晚期非小细胞肺癌疗效关系的研究
梁剑苗 邓燕明* 冯卫能 胡维维 陈泽程 唐溢聪 张 华 冼海兵 张顺达
(1 广东省佛山市第一人民医院头颈胸肿瘤内科,广东 佛山 528000;2 广东省佛山市第一人民医院病理科,广东 佛山 528000)
肺癌是目前最常见的恶性肿瘤之一,非小细胞肺癌(NSCLC)是肺癌的主要病理类型[1],吉西他滨联合铂类是晚期NSCLC一线治疗的主要化疗药物之一,核苷酸还原酶1(RRM1)是吉西他滨的主要靶点之一。本研究回顾性分析44例使用含吉西他滨方案一线化疗的晚期非小细胞肺癌的RRM1表达,探讨RRM1表达与吉西他滨疗效的相关性。
1 材料与方法
1.1 研究对象
收集我院2008年1月至2010年8月一线治疗的晚期非小细胞肺癌患者,入组病例符合以下条件:①经组织学或细胞学确诊为非小细胞肺癌;②PS评分0~1分;③至少有一个可测量病灶;④使用含吉西他滨方案化疗;⑤至少化疗2周期。
1.2 治疗方案
吉西他滨(美国礼来公司,健择)1000mg/m2,静脉滴注,第1天;或联合顺铂75mg/m2,静脉滴注,第1天,或联合卡铂AUC=5,静脉滴注,第1天。21d为1周期。
1.3 疗效评价
每化疗2周期进行疗效评价,按照实体瘤疗效评价标准(RECIST1.1版),分为完全缓解(CR)、部分缓解(PR)、稳定(SD)和进展(PD),客观有效率(RR)为CR+PR,疾病控制率(DCR)为CR+PR+SD。无疾病进展时间(PFS)为治疗开始至肿瘤复发或进展的时间;总生存时间(OS)为治疗开始至死亡或末次随访的时间。末次随访时间为2011年12月。
1.4 RRM1表达的检测
免疫组织化学采用Envision二步法,检测系统试剂盒和RRM1抗体均购自Dako公司,RRM1蛋白表达阳性为细胞浆或(和)细胞核出现棕黄色颗粒为阳性。
1.5 统计学分析
所有资料采用SPSS17.0进行统计学分析,疗效分析采用χ2检验,生存分析采用Kaplan-Meier法,P<0.05为有统计学意义。
2 结 果
2.1 临床资料
共收集44例肺癌患者资料,其中Ⅲb期6例(13.6%),Ⅳ期38例(86.4%);男性23例(52.3%),女性21例(47.7%);中位年龄(57.5±11.5)岁(30~76岁);腺癌32例(72.7%),鳞癌12例(27.3%);使用吉西他滨联合顺铂方案25例(56.8%),吉西他滨联合卡铂方案15例(34.1%),单药吉西他滨4例(9.1%);中位周期数(4±1.14)周期(2~6周期)。
2.2 RRM1免疫组化结果
44例患者中,RRM1阳性(+)40.9.8%(18/44),RRM1阴性(-)59.1%(26/44)。
2.3 疗效
该研究的44例患者中,PR 17例(38.6%),SD 16例(36.4%),PD 11例(25.0%);客观有效率(RR)38.6%(17/44),疾病控制率(DCR)75.0%(33/44);中位无疾病进展时间(PFS)6.8个月(5.9~7.7个月),中位生存时间(OS)15.4个月(12.4~18.4个月)。
2.4 相关性分析
该研究中,RRM1阳性患者RR为27.8%(5/18),RRM1阴性患者RR为46.2%(12/26),差异无统计学意义(P=0.218);RRM1阳性患者DCR为55.6%(10/18),RRM1阴性患者RR为88.5%(23/26),差异有统计学意义(P=0.013);RRM1阳性患者PFS为5.5个月,RRM1阴性患者PFS为7.2个月,差异有统计学意义(P=0.01);RRM1阳性患者OS为15.3个月,RRM1阴性患者OS为18.8个月,差异无统计学意义(P=0.127)。见图1。
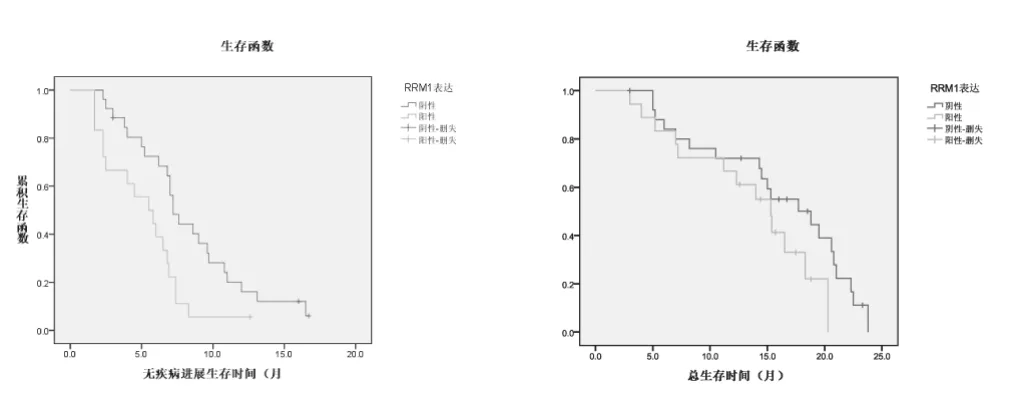
图1 RRM1表达对PFS和OS的影响
3 讨 论
吉西他滨是嘧啶类抗代谢药物,为核苷酸还原酶(RR)抑制剂,在细胞内经过核苷激酶的作用转化成具有活性的二磷酸核苷(dFdCDP)及三磷酸核苷(dFdCTP),从而抑制DNA合成[2,3]。核苷酸还原酶(ribonucleotide reductase,RR)是DNA合成通路中的限速酶,RRM1是RR的亚单位,是核苷酸结合位点,控制底物的特异性和整个酶的活性,同时也是吉西他滨的结合位点[4]。
多项研究显示RRM1表达可能可预测吉西他滨化疗的疗效。Bergman等[5]2005年建立的第一个体内吉西他滨耐药模型显示吉西他滨耐药细胞株的RRM1 mRNA水平明显升高。Rosell等[6]采用实时PCR检测100例晚期NSCLC患者病理标本RRM1的mRNA水平,发现RRM1低表达患者使用吉西他滨联合顺铂方案缓解率较高,中位生存期较高表达患者明显延长(P=0.009)。Lee JJ等[7]使用免疫组化方法检测使用吉西他滨为基础的方案化疗的晚期非小细胞肺癌患者的RRM1表达水平,研究显示RRM1阳性患者的总生存期较阴性患者缩短(P=0.022),疾病控制率也低于阴性组(P=0.053)。高志强等[8]使用免疫组化方法检测吉西他滨联合顺铂化疗的晚期肺癌患者RRM1蛋白表达,研究显示RRM1蛋白高表达组的化疗有效率低于低表达组(P=0.005);RRM1高表达组的1年生存率低于低表达组(P=0.009);RRM1蛋白高表达组的疾病进展时间低于低表达组(P=0.042);但两组的中位生存期无明显差异(P=0.245)。由于RT-PCR在mRNA水平检测RRM1表达,而免疫组化在蛋白水平检测RRM1表达,因此mRNA与蛋白表达之间可能存在一些差异。Gong W等[9]对18项临床研究进行Meta分析,亚组分析显示免疫组化似乎乎比RT-PCR技术更好地预测晚期非小细胞肺癌患者使用含吉西他滨化疗的客观反应率。本研究也采用免疫组化方法检测RRM1蛋白表达,显示RRM1阴性患者疾病控制率高于阳性患者,无疾病进展时间延长,但有效率及总生存时间无统计学差异。
综上所述,RRM1表达水平是吉西他滨治疗非小细胞肺癌的敏感性的重要因素,然而仍需要大型的Ⅲ期随机临床试验明确RRM1是否能作为晚期非小细胞肺癌吉西他滨方案敏感性及预后的预测指标。另外,使用何种检测手段更能预测临床疗效,如何判断RRM1表达水平高低等问题仍需进一步研究证实。
[1]Jemal A,Siegel R,Ward E,et al.Cancer statistics,2009[J].CA Cancer J Clin,2009,59(4):225-249.
[2]Rosell R,Cobo M,Isla D,et al.Pharmacogenomics and gemcitabine[J].Ann Oncol,2006,17(5):13-16.
[3]Ueno H,Kiyosawa K,Kaniwa N.Pharmacogenomics of gemcitabine:can genetic studies lead to tailor-made therapy?[J].Br J Cancer,2007,97(2):145-151.
[4]Smith BD,Karp JE.Ribonucleotide reductase: an old target with new potential[J].Leukemia Res,2003,27(12):1075-1076.
[5]Bergman AM,Eijk PP,Ruiz van Haperen VW,et al.In vivo induction of resistance to gemcitabine results in increased expression of ribonucleotide reductase subunit M1 as a major determinant[J].Cancer Res,2005,65(20):9510-9516.
[6]Rosell R,Danenberg KD,Alberola V,et al.Ribonucleotide reductase messenger RNA expression and survival in Gemcitabine /Cisp latintreated advanced non-small-cell lung cancer patients[J].Cli Cancer Res,2004,10(4):1318-1325.
[7]Lee JJ,Maeng CH,Baek SK,et al.The immunohistochemical overexpression of ribonucleotide reductase regulatory subunit M1(RRM1) protein is a predictor of shorter survival to gemcitabinebased chemotherapy in advanced non-small cell lung cancer(NSCLC)[J].Lung Cancer,2010,70(2):205-210.
[8]Gao Z,Han B,Shen J,et al.Relations between RRM1 protein expression levels and effects of gemcitabine and cisplatin chemotherapy in advanced non-small cell lung cancer patients[J].Chin J Lung Cancer,2011,14(4):340-344.
[9]Gong W,Zhang X,Wu J,et al.RRM1 expression and clinical outcome of gemcitabine-containing chemotherapy for advanced non-small-cell lung cancer: A meta-analysis[J].Lung Cancer,2012,75(3):374-380.

