2,3,6,7-四甲基三蝶烯的新型有效合成及表征
刘嘉川,程琳
(华侨大学材料科学与工程学院,福建厦门361021)
2,3,6,7-四甲基三蝶烯的新型有效合成及表征
刘嘉川,程琳
(华侨大学材料科学与工程学院,福建厦门361021)
以苯甲醇和邻二甲苯为反应体系的溶剂,在无水三氯化铝催化作用下,经碳正离子机理反应得到了2,3,6,7-四甲基蒽.然后,将2,3,6,7-四甲基蒽与原位生成的苯炔经Diels-Alder反应生成具有独特三维刚性芳香结构的2,3,6,7-四甲基三蝶烯.最后,用红外光谱(IR)和核磁共振氢谱(1H NMR)表征了2,3,6,7-四甲基蒽和2,3,6,7-四甲基三蝶烯的结构.
2,3,6,7-四甲基蒽;2,3,6,7-四甲基三蝶烯;Diels-Alder反应;苯甲醇;邻二甲苯
蒽是具有高荧光性和平面大π键结构的有机分子.蒽及其衍生物基本上都是利用其中较为活泼的9,10-位氢,发生诸如溴甲基化、醛化、溴化等反应,进而与其他化合物作用形成功能材料[1-5]的.然而,蒽的有限的活性反应位点,制约了蒽基衍生物的种类及蒽基衍生物的材料性能的拓展.通过增加蒽的反应活性位点,特别是2,3,6,7位,将使蒽的平面大π键结构、高刚性及高荧光性得到进一步的利用,成为拓展蒽的衍生物的种类和材料性能非常有效的途径.三蝶烯及其衍生物是一类具有D3h对称性、独特三维刚性结构的化合物.1956年,Wittig等[6]通过苯炔和蒽的加成反应一步合成了三蝶烯;随后,Stiles等[7]进一步改进了苯炔的制备方法,更方便地实现了三蝶烯的制备,大大地提高了与蒽及其衍生物反应生成三蝶烯的产率,使的三蝶烯合成化学飞速发展.文中报道课题组在合成三蝶烯-2,3,6,7-四甲酸二酐[8]的过程中,发现了一种由苯甲醇和邻二甲苯一步反应制得2,3,6,7-四甲基蒽的简便方法,并进一步反应成功制备了高纯度的2,3,6,7-四甲基三蝶烯.
1 实验部分
1.1 仪器与试剂
1)仪器.Nexus 470型傅里叶变换红外光谱仪(美国尼高力公司);DMXO400NMR型核磁共振仪(TMS为内标,德国Bruker公司);DSC-2910型热分析仪,氮气氛围下升温速率为10℃·min-1.
2)试剂.邻氨基苯甲酸,根据文献[9]的方法合成;邻二甲苯(分析纯,辽宁沈阳化学试剂五厂);苯甲醇、二氯乙烷、无水三氯化铝、甲醇、氢氧化钠(分析纯,上海国药集团试剂有限公司);二乙二醇二甲醚(化学纯,上海国药集团试剂有限公司);亚硝酸异戊酯(分析纯,上海科丰化学试剂有限公司).
1.2 2,3,6,7-四甲基蒽合成
在250 m L洁净、干燥的三口烧瓶中,于冰浴搅拌下加入80.0 m L邻二甲苯和8.0 m L(0.075 mol)苯甲醇,混合均匀后,再加入35.0 g(0.26 mol)的AlCl3;加料完毕,撤去冰浴,常温下反应3 h,之后油浴中慢慢升温至115℃,并在该温度下反应4 h,停止反应后,撤去油浴,稍冷,于冰盐酸中沉降,充分搅拌,静置,待溶液全黄且明显分层后开始抽滤.最后,经50 m L水洗,100 m L乙酸乙酯洗,50 m L饱和碳酸氢钠洗,再用50 m L水洗,在真空烘箱中烘干,得浅黄色固体8.5 g.实验测得其产率为43%,熔点为299~300℃,与文献[10]报道的熔点一致.2,3,6,7-四甲基蒽合成的具体反应式,如图1所示.
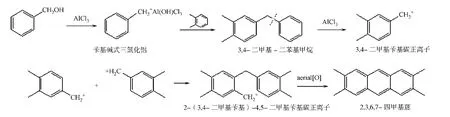
图1 2,3,6,7-四甲基蒽的合成Fig.1 Synthesis of 2,3,6,7-tetramethylanthracene
由图1的反应式可知:合成反应是以邻二甲苯和苯甲醇为反应体系的溶剂,邻二甲苯与苯甲醇在无水三氯化铝催化作用下,经过程序升温后生成2,3,6,7-四甲基蒽.体系中,无水三氯化铝作为路易斯酸对水特别敏感,微量的水也会导致三氯化铝失去催化活性,因此反应仪器与试剂必须预先干燥以保证体系在无水的条件下进行反应.反应中,无水三氯化铝首先与苯甲醇生成络合物苄基碱式三氯化铝;然后,该络合物与邻二甲苯发生傅式烷基化反应,生成3,4-二甲基-二苯基甲烷.
在无水三氯化铝的作用下,3,4-二甲基-二苯基甲烷断键生成3,4-二甲基苄基碳正离子,而两分子3,4-二甲基苄基碳正离子偶联在空气中进一步氧化得到2,3,6,7-四甲基蒽[11].络合物的生成过程中反应速度较快,会放出热量,因此,为了保证反应正常进行,应将温度控制在0℃以下.
1.3 2,3,6,7-四甲基三蝶烯的合成
在250 m L的三口烧瓶中加入2.0 g的2,3,6,7-四甲基蒽,100.0 m L二氯乙烷、25.0 m L二乙二醇二甲醚,加热到回流.在恒压漏斗中同时滴入4.5 g的邻氨基苯甲酸,溶于50.0 m L二乙二醇二甲醚,12.0 m L亚硝酸异戊酯和60.0 m L 1,2-二氯乙烷的混合液,4 h内滴加完毕,继续回流反应3 h.蒸出溶剂,直至蒸气温度达160℃为止,待溶液稍冷后,加入2.0 g顺丁烯二酸酐,回流25 min,冷却到室温;然后,加入6.5 g氢氧化钠溶于50.0 m L乙醇和50.0 m L水的溶液,回流15 min.冷却,抽滤,滤饼用1∶1(体积比)乙醇-水洗涤,干燥,用1∶9(体积比)二氯甲烷-石油醚为洗脱剂,经柱色谱分离得到高纯度的白色固体2.50 g.测得其收率为53.8%,熔点为240~241℃,与文献[8]报道的熔点一致.2,3,6,7-四甲基三蝶烯合成的具体反应式,如图2所示.
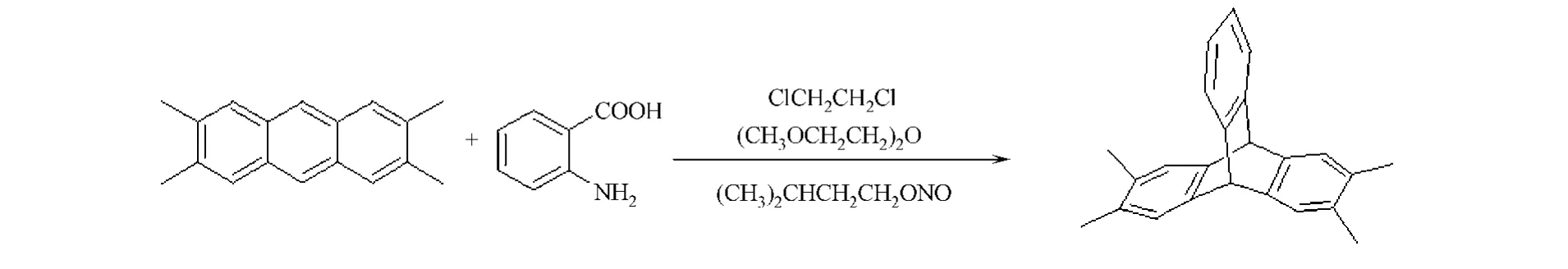
图2 2,3,6,7-四甲基三蝶烯的合成Fig.2 Synthesis of 2,3,6,7-tetramethyltriptycene
由图2的反应式可知:在2,3,6,7-四甲基三蝶烯的合成过程中,2,3,6,7-四甲基蒽与原位生成苯炔发生Diels-Alder反应生成2,3,6,7-四甲基三蝶烯.苯炔是极其活泼的反应中间体,它不仅可以作为亲双烯体与2,3,6,7-四甲基蒽发生Diels-Alder环加成反应,而且还具有亲电性,能与亲核试剂水、邻氨基苯甲酸等的亲核基团发生加成反应.
为了保证反应高效、平稳、有序地进行,加料的方式至关重要.具体操作是先将2,3,6,7-四甲基蒽一次性加入,邻氨基苯甲酸和亚硝酸异戊酯应分别慢慢滴加到反应体系中,以保证体系中生成苯炔的浓度很低,一生成就迅速与2,3,6,7-四甲基蒽反应.在最优化研究中,2,3,6,7-四甲基蒽、邻氨基苯甲酸和亚硝酸异戊酯的最佳摩尔比是1∶3∶8.
据文献[12,13]报道,取代的蒽和苯炔间的Diels-Alder反应不仅发生在蒽的9,10位生成取代的三蝶烯,而且还会发生在1,4或5,8位生成异构体,并且区域选择性加成受取代基的电子效应和空间效应的综合影响.由于该此反应极其复杂,副产物多,加之有异构体的存在,使用重结晶已经不能达到预期的分离效果,因此,需要硅胶柱色谱分离,以二氯甲烷-石油醚的体积比1∶9为洗脱剂进行洗脱,可以得到高纯度的2,3,6,7-四甲基三蝶烯.
2 结果与讨论
2.1 化合物结构的红外光谱表征
2,3,6,7-四甲基蒽的2,3,6,7-四甲基三蝶烯的红外光谱(IR),如图3所示.从图3(a)可知:在波数(ν)为2 952,2 855,1 380 cm-1处有甲基的特征吸收峰;而在1 462 cm-1处为2,3,6,7-四甲基蒽的骨架振动.从图3(b)可知:在波数(ν)为2 954,2 857,1 382 cm-1处有甲基的特征吸收峰;而在1 462 cm-1处为2,3,6,7-四甲基三蝶烯的骨架振动.
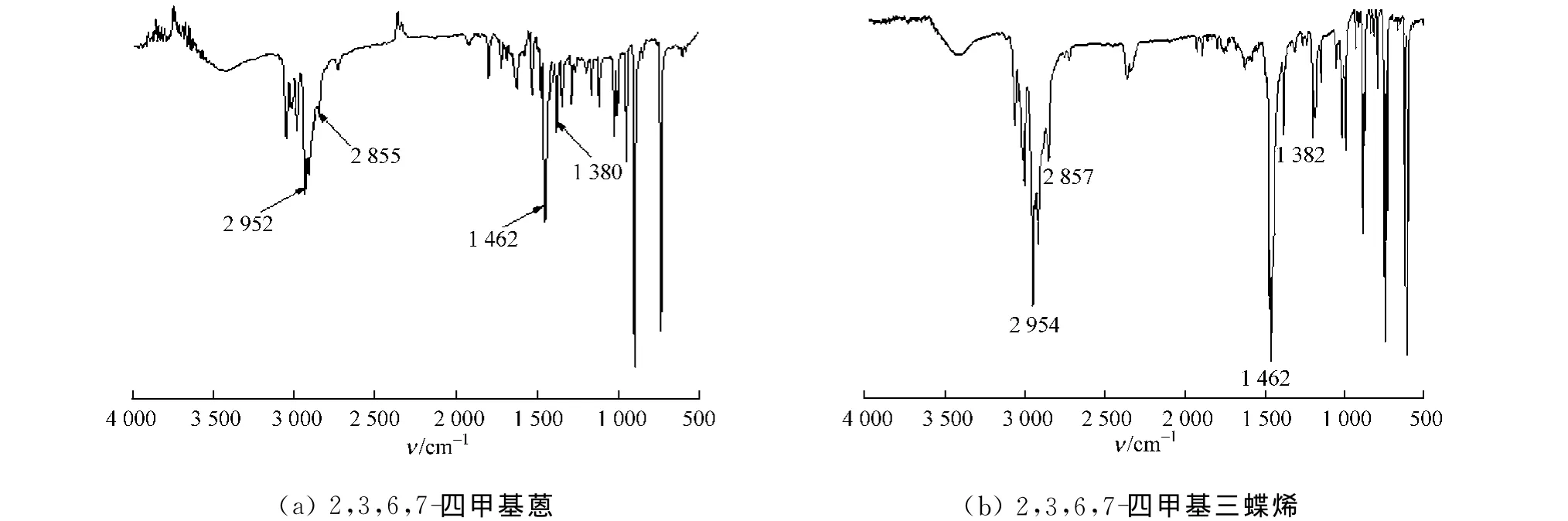
图3 化合物的红外光谱图Fig.3 IR spectra of compounds
2.2 化合物结构的核磁共振氢谱表征
2,3,6,7-四甲基蒽的2,3,6,7-四甲基三蝶烯的核磁共振氢谱(1H NMR),如图4所示.从图4(a)可知:1H NMR(400 MHz,CDCl3)谱图中共有5种氢,化学位移(δ)为7.23是溶剂氘代氯仿的峰,δ为1.53是水中氢原子峰,其余为2,3,6,7-四甲基蒽中3种氢的峰,δ值分别为2.43(s,12H,CH3),7.68(s,4H,H-1,4,5,8),8.13(s,2H,H-9,10).核磁谱图分析与其结构相吻合,证明了其结构的正确性.
从图4(b)可知:2,3,6,7-四甲基三蝶烯是结构对称的分子,一共含有5种氢,1H NMR(400 MHz,CDCl3)谱图上共出现了7种氢,δ为1.52~1.58的峰是水上氢原子的峰,δ为7.27~7.29的峰是溶剂氘代氯仿的峰,剩余H的δ值分别为2.18(s,12 H,CH3),5.32(s,2 H,H-9,10),6.95~7.00(m,2 H,H-12,13),7.20(s,4H,H-1,4,5,8),7.34~7.38(m,2H,H-11,14).分析结果表明:所得谱图数据与参考文献[8]报道一致且与化合物结构相吻合,证明合成的2,3,6,7-四甲基三蝶烯是所要的目标产物.
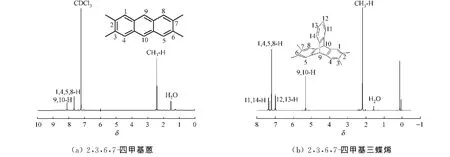
图4 化合物的核磁共振氢谱图Fig.41H NMR spectra of compounds
3 结束语
以苯甲醇和邻二甲苯,在无水AlCl3条件下,经Friedel-Crafts Alkylation反应得到2,3,6,7-四甲基蒽;然后,将其与邻氨基苯甲酸经Diels-Alder反应生成具有独特三维刚性芳香结构的2,3,6,7-四甲基三蝶烯,并通过IR和1H NMR谱的证明.该方法大大缩短合成2,3,6,7-四甲基三蝶烯的实验步骤,提高了其收率,不仅为合成蒽的衍生物提供一种可靠方法,也为三蝶烯的进一步功能化奠定了基础.
[1] NISHIMURA G,SHIRAISHI Y,HIRAI T.A fluorescent chemosensor for wide-range p H detection[J].Chem Commun,2005,1(42):5313-5315.
[2] WONGKONGKATEP J,MIYAHARA Y,OJIDA A,et al.Label-free,real-time glycosylt ransferase assay based on a fluorescent artificial chemosensor[J].Angew Chem Int Ed,2006,45(4):665-668.
[3] WANG Li-duo,DUAN Lian,LEI Gang-tie,et al.Bright white organic light-emitting diodes based on anthracene derivatives and rubrene[J].Japanese Journal of Applied Physics,2004,43(4B):L560-L562.
[4] HA J,VACHA M,KHANCHAITIT P,et al.Synthesis and characterization of novel light-emitting copolymers containing triphenylamine derivatives[J].Synthetic Metals,2004,144(2):151-158.
[5] ZHENG Jin-yun,ZHAN Cai-mao,WU Song,et al.A highly soluble blue light emitting copolymer of anthracene and dialkyloxyl benzene prepared by oxidative-coupling reaction[J].Polymer,2002,43(6):1761-1765.
[6] WITTIG G,LUDWIG R.Triptycen ausanthracen und dehydrobenzol[J].Angew Chem,1956,68(1):40.
[7] STILES M,MILLER R G.Decomposition of benzenediazonium-2-carboxylate[J].J Am Chem Soc,1960,82(14):3802.
[8] 汪家喜,荆彬,程琳,等.三蝶烯-2,3,6,7-四甲酸二酐的合成与表征[J].华侨大学学报:自然科学版,2010,31(6):645-648.
[9] 王清廉,沈凤嘉.有机化学实验[M].北京:高等教育出版社,2001:220-221.
[10] WOLTHUIS E.Synthesis of some methyl-substituted anthracenes[J].Journal of Organic Chemistry,1961,26(7)2215-2220.
[11] GONG Y,ZHOU Yu-chao,QIN Jian-bo,et al.Synthesis,crystal structure and photoluminescence of 2,6-dimethylanthracene and its pseudo-triptycene derivatives[J].Journal of Molecular Structure,2010,963(1):76-81.
[12] GODINEZ C E,ZEPEDA G,MORTKO C J,et al.Molecular crystals with moving parts:Synthesis,characterization,and crystal packing of molecular gyroscopes with methyl-substituted triptycyl frames[J].J Org Chem,2004,69(5):1652-1662.
[13] RYBÁĈKOVÁM,BĚLOHRADSKýM,HOLýP,et al.Synthesis of highly symmetrical triptycene tetra-and hexacarboxylates[J].Synthesis,2007(10):1554-1558.
New Efficient Synthesis and Characterization of 2,3,6,7-Tetramethyltriptycene
LIU Jia-chuan,CHENG Lin
(College of Materials Science and Engineering,Huaqiao University,Xiamen 361021,China)
O-xylene and benzyl alcohol underwent friedel-crafts alkylation reaction with anhydrous aluminum chloride as catalyst,by way of carbonium ion mechanism to afford 2,3,6,7-tetramethylanthracene.Then,2,3,6,7-tetramethylanthracene and benzyne generated in situ underwent a Diels-Alder reaction to give 2,3,6,7-tetramethyltriptycene containing an unique three-dimensional rigid aromatic structure.Finally,the structures of 2,3,6,7-tetramethylanthracene and 2,3,6,7-tetramethyltriptycene were characterized by IR and1H NMR spectroscopy.
2,3,6,7-tetramethylanthracene;2,3,6,7-tetramethyltriptycene;Diels-Alder reaction;benzyl alcohol;o-xylene
O 625.522
A
(责任编辑:钱筠 英文审校:熊兴泉)
1000-5013(2012)05-0518-04
2012-03-26
程琳(1964-),男,教授,主要从事高性能、功能性高分子材料的研究.E-mail:cheng@hqu.edu.cn.
国家自然科学基金资助项目(50673031,50973036)

