丹参注射液超声雾化前后三种成分的质量分析*
★ 韩飞 肖雄* 夏梦欣 李瀚南 罗晓健
(1.江西中医药大学 江西 南昌 330004;2.中药固体制剂制造技术国家工程中心 江西 南昌 330006)
丹参注射液具有活血化淤、理气开窍、养血安神、调经止痛、凉血消痈之功效,同时还具有扩张血管、增进冠状动脉血流量的作用[1,2]。临床上主要用于治疗胸闷、心悸、心绞痛,急慢性心肌梗塞,缺血性脑中风,脑梗塞或中风后遗症等病症。
近年来,有大量文献报道丹参注射液可采用超声雾化吸入的方式治疗毛细支气管炎、急性肺炎、咽炎,甚至心绞痛等疾病,并取得了较好的疗效[3-7],但目前大多数报道只关注其雾化吸入的实际疗效,而很少从制剂基础研究的层面上去探讨其雾化吸入的可行性,本文建立了同时测定丹参注射液超声雾化液中原儿茶醛、丹酚酸B、丹参酮ⅡA的含量检测方法,并对比超声雾化前后三种成分含量的变化,初步研究了丹参注射液雾化吸入的可行性。
1 仪器与试剂
鱼跃牌4021AI超声雾化器(江苏鱼跃医疗设备股份有限公司,苏药管械准字2002第223);EPED-20TH纯水器(上海精密仪表有限公司);KQ5200DA超声清洗器(昆山市超声仪器有限公司);分析天平(北京赛多利斯仪器系统有限公司,感量0.01mg);Agilent-1200高效液相色谱仪:Agilent-1200泵,VWD检测器,Agilent-1200化学工作站。
原儿茶醛对照品,丹酚酸B对照品,丹参酮ⅡA对照品(均购自中国药品生物制品检定所,批号110810-201007,111562-201111,110766-201019);丹参注射液(上海中西制药有限公司,国药准字Z31020345,规格2mL/支);甲醇(色谱纯,上海星可化学试剂有限公司);磷酸(分析纯,天津市永大化学试剂有限公司);水为超纯水,其他试剂均为分析纯。
2 方法与结果
2.1 色谱条件 色谱柱:Phenomenex Gemini 5u C18110A(250mm×4.6mm,5μm,美国菲罗门);流动相 甲醇(B)-0.1%磷酸水(A)按表1的程序梯度洗脱;流速1.0mL/min;进样量5μL;柱温30℃;检测波长280nm;原儿茶醛的保留时间(tR)2.368min,丹酚酸B的保留时间(tR)3.471min,丹参酮ⅡA的保留时间(tR)11.582min。在上述色谱条件下,三种成分与相邻成分有较好的分离,各成分的理论塔板数均大于5000,色谱图见图1。
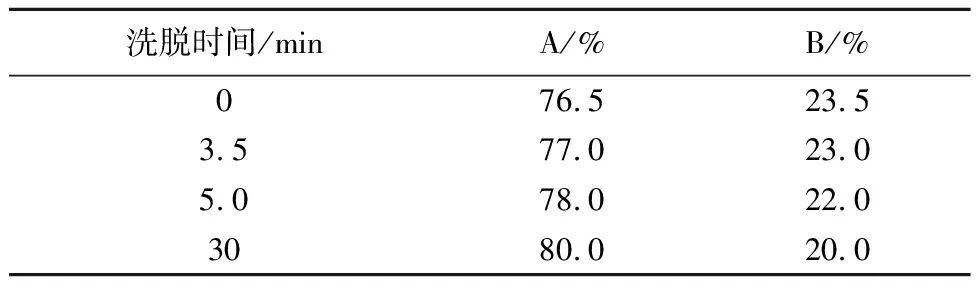
表1 流动相洗脱程序表
2.2 溶液的制备
2.2.1 混合对照品溶液的制备 分别精密称取原儿茶醛、丹酚酸B、丹参酮ⅡA对照品适量,色谱甲醇溶解,置10mL容量瓶中,称重,超声20min,放冷,甲醇补足失重,用0.45μm微孔滤膜过滤,取续滤液,即得原儿茶醛(0.146mg/mL)、丹酚酸B(0.096mg/mL)、丹参酮ⅡA(0.343mg/mL)的混合对照品溶液。
2.2.2 丹参(甲醇)溶液的制备 精密量取4.0mL丹参注射液(批号:20140315),色谱甲醇溶解,置50mL容量瓶中,称重,超声两次,每次15min,放冷,甲醇补足失重,用0.45μm微孔滤膜过滤,取续滤液,即得丹参(甲醇)溶液。
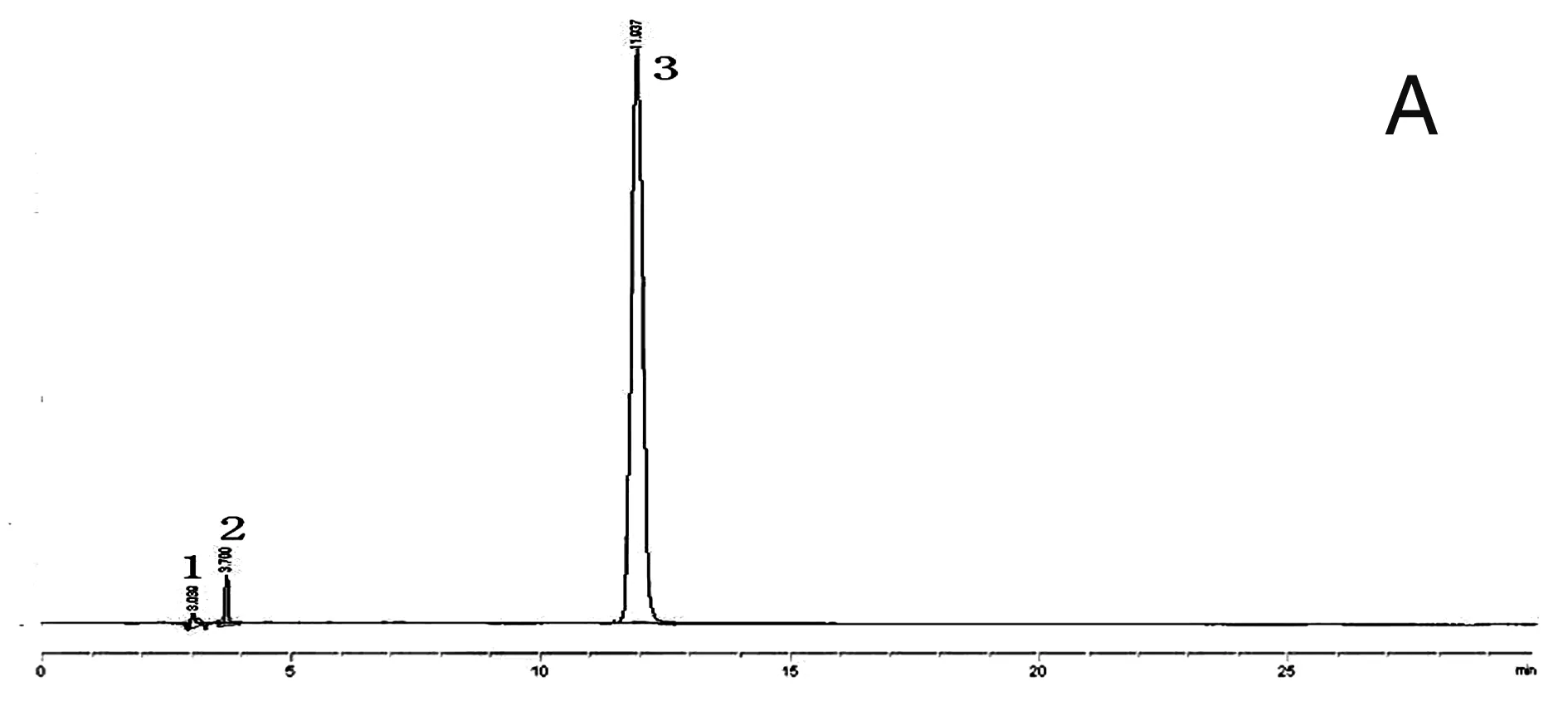
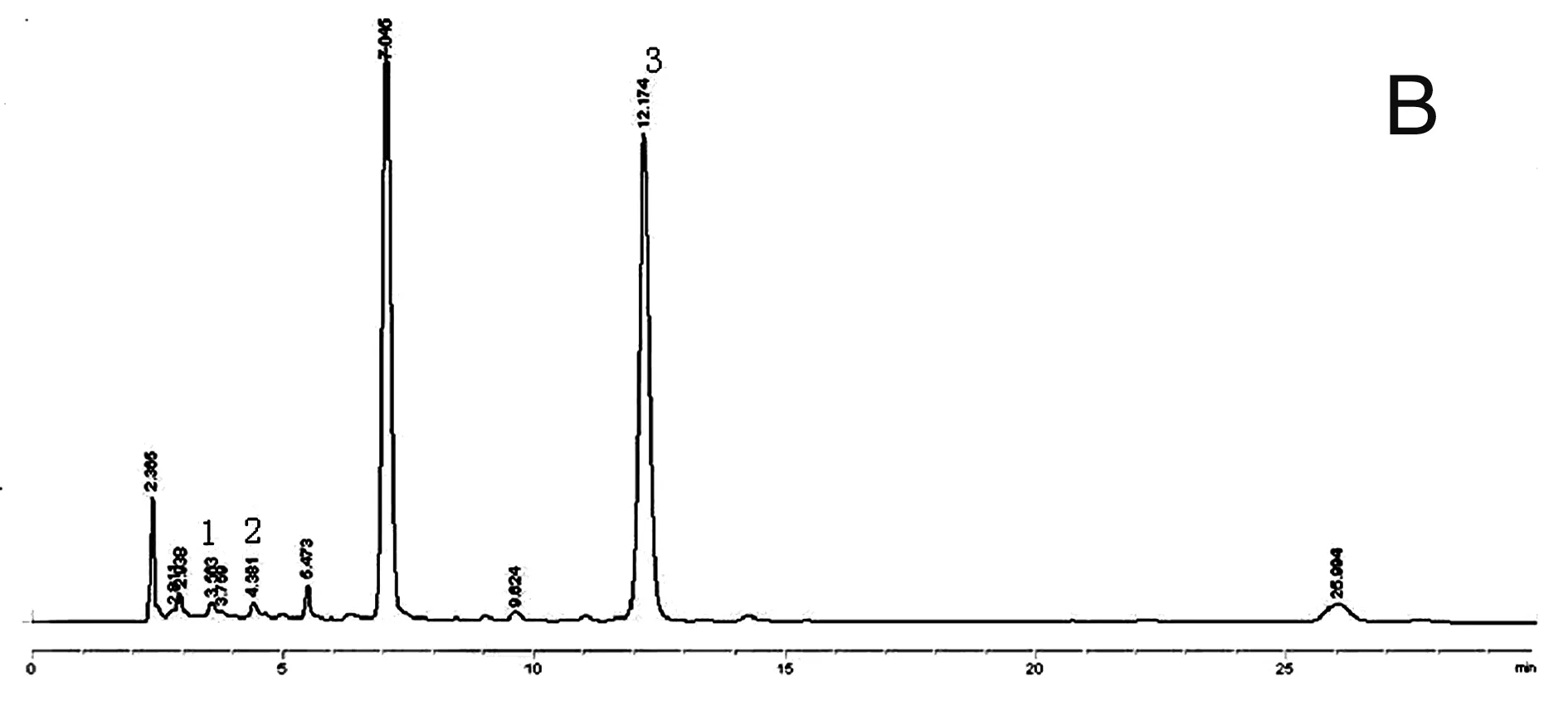
1.原儿茶醛;2.丹酚酸B;3.丹参酮ⅡA
2.2.3 丹参注射液超声雾化液的收集 取干燥的锥形瓶一个,置于装满500mL水的烧杯中,冷冻12 h,取出,将同口径的雾化导管接于锥形瓶上,密封膜缠封,经检查气密性良好。大雾化杯中装入约500mL超纯水,小雾化杯中加入2.2.2项下制备的150mL溶液,盖上顶盖,频率调至1.7MHz±10%;雾化量调至4mL/min;打开电源,雾化30min后,关闭电源,转移至40℃恒温水浴锅中加热,收集所得雾化液,用0.45μm微孔滤膜过滤,取续滤液,即得丹参注射液超声雾化液。
2.4 线性关系考察 分别精密量取原儿茶醛(0.146mg/mL)、丹酚酸B(0.096mg/mL)、丹参酮ⅡA(0.343mg/mL)对照品溶液,各0.1,1,2,4,6,8,10mL,分别置10mL容量瓶中,加甲醇稀释至刻度,摇匀,定容,分别精密吸取溶液各10μL,注入色谱仪,记录峰面积,以峰面积(Y)为纵坐标,进样量(X)为横坐标进行线性回归,绘制标准曲线,结果表明在进样量范围内线性关系良好,见表2。
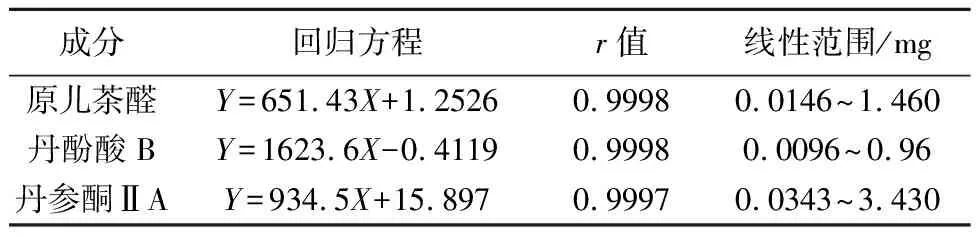
表2 三种成分线性回归方程
2.5 精密度试验 精密吸取2.2.1项下对照品溶液10μL,在上述色谱条件下,连续进样6次,测定峰面积,结果显示原儿茶醛、丹酚酸B、丹参酮ⅡA峰面积相对标准偏差(RSD)分别为1.743%,1.430%,1.288%,表明仪器精密度良好。
2.6 重复性试验 按2.2.2和2.2.3项方法平行制成6份超声雾化液(批号20140323),在上述色谱条件下,进样10μL,测定峰面积,结果显示原儿茶醛、丹酚酸B、丹参酮ⅡA峰面积RSD分别为1.257%,1.792%,1.318%,表明该方法重现性良好。
2.7 稳定性试验 精密吸取同一超声雾化液(批号20140323)10μL,分别于0,2,4,8,12,24 h,在上述色谱条件下,测定峰面积,结果显示原儿茶醛、丹酚酸B、丹参酮ⅡA峰面积RSD分别为1.191%,1.223%,1.607%,表明超声雾化液样品在24h内稳定性良好。
2.8 加样回收率试验 精密称取18份任意批号的丹参注射液,分成3组,每组6份,分别加入各对照品适量,按2.2.2和2.2.3项的方法制备成样品溶液,精密吸取样品溶液10μL,在上述色谱条件下,测定峰面积,各成分回收率在98.03%~101.66%,RSD<2%,结果见表3。
2.9 样品测定 按2.2.1项方法制备成供试品五批,在按照2.3项方法制备成超声雾化液,精密吸取10μL,在上述色谱条件下测定,按照外标法计算各成分的含量,结果见表4。
2.10 超声雾化前后三种成分含量变化 按照2.2.2和2.2.3项的方法,各制备一批样品溶液,分别吸取上述两种溶液各10μL,在上述色谱条件下测定,记录色谱峰面积,测定各成分的含量等,见表5,图2。
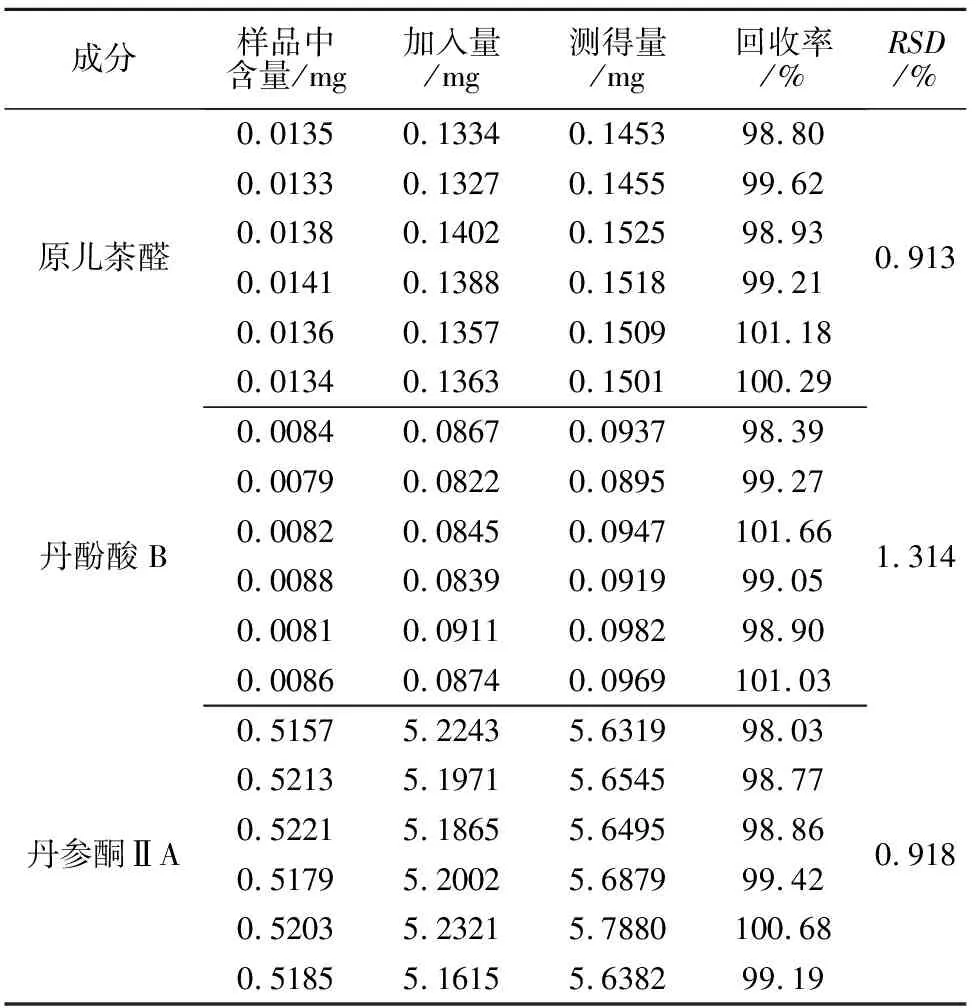
表3 加样回收率实验结果
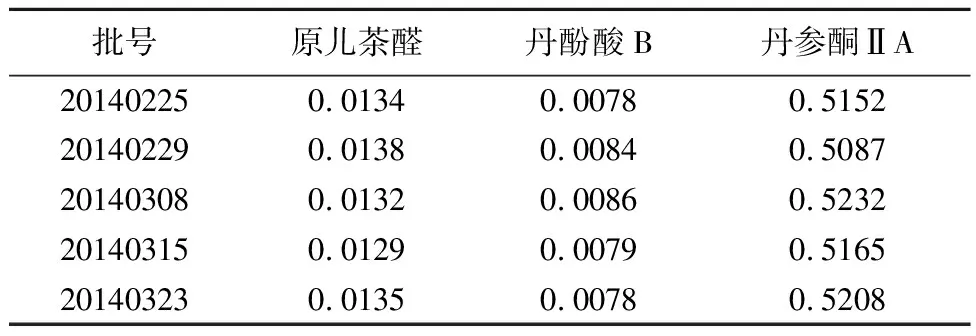
表4 不同样品三种成分测定结果 /mg·mL-1
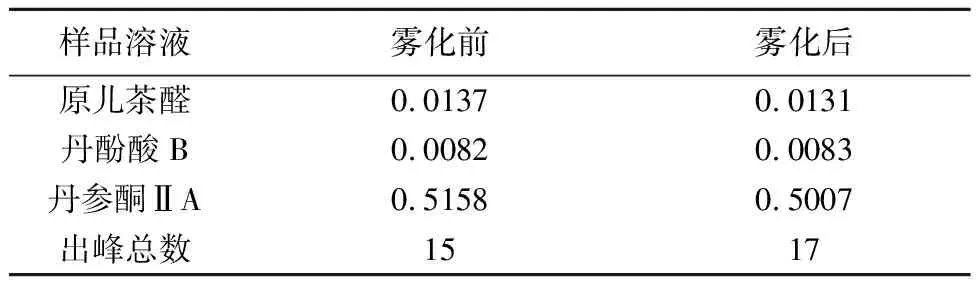
表5 雾化前后各成分含量变化 /mg·mL-1
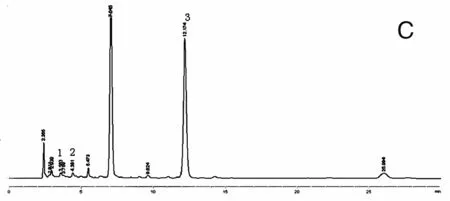
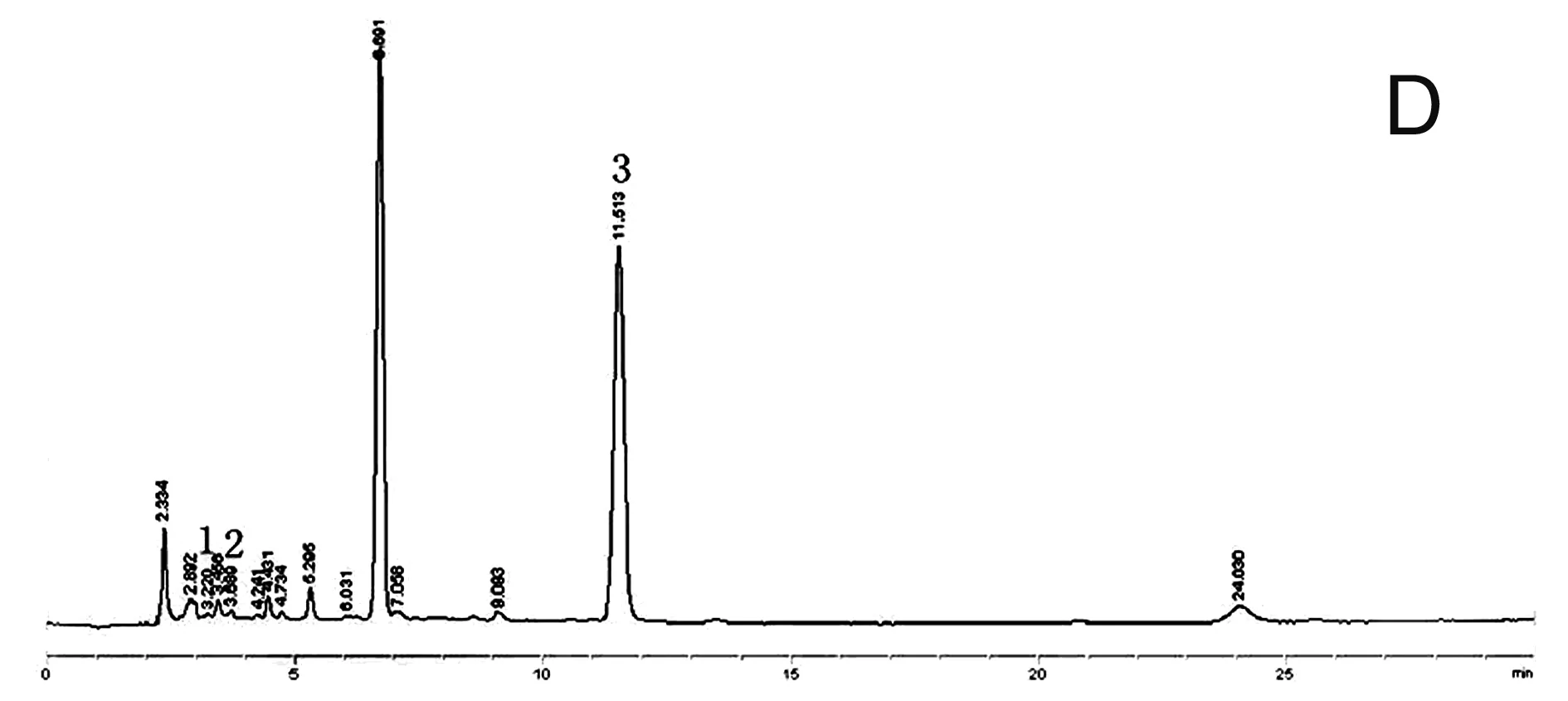
C.雾化前色谱图;D.雾化后色谱图
3 讨论
3.1 流动相的选择 本实验根据文献报道[9-12]曾尝试过乙腈-水(73∶27),甲醇-0.5%磷酸溶液(4∶96),甲醇-0.1%磷酸溶液(85∶15),甲醇-水-冰醋酸(21∶78∶1)等流动相,结果分离效果均不好。最终确定采用甲醇-0.1%磷酸水梯度洗脱(表1),此流动相可同时分离三种成分,且该方法简便、准确,重复性好,分离度高,所用时间仅为30min。
3.3 收集装置的选择 在现用装置前曾尝试连接冰冷冻过的冷凝管,但雾化后小液滴的温度较低,且为液态,而非气态,所以使用热交换法使其冷凝的方式几乎无效,故采用本实验装置,使小液滴在相对封闭的环境中达一定压力从而凝聚为大液滴而形成雾化收集液。另雾化管中亦有雾化液残留,收集量可观,约占最终收集液的90%。同时,雾化过程中,顶盖出雾口有回流现象,故小雾化杯中存留的大量药液有一部分也经过了雾化过程,符合雾化吸入的条件。
3.4 超声雾化参数 本实验所采用的超声雾化参数(超声频率:1.7MHz±10%;雾化量:4mL/min;雾化时间:30min),参考了相关文献[5,7],与临床上采用的参数基本一致,具有一定的代表性,但雾化的方式不同,如采用氧驱动雾化吸入,三种成分的含量是否变化还有待于进一步研究[13,14]。
3.6 超声雾化前后的变化 通过对比丹参注射液雾化前后三种成分的变化发现,其含量的改变极小,出峰数基本相同,由图2,表5可知,雾化后出峰数甚至多出2个,出峰时间集中在2.5~5min。分析原因可能是经过超声雾化后,促进了样品中水溶性成分的溶解,使得原本在甲醇中溶解度不大的成分可在流动相中洗脱,故产生了“多峰现象”,但总体来说,其峰面积小于7,含量几乎可以忽略不计。此结果为探讨丹参注射液雾化吸入给药的可行性,提供了初步的实验依据。
[1]李文华.丹参注射液的临床应用与不良反应[J].中国医药指南,2014,12(3):169-170.
[2]陈海芹.丹参类制剂的药理活性及临床应用[J].中国医学工程,2014,22(2):165.
[3]戈艳蕾,刘香玉,李建,王红阳,李繁丽.丹红注射液及肝素雾化吸入治疗间质性肺炎疗效[J].时珍国医国药,2013,24(7):
1 668-1 669.
[4]朱惠萍.盐酸氨溴索葡萄糖注射液联合丹参注射液超声雾化吸入佐治毛细支气管炎60例[J].山西职工医学院学报,2011,21(1):38-39.
[5]王洁翡,潘玉娜.丹参注射液超声雾化吸入治疗毛细支气管炎疗效观察[J].中外医疗,2009,14:94-95.
[6]林东浩.复方丹参注射液在小儿支气管肺炎治疗中的应用价值[J].河北医药,2010,32(12):1 580-1 581.
[7]朱昌周.黄芪注射液与丹参注射液雾化吸入治疗顽固性充血性心力衰竭96例临床观察[J].吉林医学,2010,31(13):1 826-
1 827.
[8]张青莲,朱雅艳,徐美华.不同厂家丹参注射液的质量考察[J].海峡药学,2013,25(5):44-47.
[9]闫占社,王开,黄飙.丹参注射液制备工艺改进研究[J].西北大学学报,2013,43(5):735-738.
[10]马志刚,曹秋娥,丁中涛.高效液相色谱法测定丹参及其复方制剂中的3个丹参酮[J].云南民族大学学报,2013,22(6):391-393.
[11]尹爱群,刘群,邱明丰.不同厂家复方丹参片中丹参酮ⅡA的含量测定[J].中国中药杂志,2010,31(20):1 729-1 731.
[12]王英,李云.不同厂家复方丹参注射液中丹酚酸B的含量比较[J].中国医药指南,2012,10(9):401-402.
[13]夏文芬.氧驱动雾化吸入与空气压缩泵雾化吸入治疗小儿哮喘的疗效比较[J].现代实用医学,2013,25(8):903-904,909.
[14]高京芹.复方丹参注射液氧驱动雾化吸入辅助治疗高原地区毛细支气管炎患儿的临床疗效观察[J].青海医药杂志,2011,41(8):25-26.

