尼妥珠单抗治疗1515例非小细胞肺癌临床疗效及不良反应的回顾性分析
倪军 斯晓燕 王汉萍 张力
中国医学科学院北京协和医学院北京协和医院呼吸科,北京 100730
无论在发达国家还是在发展中国家,肺癌的发病率和死亡率均居首位。近年来,随着对肺癌驱动基因研究的不断深入,使得晚期非小细胞肺癌(non-small lung cancer,NSCLC)的治疗已由病理决策为主转变到病理与驱动基因共同决定治疗选择的时代。表皮生长因子(epidermal growth factor receptor,EGFR)是一种具有酪氨酸激酶活化作用的受体,其参与细胞的增殖、生长、迁移与活化,在肿瘤形成中起到重要作用。大多数NSCLC肿瘤组织表达或高度表达EGFR[1-3]。目前,西妥昔单抗以EGFR为靶点被用于治疗NSCLC[4],但其为一种人鼠嵌合型IgG1单克隆抗体,临床应用中存在痤疮样皮疹、发热、恶心/呕吐等不良反应。尼妥珠单抗(nimotuzumab)是一种抗EGFR胞外配体结构域的人源化IgG1单克隆抗体,临床耐受性好,不良反应轻[5-6]。国家食品药品监督管理局(SFDA)批准其可以与放疗联合治疗EGFR表达阳性的Ⅲ/Ⅳ期鼻咽癌,但目前尚缺乏该药治疗NSCLC患者的疗效及安全性方面的数据。本研究收集了北京协和医院2012年2月至2014年3月接受尼妥珠单抗治疗的晚期NSCLC患者的临床资料,并分析了尼妥珠单抗临床疗效和不良反应。
1 资料与方法
1.1 临床资料
选取2012年2月至2014年3月在北京协和医院接受尼妥珠单抗治疗的晚期NSCLC患者。纳入标准:①经病理组织学确诊为原发性NSCLC;②临床分期为ⅢB期、Ⅳ期或不可手术切除的ⅢA期。③按实体瘤疗效评价标准(response evaluation criteria in solid tumors,RECIST)评价为治疗前有可测量靶病灶。④自愿接受尼妥珠单抗治疗。
按照上述标准共纳入15例患者(表1),其中男性13例,女性2例,年龄在35~76岁,中位年龄55岁;美国东部肿瘤协作组(Eastern Cooperative Oncology Group,ECOG)的体力状态评分在0~1分者10例,2~4分者5例。15例患者中最常见的转移部位为肺内转移(9例,60%),其次是骨转移(8例,53%)、颅内转移(7例,47%)及胸膜转移(7例,47%)。其中鳞癌患者7例,腺癌患者8例;EGFR突变阳性患者1例,阴性患者11例,突变情况不详者2例。棘皮动物微管结合蛋白样蛋白4(echinoderm microtubule-associated protein-like 4,EML4)和间变型淋巴瘤激酶(anaplastic lymphoma kinase,ALK)的融合基因(EML4-ALK)阳性1例,阴性2例,情况不详12例。所有患者预计生存期均大于3个月,尼妥珠单抗治疗前血常规、肝肾功能及心电图均在正常范围内。
1.2 治疗方案
全部病例均采用含尼妥株单抗的方案治疗。治疗方法:将尼妥株单抗400 mg稀释于250 ml 0.9%的氯化钠注射液中,静脉滴注,给药时程控制在60分钟以上,每周一次。尼妥珠单抗给药结束1小时内不滴注除生理盐水以外的其他药物。尼妥珠单抗给药前无预处理。每6周进行疗效评估。若联合其他化学治疗,则在同一天给药,之后每周给药一次,初治患者根据病理类型给予一线化疗方案,复治患者给予既往未使用或与既往使用药物无交叉耐药的化疗药物,一般采用常规剂量。若联合其他靶向治疗患者,则在同一天口服靶向药物,之后每周给药一次。若联合放疗患者,即为同步放疗。所有患者均接受至少1次含尼妥株单抗的治疗。其中接受单药周疗者2例,联合紫杉醇或多西他赛为主方案者6例,联合吉西他滨者1例,联合依托泊苷者3例,联合培美曲赛者1例,联合放疗者2例,联合自体细胞回输者1例,联合替莫唑胺者2例。其中1例中分化鳞癌患者的一线方案为尼妥珠单抗同步放疗,二线方案为尼妥珠单抗联合吉西他滨,三线方案为尼妥珠单抗联合自体细胞回输。

表1 1 5 1 5例患者的基线特征
1.3 EGFR EGFR的表达评价
根据肿瘤细胞膜EGFR的免疫组化染色结果,我院病理科医师对肿瘤细胞的EGFR表达情况予以评分,且所有检测均由同一名病理医师完成。
1.4 EML EML44-ALK-ALK融合基因表达评价
根据肿瘤细胞质内EML4-ALK免疫组化染色结果,我院病理科医师对肿瘤细胞EML4-ALK融合基因的表达结果予以评价,且所有检测均由同一名病理医师完成。
1.5 疗效、不良反应和体力状态评价
患者接受尼妥珠单抗给药6周后对其进行随诊,并参照RECIST 1.0标准进行疗效评价。评价结果分为完全缓解(complete response,CR)、部分缓解(partial response,PR)、疾病稳定(stable disease,SD)和疾病进展(progressive disease,PD)。以CR+PR计算客观有效率(objective response rate,ORR),以CR+PR+SD计算疾病控制率(disease control rate,DCR)。无进展生存期(progression-free survival,PFS)定义为从治疗开始至病情进展或死亡的时间;总生存期(overall survival,OS)定义为从治疗开始至死亡的时间。
按美国国家癌症研究所(National Cancer Institute,NCI)的常见不良反应评价标准(common terminology criteria for adverse events,CTCAE)3.0版,医师于每周期治疗前均评价药物不良反应。
所有患者每接受尼妥珠单抗治疗2次后均进行ECOG PS评分。
2 结果
全部患者随访至2014年3月20日。至截止日期有14例患者已结束尼妥珠单抗治疗,1例患者仍在接受尼妥珠单抗治疗。
2.1 客观疗效
15例患者均接受至少2周的尼妥珠单抗治疗,均可进行安全性的评价;其中11例患者完成了6周以上尼妥珠单抗治疗,可进行疗效评价(表2)。这11例患者中,治疗首个6周后,8例达SD,3例PD,DCR为72.7%(8/11)。
在4例不能进行疗效评价的患者中,1例于截止日期时用药未满6周;3例于治疗2周或4周时因疾病进展而中断治疗:其中1例在接受2周尼妥珠单抗治疗后死亡,1例接受2周尼妥珠单抗治疗后因出现咳嗽、咳痰症状加重,肺内肿瘤增大而中断尼妥珠单抗治疗,1例接受4周尼妥珠单抗治疗后因出现新发的颅内转移而中断治疗。
2.2 ECOGPS评分情况
15例患者均接受了2周以上的含尼妥珠单抗方案治疗。ECOG PS评分结果显示,在第2周末,与用药前相比,仅1例患者出现ECOG PS评分升高(由4分升至5分),3例患者的ECOG PS评分有所改善(均由2分降为1分)。
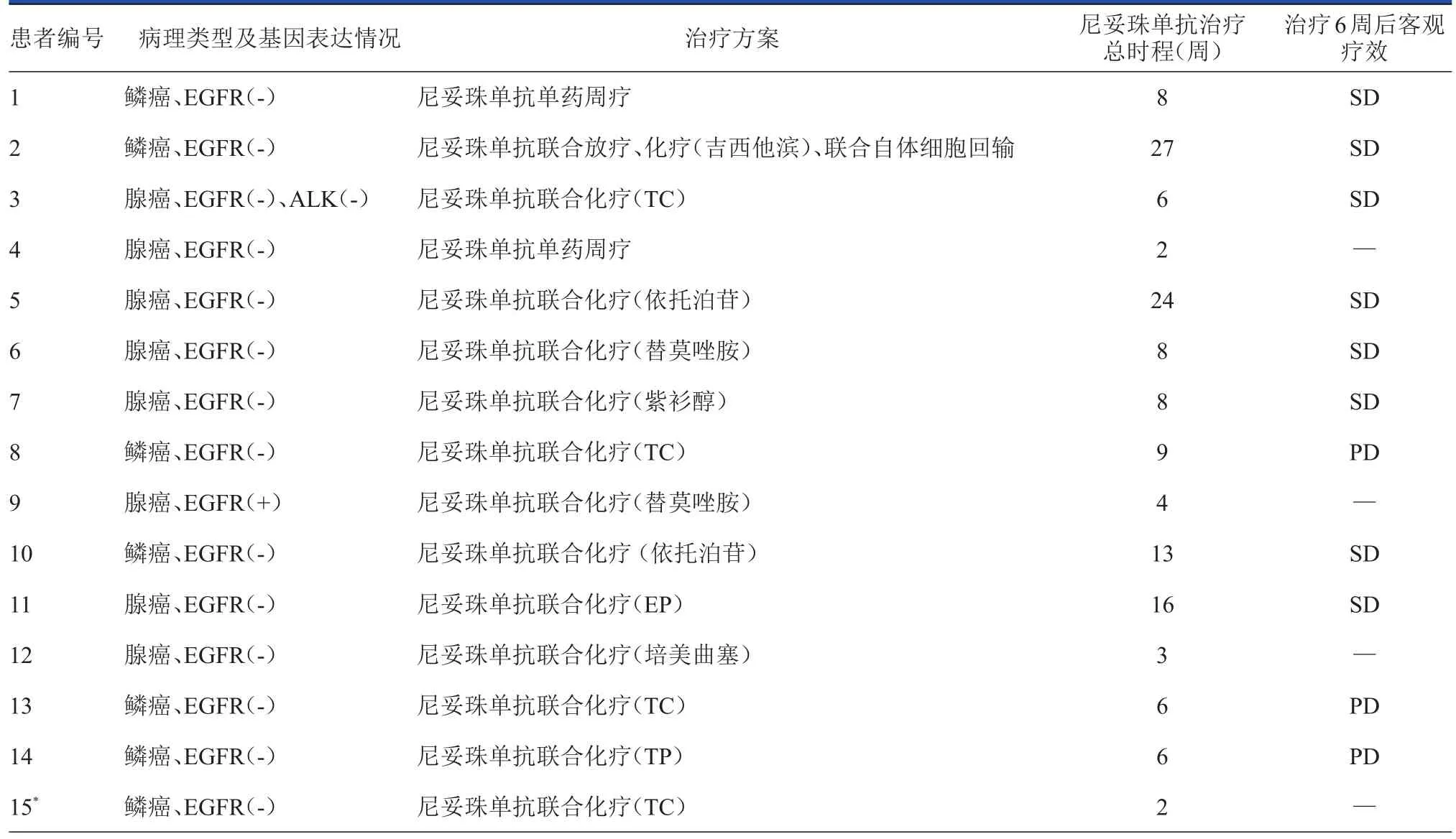
表2 1 5 1 5例患者的临床特征及治疗6 6周后的客观疗效评价结果
2.3 安全性评价情况
在整个治疗过程中,患者对尼妥珠单抗治疗的耐受性较好。其中3例出现不良反应的患者均为联合化疗患者。仅1例出现了3~4级不良反应,为3级中性粒细胞减少。其中与尼妥珠单抗相关的非血液系统不良反应为:恶心呕吐1例,全身乏力1例。上述不良反应经对症处理或休息后均得到缓解。
3 讨论
本研究回顾性总结了15例尼妥珠单抗(400 mg)治疗晚期NSCLC患者的病例资料。研究结果显示,经含尼妥珠单抗方案治疗6周后,达SD的患者有8例,PD者3例,疾病控制率为72.7%(8/11)。经含尼妥珠单抗方案治疗2周后,患者的ECOG PS评分改善率为20%(3/15)。Bebb等[7]的一项关于晚期NSCLC患者的研究表明,尼妥珠单抗联合放疗的客观有效率为66%,疾病控制率为94%。此结果亦被Choi等[8]证实。由此可见,尼妥珠单抗联合化疗或放化疗能提高晚期NSCLC患者的疾病控制率。
痤疮样皮疹是EGFR抑制剂最常见的不良反应,发生率为50%~80%,且多项研究证实EGFR类单抗药物皮疹的出现与ORR、DCR明显相关[9]。然而,在本项研究中,未观察到药物相关性皮疹的出现,且很多临床获益者未出现皮疹,这提示尼妥珠单抗带来的临床获益与皮疹出现与否无关。此外,与西妥昔单抗治疗伴随约50%的腹泻发生率相比,本组患者未发生腹泻。本研究的病例中仅1例患者于联合化疗治疗2周后出现3级中性粒细胞减少,1~2级不良反应分别为恶心呕吐和乏力,其发生率为13.3%(2/15),经对症处理或休息后均得到缓解。考虑因尼妥珠单抗是人源化的IgG1型单克隆抗体,其安全性较好,所以不良反应的发生率较低。
限于本研究为回顾性病例分析,入组病例少,且尼妥珠单抗治疗的费用昂贵,故其结论仍需进一步扩大样本量来验证,以便得出该药治疗中国患者的更可靠数据。
[1]Tsao MS,Sakurada A,Cutz JC,et al.Erlotinib in lung cancer-molecular and clinical predictors of outcome[J].N Engl J Med,2005,353(2):13.4.
[2]Hinch FR,Varella-Gareia M,Bunn PA Jr,et al.Molecular predictors of outcome with gefitinib in a phaseⅢplacebo-controlled study in advanced non-small cell lung cancer[J].J Clin Oncol,2006,24(31):5034-5042.
[3]Brabender J,Danenberg KD,Metzger R,et al.Epidermal growth factor receptor and HER2-neu mRNA expression in non-small cell lung cancer is correlated with survival[J].Clin Cancer Res,2001,7(7):1850-1855.
[4]Lacouture ME,Anadkat MJ,Bensadoun RJ,et al.Clinical practice guideline for the prevention and treatment of EGFR inhibitor as sociated dermatologic toxicities[J].Support Care Cancer,2011,19(8):1079-1095.
[5]Crombet-Ramos T,Rak J,Pérez R,et al.Antiproliferative.antiangiogenic and proapoptotic activity of h-R3:a humanized anti-EGFR antibody[J].Int J Cancer,2002,101(6):567-575.
[6]Akashi Y,Okamotol I,Iwasa T,et al.Enhancement of the antitumor activity of ionizing radiation by nimotuzumab,a humanized monoclonal antibody to the epidermal growth factor receptor,in non-small cell lung cancer cell lines of differing epidermal growth factor receptor status[J].Br JCancer,2008,98(4):749-755.
[7]Bebb G,Smith C,Rorke S,et al.PhaseⅠ clinical trial of the anti-EGFR monoclonal antibody nimotuzumab with concurrent external thoracic radiotherapy in Canadian patients diagnosed with stageⅡb,Ⅲ orⅣ non-small cell lung cancer unsuitable for radical therapy[J].Cancer Che-mother Pharmacol,2011,67(4):837-845.
[8]Choi HJ,Sohn JH,Lee CG,et al.A phaseⅠ study of nimotuzumab in combination with radiotherapy in stagesⅡB-Ⅳ non-small cell lung cancer unsuitable for radical therapy:Korean results[J].Lung Cancer,2011,71(1):55-59.
[9]Saif MW,Kim R.Incidence and management of cutaneous toxicities associated with cetuximab[J].Expert Opin Drug Saf,2007,6(2):175-182.

