白术多糖的提取及其抗氧化活性的研究
吴铭,韩丹,郭立泉
(吉林工商学院,粮油食品深加工吉林省高校重点实验室,吉林长春130507)
白术(Atractylodes macrocephala)是菊科苍术属的一种植物,以根茎入药,具有利水消肿、健脾益气,止汗,安胎等功效[1]。现代医药研究发现白术多糖可以影响内分泌系统,能有效调节免疫功能[2]。白术含有大量的生物活性成分,包括多糖、苍术酮和醇、白术内酯、氨基酸等[3]。白术多糖是白术主要生物活性成分之一,有研究表明,白术多糖有抗肿瘤,抗氧化,抗高血压和免疫调节活动[4]。
目前白术多糖的提取方法主要是热水浸提法、酶法、微波辅助提取法,最常见的提取方法是热水浸提法,但是该方法通常需要浸提温度高,并且浸提次数多,但提取效率较低[5]。酶法提取对酶法复合酶有所要求,提取次数2次[6]。微波辅助提取法提取工艺比较复杂,且提取率不高[7]。最近超临界流体萃取,超声波提取等新技术被应用于从植物中提取的多糖,其中,超声波提取方法能产生更少的损害植物材料的结构和分子性质[8]。利用超声波的空化作用、机械效应和热效应可以加强胞内物质的释放、扩散和溶解,从而显著提高提取效率[9]。本研究就是利用超声波提取方法从白术中提取白术多糖,利用正交试验法优化提取条件,然后通过超氧阴离子自由基体系和DPPH自由基体系对对白术多糖的抗氧化活性进行初步研究。
1 材料和方法
1.1 试剂和仪器
干白术购买于吉林长春当地药店;DPPH、BHT、NADH和NBT从西格玛公司购买;其他的化学试剂均为分析纯。
TU-1901紫外分光光度计:北京普析通用仪器有限责任公司;GT-2013QTS超声波清洗器:广东固特超声股份有限公司。
1.2 白术多糖的提取
将干白术磨成细粉,过40目筛。然后将干粉沉浸在蒸馏水中,按照固体/液体比率分5组1∶10、1∶15、1 ∶20、1 ∶25、1 ∶30(g/mL),进行超声波辅助提取时间为 10、20、30、40、50 min,温度水平为 35、45、55、65、75 ℃和功率设为 30、40、50、60、70、80 W。收集提取液,于3 000 r/min离心10 min,取上清,按sevag法(氯仿/正丁醇=5∶1)脱蛋白,用真空旋转蒸发仪将滤液浓缩,取滤液加4倍的95%的乙醇沉淀,放置过夜,次日以3 000 r/min离心10 min,取沉淀用丙酮和乙醇清洗,得到粗多糖,多糖的提取率是按照下列公式计算:
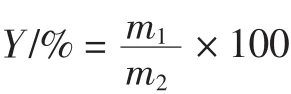
式中:Y代表多糖的提取率;m1代表了多糖的重量,g;m2代表了干样品重量,g。
1.3 测定白术多糖的抗氧化活性
1.3.1 DPPH自由基体系[10]
将白术多糖和二叔丁基对甲酚(BHT)配成不同浓度的待测液,另外用50%的乙醇配置6 mg/100 mL的DPPH溶液。在试管中依次加入2 mL的DPPH溶液和1 mL 不同浓度待测液(0.05、0.1、0.15、0.2、0.25、0.3 mg/mL),室温放置(避光)反应 30 min,然后在517 nm处测定吸光度,以1mL的50%乙醇加入到2mL的DPPH溶液中做空白对照。以二叔丁基对甲酚(BHT)作为参照物。每个样品做3个平行样,取其平均值,清除率计算公式如下:
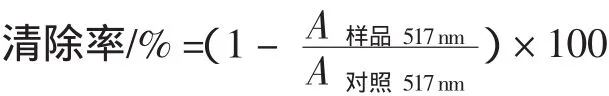
1.3.2 超氧阴离子自由基体系[10]
将白术多糖和二叔丁基对甲酚(BHT)配成不同浓度的待测液(0.05、0.1、0.15、0.2、0.25、0.3 mg/mL),配置NTB溶液:156 μmol/L的NBT溶于100 mmol/L的磷酸盐缓冲液,pH7.4;NADH 溶液 :468 μmol/L 的 NADH溶于100 mmol/L的磷酸盐缓冲液,pH7.4;PMS溶液:60 μmol/L的PMS溶于100 mmol/L的磷酸盐缓冲液,pH7.4。在试管中分别加入1 mL的NTB溶液,1 mL的NADH溶液和1 mL不同浓度的白术多糖待测液,混匀后,加入100 μL的PMS溶液,混匀后置于25℃水浴中反应5 min,然后在560 nm处测定吸光度,以空白样品作为对照。以二叔丁基对甲酚(BHT)作为参照。每个样品做3个平行样,取其平均值,清除率计算公式如下:
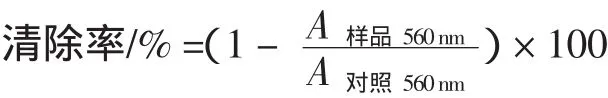
2 结果与讨论
2.1 各种因素对白术多糖的提取率的影响
固体/液体比率、超声波提取时间、温度和功率四个因素对白术多糖的提取率的影响,见图1。

图1 各种因素对白术多糖提取率的影响Fig.1 Effects of various factors on the extraction yield of Atractylodes macrocephala polysaccharides
由图1(A)可知,固液比率对白术多糖提取率的影响,最佳的固液比为 1 ∶20(g/mL);由图 1(B)可知,提取时间对白术多糖提取率的影响,最适合的提取时间为40 min;由图1(C)可知,超声功率对白术多糖提取率的影响,最适合的超声波功率是60 W;由图1(D)可知,提取温度对白术多糖提取率的影响,最适宜的提取温度为55℃。
2.2 白术多糖提取最佳条件
根据单因素试验的结果,设计正交试验L9(34),见表1。

表1 正交试验结果与分析Table 1 Results and analysis of orthogonal test
由表1可知,最佳提取条件组合是A2B2C3D1,即固体/液体的比率 1 ∶20(g/mL),提取 40 min,超声波功率65 W和提取温度55℃,白术多糖的提取率为8.52%。比较试验中A,B,C,D极差的大小,可以看出4个因素的主要关系式A>B>D>C。并且将最佳组合A2B2C3D1与K值得最佳组合A2B2C3D2进行比较试验,发现提取率还是A2B2C3D1组合较高,因此最佳组合是A2B2C3D1。
2.3 白术多糖的抗氧化活性检测
白术多糖的抗氧化活性检测结果见图2。
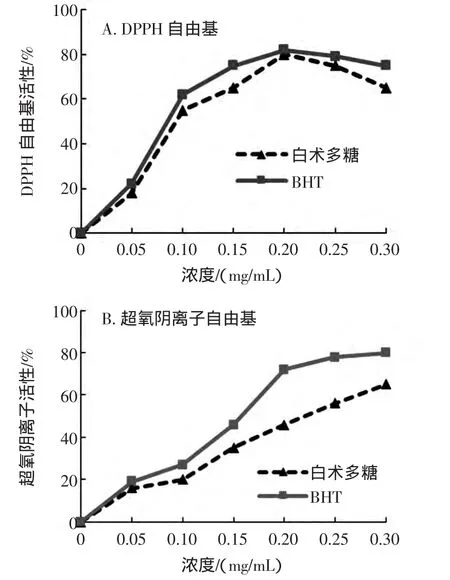
图2 白术多糖抗氧化活性检测Fig.2 Antioxidant activities assay of Atractylodes macrocephala polysaccharides
由图2(A)可知,白术多糖清除DPPH自由基的活性比二叔丁基对甲酚弱,但是随着浓度的升高,白术多糖清除DPPH自由基的活性也在升高。由图2(B)可知,随着样品浓度的增加,白术多糖和二叔丁基对甲酚清除超氧阴离子自由基的活性都随之增强,但是二叔丁基对甲酚比白术多糖更有效率。结果表明,白术多糖具有清除DPPH自由基的活性和超氧阴离子自由基的活性。
3 小结
超声波辅助提取法已经被广泛的应用于植物多糖的快速提取,通过试验表明利用超声波辅助提取法提取白术多糖的最佳提取条件是固体/液体的比率1 ∶20(g/mL),提取 40 min,超声波功率 65 W 和提取温度55℃,白术多糖的提取率为8.52%。此外,通过超氧阴离子自由基体系和DPPH体系对对白术多糖的抗氧化活性的研究表明,白术多糖具有清除DPPH自由基和超氧阴离子自由基的抗氧化活性,白术多糖的抗氧化活性和抗氧化机制期待进一步的研究。
[1] 王艳丽,张静,孙润广,等.超声参数对白术多糖抗氧化活性的影响[J].生物加工过程,2012(1):7-12
[2] 陈文,何鸽飞,姜曼花,等.近10年白术的研究进展[J].时珍国医国药,2008,19(2):338-342
[3] 季宇彬,于蕾,中药多糖的化学及药理[M].北京:人民卫生出版社,2005:20-25
[4] 付学军,崔志峰.小分子量海参肽对小鼠的抗疲劳作用[J].食品科技,2007(4):259-261
[5] 刘军海.响应面分析法优化白术多糖提取工艺[J].中成药,2008(5):48-51
[6] 侯轩,周家容,田允波.复合酶法提取白术多糖的工艺研究[J].广东化工,2008(12):91-94
[7]王洁.白术多糖提取方法的筛选及其对樱桃谷鸭饲用价值的研究[D].长沙:湖南农业大学,2007:60-70
[8] 吴铭,周桃英,陈年友,等.黄芪多糖抗疲劳作用研究[J].湖北农业科学,2014,53(1):175-177
[9] Wu Ming,Han Dan,Ma Chuanfuetal,Effects of polysaccharides from Radix Astragali on oxidative stress induced by exhaustive swimming exercise in liver and muscle of mice[J].Applied Mechanics and Materials Vols,2014(633/634):558-561
[10]Wu Ming,Ma Chuanfu,KanJunmanet al,Ultrasonic-assisted extraction and antioxidant activities of polysaccharides from Radix Astragali[J].Advanced Materials Research Vols,2014(864/867):549-552

