药物载体非PEG空白脂质体的制备及稳定性研究
袁孟娟,韩军
(聊城大学 药学院,山东 聊城 252059)
药物载体非PEG空白脂质体的制备及稳定性研究
袁孟娟,韩军Δ
(聊城大学 药学院,山东 聊城 252059)
目的 制备药物载体非PEG空白脂质体,并对其稳定性进行研究。方法 以高纯度蛋黄卵磷脂、胆固醇为成膜材料,分别采用高压均质法-挤出法和高压均质法-超声法2种方法制备非PEG空白脂质体,并研究挤出法以及超声法对空白脂质体粒径的影响,考察制得的非PEG空白脂质体的物理稳定性。结果 高压均质法-挤出法制备的非PEG空白脂质体平均粒径为86.73 nm,多分散系数(polydispersity index,PDI)为0.170;高压均质法-超声法制备的空白脂质体平均粒径为91.68 nm,PDI为0.362。结论 与高压均质法-超声法相比,高压均质法-挤出法制备的空白脂质体粒径较小、分布均匀、稳定性好。
非PEG空白脂质体;高压均质法;挤出法;超声法
脂质体由于具有天然靶向性,其作为药物载体又具有长效作用、不良反应低的特点,因此脂质体作为药物载体用于临床具有非常重大的意义,并具有非常广阔的前景。但目前大部分脂质体,如:里葆多,DOXIL, CAELYX 和LIPODOX都是采用stealth 技术的长循环脂质体,有和载体辅料(PEG)相关的毒性[1]。而非PEG脂质体可避免大剂量使用时手足综合征等皮肤毒性的产生。常用的脂质体的制备方法众多,如:薄膜分散法、超声法、冷冻干燥法、注入法等。而高压均质法[2]制备的脂质体可大规模生产且重现性好,挤出法[3]制备的脂质体具有粒径分布均匀、稳定性好等优点。本实验采用高压均质法-挤出法联用的方法制备非PEG空白脂质体,并对高压均质法-挤出法并与高压均质法-超声法制备的空白脂质体进行了对比,此类研究国内外相关报道较少。
1 材料与方法
1.1 试剂与药品 蛋黄卵磷脂EPC(德国Lipoid 公司);胆固醇CHOL(德国Lipoid 公司);无水乙醇(莱阳经济技术开发区精细化工厂);一水合柠檬酸(天津市风船化学试剂科技有限公司)
1.2 仪器 FB224自动内校电子分析天平(上海舜宇恒平科学仪器有限公司);pH 计[梅特勒-托利多仪器(上海)有限公司];0.22 μm滤膜(上海市新亚净化器件厂);一次性注射器(常州悦康医疗器材有限公司);Mini-extruder(Avanti);100 nm聚碳酸酯膜(Avanti);水浴锅(金坛市科析仪器有限公司);控温磁力搅拌器(SZCL-4D恒温加热磁力搅拌器);D-3L型高压均质机(美国PhD科技有限公司);透析袋MD18(截留分子量1000,美国Spectrum公司);Zetasizer nano ZSP纳米粒度仪(英国马尔文仪器有限公司)
1.3 方法
1.3.1 相关溶液的配制:配制0.3M,pH 4.0的柠檬酸溶液;并用0.22 μm滤膜过滤除菌,保存于4 ℃冰箱中备用。
1.3.2 空白脂质体的制备:蛋黄卵磷脂,胆固醇按摩尔比3:1在55 ℃水浴条件下溶于少量无水乙醇;0.3 M,pH 4.0的柠檬酸溶液于圆底烧瓶中55 ℃加热、转速30 r/ min 磁力搅拌下,用一次性注射器将上述油相缓慢注入柠檬酸溶液中,并继续搅拌30 min,得到脂质体混悬液[4]。将上述脂质体混悬液经高压均质机在15 000 psi压力下循环匀质30 min。再将均质后的脂质体溶液通过挤出器(双层100 nm聚碳酸酯膜)反复多次挤出[5-6]或者在冰浴条件下进行超声[7-9]。最后,用10倍体积的0.3 M,pH 4.0的柠檬酸溶液透析除去乙醇,即得到空白脂质体。
1.3.3 空白脂质体的稳定性研究:将空白脂质体静置于4 ℃冷藏、25 ℃室温条件下,于0、1、7、15、30、60 d分别取样进行外观观察并测量其粒径、Zeta电位,取平均值[10]。
1.3.4 空白脂质体粒径、Zeta电位的测定:取空白脂质体,加入适量MiliQ水稀释后,用Zetasizer nano ZSP纳米粒度仪测定其粒径及粒径分布、Zeta电位,取平均值。
2 结果
2.1 高压均质法-挤出法制备空白脂质体
2.1.1 高压均质时间对空白脂质体粒径的影响:实验结果表明:随着均质时间的延长,空白脂质体粒径逐渐减小(见表1)。由于随着均质时间的延长,空白脂质体混悬液温度会随之上升;当均质时间为30 min时,混悬液温度已有所升高。为此,从空白脂质体的稳定性角度考虑,最终选择空白脂质体的高压均质时间为30 min。
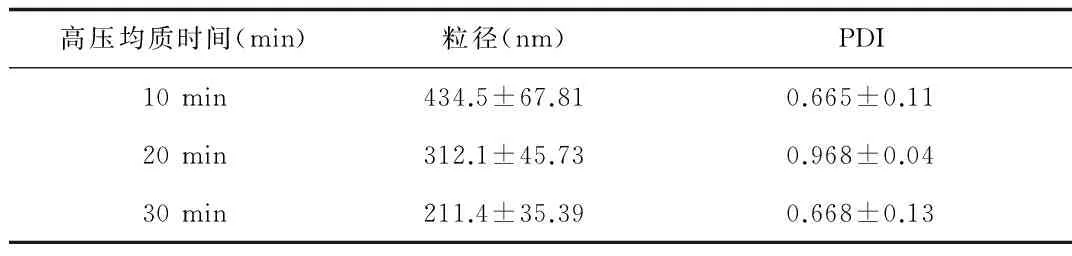
表1 高压均质时间对空白脂质体粒径的影响(n=3)Tab.1 How high pressure homogeneous time influences particle size of blank liposomes(n=3)
2.1.2 挤出次数对空白脂质体粒径的影响:实验结果表明:在一定范围(0~50次)内,随着挤出次数的增加,空白脂质体粒径(Z-Average)逐渐减小;当挤出次数超过50次时,空白脂质体的粒径(Z-Average)不再减小而是出现了平台期(见表2)。因此,最终选择的挤出次数为50次。
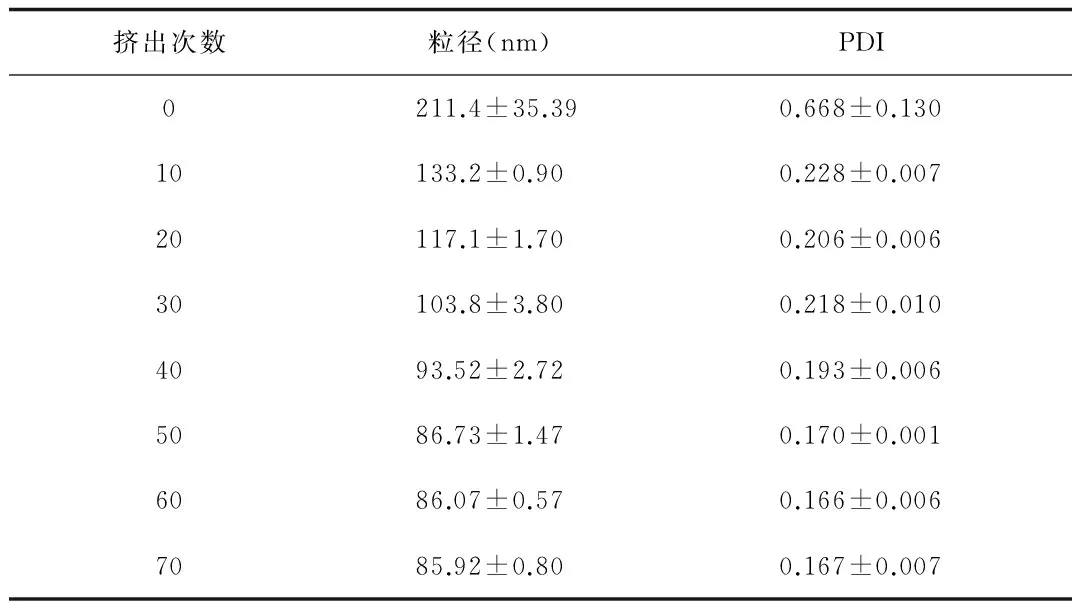
表2 挤出次数对空白脂质体粒径的影响(n=3)Tab.2 How extrusion times influence particle size of blank liposomes(n=3)
2.1.3 高压均质法-挤出法制备空白脂质体的粒径:空白脂质体初乳经过高压均质(时间30 min)、挤出(挤出次数50次),最终得到粒径(Z-Average)86.73 nm的空白脂质体,PDI为0.170。
2.2 高压均质法-超声法制备的空白脂质体
2.2.1 超声时间对空白脂质体粒径的影响:实验结果表明:超声功率功率固定时,在一定范围(0~6 min)内,随着超声时间的延长,空白脂质体粒径(Z-Average)逐渐减小;当超声时间超过6 min时,空白脂质体粒径(Z-Average)不再减小反而增加(见表3)。

表3 超声时间对空白脂质体粒径的影响(n=3)Tab.3 How ultrasonic time influences particle size of blank liposomes(n=3)
2.2.2 超声功率对空白脂质体粒径的影响:实验结果表明:超声时间固定时,在一定范围(0~200 W)内,随着超声功率的增大,空白脂质体粒径(Z-Average)逐渐减小;当超声功率超过200 W时,空白脂质体粒径(Z-Average)不再减小反而增加(见表4)。
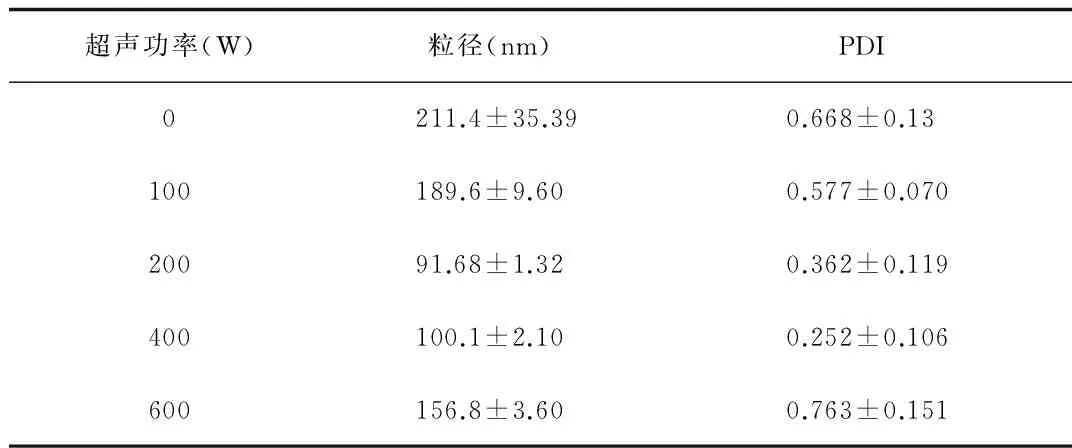
表4 超声功率对空白脂质体粒径的影响(n=3)Tab.4 How ultrasonic power influences particle size of blank liposomes(n=3)
2.2.3 高压均质法-超声法制备空白脂质体的粒径:空白脂质体初乳经过高压均质(时间30 min)、超声(功率200 W,时间6 min),最终得到粒径(Z-Average)91.68 nm的空白脂质体,PDI为0.362。
2.3 2种制备空白脂质体方法的比较 通过表2和表3中空白脂质体的粒径大小及其PDI可以看出:与高压均质法-超声法制备的空白脂质体相比,高压均质法-挤出法制备的空白脂质体粒径更小、分布均匀。因此,在后续制备过程中多采用高压均质法-挤出法来制备空白脂质体,高压均质时间为30 min、挤出次数为50次。
2.4 空白脂质体的稳定性研究 实验结果表明,在考察时间范围内,高压均质法-挤出法制备的空白脂质体在4 ℃冷藏条件下保持稳定,稳定性考察结果见表5。
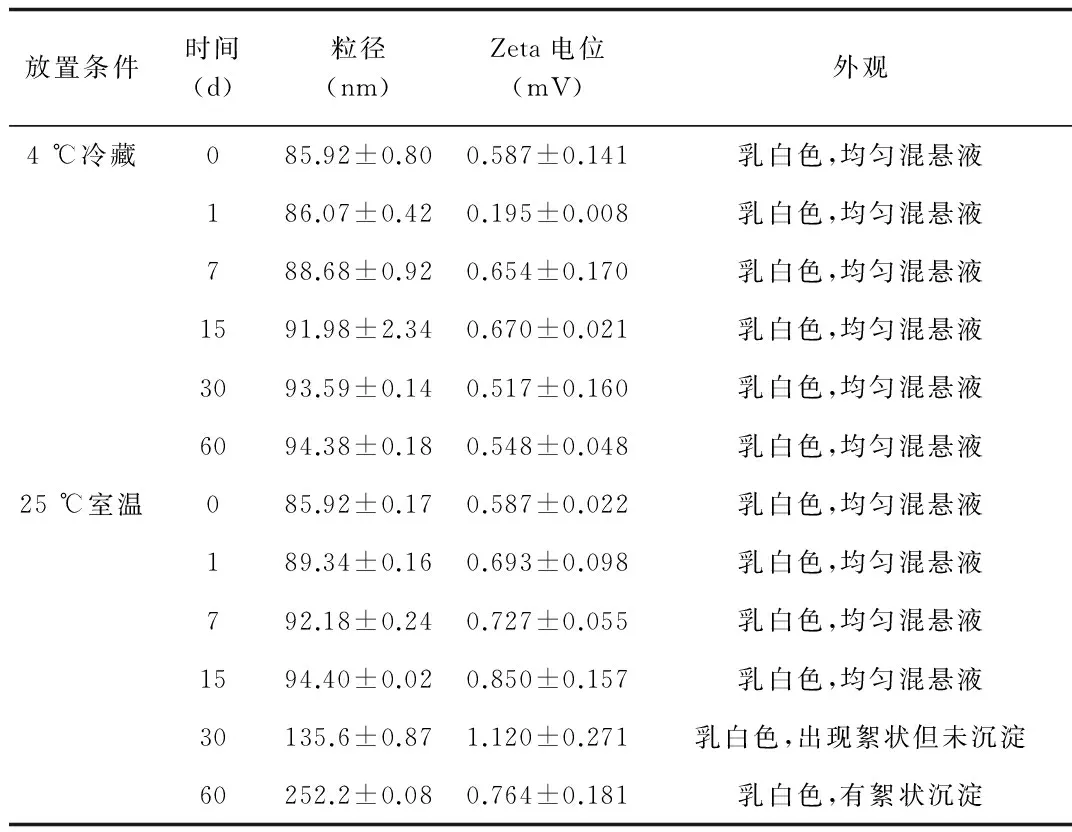
表5 空白脂质体稳定性考察结果(n=3)Tab.5 Results of stability experiment of blank liposomes (n=3)
3 讨论
以空白脂质体为药物载体包埋水溶性药物而形成的载药脂质体, 与其他制备方法比较,具有操作简单、载药量高、适用于多种水溶性药物载药脂质体的制备等优点。本研究采用高压均质法-挤出法(高压均质时间为30 min、挤出次数为50次)制备的空白脂质体粒径86.73 nm、PDI为0.170;并且在4 ℃冷藏条件下储存60d,粒径、Zeta电位及外观均无明显变化。由此可见,高压均质法-挤出法联用制备的空白脂质体不但具有可大规模生产、重现性好、粒径分布均匀、稳定性好等优点,而且在制备过程中未使用PEG、Tween 80等表面活性剂,从而避免了大剂量使用时手足综合征等皮肤毒性的产生。因此,高压均质法-挤出法联用制备非PEG空白脂质体的技术是对脂质体剂型的优化改进,这样就可既保证了其无PEG毒性,又可方便用于医疗,具有非常广阔的应用前景。
[1] Schmid P, Krocker J, Kreienberg R, et al.Non-pegylated liposomal doxorubicin and docetaxel in metastatic breast cancer: final results of a phase II trial [J].Cancer Chemother Pharmacol, 2009, 64(2): 401-406.
[2] 周本宏,吴燕,何文,等.羟基喜树碱包衣纳米脂质体的制备及体外释药研究[J].中国药师, 2005, 8(4): 270-273.
[3] 王九成,惠民权,焦亚奇,等.三瓶装阿霉素脂质体注射液制剂研究[J].世界最新医学信息文摘, 2003, 2(4): 746-749.
[4] Tardi PG1, Boman NL, Cullis PR.Liposomal doxorubicin[J].J Drug Target.1996, 4(3): 129-140.
[5] Abraham SA, Waterhouse DN, Mayer LD, et al.The liposomal formulation of doxorubicin.[J].Methods Enzymol, 2005, 391(391): 71-97.
[6] Miller CR, Perry A.Glioblastoma[J].Arch Pathol Lab Med,2007,131(3):397-406.
[7] 陈浩,戴俊东,王玉蓉,等.薄膜超声法制备槲皮素脂质体研究[J].药学实践杂志,2012,30(1):32-34.
[8] 田菊霞,解宇,杨艳宏.薄膜分散-超声法制备BMPs磁性脂质体[J].健康研究,2012,32(1):1-3.
[9] 邓璇,梁兰,高漫路,等.薄膜分散—探头超声法制备HV12p-rPA脂质体初探[A]//中国药学会(Chinese Pharmaceutical Association)、天津市人民政府.2010年中国药学大会暨第十届中国药师周论文集[C],2010:6.
[10] 危丽雯.盐酸阿霉素纳米脂质体的制备及体外抗肿瘤研究[D].湖南:中南大学,2011.
(编校:谭玲)
Preparation and properties of drug carrier non-PEG blank liposomes
YUAN Meng-juan, HAN JunΔ
(Department of Pharmacy, Liaocheng University, Liaocheng 252059, China)
ObjectiveTo prepare drug carrier non-PEG blank liposomes, and study its properties.MethodsHigh purity of egg yolk lecithin and cholesterol were used as film forming material.The high pressure homogeneous method-extrusion method and high pressure homogeneous method-ultrasonic method were used to prepare non-PEG blank liposomes.After that how the method of high pressure homogeneous, extrusion and ultrasonic influence the particle size of blank liposomes were studied, and the physical stability of blank liposomes were investigated.ResultsThe particle size of blank liposomes prepared by high pressure homogeneous method-extrusion method was about 86 nm, and its polydispersity index was 0.170.While the particle size of the blank liposomes prepared by high pressure homogeneous method-ultrasonic method was about 91 nm, and its polydispersity index was 0.362.ConclusionCompared with high pressure homogeneous method- ultrasonic method, the blank liposomes prepared by high pressure homogeneous method-extrusion method had some advantanges, such as smaller particle size, narrow particle size distribution and high stability.
non-PEG blank liposomes; high pressure homogeneous method; extrusion method; ultrasonic method
山东省科技发展计划项目(2014GSF118121);聊城市科技发展计划项目(2013GJH16)
袁孟娟,女,硕士,研究方向:药物制剂研究,E-mail: yuanmengjuan1990@163.com;韩军,通讯作者,男,博士,教授,研究方向:药物制剂研究,E-mail: junhanmail@163.com。
R94
A
1005-1678(2015)07-0022-03

