一种水溶性探针的合成及对双氧水的比色荧光检测
邓燕, 文思雨, 皮毅兵, 蒋倩婷, 梁敏, 刘亮亮, 郭雨芳, 严奉梅, 张春香, 申有名,郑清云, 张向阳
一种水溶性探针的合成及对双氧水的比色荧光检测
邓燕, 文思雨, 皮毅兵, 蒋倩婷, 梁敏, 刘亮亮, 郭雨芳, 严奉梅, 张春香, 申有名,郑清云, 张向阳
(湖南文理学院 化学化工学院, 湖南 常德, 415000)
以4-溴-1, 8-萘二甲酸酐为原料, 经过Suzuki偶联反应、氨解反应, 合成了一种水溶性的荧光探针, 其结构经过1H NMR、MS进行了表征。利用荧光光谱、紫外光谱探讨了该探针对双氧水响应的性能。结果表明,该探针在纯水中对双氧水具有高选择性、高灵敏性, 双氧水浓度在 3.3×10-8~1×10-4mol/L范围内探针对双氧水具有较好的线性, 检测下限为0.1 μg/mol。
荧光探针; 双氧水; 比色; 合成
1 实验
1.1 仪器与试剂
核磁共振分析采用Bruker AVB-500测定, 质谱采用Agilent1100型液质联用仪测定, 紫外光谱吸光度采用UV2500测定, 荧光光谱强度采用FL-7000荧光光谱仪测定。化合物1按照文献[16]的方法合成, 其它试剂均为分析纯。
1.2 化合物2的合成
向100 mL单口瓶中加入化合物1 (0.32 g, 1 mmol)、6-氨基正己酸(0.26 g, 2 mmol)和无水乙醇(5 mL), 氮气保护下, 加热搅拌回流12 h。TLC(薄层色谱)跟踪反应进程, 反应完毕, 冷却至常温, 旋转蒸发仪除去溶剂, 粗品柱层析分离(V二氯甲烷∶V甲醇= 20∶1)得到白色固体化合物2 (0.41 g, 产率93%)。化合物2的核磁表征1H NMR (500 MHz, CDCl3) δ (ppm): 9.10 (d, J = 8.5 Hz,1H), 8.59 (d, J = 7.0 Hz,1H),8.55 (d, J =7.0 Hz, 1H), 8.28 (d, J = 7.0 Hz,1H), 7.76 (d, J = 8.5 Hz,1H), 4.18 (t, J = 7.5 Hz,2H), 2.38 (t, J = 7.5 Hz,2H), 1.71-1.78 (m,4H), 1.47- 1.52 (m,2H), 1.45 (s,12H);13C NMR (125 MHz, CDCl3) δ (ppm):178.3, 164.3, 164.3, 135.8, 135.3, 135.0, 131.3, 131.0, 129.9, 127.9,127.1, 127.0, 124.7, 84.6, 40.2, 33.7,27.7, 26.6, 25.0, 24.4; ESI-MS calcd for C24H28BNO6[M + 1]+ 438.293 2, found 438.208 2。化合物2的具体合成路线如图1所示, 其1H NMR谱图、13C NMR谱图和质谱图分别见图2、3和4。

图1 化合物2的合成路线
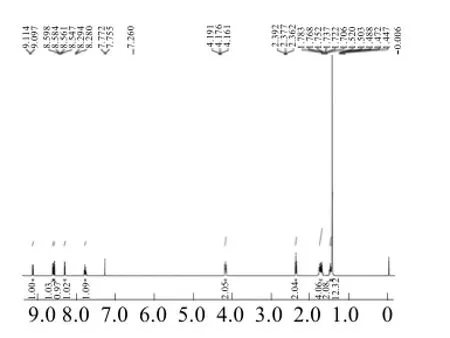
图2 化合物2的1H NMR谱图
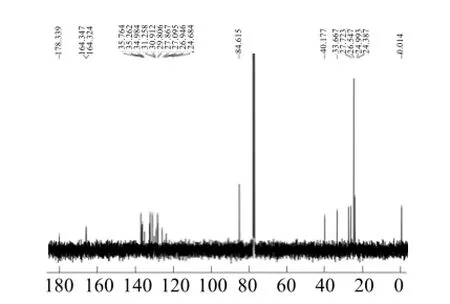
图3 化合物2的13C NMR谱图
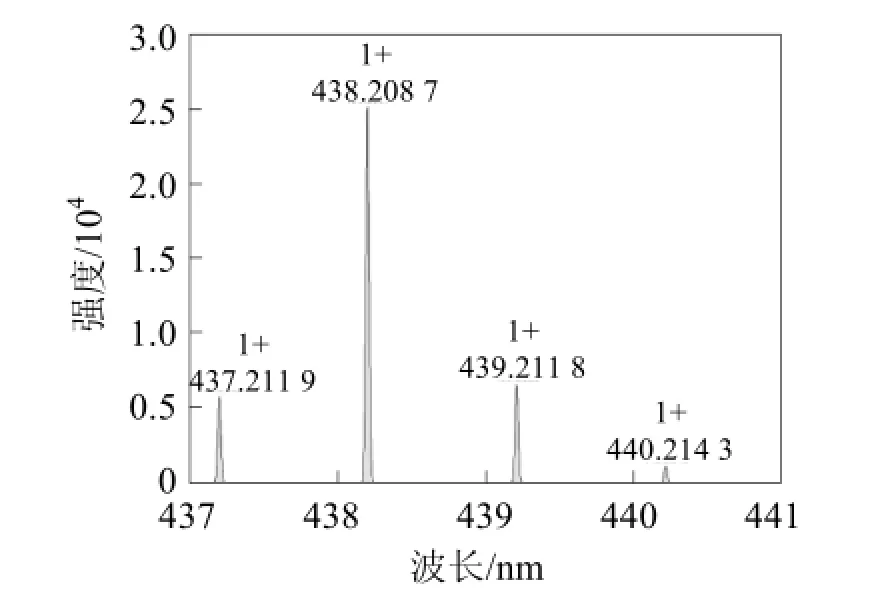
图4 化合物2的质谱谱图
1.3测试过程
准确称取NaH2PO4·2H2O 0.39 g, Na2HPO4·12H2O 3.58 g和NaCl 0.73 g置于250 mL烧杯中, 然后溶解调节pH值, 最后定容至250 mL容量瓶, 得到50 mg/mol pH值为7.4的PBS缓冲溶液。
准确称取一定量的化合物2, 将其溶于PBS缓冲溶液(50 mg/mol, pH值为7.4)中配成200 μg/mol的母液待用。然后将 PBS缓冲溶液配成不同浓度的探针溶液。将事先准备好的双氧水加入到探针溶液中, 混合均匀, 在室温下进行测试。以468 nm为激发波长, 激发光狭缝宽度10 nm, 发射光狭缝宽度10 nm, 根据化合物2在445 nm激发下的荧光强度来定量分析双氧水。
2 结果与讨论
2.1化合物2的光谱性质
2.1.1紫外光谱
图5记录的是探针1 (5 μg/mol)在室温条件下,加入双氧水前后的紫外光谱图。由图 5可看出, 在双氧水加入前, 探针1在350 nm时吸光度最大, 加入双氧水之后, 紫外光谱在 445 nm有一个新的吸收峰出现, 探针溶液的颜色由无色变成了黄色。探针 1在加入双氧水前后的紫外吸收红移了 95 nm,这可能是由于化合物2中的硼酸酯与双氧水发生了反应, 化合物2分子中出现了分子内电荷转移(ICT)引起的。
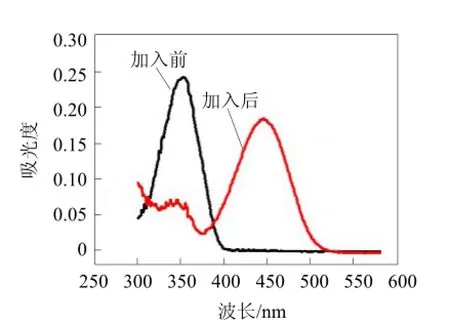
图5 化合物1中加入双氧水前后的紫外光谱图
2.1.2荧光光谱
图6是化合物2的荧光强度随双氧水浓度变化的荧光图。从图 6可以看出, 化合物 2本身在 557 nm处只有微弱的荧光。加入H2O2后, 在557 nm处荧光强度随着双氧水浓度的增大而增强。这表明,双氧水能够与化合物 2发生反应, 其对双氧水浓度检测范围为3.3 × 10-8~1.0 × 10-4mol/L, 检测下限为0.1 μg/mol。
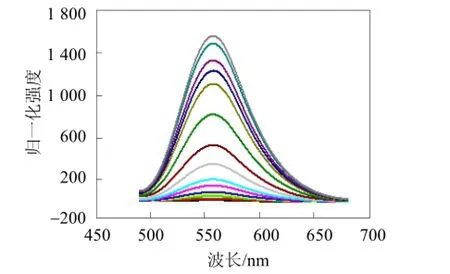
图6 化合物2的荧光强度与双氧水浓度的变化关系
2.1.3选择性考察
为了研究探针在模拟生理条件(pH值为 7.4)对双氧水具有高度的选择性。用化合物2分别对一系列的活性氧、活性氮物质如O2-, OH,1O2, ONOO-,NO, ClO-, H2O2,tBuOOH进行检测。如图 7所示,化合物 2对双氧水有明显响应, 而其他分析物与化合物 2没有响应。这表明, 探针对双氧水具有高度的选择性, 不会受其他物质干扰, 因此, 探针可以检测生物环境中的双氧水。

图7 化合物2对双氧水的选择性
2.1.4pH值考察
为了研究 pH值对反应的影响, 考察了加入双氧水后探针在不同 pH值溶液中的荧光性质。如图8所示, 当加入双氧水后, 化合物 2的荧光强度随pH值的变化而变化。结果表明, 化合物2可以在生理pH值条件下检测双氧水。
2.1.5时间考察
反应时间也是影响反应体系的一个非常重要的因素, 因此考察了在双氧水存在下化合物 2随时间变化的荧光光谱(图9)。图9表明, 化合物2的荧光强度会随着时间的推移而增强, 在40 min时荧光强度增强到最大值, 然后基本保持不变。因此, 探针能够很好地实时检测双氧水。

图8 pH值对化合物2的影响

图9 化合物2中加入双氧水后荧光强度随时间的变化
3 结论
本文设计合成了一种新型用于双氧水检测的硼酸酯荧光探针, 利用荧光光谱和紫外光谱研究了其对双氧水响应的性能。实验结果表明, 该探针能够选择性检测双氧水, 探针随着双氧水浓度的增大荧光强度逐渐增强, 且在实现荧光增强检测双氧水的同时还能实现比色检测。因此, 该方法给双氧水的检测提供了新的思路。
[1] Hachem C, Bocquillon F, Zahraa O, et al. Decolourization of textile industry wastewater by the photocatalytic degradation process [J]. Dyes Pigm, 2001, 49: 117-125.
[2] Balaban R S, Nemoto S, Finkel T. Mitochondria, oxidants, and aging [J]. Cell, 2005, 120: 483-495.
[3] Rhee S G. H2O2, a necessary evil for cell signaling [J]. Science, 2006, 312: 1 882-1 883.
[4] Lin M T, Beal M F. Mitochondrial dysfunction and oxidative stress in neurodegenerative diseases [J]. Nature, 2006, 443:787-795.
[5] Mattson M P. Pathways towards and away from Alzheimer’s disease [J]. Nature, 2004, 430: 631-639.
[6] Ohshima H, Tatemichi M, Sawa T. Arch Chemical basis of inflammation-induced carcinogenesis [J]. Biochem Biophys,2003, 417: 3-11.
[7] Klassen N V, Marchington D, McGowan H C E. H2O2determination by the 13 method and by KMnO4titration [J]. Anal Chem, 1994, 66: 2 921-2 925.
[8] Xu M, Bunes B R, Zang L. Paper-based vapor detection of hydrogen peroxide: colorimetric sensing with tunable interface [J]. ACS Appl Mater Interfaces, 2011, 3: 642-647.
[9] Yuan P X, Zhuo Y, Chai Y Q, et al. Dendritic silver/silicon dioxide nanocomposite modified electrodes for electrochemical sensing of hydrogen peroxide [J]. Electroanalysis, 2008, 20: 1 839-1 844.
[10] Shan G, Zheng S, Chen S P, et al. Detection of label-free H2O2based on sensitive Au nanorods as sensor [J]. Colloids Surf B, 2013, 102: 327-330.
[11] Shu X H, Chen Y, Yuan H Y, et al. H2O2Sensor based on the room-temperature phosphorescence of nano TiO2/SiO2composite [J]. Anal Chem, 2007, 79: 3 695-3 702.
[12] Qian Y Y, Xue L, Hu D X, et al. Quinoline-based fluorescent probe for ratiometric detection of hydrogen peroxide in aqueous solution [J]. Dyes and Pigments, 2012, 9: 373-376.
[13] Xu J, Li Q, Yue Y, et al. A water-soluble BODIPY derivative as a highly selective “Turn-On” fluorescent sensor for H2O2sensing in vivo [J]. Biosensors and Bioelectronics, 2014, 56: 58-63.
[14] Sun X L, Xu S Y, Flower S E, et al. “Integrated” and “insulated” boronate-based fluorescent probes for the detection of hydrogen peroxide [J]. Chem Commun, 2013, 49: 8 311-8 313.
[15] Yu F B, Li P, Song P, et al. Facilitative functionalization of cyanine dye by an on-off-on fluorescent switch for imaging of H2O2oxidative stress and thiols reducing repair in cells and tissues [J]. Chem Commun, 2012, 48: 4 980-4 982.
(责任编校: 刘晓霞)
Synthesis of a water solution probe and fluorescence and colorimetric sensor for detection of H2O2
Deng Yan, Wen Siyu, Pi Yibing, Jiang Qianting, Liang Ming, Liu Liangliang, Guo Yufang, Yan Fengmei, Zhang Chunxiang, Shen Youming, Zheng Qingyu, Zhang Xiangyang
(Department of Chemistry and Chemical Engineering, Hunan University of Arts and Science, Changde 415000,China)
A water solution fluorescent probe is synthesized via Suzuki coupling reaction, oxidative reaction,ammonolysis reaction from 4-bromo-1, 8-naphthalic anhydride. Its structure is characterized by1H NMR and MS. The spectroscopic properties, the target probe with H2O2is investigated by the fluorescence spectrum and ultraviolet spectrum. The results show that the probe can detect H2O2.The compound displays off/on ratio singles,highly selective and sensitive towards H2O2in 100% water. The fluorescence intensity is proportional to the concentration of glucose over a range of 3.3 × 10-8~1 × 10-4mol/L, with a limit of detection of 0.1 μg/mol.
fluorescent probe; H2O2; colorimetric; synthesis
O 657.3
1672-6146(2016)03-0006-04
10.3969/j.issn.1672-6146.2016.03.002
张春香, cxzhang81@163.com; 申有名, ymshen79@163.com。
2016-03-17
湖南省教育厅一般项目(15C0954); 湖南文理学院科学研究项目(14YB05); 湖南文理学院大学生创新项目; 湖南省十二五重点建设学科——应用化学资助。不利于应用[14-15]。因此, 研制一种快速、简单、水溶性高以及对双氧水响应的荧光探针是十分必要的。本实验合成了一种简单的、水溶性荧光探针, 该探针在双氧水的存在下可以实现比色和荧光增强检测, 相对单一的荧光探针, 比色、荧光增强双通道荧光探针能够有效、简单、方便地检测生物体内活性物质。
双氧水参与细胞生长调节、重要物质的合成和代谢、能量转化及细胞内信号转导[1-4], 但其浓度过大又会对体内的蛋白质、核酸等产生不同程度的损伤, 导致一些疾病[5-6]。因此, 准确及时地检测双氧水对一些疾病的预防和诊断具有重要的意义。目前, 对双氧水的检测方法比较多, 如滴定法[7]、比色法[8]、电化学法[9]、博层色谱法[10]以及荧光分析法[11]等。在这些检测方法中, 荧光探针检测法由于在物质的检测中可达到单分子检测的高灵敏度, 所以能够实现开关操作以及人与分子的直接通讯, 对亚微粒具有可视的亚纳米空间分辨能力和亚毫秒时间分辨能力。作为一种灵敏度高、选择性好、检出限低的微量分析技术, 荧光探针还可以对单(多)种对象进行实时、在线检测, 克服了传统环境检测分析手段样品预处理过程繁琐冗长、成本高、不能实时在线分析的缺点, 因而受到科学家的广泛关注[12-13]。然而, 已报道的荧光探针对双氧水的检测大多存在反应时间长、合成过程复杂以及低水溶性等问题,

