类风湿性关节炎患者Th17/Treg及其相关细胞因子的研究
何 媛(九江学院附属医院检验科,江西 九江 332000)
类风湿性关节炎患者Th17/Treg及其相关细胞因子的研究
何 媛(九江学院附属医院检验科,江西 九江 332000)
目的 探讨外周血辅助性T细胞17(Th17)与调节性T细胞(Treg)及血清中相关细胞因子白介素-17(IL-17)、白介素-6(IL-6)和转化生长因子β1(TGF-β1)在类风湿性关节炎(RA)中的作用。方法选取71例RA患者(RA组)和40例健康受试者(对照组),其中RA患者按照疾病活动度DAS28积分分为低度(2.6
类风湿性关节炎; 辅助性T细胞17; 调节性T细胞; 白介素-17; 白介素-6; 转化生长因子β1
类风湿性关节炎(RA)是一种系统性的自身免疫性疾病。主要临床表现为对称性多关节炎、大小关节滑膜的炎性反应、伴或不伴晨僵,具有较高的发病率和致残率。RA病因和发病机制目前并不非常清楚,调节性T细胞(Treg)和辅助性T细胞(主要是Th17细胞)免疫调节异常在其发病机制中的作用成为研究热点。本研究通过分析Th17、Treg及相关细胞因子在RA患者中的变化,探讨两者在RA发病中的作用。
1 对象与方法
1.1 研究对象
选自2013年3月至2015年12月九江学院附属医院风湿免疫科住院的RA患者71例(RA组),其中男20例,女51例,年龄29~82岁,平均(52.5±11.5)岁,均符合美国风湿病学会2009年ACR/EULAR的诊断标准[1],并排除心、肾、肺、肝等器质性疾病和糖尿病、高血压病、各种肿瘤、炎症和其他一些自身免疫性疾病。RA患者按照疾病活动度DAS28积分进行分组,分为低度(2.6
1.2 仪器与试剂
1.2.1 仪器
BD FACSCanto Ⅱ流式细胞仪(美国BD公司生产),ST-360洗板机和酶标仪(均为上海科华实验系统有限公司生产)。
1.2.2 主要试剂
CD3-FITC、CD4-PC5、PE-IL-17、CD4-FITC、CD25-PC5及固定破膜剂购自美国BD公司,白介素-17(IL-17)、白介素-6(IL-6)、转化生长因子β1(TGF-β1)酶联试剂为美国GBD公司产品。
1.3 方法
1.3.1 标本的采集
所有待测者清晨空腹抽静脉血3 mL,血液凝固后在抽血当日于3000 r·min-1离心5 min,取出血清-80 ℃保存,用于检测IL-17、IL-6、TGF-β1;另取空腹抗凝静脉血2 mL,抗凝剂为EDTA-K2,用于检测Th17和Treg。
1.3.2 检测方法
1)Th17细胞和Treg细胞的流式检测:分离出外周血单核细胞,在分离好的单核细胞及对照组中加入CD3和CD4的酶标抗体进行表面标记,用于Th17细胞的标记;同时取外周全血200 μL及对照组加入CD4和CD25的单抗,混匀避光孵育20 min。孵育好的全血样本PBS洗涤后,进行固定破膜。最后加入酶标Foxp3抗体进行细胞内细胞因子标记,对照管加入FoxP3对照抗体,孵育30 min。而孵育后的PBMCs标本用RPMI-1640培养液洗涤,并加入到特殊培养液中(含新生牛血清、刺激剂、莫能霉素和离子霉素),放入37 ℃温箱孵育18~20 h。培养后的细胞及对照组同样进行固定破膜之后加入酶标IL-17抗体和对照抗体,孵育30 min 后PBS洗涤。最后,应用流式细胞仪测定标记细胞的荧光强度,采用BD Cell Quest软件分析测定Th17/Treg的比值。
2)IL-17、IL-6、TGF-β1的检测:采用酶联免疫吸附法(ELISA法),严格按照说明书进行操作,并绘制标准曲线,计算出浓度。
1.4 统计学方法
数据分析应用SPSS18.0统计软件,对不符合正态分布的计量资料,经LG10对数转换成正态分布,组间比较采用t检验。相关系数采用Spearman秩相关性检验分析,P<0.05为差异有统计学意义。
2 结果
2.1 各组外周血Th17、Treg占CD4+T细胞比例的比较
和对照组相比,RA组患者外周血Th17占CD4+T细胞比例和Th17/Treg比值均升高,外周血Treg占CD4+T细胞比例下降(均P<0.05);RA组患者外周血Th17占CD4+T细胞比例和Th17/Treg比值:高度活动期RA组>中度活动期RA组>低度活动期RA组(均P<0.05)。RA患者外周血Treg占CD4+T细胞比例:高度活动期RA组<中度活动期RA组<低度活动期RA组(均P<0.05),见表1。
2.2 各组血清细胞因子的比较
和对照组相比,RA患者血清IL-17、IL-6水平均升高,血清TGF-β1水平降低 (均P<0.05)。RA组患者血清IL-17、IL-6水平:高度活动期RA组>中度活动期RA组>低度活动期RA组;血清TGF-β1水平:高度活动期RA组<中度活动期RA组<低度活动期RA组(均P<0.05)。见表2。
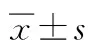
表1 各组外周血Th17、Treg占CD4+T细胞比例的比较
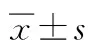
表2 各组血清细胞因子的比较
2.3 各指标与DAS28的相关性分析
Th17、IL-17、Th17/Treg、IL-6与DAS28积分均呈正相关(r=0.701、0.632、0.439、0.516,均P<0.05),Treg、TGF-β1与DAS28积分均呈负相关(r=-0.436、-0.388,均P<0.05)。
3 讨论
RA的发病与免疫复合物形成和炎性细胞浸润有关,属于一种自身免疫性疾病。Th17细胞是CD4+T细胞亚群,属于辅助性T细胞,可分泌IL-17、IL-22、IL-21、IL-6等多种相关细胞因子,具有介导炎症反应的功能[2-3]。而IL-17是Th17分泌的最主要细胞因子,可通过介导中性粒细胞促进前炎症反应,诱导趋化因子、促炎细胞因子(如IL-6、TNF)和基质金属蛋白酶的表达,引起组织细胞侵润与破坏。IL-17可存在于RA患者的血清和关节液中,有报道[4]说RA患者滑膜液中IL-17表达与疾病的进展和严重性相关。周洁如等[5]研究发现,和健康对照组相比,未经治疗的活动期RA患者外周血Th17细胞数量升高。本研究发现,RA患者外周血Th17占CD4+T细胞比例和血清IL-17水平高于对照组,DAS28得分高组,两指标亦高于得分低组,同时Th17百分数和IL-17均与DAS28得分呈正相关(r=0.701、0.632,P<0.05)。提示Th17细胞参与了RA疾病的发生和发展。
Treg是一类具有免疫抑制功能的T细胞亚群,可阻止自身免疫性疾病产生,此外,可限制免疫防御中T、B细胞过度活化,避免组织损伤[6]。Treg细胞的功能缺陷或数量减少,可导致多种自身免疫性疾病。在本研究中,RA组Treg的百分数比对照组低,这与赵俊桃[7]的研究相符。本研究还发现处于活动性越强的RA患者Treg百分数比活动性较弱的RA患者更低,Treg百分数与DAS28得分呈显著的负相关(r=-0.436,P<0.05)。提示Treg与RA的病程发展相关,可通过检测外周血Treg的数量来监测RA疾病活动性和严重性。
Th17可介导促炎反应并促进自身免疫性疾病发生,但Treg具有抗炎反应和维持机体自身免疫耐受的功能。两者只有维持动态平衡,才能保证机体处于免疫稳态。在多种自身免疫性疾病中,Th17/Treg失衡发挥了重要作用[8]。本研究结果表明,和对照组相比,Th17/Treg比值升高,并且随着RA疾病活动性增强,比值增加也更明显,说明Th17/Treg失衡也更显著。Th17/Treg比值与DAS28得分呈正相关(r=0.439,P<0.05)。说明Th17/Treg失衡参与了RA的免疫应答过程,并且和RA疾病活动性相关。
IL-6生物活性广泛,可刺激B淋巴细胞合成自身抗体,并促进RF等其他细胞因子的合成,从而使关节软骨组织病变加重,加快炎症反应进程。有报道[9]称IL-6可预测早期RA患者持续性骨质破坏。TGF-β1作为一种多能细胞因子,具有拮抗炎症因子的致炎作用,抑制免疫反应。荆炳霞等[10]检测缓解期和活动期RA 2组患者的TGF-β1,发现这2组的TGF-β1水平比对照组要高,可帮助了解RA患者的病情。Th17细胞的启动和分化依赖于TGF-β1和IL-6,当机体处于无炎症损伤状态时,缺乏IL-6,单独存在的TGF-β1抑制效应T细胞增殖,诱导Treg细胞产生,从而维持机体免疫耐受功能。故Th17和Treg在TGF-β1和IL-6两者作用下,相互抑制。在本研究中,和对照组相比,RA组IL-6水平升高,TGF-β1水平下降。按照DAS28积分分组,IL-6水平变化为高度活动期RA组>中度活动期RA组>低度活动期RA组,而TGF-β1水平变化正好相反。与DAS28得分相关性分析显示,IL-6呈正相关,TGF-β1呈负相关。提示IL-6和TGF-β1参与RA疾病的活动。
综上所述,Th17、Treg的百分数异常和Th17/Treg的失衡,参与了RA的发生和疾病的活动,提示在RA发病机制中,CD4+细胞不同亚群功能紊乱发挥了重要作用。深入研究Th17相关细胞因子和Treg等CD4+细胞不同亚群之间的联系,有助于RA发病机制的阐明和疾病活动性的监测。
[1] 黄嘉,黄慈波.类风湿关节炎的诊断治疗进展[J].临床药物治疗杂志,2010,8(1):1-5.
[2] Zheng Y,Danilenko D M,Valdez P,et al.Interleukin-22,a T(H)17 cytokine, mediates IL-23-induced dermal inflammation and acanthosis[J].Nature,2007,445(7128):648-651.
[3] Nurieva R,Yang X O,Martinez G,et al.Essential autocrine regulation by IL-21 in the Generation of inflammatory T cel-ls[J].Nature,2007,448(7152):480-483.
[4] Miossec P.IL-17 and Th17 cells in human inflammatory diseases[J].Microbes Infect,2009,11(5):625-630.
[5] 周洁如,邓筠,李凝,等.青藤碱联合甲氨蝶呤对RA患者外周血Treg及Th17细胞的影响及其临床意义[J].现代免疫学,2013,33(1):46-50.
[6] Yasumi Y,Takikawa Y,Endo R,et al.Interleukin-17 as a new marker of severity of acute hepatic injury[J].Hepatol Res,2007,37(4):248-254.
[7] 赵俊桃.类风湿关节炎患者外周血Th17,Treg细胞及相关指标的变化[J].山东医药,2013,53(13):74-76.
[8] Noack M,Miossec P.Th17 and regulatory T cell balance in autoimmune and inflammatory diseases[J].Autoimmun Rev,2014,13(6):668-677.
[9] Saeki Y,Kudo Tanaka E,Ohshima S,et al.Baseline anti-citrullinated peptide antibody(ACPA) titers and serum interleukin-6 (IL-6) levels possibly predict progression of bone destruction in early stages of rheumatoid arthritis(ERA)[J]. Rheumatol Int,2013,33(2):451-456.
[10] 荆炳霞,朱静,张晓懿.RA患者血清TGF-β1、MMP-3、IL-18和CRP测定的临床意义[J].放射免疫学杂志,2013,26(2):137-140.
(责任编辑:钟荣梅)
2016-05-07
R593.22
A
1009-8194(2016)09-0017-03
10.13764/j.cnki.lcsy.2016.09.006

