穿心莲内酯衍生物的合成研究进展
骆瑜 邱慧 汪保林


[摘要]穿心莲内酯为爵床科植物穿心莲的重要天然活性成分之一,穿心莲内酯及其衍生物具有抗炎、抗病毒、抗肿瘤、抗HIV、保肝活性以及α葡萄糖苷酶抑制等活性,由于其广泛的药理活性而备受研究者关注。该文对穿心莲内酯衍生物的合成进行综述,并简述其相关的药理活性报道。
[关键词]穿心莲内酯; 衍生物; 合成
[Abstract]Andrographolide is one of the major natural active constituents in Andrographis panniculata of Acanthaceae family Andrographolide and its derivatives are proved to posses a wide range of biological activities, such as antiinflammatory, antiviral, antitumor, antihuman immunodeficiency virus(HIV), hepatoprotective and αglucosidase inhibition activity In this paper, the development of synthesis of rographolide derivatives and their related pharmacological activities were reviewed.
[Key words]andrographolide; derivatives; synthesis
穿心莲内酯(andrographolide),别名穿心莲乙素、雄茸内酯,为爵床科Acanthaceae植物穿心莲Andrographis paniculata(Burmf) Nees的主要二萜内酯类活性成分之一,临床上主要用于清热解毒、抗菌消炎,尤其是对上呼吸道感染的治疗疗效显著[1]。现代药理研究表明,穿心莲内酯及其衍生物具有抗炎[23]、抗病毒[4]、抗肿瘤[56]、抗HIV[78]、保肝活性[9]以及α葡萄糖苷酶抑制[1011]等活性,临床应用广泛且疗效显著,一直以来备受研究者关注。
穿心莲内酯结构中包含1个环外端烯键、3个羟基以及α,β不饱和γ丁内酯,这些官能团的构成特点为穿心莲内酯的结构修饰提供了多个有效的活性位点。本文主要从双键加成反应,酯化、氧化、还原、醚化反应以及分子内环化与内酯环替换3个方面介绍其衍生物合成研究进展。
1双键加成反应
20世纪70—80年代,秦国伟等[12]以穿心莲内酯或脱水穿心莲内酯为原料,通过与亚硫酸氢钠加成,在穿心莲内酯的C12位上引入亲水性基团,制成亚硫酸氢钠穿心莲内酯2a(图1)(莲必治注射液),临床试验表明其对上呼吸道感染等疾病具有良好的疗效。1981年,孟正木等[13]合成了3,19乙酰基12磺酸基脱水穿心莲内酯2b,三乙酰基穿心莲内酯3(图1)。之后,唐春山等公开专利水溶性穿心莲内酯磺化工艺,其相关临床产品为“喜炎平”,并对“喜炎平”的生产原料穿心莲内酯总硫酸酯化物进行了系统的化学研究,先后分离获得多个穿心莲内酯衍生物4~7(图1)[1416]。这种修饰与改造的目的主要有2个优势,一方面可以增加大分子多样性,引入更多基团,并探索这些基团对母核活性的影响;另一方面,将α,β不饱和内酯的双键由环外改为环内,使得分子相对稳定而药效延长。
a化合物2a [①乙酸,乙酸酐,硫酸乙酸(3∶5);②氯仿提取;③氢氧化钠,pH 65~70,95%乙醇],化合物2b乙酸酐,丙酮,乙醇石油醚重结晶;b乙酸酐,氯化锌,100 ℃,乙醇重结晶。
2005年,黄文龙课题组[1718]首次利用协同前药原理在结构中引入硝酸酯,旨在形成NO供体以产生抗癌活性,并合成了16个穿心莲内酯硝甲基衍生物8~20,并运用Michael加成原理合成了化合物20a和20b;随后又以化合物20a为反应中间体,合成了一系列N乙酰基12氨基亚甲基14脱氧穿心莲内酯衍生物21~22 (图2),并用MTT方法测定了目标化合物的抗肿瘤活性,结果显示化合物22c对人肝癌细胞SMMC7721的抑制百分率超过穿心莲内酯。2006年,Srinivasa等[19]的体外抗癌研究显示化合物8~10对MCF7(乳腺癌细胞系)及HCT116(结肠癌细胞系)具有一定的抑制作用,其中化合物8选择性的抑制白血病癌细胞和结肠癌细胞,化合物10可选择性的抑制白血病,乳房以及肾癌细胞的生长。不同的使用剂量及时间间隔下,化合物8和10在非特异性阶段对MCF7细胞生长具有周期阻滞作用。2007年,黄文龙课题组[20]继续以穿心莲内酯为原料,在无水甲醇中,经氯化氢气体醇解、酰胺化生成系列衍生物23~33(图3),并采用蛋白质印迹免疫分析法(Western blot)测试这些化合物对脂多糖诱导的小鼠巨噬细胞中COX2的表达抑制活性,结果表明化合物30,31,32a表现出与穿心莲内酯相当的抑制活性,其他化合物由于水溶性增強,不易进入细胞内而表现出较弱的抑制活性,该部分内容仍有待于进一步研究。
a2,2二甲氧基丙烷,4甲基苯磺酸吡啶鎓,二甲基亚砜,苯;b乙酸酐;c乙酸,水;d发烟硝酸,乙酸酐,二氯甲烷;e浓盐酸;f发烟硝酸,乙酸酐;g硼氢化钠,氯化镍六水合物,甲醇;h化合物20a硝基甲烷,甲醇钠,化合物20b (①硝基甲烷,甲醇钠,甲醇;②发烟硝酸,乙酸酐,二氯甲烷);i铁,乙酸酐,乙酸;jRCOOH,N,N′二环己基碳二亚胺,4二甲氨基吡啶。
a浓盐酸;b盐酸(气态),无水甲醇;c氨,甲醇;d硼氢化钠;氯化镍六水合物,甲醇;eNH2R,甲醇;f丁胺,N,N′二基甲酰胺;g2,2′二甲氧基丙烷,二氯甲烷,对甲苯磺酸吡啶鎓。endprint
骆瑜等:穿心莲内酯衍生物的合成研究进展
关于穿心莲内酯C12C13位双键的加成,Mondal等[2123]利用靛红衍生物或二氧化苊与肌氨酸、N苄基甘氨酸或脯氨酸作为反应底物,与穿心莲内酯结构中的C12C13位双键发生1,3偶极环加成反应得到一系列具有双螺结构的穿心莲内酯衍生物34~36(图4)。进一步药理活性研究表明,化合物35e~35g在部分癌细胞中的细胞毒活性强于穿心莲内
酯,其中又以衍生物35f的活性最强,拥有着与穿心莲内酯相似的抗癌机理,如ROS依赖的线粒体途径。 这一合成与活性研究具有十分重要的意义,不仅在很大程度上丰富了穿心莲内酯衍生物的合成设计思路,且极具合成价值,有望进一步开发成为新的极具抗癌活性价值的先导化合物。
2酯化,氧化,还原,醚化反应
1978年,我国四川省中药研究所药化室穿心莲研究组[24]以穿心莲内酯为原料,利用酯化反应与琥珀酸酐在负压条件(520~ 620 mmHg)下首次合成了脱水穿心莲内酯的琥珀酸半酯单钾盐37d(图5),提高了水溶性,增加生物利用度,药效增强,并制成抗病毒抗感染良药穿琥宁注射液,临床上用于治疗病毒性肺炎,上呼吸道感染以及急性菌痢,具有良好的疗效。1991年,Chang等[25]的药理研究显示穿心莲内酯琥珀酸单酯37b和37c(图5)具有抗HIV活性,其对HIV1(IIIB)的最小抑制浓度为16~31 mg·L-1(均值为20 mg·L-1)。2006年,胡士高等[26]对脱水穿心莲内酯二琥珀酸半酯的合成工艺进行了改进,将原方法使用真空度520~620 mmHg条件下沸水浴改为在氮气保护下加入无水吡啶、琥珀酸酐、无水硫酸钠,油浴控温70~80 ℃反应生成炎琥宁的重要中间体脱水穿心莲内酯二琥珀酸半酯,总收率417%,此法工序相对简单,且成本低,收率高。
试剂与条件:a微波照射,甲醇,100 ℃,15 min。
a丁二酸酐,亚硫酸钠吡啶,真空(520~620 mmHg),回流。
2004年,Nandur课题组[27]对穿心莲内酯分别进行了脱水、还原、氧化以及酯化等反应,合成了一系列的穿心莲内酯类似物38~48(图6),并进行了抗肿瘤活性研究和构效关系研究,结果表明穿心莲内酯的8,17位端烯键环氧化物(化合物43)抗肿瘤活性保持不变;对化合物43上的羟基进行酯化可使其细胞毒活性增强;然而,该研究还指出化合物43的三乙酰化物(化合物45a)的抗细胞毒性较低。2006年,韩光等[28]以穿心莲内酯为底物合成了衍生物38,40,49(图6)和14(图2),并采用蛋清致大鼠足肿胀模型观察这些化合物的抗炎活性,同时进行小鼠碳粒廓清实验观察其免疫活性,结果衍生物49的抗炎活性以及免疫抑制作用与穿心莲内酯相当,表明五元环的打开与否与抗炎免疫抑制作用无关。
a①2,2二甲氧基丙烷,苯,二甲基亚砜,4甲基苯磺酸吡啶鎓,回流,2 h,得率95%,②硼氢化钠,氢氧化钠,室温,1 h,得率85%,③乙酸水(7∶3),室温,15 min,得率90%,b①乙酸酐,氯化锌,室温,1 h,得率97%,②干燥吡啶,回流,4 h,得率80%,③10%盐酸甲醇溶液,室温,8 h,得率80%;c①乙酸酐,氯化锌,室温,1 h,得率97%,②硼氢化钠,氢氧化钠,室温,1 h,得率85%,③10%盐酸甲醇溶液,室温,8 h,得率80%;d乙酸,70 ℃,6 h,得率40%;e①三苯基氯甲烷,吡啶,60 ℃,6 h,得率80%,②间氯过氧苯甲酸,二氯甲烷,室温,2 h,得率70%;f间氯过氧苯甲酸,二氯甲烷,甲醇,室温,8 h,得率90%;g氢氧化钠水溶液,回流,1 h;h化合物45f间氯过氧苯甲酸,二氯甲烷,回流,4 h,得率70%;i化合物45d,45e,和45 g,①乙酸酐或丙酸酐,回流,30 min,②甲酸,二氯甲烷,室温,30 min;j化合物45a~45b乙酸酐或丙酸酐,回流,30 min,得率70%;k2,2二甲氧基丙烷,苯,二甲基亚砜,4甲基苯磺酸吡啶鎓,回流,8 h,得率70%;l化合物45c (①乙酸,回流,1 h,得率80%;②乙酸水(7∶3),室温,15 min,得率85%);化合物45h和45k (①R1COOH,氯甲酸乙酯,二氯甲烷,回流,1 h,得率60~80%;②乙酸水(7∶3),室温,15 min,得率85%;③乙酸酐或丙酸酐,回流,30 min,得率65%~75%);m三氟化硼乙醚,二氯甲烷,0 ℃,10 min;n硼氢化钠,甲醇,0 ℃,10 min;o氢氧化甲,乙醇,回流,盐酸。
2004年,吴晓明课题组通过三苯甲醚保护伯醇、氧化仲醇、脱去保护基的方法合成了3酮基12羟基13,14烯穿心莲内酯54(图7)[29]。2010年,黄文龙课题组[7]采用相似的方法,合成了穿心莲内酯衍生物56~58(图7),并评价了其体外抗HIV活性,结果显示化合物58h的活性最优。
2006~2007年,刘宏民课题组[3033]通过构效关系研究初步发现穿心莲内酯衍生物具有α葡萄糖苷酶抑制活性,并且以穿心莲内酯为原料合成了53个新穿心莲内酯衍生物59~68(图8),活性实验研究结果表明大多数化合物均显示出对α葡萄糖苷酶的選择性抑制活性,其中以γ亚烷基丁烯酸内酯穿心莲内酯或者在3,19位引入芳香基团的化合物活性较好,而这些化合物中又以59f,63c,68d对α葡萄糖苷酶的抑制活性最强,其IC50分别为16,83,6 μmol·L-1。随后,该课题组[3]继续考察了化合物38,59f,59i,67以及68d的抗炎活性,结果表明化合物68d的抗炎活性最强,其抗炎机制主要在于其能够降低血液中iNOS活性并且抑制NO和PGE2的产生。2013年,该课题组[34]新合成了化合物69及其羧酸盐,并对上述部分化合物进行抗癌活性筛选,结果发现化合物59a,59e,59f以及59i具有潜在的抗SGC7901,PC3,A549,HT29以及Ec109癌细胞系迁移活性,其机制经证实与MMPs的下调有关。endprint
2006年,Jada等[35]将穿心莲内酯C3,19位羟基与芳醛
a4甲基吗啉,三苯甲基氯,N,N二甲基甲酰胺,38~40 ℃,42 h;b重铬酸吡啶鎓,N,N二甲基甲酰胺,40 ℃,7 h;c甲酸,二氯甲烷,室温,1 h;d铬酸吡啶鎓,N,N二甲基甲酰胺,室温,1 h;e浓盐酸,室温;f三苯甲基氯,N甲基吗啉,二氯甲烷,室温;g化合物56a~56c酸酐,4二甲氨基吡啶,二氯甲烷,室温,化合物58a~58g酸酐或苯甲酰氯,甲苯,回流,化合物58h~58i酸,二环己基碳二亚胺,4二甲氨基吡啶,二氯甲烷,室温;h甲酸,二氯甲烷,室温。
偶联形成1′,3′二氧六环结构衍生物70~72(图9),并研究其分别对MCF7乳腺癌细胞与HCT116结肠癌细胞的抑制活性,结果表明大多数化合物均显示出较为相近的抗癌活性,其中化合物71h对MCF7与HCT116的GI50分别为07,27 μmol·L-1,其抑制活性明显优于穿心莲内酯,同时毒性也相对更低。实验进一步考察了衍生物70d~70g,70i,71k,71t~71u对九大类型肿瘤细胞的抑制活性,通过对GI50,TGI以及LC50进行分析,指出在C3和C19位引入烷基或芳香基团对其抗癌活性的提高有重要的促进作用。2010年,Memon等[36]利用活性Amberlyst15@在非水系统中合成了系列穿心莲内酯衍生物65h~65j(图8),71j,71v~71w,72a~72c(图9),该报道还研究了这些衍生物对人肺腺癌细胞系A549的体外抗癌活性,结果显示衍生物71j,71v,71w活性最好,其IC50介于22~31 mg·L-1质量浓度水平。
2007年,Li等[37]以穿心莲内酯为原料,合成了一系列的穿心莲内酯衍生物73~79(图10),药理活性实验研究表明这些化合物多数均显示出对鼠巨噬细胞中THFα与IL6炎症因子的释放具有一定的抑制作用,其中化合物73c,73e以及79f抑制LPS诱导的TNFα表达强于穿心莲内酯,而化合物79g,79j,79k,79l以及79n则表现出对IL6炎症因子更强的抑制作用。2009年,李爽风等[38]以N,N′二环己基碳二亚胺(DCC)为缩合剂,4二甲氨基吡啶(DMAP)为催化剂,合成了异穿心莲内酯3,19双酯衍生物及单酯衍生物80a~80j(图10),以期从中寻找新的具有抗细胞毒活性的先导化合物。
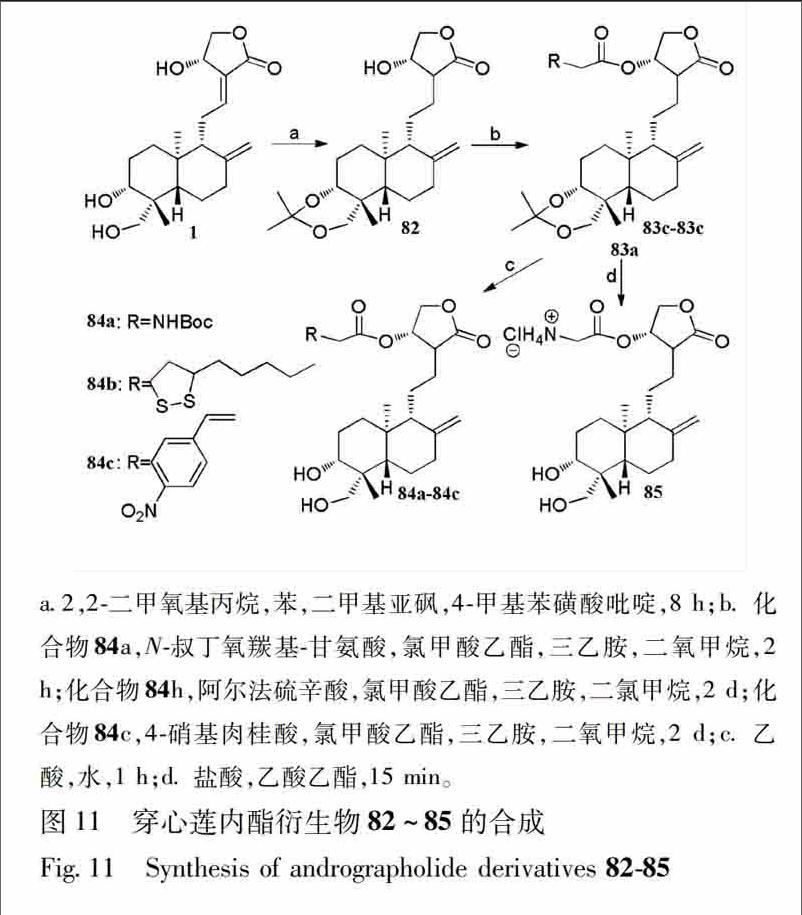
Jiang等[39],选择性地将穿心莲内酯C14位上的羟基与酰氯发生亲核取代反应生成衍生物84a~84c,85(图11),并研究了其抗菌与抑制毒力因子的生成实验,研究发现衍生物84a~84c,85均可抑制金黄色葡萄球菌的生成;此外,01 μmol·L-1浓度水平的穿心莲内酯及衍生物84a~84c,85可有效抑制绿脓杆菌(PA)毒力因子绿脓菌素与蛋白酶的产生,其中衍生物84b的抑制效果最为显著,它与红霉素联用可使PAO1菌株的存活力降至408%,接近环丙沙星/红霉素联用所致的存活率,有望被开发为新的抗PA药物。
2010年,Chowdhury课题组,以化合物8为反应中间体,对穿心莲内酯C14位进行选择性的结构修饰,引入琥珀酸苷、戊二酸酐、马来酸酐以及邻苯二酸酐,与C14位羟基成酯后获得一系列穿心莲内酯类似物86~90(图12),对人体白血病细胞系的体外毒性筛选实验显示类似物87a和87d具有较穿心莲内酯更强的细胞毒性,然而其对人正常细胞系毒性也较穿心莲内酯强,该研究还指出穿心莲内酯中α亚烷基γ丁内酯基团的存在对此类活性的提高扮演着十分重要的角色[40];随后在2014年,该课题组继续以化合物8为反应中间体,通过对端烯键环氧化并在C14位引入单卤代化物成酯的方式合成一系列穿心莲内酯衍生物91~96(图12),并通过多种抗癌药理活性评价实验发现化合物94a,94c以及96c对肾HEK293和乳腺MCF7肿瘤细胞有明显优于穿心莲内酯的抑制活性[6]。
构效关系研究显示在穿心莲内酯C19位引入甲硅烷基醚或三苯甲醚结构可增强其抗癌活性,Sirion等[41]通过对穿心莲内酯中的3个羟基进行结构修饰,获得了19个穿心莲
a间氯过氧苯甲酸,三氯甲烷,回流,2 h;b甲醇,碳酸钠,乙醛,回京戏;c二氧化镍,甲醇,0~5 ℃,05 h;d吡啶,三氧化二铝,甲苯,回流,6 h;e甲醇,碳酸钠,回流,5~24 h;f甲醇;三乙胺,室温,48 h;g硫酸,四氢呋喃,回流;h三氯甲烷,间氯过氧苯甲酸,室温,2 h;i四氢呋喃,硫酸,多聚甲醛,回流,1 h;j醛类,碳酸钠,甲醇,回流,3~5 h;k三氯甲烷,烟碱酸氯,三乙胺,回流,3 h;l乙醛,碳酸鈉,甲醇,回流,3~6 h;m甲醇,硼氯化钠;n三氯甲烷,三乙胺,回流,3 h。
a氯化锌,二甲基亚砜,室温,5~6 h;b对甲苯磺酸吡淀鎓,二甲基亚砜,60~70 ℃,2~3 h。
内酯类似物97~109(图13),多数化合物对癌细胞,如P338,KB,COL2,MCF7,LU1以及ASK,均显示出较穿心莲内酯更强的癌细胞毒性。其中19O三苯甲基穿心莲内酯醚(化合物107)显示出了高于玫瑰树碱的癌细胞毒性,此化合物可作为潜在的抗癌先导化合物。
范倩倩等[42]以穿心莲内酯为先导物,合成了一系列结构为12N取代14脱氧穿心莲内酯衍生物111a~111h(图14),并通过MTT筛选实验初步评价了这些衍生物的体外抗肿瘤活性,发现化合物111d具有显著的体内抗人肝癌HepG2细胞和体外抗小鼠H22和S180皮下移植性
a浓盐酸,室温;b化合物73a~73c,73f乙酸酐,二氯甲烷,回流;化合物73d~73e R1COCl,二氯甲烷,回流;化合物80a~80s i)乙二酰氯,室温,5 h,ii)铑,三乙醇胺,室温,过夜;化合物80t~80u i)壬二酰氯或癸二酰氯,室温,5 h,ii)甲醇,二乙胺,室温,6 h;化合物81a~81j R1OH,N,N′二环己基碳二亚胺,4二甲氨基吡啶,二氯甲烷,室温,4~6 h;c氯化亚砜,回流;d三苯甲基氯,N甲基吗啉,二氯甲烷,室温;e(R1CO)2O,4二甲氨基吡啶,二氯甲烷,室温;f甲酸,二氯甲烷,室温;g2二甲氧基丙烷,对甲苯磺酸吡淀NDFA1,二氯甲烷,回流;h重铬酸吡啶NDFA1,二氯甲烷;i化合物78a~78c(RCO)2O,二氯甲烷,室温;化合物78d RCOCl,二氯甲烷,室温,化合物78e~78h RCOOH,N,N′二环己基碳二亚胺,4二甲氨基吡啶,二氯甲烷,室温;j乙酸/水,室温。endprint
a2,2二甲氧基丙烷,苯,二甲基亚砜,4甲基苯磺酸吡啶,8 h;b化合物84a,N叔丁氧羰基甘氨酸,氯甲酸乙酯,三乙胺,二氧甲烷,2 h;化合物84h,阿尔法硫辛酸,氯甲酸乙酯,三乙胺,二氯甲烷,2 d;化合物84c,4硝基肉桂酸,氯甲酸乙酯,三乙胺,二氧甲烷,2 d;c乙酸,水,1 h;d盐酸,乙酸乙酯,15 min。
腫瘤的作用,其机制可能与激活p53依赖性凋亡诱导途径有关。
2005年,王秀萍等[43]对穿心莲内酯的C3位和C19位羟基进行糖苷化,合成了多种穿心莲内酯糖苷衍生物112~113(图15)。
3分子内环化、内酯环替换以及骈合成环反应
2004年,Nanduri等[27]合成了含氧杂环的穿心莲内酯衍生物47,抗肿瘤活性测试表明其具有中等强度的抗肿瘤活性(GI50 30~50 μmol·L-1)(图6)。2004 年,该课题组采用穿心莲内酯为原料,并以化合物114为重要反应中间体,通过一系列酯化、环化等反应,合成limonidilactone类似物118和126 [44](图16),进一步丰富了穿心莲内酯衍生物的基本骨架。2005年,吴晓明课题组[45]以穿心莲内酯为原料,异构化为异穿心莲内酯再草酰氯酰化、酯化和酰胺化方法以及长链酸酰氯甲酯化合成了21个新的异穿心莲内酯衍生物80(图10),初步体外药理活性表明部分异穿心莲内酯衍生物具有抗肿瘤活性。其中化合物3,19双(二正丁胺基羰基酰氧基)异穿心莲内酯80p表现出和穿心莲内酯相近的抗HL60作用,且化学稳定性要比穿心莲内酯高得多。
a2,2二甲氯基丙烷,对甲苯磺酸催化剂,丙酮,回流,2 h;b硼氢化钠,甲醇,零摄氏度至室温,1 h;c琥珀酸或戊二酸或马来酸或邻苯二甲酸酐,4二甲基氨基吡啶催化剂,二氯甲烷,室温,4~6 h;d乙酸水(7:3),室温;30 min;e氯乙酰氯,溴乙酰溴,吡啶,4二甲氨基吡啶干四氢呋喃,0 ℃,30 min;f间氯过氧苯甲酸,0 ℃,二氧甲烷,3 h,得率51%~54%;g乙酸水(7∶3),室温,30 min;h碘化钠,丙酮,室温,3 h。
a叔丁基二甲基氯硅烷、吡啶,室温,1 h;b乙酸酐,70 ℃,18 h;c叔丁基二苯基氯硅烷,吡淀,室温,1 h;d乙酸酐,70 ℃,6 h;e三异丙基氯硅烷,吡淀,室温,4 h;f乙酸酐,140 ℃,3 h;g①叔丁基二甲基氯硅烷,吡啶,室温,1 h,②乙酸酐,70 ℃,18 h;h甲酸水(9∶1),四氢呋喃,0 ℃,30 min;i乙酸酐,80 ℃,1 h;j①叔丁基二甲基氯硅烷,吡啶,室温,1 h, ②乙酸酐,145 ℃,1 h;k甲酸水(9∶1),甲氢呋喃,0 ℃,30 min;l三苯甲基氯,吡啶,70 ℃,25 h;m乙酸酐,140 ℃,1 h;n2,2二甲氧基丙烷,对甲苯磺酸吡啶鎓,丙酮。
a二甲基亚磷酸,对甲苯磺酸吡啶鎓,二氯甲烷/二甲基甲酰胺,回流,1 h;b甲基磺酰氯,三乙胺,二氯甲烷,室温,2 h;ci)胺类,二氯甲烷,回流,2 h,ii)对甲苯磺酰胺,甲醇,室温,过液。
aBrR1,碳酸银/吡啶;b碳酸钾/甲醇。
穿心莲内酯结构中的五元内酯环是其主要的活性部位之一,但对其进行结构修饰的报道很少。2004年Nanduri等[46]首次对内酯环进行替换,通过对穿心莲内酯的C12,13位的双键进行选择性的氧化降解,合成中间体128,然后以此为基础合成14个穿心莲内酯类似物(图17);药理研究表明,图中化合物131a~131c对人类多种癌细胞有着广泛的抗癌活性,其GI50浮动于2~20 μmol·L-1;化合物134b具有潜在的抗前列腺癌细胞(DU145)活性,其相应的GI50为078 μmol·L-1,化合物132和130c选择性的对抗DU145的GI50分别为02,017 μmol·L-1,此外,化合物133对乳腺癌细胞(MCF7)的GI50可达001 μmol·L-1。
2006年,Mang等[47]从穿心莲内酯出发,通过臭氧氧化合成中间体136(图18),合成了系列噻唑环化合物139~143,其中化合物142与R2中的AX可理论上组合形成360种不同的化合物,并通过液相色谱在215 nm下检测到其中的298个类似物。
2015年,Xiao等[48]以穿心莲内酯为原料,使用过硫酸钾为催化剂,进行以自由基转移为机制的分子内环化反应,合成了系列衍生物144~149(图19)。2016年,汪豪课题组[49]对原料药亚硫酸氢钠穿心莲内酯的相关物质研究中发现亚硫酸氢钠穿心莲内酯的水溶液在紫外光照射下即可生成144。这些化合物结构新颖,为穿心莲内酯衍生物的合成提供了新的思路,然而缺乏相关的药理活性研究,其潜在价值仍有待于进一步挖掘。
4衍生物与药理活性的构效关系总结
结合上述结构改造研究成果,本文对衍生物及其药理活性之间的构效关系做一初步总结,分为以下几个方面:第一,抗肿瘤活性方面,通过对C3,14和C19上的羟基进行修饰(如引入烷基或芳香基团)、内酯环的替换反应、C8,17烯键环氧化(图 20),均有助于提高抗肿瘤活性,C12,13位双键加氢还原可减弱其抗肿瘤活性,然而也有例外,如化合物130c,132,133(图 17);第二,抗炎抑菌活性方面,通过对C12,13位双键进行加成磺酸化、C3,19位羟基酯化引入亲水性官能团以及C14位的酯化反应等均可保持其抗炎活性,且部分化合物水溶性增强,利于人体吸收利用,结构方面,内酯环C(图 20)成环与否并不影响其抗炎抑菌活性,如化合物49(图 6);第三,α葡萄糖苷酶的抑制活性方面,γ亚烷基丁烯酸内酯穿心莲内酯或者在C3,19位引入芳香基团的化合物活性较好;第四,抗HIV活性方面,异穿心莲内酯衍生物以及C3,19位取代产物,如化合物37b,37c(图 5)以及58h(图 7),均有一定的抗HIV活性。endprint
綜上所述,有关穿心莲内酯衍生物的合成一直以来都是研究的热点,衍生物的结构修饰多样化,包括引入极性官能团以提高水溶性、引入NO供体、以自由基转移为基础的分子内环化反应等等,这些衍生物均展现出不同程度的抗肿瘤、抗炎、抗HIV以及α葡萄糖苷酶抑制活性。由于各种原因,也有不少研究团队仅是停留在合成阶段,缺乏后续药物在体内的活性或毒性方面的深入研究。
本文对穿心莲内酯衍生物的合成进行综述,旨在为广大穿心莲内酯衍生物合成团队提供思路,从而筛选出低毒高效的先导化合物,像莲必治注射液、喜炎平注射液以及穿琥宁注射液这样成功上市销售并创造社会价值。
a①2,2二甲氧基丙烷,对甲苯磺酸吡啶鎓,二甲基亚砜,苯,回流,2 h,②重铬酸吡淀,二氯甲烷,室温,5 h,③叔丁基二甲基氯硅烷,咪唑,N,N二甲基甲酰胺,室温,8 h,④乙酸,水,室温,15 min;b乙酸酐,吡啶,室温,6 h;c二氧化硒,过氧化氢叔丁醇,二氯甲烷,室温,48 h;di)甲基磺酰氯,吡啶,二氯甲烷,室温,1 h;ii)乙酸钠,丙酮,水,回流,2 h;e碘苯二乙酸酯,甲基丙烯酸酯,二氯甲烷,室温,1 h;f①20%二异丁基氢化铝甲苯溶液,-78 ℃,2 h,②乙酸酐,吡啶,室温,2 h;k紫外光照,氧,N,N二异丙基乙胺,孟加拉红;g硼氢化钠,四氢呋喃,0 ℃,2 h;h硼氢化钠,四氢呋喃,0 ℃,2 h;i乙酸水(7∶3),室温,24 h。
a2,2二甲氧基丙烷,对甲苯磺酸吡啶鎓,苯/回流,得率95%;b乙酸酐,三乙胺,二氯甲烷,室温,得率95%;4二甲氨基吡啶,二氯甲烷,室温,得率80%;c高锰酸钾溶液,四氢呋喃,室温,得率62%;d①绕丹宁,噻唑烷二酮;羟吲哚,β丙氨酸,苯,回流,②乙酸水(7∶3),室温,e①乙酸水(7∶3),室温,②苄基溴化物取代的维蒂格盐,氢化钠,苯,室温;f①溴乙酸乙酯,锌,苯,回流,得率70%,②重铬酸吡淀鎓,二氯甲烷,室温,得率90%;iii)盐酸胍,甲醇钠,甲醇,回流,得率60%;g①乙酰乙酸乙酯,四氯化钛,吡啶,②硼氢化钠,甲醇,③重铬酸吡啶鎓,二氯甲烷,④盐酸胍,甲醇钠,甲醇,回流;h化合物129a~129b二异丙基氨基锂,-80 ℃;化合物129c ①二异丙基氨基锂,-78 ℃,②重铬酸吡。
a①醋酸酐,吡啶,室温,②臭氧,二氧甲烷,吡啶,-78 ℃,③过氧化氢;b①二甲氧基丙烷,盐酸,②醋酸酐,吡啶;c十六烷基三甲基溴化铵,甲氢呋喃;d硫脲,吡啶,80 ℃;e酰氯或磷酰氯,吡啶;f取代的硫脲或硫代酰胺,吡啶或丁醇,回流;g氢氧化钠,四氢呋喃/甲醇;h胺,向山试剂,4二甲氮基吡啶;N,N二异丙基乙胺,二氯甲烷。
a乙醇水(10∶1),亚硫酸氢钠,回流,15 h,得率92%;b过硫酸钾,水,35~40 ℃,21 h,得率75%;c乙酸酐,吡啶,100 ℃,05 h,得率99%;d二氯甲烷,二氯亚砜,二甲基甲酰胺,回流,3 h,得率96%;e氯化铜,三乙胺,盐酸,甲苯,120 ℃,3 h;f氮气,苄基醚,160 ℃,2 h,得率74%。
[参考文献]
[1]杨静 穿心莲内酯的研究进展 [J]. 中草药, 2009, 7(7): 1168.
[2]Suebsasana S, Pongnaratorn P, Sattayasai J, et al Analgesic, antipyretic, antiinflammatory and toxic effects of andrographolide derivatives in experimental animals [J] Arch Pharm Res, 2009, 32(9): 1191.
[3]Dai G F, Zhao J, Jiang Z W, et al Antiinflammatory effect of novel andrographolide derivatives through inhibition of NO and PGE2 production [J]. Int Immunopharmacol, 2011, 11(12): 2144.
[4]Chen J X, Xue H J, Ye W C, et al Activity of andrographolide and its derivatives against influenza virus in vivo and in vitro [J]. Biol Pharm Bull, 2009, 32(8): 1385.
[5]Ekalaksananan T, Sookmai W, Fangkham S, et al Activity of andrographolide and its derivatives on HPV16 pseudovirus infection and viral oncogene expression in cervical carcinoma cells [J]. Nutr Cancer, 2015,67(4): 687.
[6]Preet R, Chakraborty B, Siddharth S, et al Synthesis and biological evaluation of andrographolide analogues as anticancer agents [J]. Eur J Med Chem, 2014, 85(15): 95.
[7]Wang B, Ge L, Huang W, et al Synthesis and preliminary antiHIV activities of andrographolide derivatives [J]. Med Chem, 2010, 6(4): 252.endprint
[8]Gu G, Lin H, Liu Y, et al Synthesis and antiHIVevaluation of novel andrographolide derivatives [J]. Lett Drug Des Discov, 2013, 10(2): 155.
[9]Tang C, Gu G, Wang B, et al Design, synthesis, and biological evaluation of andrographolide derivatives as potent hepatoprotective agents [J]. Chem Biol Drug Des, 2014, 83(3): 324.
[10]Moorthy N H N, Ramos M J, Fernandes P A Prediction of the relationship between the structural features of andrographolide derivatives and αglucosidase inhibitory activity: a quantitative structureactivity relationship(QSAR) Study [J]. J Enzyme Inhib Med Chem, 2011, 26(1): 78.
[11]Xu J, Huang S, Luo H, et al QSAR studies on andrographolide derivatives as αglucosidase inhibitors [J]. Int J Mol Sci, 2010, 11(3): 880.
[12]上海市穿心蓮科研协作组水溶性穿心莲内酯的研究 [J]. 中草药通讯, 1976(3): 10.
[13]孟正木 穿心莲内酯亚硫酸氢钠加成物的结构研究 [J]. 药学学报, 1981, 16(8): 571.
[14]唐春山 水溶性穿心莲内酯磺化工艺: 中国, CN1349986 [P]. 2002522.
[15]唐春山, 叶文才, 胡永美, 等. 穿心莲内酯磺化衍生物及其药物组合物: 中国, CN 1687049 A [P]. 20051026.
[16]许卉, 王功富, 韩飞, 等. 穿心莲内酯硫酸酯化反应体系中四个新的衍生物的分离与表征 [J]. 化学学报, 2009, 67(3): 261.
[17]徐浩, 黄文龙, 张惠斌, 等. 穿心莲内酯硝甲基衍生物的合成[J]. 中国药物化学杂志, 2005, 15(4):212.
[18]徐浩, 王新扬, 黄文龙, 等. N乙酰基12氨基亚甲基14脱氧穿心莲内酯衍生物的合成及其抗肿瘤活性[J]. 中国药科大学学报, 2005, 36(6): 496.
[19]Jada S R, Subur G S, Matthews C, et al Semisynthesis and in vitro anticancer activities of andrographolide analogues[J]. Phytochemistry, 2007, 68(6): 904.
[20]李晶, 黄文龙, 张惠斌, 等. 穿心莲内酯酰胺类衍生物的合成及其COX2表达抑制活性[J]. 中国药科大学学报, 2007, 38(4): 299.
[21]Hazra A, Paira P, Sahu K B, et al Chemistry of andrographolide: formation of novel dispiropyrrolidino and dispiropyrrolizidinooxindole adducts via onepot threecomponent [3+2]azomethine ylide cycloaddition[J].Tetrahedron Lett, 2010, 51(12): 1585.
[22]Hazra A, Bharitkar Y P, Chakraborty D, et al Regio and stereoselective synthesis of a library of bioactive dispirooxindolo/acenaphthoquino andrographolides via 1, 3dipolar cycloaddition reaction under microwave irradiation[J]. ACS Comb Sci, 2012, 15(1): 41.
[23]Dey S K, Bose D, Hazra A, et al Cytotoxic activity and apoptosisinducing potential of dispiropyrrolidino and dispiropyrrolizidino oxindole andrographolide derivatives[J]. PLoS ONE, 2013, 8(3): e58055.
[24]四川省中药研究所药化室穿心莲研究组 脱水穿心莲内酯琥珀酸半酯单钾盐及其注射剂的研究[J]. 中草药通讯, 1978(8): 1.
[25]Chang R S, Ding L, Chen G Q, et al Dehydroandrographolide succinic acid monoester as an inhibitor against the human immunodeficiency virus [J]. Proc Soc Exp Biol Med, 1991, 197(1): 59.endprint
[26]胡土高, 柏俊, 刘燕 脱水穿心莲内酯二琥珀酸半酯的合成工艺改进[J]. 安徽医药, 2006, 10(3):173.
[27]Nanduri S, Nyavanandi V K, Thunuguntla S S A, et al Synthesis and structureactivity relationships of andrographolide analogues as novel cytotoxic agents [J]. Bioorg Med Chem Lett, 2004, 14(18): 4711.
[28]韩光, 曾超, 杜钢军, 等. 穿心莲内酯衍生物的合成及其抗炎免疫活性 [J]. 中草药, 2006, 37(12): 1771.
[29]王新杨, 吴晓明, 黄文龙, 等. 3酮基12羟基13,14烯穿心莲内酯的合成 [J]. 中国药物化学杂志, 2004, 14(1):36.
[30]Dai G F, Xu H W, Wang J F, et al Studies on the novel alphaglucosidase inhibitory activity and structureactivity relationships for andrographolide analogues [J]. Bioorg Med Chem Lett, 2006 16(10): 2710.
[31]Xu H W, Dai G F, Liu G Z, et al Synthesis of andrographolide derivatives: a new family of αglucosidase inhibitors [J]. Bioorg Med Chem, 2007, 15(12): 4247.
[32]Xu H W, Liu G Z, Dai G F, et al Modification of 15akylidene andrographolide derivatives as alphaglucosidase inhibitor [J]. Drug Discov Ther, 2007, 1(1): 73.
[33]黄利华, 徐海伟, 刘改芝,等. (8R,13R)8,12,13,17四氢穿心莲内酯的合成、晶体结构和葡萄糖苷酶抑制活性[J]. 高等学校化学学报, 2007, 28(7):1304.
[34]Wu Z W, Xu H W, Dai G F, et al Improved inhibitory activities against tumorcell migration and invasion by 15benzylidene substitution derivatives of andrographolide [J]. Bioorg Med Chem Lett, 2013, 23(23): 6421.
[35]Jada S R, Hamzah A S, Lajis N H, et al Semisynthesis and cytotoxic activities of andrographolide analogues [J]. J Enzyme Inhib Med Chem, 2006, 21(3): 145.
[36]Menon V, Bhat S Anticancer activity of andrographolide semisynthetic derivatives [J]. Nat Prod Commun, 2010, 5(5): 717.
[37]Li J, Huang W, Zhang H, et al Synthesis of andrographolide derivatives and their TNFα and IL6 expression inhibitory activities [J]. Bioorg Med Chem Lett, 2007, 17(24): 6891.
[38]楊爽风, 顾军, 李灵芝 异穿心莲内酯3, 19双酯类衍生物的合成与表征 [J]. 华西药学杂志, 2009, 24(2): 110.
[39]Jiang X, Yu P, Jiang J, et al Synthesis and evaluation of antibacterial activities of andrographolide analogues [J]. Eur J Med Chem, 2009, 44(7): 2936.
[40]Das B, Chowdhury C, Kumar D, et al Synthesis, cytotoxicity, and structureactivity relationship(SAR) studies of andrographolide analogues as anticancer agent [J]. Bioorg Med Chem Lett, 2010, 20(23): 6947.
[41]Sirion U, Kasemsook S, Suksen K, et al New substituted C19andrographolide analogues with potent cytotoxic activities [J]. Bioorg Med Chem Lett, 2012, 22(1): 49.
[42]范倩倩, 王秋娟, 曾步兵, 等. 新型穿心莲内酯衍生物的合成及抗肿瘤作用 [J]. 中国药科大学学报, 2010, 41(4): 326.endprint
[43]王秀萍, 费瀚雨 穿心莲内酯糖苷衍生物的合成[J]. 中国药师, 2005, 8(6):446.
[44]Siva S R T, Vijay K N, Srinivas N A facile route for the synthesis of limonidilactone analogues from andrographolide [J]. Tetrahedron Lett, 2004, 45(51):9357.
[45]王新杨, 徐浩, 吴晓明,等. 异穿心莲内酯衍生物的合成及其抗肿瘤活性[J]. 中国药科大学学报, 2005, 36(6):504.
[46]Nanduri S, Nyavanandi V K, Thunuguntla S S R, et al Novel routes for the generation of structurally diverse labdane diterpenes from andrographolide [J]. Tetrahedron Lett, 2004, 45(25):4883.
[47]Mang C, Jakupovic S, Schunk S, et al Natural products in combinatorial chemistry: an andrographolidebased library [J]. J Comb Chem, 2006, 8(2): 268.
[48]Xiao X, Xu Z Y, Zeng Q, et al Construction of the isocopalane skeleton: application of a desulfinylative 1,7hydrogen atom transfer strategy [J]. Chem Eur J, 2015, 21(23): 8351.
[49]Hou J Q, Wang B L, Huang X J, et al Isolation and characterization of related impurities in andrographolide sodium bisulphite injection[J]. RSC Adv, 2016, 6(34): 28830
[責任编辑丁广治]endprint

