黑米中黄酮类化合物的稳定性分析
王磊,刘长姣,吴婕
(吉林工商学院粮食学院,吉林长春130507)
黑米又称紫米、乌米,在中国和东亚地区被誉为“补血米”、“长寿米”等[1]。黑米营养丰富,蛋白质平均含量为13%左右,比普通白米高46%~66%;氨基酸组成齐全,含有17种人体必需的氨基酸,组成比例优于白米且氨基酸组成模式接近人体模式[2]。此外,黑米中富含铁、锌、铜、锰等微量元素及VB1、VB2等B族维生素,还含有花色苷、黄酮、生物碱、甾醇等一些对人体健康有益的生物活性物质[3-4],属于绿色保健食品,极具开发价值。黑米中含有黄酮类物质,黄酮类化合物是一类重要的具有多样生物活性的含氧杂环天然有机化合物,广泛存在于植物中[5]。黄酮不仅具有抗菌、消炎镇痛、降血压、降血脂、清热解毒等作用,在抗氧化、抗衰老、抗肿瘤、抑制脂肪酶等方面也有显著效果,是目前功能性食品和医药品竞相开发的重点领域[6]。本文以超声波辅助水浴浸提黑米中黄酮类化合物,考察温度、pH值、光照、氧化剂、还原剂和金属离子等对黑米黄酮稳定性的影响,为生产中有效利用黑米总黄酮、提高黑米的附加值提供理论依据。
1 材料与方法
1.1 材料与试剂
黑米:产自黑龙江省五常县;芦丁标准品:国药集团化学试剂有限公司;无水乙醇、硝酸铝、氢氧化钠、亚硝酸钠等试剂均为分析纯。
1.2 仪器与设备
722可见分光光度计:上海佑科仪器仪表有限公司;SC-3610高速离心机:安徽中科中佳科学仪器有限公司;FA2004W电子天平:上海精密科学仪器有限公司;KQ-500E型超声波清洗器:昆山市超声仪器有限公司;GZX-9070MBE数显鼓风干燥箱:上海博迅实业有限公司医疗设备厂。
1.3 方法
1.3.1 黑米黄酮的提取工艺流程
黑米(烘干后)→粉碎过60目筛→取样→加一定浓度的乙醇→超声波辅助水浴浸提(液料比60 mL/g、乙醇浓度45%、超声时间45 min、提取温度50℃)→抽滤→离心(3 500 r/min,10 min)→上清液定容→510nm处测吸光度。
1.3.2 标准曲线的制作
标准曲线的制作方法见参考文献[7]。
1.3.3 黄酮类化合物含量的测定
采用亚硝酸钠-硝酸铝比色法[8]测定提取液中黄酮类化合物含量。
1.3.4 黑米中黄酮类化合物稳定性研究
1.3.4.1 温度对黄酮类化合物稳定性的影响
取5支洁净试管,各加入10 mL黄酮提取液,将提取液分别在20、40、60、80、90 ℃下水浴锅内恒温60 min,然后取出冷却至室温,在波长510 nm下测吸光度。
1.3.4.2 pH值对黄酮类化合物稳定性的影响
取8支洁净试管,各加入10 mL黄酮提取液,用HCl、NaOH 调节黄酮提取液的 pH 值至 3.0、4.0、5.0、6.0、7.0、8.0、9.0、10.0,在室温避光条件下放置 6 h,然后在波长510 nm下测吸光度。
1.3.4.3 光照对黄酮类化合物稳定性的影响
取5支洁净试管,各加入10 mL黄酮提取液,密闭在自然光照射下放置,用黑暗避光的样品做对照,于1、2、3、4、5 d 时定时取样,在波长 510 nm 下测吸光度。
1.3.4.4 H2O2对黄酮类化合物稳定性的影响
H2O2在食品中的允许使用量应不超过2%(质量分数),因此选取0%~2%H2O2溶液进行试验。量取30%H2O2配制成0.1 g/mL的H2O2溶液。取6支洁净试管分别加入 H2O2溶液 0、0.4、0.8、1.2、1.6、2.0 mL,用蒸馏水稀释至5 mL,然后加5 mL样液,即H2O2溶液的终浓度为0%、0.4%、0.8%、1.2%、1.6%、2.0%,摇匀后在室温下静置3 h,然后在波长510 nm下测吸光度。
1.3.4.5 Na2SO3对黄酮类化合物稳定性的影响
Na2SO3在食品中的允许使用量应不超过0.05%(质量分数),因此选取0%~0.05%Na2SO3溶液进行试验。称取0.625 gNa2SO3配制成2.5 g/L的Na2SO3溶液。取 6支洁净试管分别加入 Na2SO3溶液 0、0.4、0.8、1.2、1.6、2.0 mL,用水稀释至5 mL,然后加5 mL样液,即Na2SO3溶液的终浓度为 0%、0.01%、0.02%、0.03%、0.04%、0.05%摇匀后在室温下静置3 h后,在波长510 nm下测吸光度。
1.3.4.6 金属离子对黄酮类化合物稳定性的影响
研究 K+、Na+、Ca2+、Al3+、Mg2+和 Fe3+等金属离子对黑米中黄酮类化合物稳定性的影响。配制0.2 mol/L的KCl、NaCl、CaCl2、AlCl3、MgCl2溶液,0.01 mol/L 的 FeCl3溶液,取6个试管分别加入金属离子溶液0、0.1、0.2、0.3、0.4、0.5 mL,均用水稀释至 5 mL,然后再加入 5 mL试液,静置6 h后观察现象测吸光度。
2 结果与分析
2.1 标准曲线的回归方程
以吸光度(A)为纵坐标,总黄酮质量浓度为横坐标绘制标准曲线,如图1所示,得到回归直线方程:Y=0.507 9X-0.003 5(Y 为吸光度;X 为质量浓度,mg/mL),R2=0.999 6。
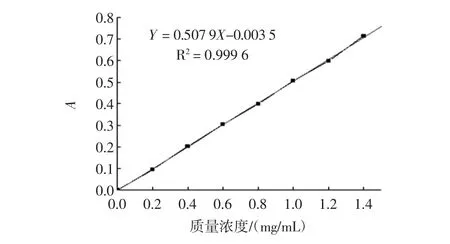
图1 芦丁标准曲线Fig.1 Standard curve of rutin
2.2 不同因素对黑米中黄酮类化合物稳定性的影响
2.2.1 温度对黑米黄酮稳定性的影响
温度对黑米黄酮稳定性的影响见图2。
由图2所示,在20℃~60℃时,黑米黄酮提取液的颜色基本无变化,吸光度值随温度变化不大,比较稳定。60℃以上时,吸光度值明显上升,提取液变成蓝紫色。当温度大于80℃以上时,提取液呈紫色,吸光度值随温度的升高而极显著增大。这可能是由于温度升高促使黄酮成分分解,产生更多的酚羟基[9]。试验表明,黑米黄酮在60℃以下显示了良好的耐热稳定性,应尽量避免在80℃以上高温条件下存放和应用。
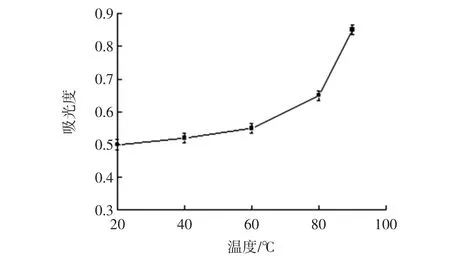
图2 温度对黑米黄酮稳定性的影响Fig.2 Effect of temperature on the stability of flavonoids in grown black rice
2.2.2 光照对黑米黄酮稳定性的影响
光照对黑米黄酮稳定性的影响见图3。
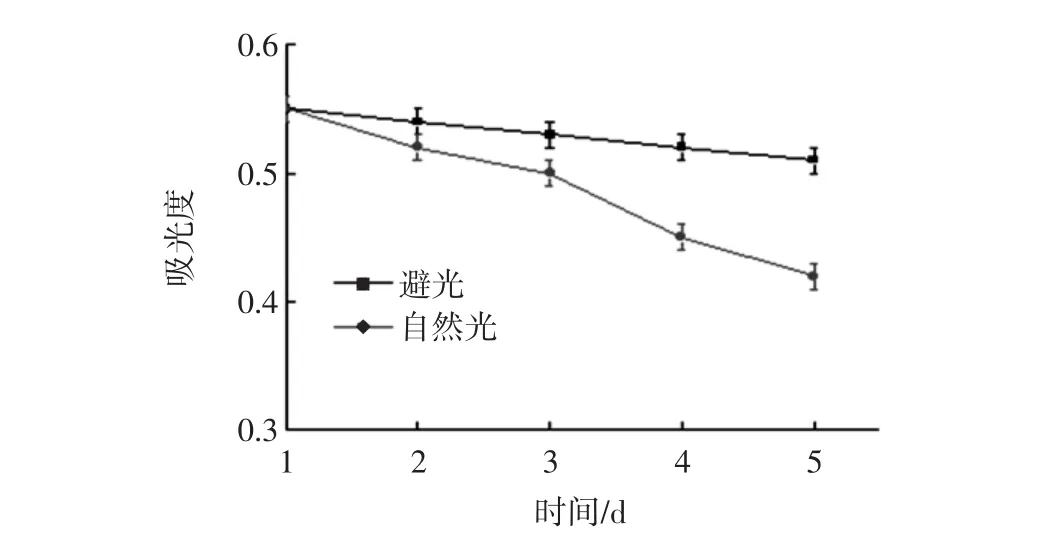
图3 光照对黑米黄酮稳定性的影响Fig.3 Effect of light on the stability of flavonoids in grown black rice
由图3可知,在自然光和避光条件下放置5 d后,黑米总黄酮提取液的吸光度均有所下降,但在自然光条件下下降更明显。这是因为在自然光条件下,黄酮类物质发生了自身氧化降解[8-9]。随着时间延长,黄酮提取液的颜色由深紫色变为浅紫色。在避光保存时,黄酮提取液的吸光度变化不大,所以黑米总黄酮提取液应在避光条件下保存为佳。
2.2.3 pH值对黑米黄酮稳定性的影响
pH值对黑米黄酮稳定性的影响见图4。
由图4可知,黑米黄酮提取液在pH6.0时,吸光度为0.58,达到最大,与原样液的吸光度接近。调节pH值,黄酮提取液颜色发生变化,pH值为2~6时,颜色为亮红色,且pH值越小,吸光度越低,颜色也越深。pH值为7~10时,颜色呈灰蓝色,随着pH值增大,提取液颜色加深且吸光度变小。说明黑米黄酮类化合物在酸碱性较强的环境中容易受到破坏,应避免强酸或强碱的环境。
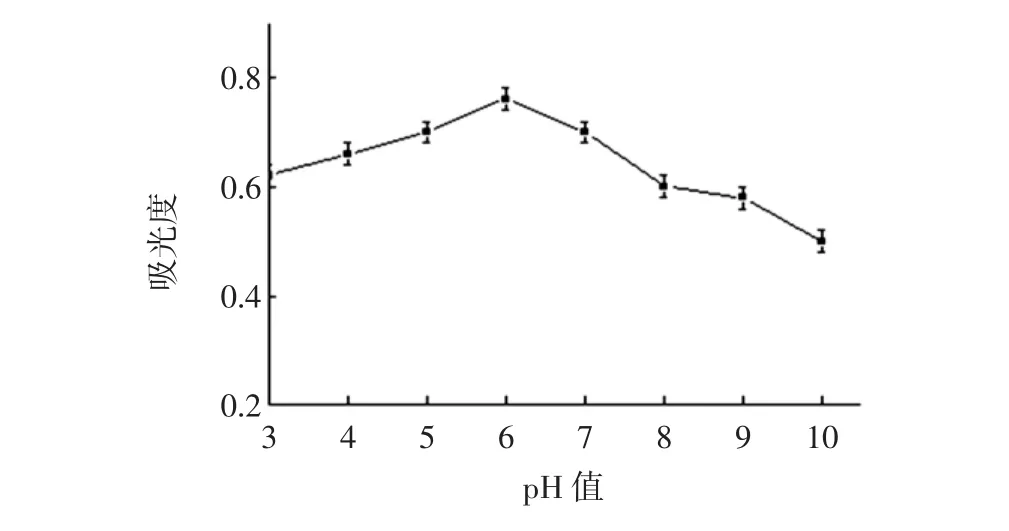
图4 pH值对黑米黄酮稳定性的影响Fig.4 Effect of pH on the stability of flavonoids in grown black rice
2.2.4 H2O2对黑米黄酮稳定性的影响
H2O2对黑米黄酮稳定性的影响见图5。
由图5可知,黑米中黄酮类化合物的吸光度随H2O2浓度的增加而缓慢减小,但变化不大。当H2O2质量分数为2.0%时,吸光度为0.51,与H2O2质量分数为0.4%、0.8%、1.2%、1.6%4组间差异不显著(p>0.05)。这表明黑米黄酮具有较好的抗氧化性。
2.2.5 Na2SO3对黑米黄酮稳定性的影响
Na2SO3对黑米黄酮稳定性的影响见图6。
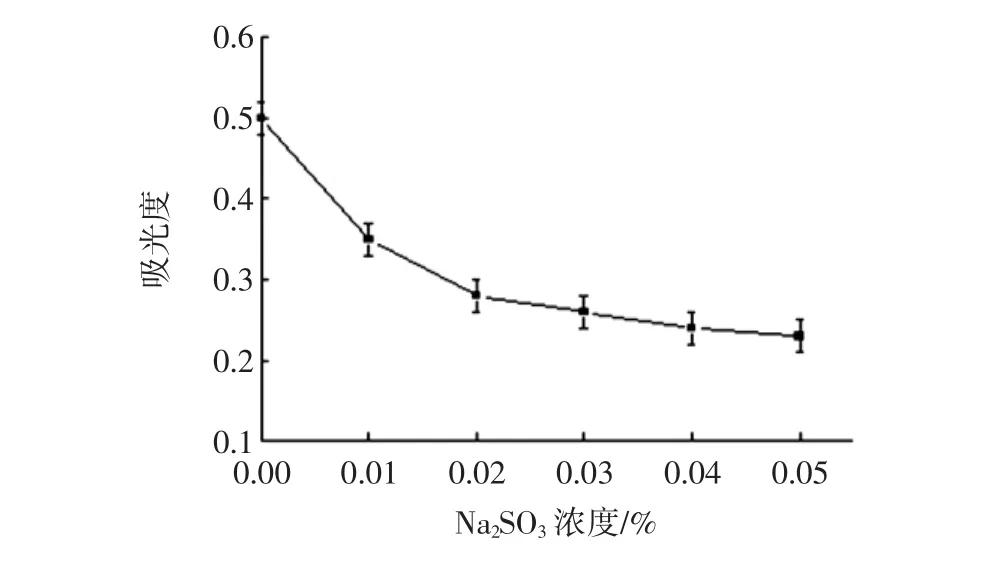
图6 Na2SO3对黑米黄酮稳定性的影响Fig.6 Effect of Na2SO3on the stability of flavonoids in grown black rice
由图6可知,黑米黄酮提取液的吸光度值随着Na2SO3溶液浓度的增加先大幅下降后逐渐趋于平缓,当浓度在0.05%时,吸光度值最低,与质量分数为0%、0.01%两组之间差异显著(p<0.01),说明还原剂Na2SO3对黑米黄酮提取液有强烈破坏作用,保存时需要避免与此类还原物质接触。
2.2.6 金属离子对黑米黄酮稳定性的影响
在相同浓度不同金属离子条件下的黑米黄酮稳定性差异很大,提取液在不同金属离子条件下的吸光度见表1。
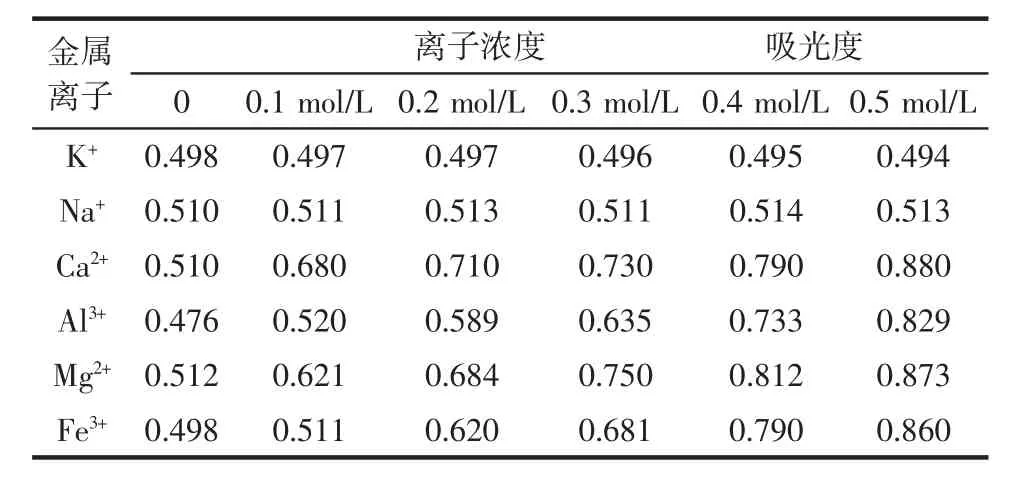
表1 不同金属离子对黑米中黄酮类化合物的稳定性影响Table 1 Effects of metal ions on the stability of grown black rice flavonoids
如表1所示,随着离子浓度增加,加入K+、Na+的提取液,吸光度变化幅度不明显,表明K+和Na+基本对黑米黄酮的稳定性没有影响;而加入Al3+、Ca2+、Mg2+、Fe3+的吸光度变化较大,表明这些金属离子对黑米黄酮的稳定性影响明显,原因可能是黄酮的邻二酚羟基与金属离子发生反应后形成络合物导致的[10]。加入Ca2+时提取液有部分沉淀生成。因此黑米黄酮在保存时应避免与含 Ca2+、Al3+、Mg2+和 Fe3+离子的容器接触。
3 结论
以黑龙江五常黑米为原料,研究黑米中黄酮类化合物的稳定性。在不同条件下,黑米黄酮的稳定性有一定的差异。在20℃~60℃时黄酮类化合物的含量基本不变;长时间的光照对黑米黄酮的稳定性影响较大;黑米中黄酮含量在酸碱性较强的环境中容易受到破坏,在弱酸性条件下比较稳定;对氧化剂H2O2具有较好的抗氧化性,但对还原剂Na2SO3显示出很大的不稳定性;K+和Na+两种金属离子对黑米黄酮稳定性几乎没有影响。而 Al3+、Ca2+、Mg2+、Fe3+能明显降低黑米黄酮的稳定性。
[1]杨志刚,张燕萍,杨海定,等.超声波辅助提取常熟黑米类黄酮及其抗氧化活性分析[J].食品科学,2013,34(18):118-122
[2]刘媛媛.黑米及黑米酒中抗氧化成分分析[D].杨凌:西北农林科技大学,2013
[3]孙晓侠,吴珊珊,王改玲.超声波强化提取黑米皮色素的工艺研究[J].中国酿造,2010,11(9):133-136
[4]PSARRA E,MAKRIS D P,KALLITHRAKA S,et al.Evaluation of the antiradical and reducing properties of selected Greek white wines:correlation with polyphenolic composition[J].Journal of the Science of Food and Agriculture,2002,82:1014-1020
[5]粱丹,张保东.黄酮类化合物提取和分离方法研究进展[J].周口师范学院学报,2007,24(5):87-89
[6]赖毅勤,周宏兵.近年来黄酮类化合物提取和分离方法研究进展[J].食品与药品,2007,9(4):54-58
[7]王丽娟,刘苏萌,李可,等.黑苦荞中黄酮类化合物的稳定性和抑菌活性研究[J].粮食与油脂,2015,28(8):62-65
[8]张慧,王遂.假酸浆中总黄酮的提取及稳定性研究[J].食品科技,2014,39(10):203-207
[9]王英,张玉刚,戴洪义.苹果皮中类黄酮的超声波辅助提取及稳定性研究[J].食品科学,2011,32(16):178-181
[10]李红姣,李巨秀,赵忠.酶法辅助提取山杏种皮黑色素工艺优化及其稳定性[J].食品科学,2016,37(10):69-75

