再生丝素蛋白溶液脱盐新工艺及其应用
李鹏飞, 邓 桦, 马 军, 刘红斌, 刘珍珠
(1. 天津工业大学 纺织学院, 天津 300387; 2. 军事医学科学院 卫生装备研究所, 天津 300161)
蚕丝主要由丝素蛋白和丝胶蛋白组成,其中丝素蛋白作为核心纤维占总质量的75%左右,是提供蚕丝力学性能并且使蚕丝表现出多种优点的主要成分[1],正逐步应用于化妆品、医学[2]和生物等多个领域。天然丝素蛋白不溶于水,目前采用溶解—精制后再加以利用,对于丝素蛋白的溶解工艺已有大量报道,目前主要是采用CaCl2-EtOH-H2O三元体系来溶解丝素,丝素溶解后,由于高浓度盐的存在使其无法被进一步利用,所以脱盐是实现丝素蛋白在其应用领域产业化的关键问题之一。
近年来人们对丝素蛋白溶液脱盐的方法进行不断的研究改进,传统上采用的是透析袋脱盐[3],该方法耗时长,耗水多。随着膜分离技术的发展,有研究人员利用超滤、纳滤和电渗析等技术[4-6]进行丝素蛋白溶液的脱盐。虽然3种方法优于透析袋脱盐[7],但是仍然存在着脱盐效率低、脱盐时间长,耗能严重等问题。
传统脱盐工艺的低效严重制约着丝素蛋白溶液的规模化使用,为了促进丝素蛋白溶液的工业化生产,本文探讨并优化一种丝素蛋白溶液(以下称为料液)的新型脱盐工艺,即扩散渗析-电渗析集成脱盐工艺,并且将该工艺条件下制备的高纯度的丝素蛋白溶液制成丝素蛋白粉,进一步探索该工艺所得产品的应用性能。本文所涉及到的2种膜堆,其中扩散渗析膜堆利用扩散渗析膜两侧溶液的浓度差为推动力来实现脱盐;电渗析膜堆则是在外加电场的作用下通过离子的定向迁移实现脱盐。二者结合对丝素蛋白溶液进行脱盐,既可充分利用丝素蛋白溶液本身的高盐浓度,又可利用电场作用来提高脱盐效率,从而达到既高效又节能的目的。
1 实验部分
1.1 材料和仪器
材料:蚕丝(市购),碳酸钠、无水氯化钙(块)、无水乙醇、盐酸、氯化铵、结晶硫酸镁、无水硫酸钠、氨水、锌粒、乙二胺四乙二钠盐、络黑T、无水乙醇,以上均为分析纯。
仪器:TD系列电子天平;DHG-9055型A烘箱;D-8401型多功能搅拌器;电热恒温水浴锅;YZ1515x型蠕动泵;85-2型恒温磁力搅拌器;DDSJ-308F型电导率仪;CR22G型超速冷冻离心机;121 MB型氨基酸自动分析仪;TM-3030型台式扫描电子显微镜。
扩散渗析模块:外形尺寸为100 mm×200 mm,有效尺寸为70 mm×120 mm,厚度为0.5 mm,扩散渗析阳膜,膜对数量为10,流量范围为20~40 L/h。
电渗析模块:外形尺寸为100 mm×200 mm,有效尺寸为70 mm×120 mm,厚度为0.5 mm,均相阴阳离子交换膜,膜对数量为10,操作电压5 V,流量范围为20~40 L/h。
1.2 不溶性丝素蛋白粉制备工艺
生蚕丝经脱胶、溶解,离心除杂后用扩散渗析-电渗析集成工艺脱盐,得到纯度较高的丝素蛋白溶液,将溶液中加入无水乙醇[8],所得白色沉淀经干燥后得到不溶性丝素蛋白粉。
1.2.1蚕丝脱胶与溶解
将蚕丝在温度为100 ℃,浴比为1∶40条件下,用质量浓度为5 g/L的Na2CO3溶液脱胶3次,每次30 min,除去丝胶蛋白,于50 ℃下烘干,得到脱胶蚕丝。按照物质的量比1∶2∶8配制氯化钙-乙醇-水(CaCl2-EtoH-H2O)三元体系溶液,以脱胶后蚕丝与三元体溶液质量比为1∶15,在60 ℃恒温水浴锅中对脱胶后的蚕丝溶解4 h,溶解后,待丝素蛋白溶液冷却至室温后用离心机8 000 r/min,离心10 min,得到丝素蛋白溶液。
1.2.2丝素蛋白溶液脱盐
取0.1 L所制备的丝素蛋白溶液,稀释至一定浓度,配制成料液。准确量取1 L去离子水为渗透液(料液与渗透液体积比为1∶10),然后将料液与渗透液分别以流量为40、20 L/h[9]通入扩散渗析模块,进行第1阶段预脱盐。待脱盐至一定脱盐率时,设置电流为0.2 A[9],料液和渗透液流量不变,进行第2阶段电渗析脱盐,至溶液电导率降至200 μS/cm,此时脱盐结束。其中料液和渗透液均由蠕动泵循环供给。
1.2.3不溶性丝素蛋白粉制备
取一定体积的丝素蛋白溶液,调制至质量分数为5%,在室温下加入适量无水乙醇,溶液中会迅速产生白色沉淀,静置至待沉淀不再产生时,过滤取沉淀,经干燥后得到不溶性的丝素蛋白粉。
1.3 测定与计算方法
溶液总溶解固体(TDS)值通过台式电导率仪进行测定。Ca2+含量采用EDTA滴定法[10]测定。计算公式为
N=T×V
β=(mi/mj)×100%
θ=(m1/m0)×100%
W=U×I×t
式中:N为实际离子总量,g;T为溶液TDS值,g/L;V为溶液的体积,L;β为脱盐率,%;mi为渗透液中含盐量,g;mj为脱盐前料液中含盐量,g;θ为丝素蛋白回收率,%;m1为脱盐后料液中蛋白质质量,g;m0为脱盐前料液中蛋白质质量,g;W为电渗析能耗(动力能耗除外),kWh;U为操作电压,V;I为操作电流,A;t为操作时间,h;η为料液体积增长率,%;V0为料液初始体积,L;Vn为nh时料液体积,L。
其中,脱盐前料液中蛋白质含量用溶解的丝素蛋白质量来衡量,而脱盐后蛋白质含量用脱盐后的料液经干燥后所剩余固体质量来衡量。
氨基酸含量测定:将丝素蛋白样品放置于水解管中,加入适量的6 mol/L的HCl溶液,真空封口,在110 ℃下水解24 h,冷却后定容、过滤、蒸干,再加入0.02 mol/L的HCl溶液,并在空气中放置30 min,上机测定氨基酸含量。
利用TM-3030型台式扫描电子显微镜观察不溶性丝素蛋白粉的微观形貌。
2 结果与讨论
2.1 料液质量分数的选择
在使用CaCl2-EtOH-H2O三元体系溶解丝素蛋白过程中,Ca2+会配位在丝素蛋白大分子链的络氨酸、丝氨酸的侧链羟基处,形成螯合物[11],这说明丝素蛋白溶液中Ca2+分为2部分:一部分是游离在溶液中的Ca2+,可对溶液的TDS值产生影响;另一部分由于与丝素蛋白螯合而没有对溶液的TDS值产生影响。这2部分Ca2+会随着溶液质量分数的不同而产生变化。有研究者通过对丝素蛋白溶液质量分数和TDS值关系的研究,发现随着质量分数的增加溶液TDS值先增大后减小且在3%时TDS值达到最大,再而考虑到水的反向渗透,最终选择丝素蛋白溶液进液质量分数为4%[12],但是这个结果对料液体积的变化情况考虑的并不充分,如图1所示。
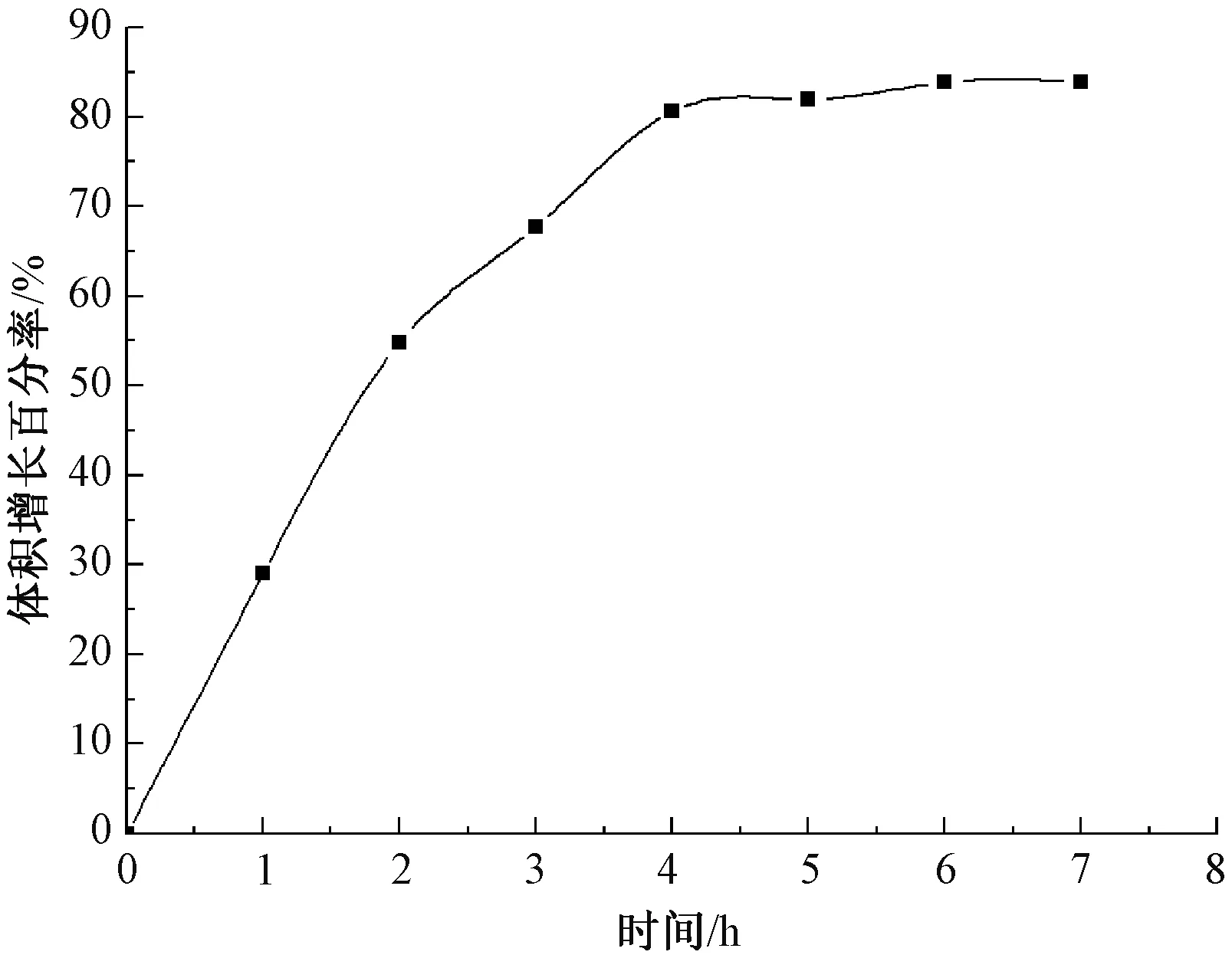
图1 料液体积增长百分率与时间的关系Fig.1 Relationship between percentage of volume growth and time
由图1可知,在脱盐过程中,由于水的反向渗透,料液体积逐渐增加且增长率可达到80%左右,料液体积稀释的程度较大。可见仅考虑4%的质量分数显然是不够的,因此选择料液质量分数为5%、4%和3%进行第1阶段扩散渗析预脱盐实验,结果见图2。
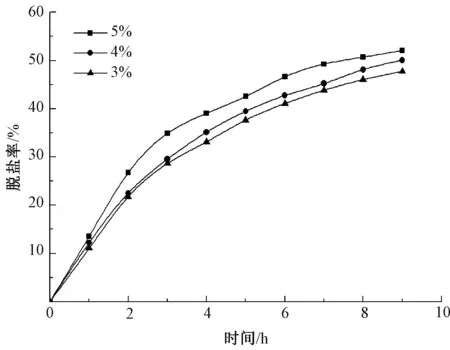
图2 不同料液质量分数下时间和脱盐率的关系Fig.2 Relationship between concentration of liquid and time and desalination rate
由图2可知,达到相同脱盐率时料液质量分数为5%的曲线用时最短,由图中曲线的斜率可知3种质量分数料液在0~4 h内脱盐效率较高。结合图1可知,当料液初始质量分数为5%时,料液质量分数将由5%降至2.8%左右,在此期间脱盐效率逐渐提升然后再下降,而初始质量分数为4%时,进行到1 h时料液质量分数已被稀释至3.0%左右,此后长时间内脱盐效率逐渐下降。
综合考虑图1和图2,选定料液质量分数5%为最佳,此时不仅浓度差推动力较大,而且最终得到的丝素蛋白溶液质量分数也较大,不溶性丝素蛋白粉的产率也相应较高。
2.2 扩散渗析预脱盐率的选择
随着脱盐过程的进行,料液中的CaCl2逐渐渗析至渗透液中,致使料液和渗透液的盐的质量分数差越来越小,脱盐效率会逐渐降低,此时溶液体系会较长时间地处于料液盐的质量分数高于渗透液盐浓度的状态,而且随着这段时间的延长,渗透液向料液中反向渗透的水会增加,这就会造成料液质量分数逐渐减小,从而会减少不溶性丝素蛋白粉的产率,但是若过大的缩短扩散渗析预脱盐时间,又会增加电渗析脱盐时间,这样会造成能耗增加;因此选定料液进液质量分数为5%,分别进行扩散渗析和电渗析脱盐实验,结果如图3所示。
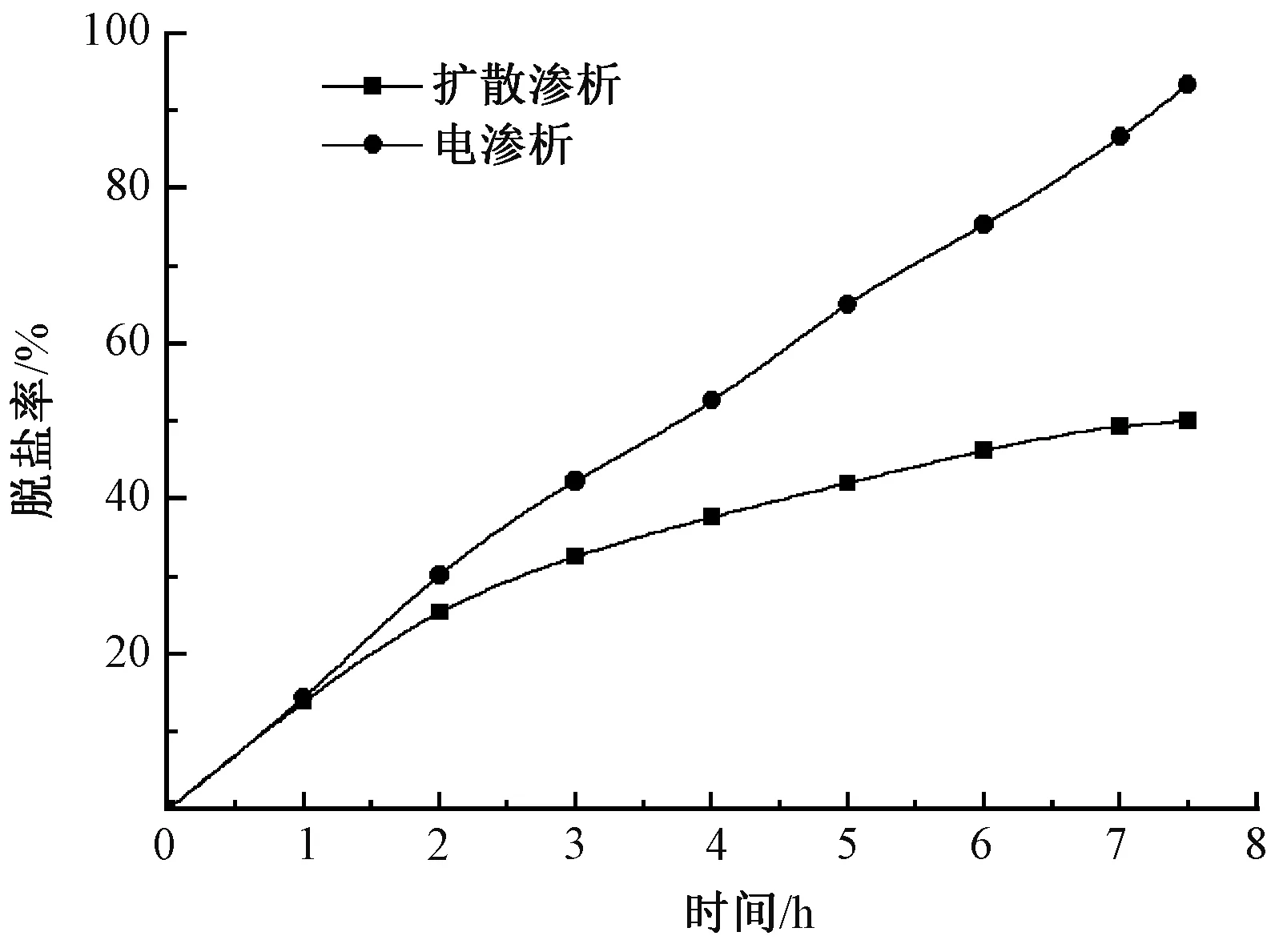
图3 不同脱盐方式下时间和脱盐率的关系Fig.3 Relationship between different desalination methods and desalting rate and time
由图3可知,电渗析脱盐所得到的是一条斜率基本不变的直线,而扩散渗析脱盐所得到的是一条斜率逐渐减小的曲线,表明前者的脱盐效率基本不受料液和渗透液之间浓度差的影响,而后者的脱盐效率随着料液和渗透液之间质量分数差的减小而下降。相同时间内,2种脱盐方式在脱盐率为60%左右差距变得越来越大。
选择预脱盐率分别为20%、40%、60%进行脱盐实验,结果如表1所示。
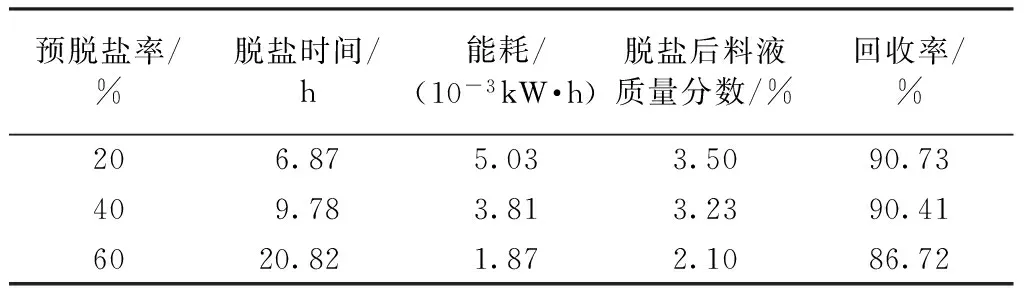
表1 不同预脱盐率脱盐实验结果Tab.1 Experimental results of desalting at different pre-desalting rates
由表1可知,不同预脱盐率对脱盐时间和能耗的影响较大,对最后所得溶液的质量分数影响较小。表中最终所得浓度比图1的分析中所提到的质量分数高,因为图1、2的数据是扩散渗析预脱盐阶段的数据,在预脱盐结束后要进行电渗析深度脱盐,此时料液中盐浓度要长时间处于低于渗透液中盐质量分数的状态,料液中的水会透过交换膜向渗透液中转移,因此会对料液达到初步浓缩的效果,且会随着电渗析脱盐时间的延长浓缩效果更加明显。
当预脱盐率为60%时,虽然能耗相对来说比较低,但是最终脱盐时间和料液质量分数是最不理想的;当预脱盐率为40%时,虽然脱盐时间比20%时长,但是此时能耗较小,而且相比于传统的透析袋来说,已经将脱盐时间由36 h缩短到了9.78 h。综合考虑,当预脱盐率为40%时,脱盐工时短,能耗小且此时溶液质量分数较佳。
2.3 丝素蛋白氨基酸组成
对脱盐后所得丝素蛋白进行氨基酸含量分析,100 g丝素蛋白中:组氨酸0.41%、赖氨酸0.49%、苯丙氨酸1.50%、天门冬氨酸2.69%、苏氨酸1.13%、丝氨酸12.60%、酪氨酸10.74%、亮氨酸0.62%、异亮氨酸1.88%、缬氨酸3.81%、甘氨酸36.55%、丙氨酸27.85%、谷氨酸2.41%。
由以上数据可看出甘氨酸、丙氨酸、酪氨酸和丝氨酸约占总组成的87%,很多功能性实验证实了这4种氨基酸以及其所构成的多肽都具有优良的生理功能,其中含量最高的甘氨酸可以很好地吸收紫外线,另外占总含量12.60%的丝氨酸不仅可与紫外线进行光化反应,还可有效地抑制黑色素的形成。
2.4 丝素蛋白结构分析
将丝素蛋白溶液直接冷冻干燥得到丝素蛋白粉样品A,取一定体积丝素蛋白溶液加入适量无水乙醇,得到白色沉淀,经干燥后得到样品B。利用扫描电镜(SEM)分别对样品A、B进行观察,结果如图4所示。

图4 丝素蛋白粉扫描电镜照片(×500)Fig.4 SEM images of silk fibroin powder(×500).(a)Sample A;(b)Sample B
对比图4(a)、4(b)可知,样品A呈块状,粒径较大,样品B的颗粒直径明显小于样品A,而且颗粒大小均匀,表面具有细小的凹凸孔洞,增大了比表面积,会增加对紫外线的散射,使其对紫外线具有更好的阻挡防护作用。样品B用于化妆品中可更加均匀地铺展到皮肤表面,另外由于丝素蛋白本身具有良好的亲和性,不会造成皮肤过敏,而且由于较小的粒径,即使进入了皮肤的毛孔也会被分解吸收。
3 结 论
本文旨在解决丝素蛋白溶液制备过程中存在的耗时和耗能等问题,通过对主要影响因素的分析研究,最终得到了较为满意工艺条件,初步达到了高效节能的项目预期,其中:
1)确定了扩散渗析-电渗析集成脱盐工艺参数:料液质量分数为5%,扩散渗析预脱盐率为40%,在此工艺条件下进行丝素蛋白溶液的脱盐可以进一步降低脱盐能耗,缩短脱盐工时。
2)测定了丝素蛋白的氨基酸组成,并且利用扫描电镜观察不溶性丝素蛋白粉的形貌特征。由氨基酸分析可看出丝氨酸和甘氨酸含量总和接近50%,由电镜扫描得到不溶性丝素蛋白粉的粒径较小且分布均匀,因此不溶性蚕丝蛋白粉不仅可以吸收一部分紫外线,还可以散射一部分紫外线,用在化妆品中既能被皮肤吸收,又具有很好的防晒功能。
参考文献:
[1] 倪莉, 王璋, 许时婴. 可溶性丝素粉末的制备[J].无锡轻工大学学报, 2000(2):146-149.
NI Li, WANG Zhang, XU Shiying. Preparation of silk fibroin powder[J]. Journal of Wuxi University of Light Industry, 2000(2):146-149.
[2] ZHU M, WANG K, MEI J, et al. Fabrication of highly interconnected porous silk fibroin scaffolds for potential use as vascular grafts [J]. Acta Biomater, 2014, 10:2014-23.
[3] TUNA Y, PEGGY C, DAVID L, et al. Vortex-induced injectable silk fibroin hydrogels [J]. Biophysical Journal, 2009, 97(7): 2044-2050.
[4] 苏锋, 杨瑞金, 许时婴. 可溶性丝素蛋白溶液脱盐技术[J]. 无锡轻工大学学报,2004(4):56-59.
SU Feng, YANG Ruijin, XU Shiying. Soluble silk fibroin solution desalination technology [J]. Journal of Wuxi University of Light Industry, 2004(4):56-59.
[5] 周凤娟, 许时婴, 杨瑞金, 等. 纳滤技术在丝素活性肽生产中的应用[J]. 膜科学与技术,2008(3):83-86,99.
ZHOU Fengjuan, XU Shiying, YANG Ruijin, et al. Application of nanofiltration technology in the production of silk fibroin bioactive peptides[J]. Membrane Science and Technology, 2008(3):83-86,99.
[6] 中国科学院上海有机化学研究所. 丝肽、制备方法和应用: 103897021A[P]. 2014-07-02.
Shanghai Institute of organic chemistry, Chinese Academy of Sciences. Silk peptide, preparation method and application: 103897021A[P]. 2014-07-02.
[7] 周凤娟, 许时婴, 杨瑞金, 等. 渗析分离丝素蛋白盐溶液的研究[J]. 膜科学与技术, 2004(6):25-28.
ZHOU Fengjuan, XU Shiying, YANG Ruijin, et al. Study on the separation of fibroin solution by dialysis[J]. Membrane Science and Technology, 2004(6):25-28.
[8] 袁慧勇. 不溶性蚕丝蛋白超细粉的制备及应用[D]. 保定:河北大学,2010:8-9.
YUAN Huiyong. Preparation and application of insoluble silk protein superfine powder [D]. Baoding: Hebei University, 2010:8-9.
[9] 刘珍珠, 刘红斌, 邓桦, 等.可溶性丝素蛋白新型脱盐工艺研究[J]. 水处理技术,2017(4):62-65.
LIU Zhenzhu, LIU Hongbin, DENG Hua, et al. Study on new desalting process of soluble silk fibroin [J]. Water Treatment Technology, 2017(4): 62-65.
[10] 刘二东, 郑斌. 配位滴定法测定生活用水的硬度[J]. 山东化工,2016(17):79-80,83.
LIU Erdong, ZHENG Bin. Determination of hardness of domestic water by complexometric titration [J]. Shandong Chemical Industry, 2016(17): 79-80,83.
[11] 董文秀,李军生,李秋杰,等. 光谱法研究钙离子对丝素蛋白溶解过程中结构的影响[J]. 分析测试学报,2014,12:1410-1415.
DONG Wenxiu, LI Junsheng, LI Qiujie, et al. The spectrum method to study the structure of the calcium ion in the process of silk fibroin dissolve effect [J]. Journal of Analysis Test, 2014, 12:1410-1415.
[12] 刘珍珠. 丝素蛋白溶液的脱盐技术研究及其在纺织上的应用[D].天津:天津工业大学,2017:22-25.
LIU Zhenzhu. Study on desalination of silk fibroin solution and its application in textile[D].Tianjin: Tianjin Polytechnic University,2017:22-25.

