益气通脉胶囊质量标准的研究
孔 燕, 王 健
(扬州市食品药品检验检测中心,江苏扬州225009)
益气通脉胶囊为宝应县中医医院经验方,由西洋参、三七、黄精、川芎、赤芍等8味药材组成,功效益气养阴、活血通脉,用于气阴不足兼血瘀症所致头昏、头晕、胸闷、胸痛,但该方并无明确详细的质量标准。因此,本实验通过查阅相关文献和反复摸索,制定三七、川芎的显微鉴别方法,确定川芎、赤芍、西洋参、三七的TLC定性鉴别方法[1],并通过HPLC法测定西洋参、三七中三七皂苷R1、人参皂苷Rg1、人参皂苷Re、人参皂苷Rb1的含有量[2], 以期控制该制剂质量[3]。
1 材料
BX51光学显微镜、3X Optical Zoom数码相机(日本 Olympus公司);MS204S电子天平 (瑞士Mettler-Toledo公司);HH-4数显恒温水浴锅 (常州国华电器有限公司);TLC Visualizer薄层成像系统 (瑞士Camag公司);硅胶G薄层板、高效硅胶G薄层板 (青岛海洋化工厂);Agilent 1200高效液相色谱仪 (美国安捷伦公司)。乙腈为色谱纯[4];其他试剂均为分析纯;水为纯化水。
川芎 (批号120918-201612)对照药材及芍药苷 (批号 110736-201741)、 三七皂苷 R1(批号110745-201619)、 人参皂苷 Rg1(批号 110703-201731)、人参皂苷Re(批号110754-201626)、人参皂苷 Rb1(批号110704-201625)、拟人参皂苷(批号841-9903)对照品均购于中国食品药品检定研究院。
3批益气通脉胶囊来自宝应县中医医院制剂室, 批号170502、 170529、 170619, 0.3 g/粒, 10粒/板,3板/盒。缺川芎、赤芍、西洋参、三七阴性样品 (同时缺西洋参、三七的为阴性对照),来自宝应县中医医院制剂室。
2 方法与结果
2.1 显微鉴别 图1~2显示,三七中树脂道碎片含黄色分泌物[7];川芎中油室大多已破碎,偶可见油室碎片,分泌细胞壁薄,含有较多的油滴[7],3批样品显微特征均稳定,易于鉴别。

图1 三七显微鉴别图Fig.1 Image for microscopic identification of Notoginseng Radix et Rhizoma
2.2 TLC定性鉴别
2.2.1 川芎 取本品内容物2 g,加25 mL乙醚轻摇,回流15 min,过滤,蒸干,残渣加1 mL乙酸乙酯溶解,作为供试品溶液[8-9];取对照药材1 g,同法制成相应溶液[3,7];取阴性样品适量,同法制成相应溶液,吸取上述3种溶液各5 μL,点于同一硅 胶 G 薄 层 板 上[6,10], 以 正 己 烷-乙 酸 乙 酯(3∶1)为展开剂,展开缸中预平衡15 min,上行展开,展距 9 cm,取出,晾干,置于紫外灯(365 nm) 下检视[4,11], 结果见图 3。 由图可知,供试品色谱中在与对照药材相应位置上显相同颜色荧光斑点[12], 阴性无干扰[13]。

图2 川芎显微鉴别图Fig.2 Image for microscopic identification of Chuanxiong Rhizoma

图3 川芎TLC色谱图Fig.3 TLC chromatogram of Chuanxiong Rhizoma
2.2.2 赤芍 取本品内容物2 g,加25 mL乙醇,轻摇,超声15 min,过滤,蒸干,残渣加1 mL乙醇溶解,作为供试品溶液[4];取芍药苷对照品适量,甲醇制成每1 mL含1 mg该成分的对照品溶液[2];取阴性样品适量,同法制成相应溶液,吸取上述3种溶液各8 μL,点于同一硅胶G薄层板上[2], 以氯仿-乙酸乙酯-甲醇-甲酸 (40 ∶5 ∶20 ∶0.5)为展开剂,展开缸中预平衡15 min,上行展开,展距9 cm,取出,晾干,再喷以5%香草醛硫酸溶液[7-8], 105 ℃下加热至斑点显色清晰[11], 置于日光下检视,结果见图4。由图可知,供试品色谱在与对照品相应位置上显相同颜色斑点[2],阴性无干扰。
2.2.3 西洋参、三七 取本品内容物2 g,加25 mL甲醇轻摇,回流30 min,滤过,滤液蒸干,残渣加20 mL水溶解,加水饱和正丁醇振摇提取2次[5], 每次 25 mL, 合并提取液[14-15], 正丁醇饱和水洗涤 2 次[2-3], 每次 10 mL, 分取正丁醇液[7,9],蒸干,残渣加1 mL甲醇溶解,作为供试品溶液[4,8]; 取拟人参皂苷 F11、 人参皂苷 Rb1、 人参皂苷Re、人参皂苷Rg1、三七皂苷R1对照品适量,甲醇制成每l mL各含2 mg上述成分的对照品溶液;取阴性对照适量,同法制成相应溶液,吸取上述3种溶液各 5 μL,点于同一硅胶 G薄层板上[4,11], 以三氯甲烷-无水乙醇-水 (20 ∶20 ∶2)为展开剂,展开缸中预平衡15 min,上行展开,展距9 cm,取出,晾干,再喷以10%硫酸乙醇溶液[11], 105 ℃下加热至斑点显色清晰[4,15], 分别置于日光、紫外光灯 (365 nm)下检视,结果见图5。由图可知,供试品色谱在与对照品相应位置上显相同颜色斑点或荧光斑点[2,10],阴性无干扰。
2.3 HPLC含有量测定
2.3.1 色谱条件和系统适应性试验 Inertsil®ODS-SP 色谱柱 (5 μm, 4.6 mm×250 mm); 流动相乙腈 (A)-水 (B), 梯度洗脱, 程序见表 1;体积流量 1.0 mL/min;柱温 28℃;检测波长203 nm;进样量10 μL,色谱图见图6。由图可知,各成分分离度良好,阴性无干扰,理论塔板数按人参皂苷Rb1计应不低于4 000。

表1 梯度洗脱程序Tab.1 Gradient elution programs
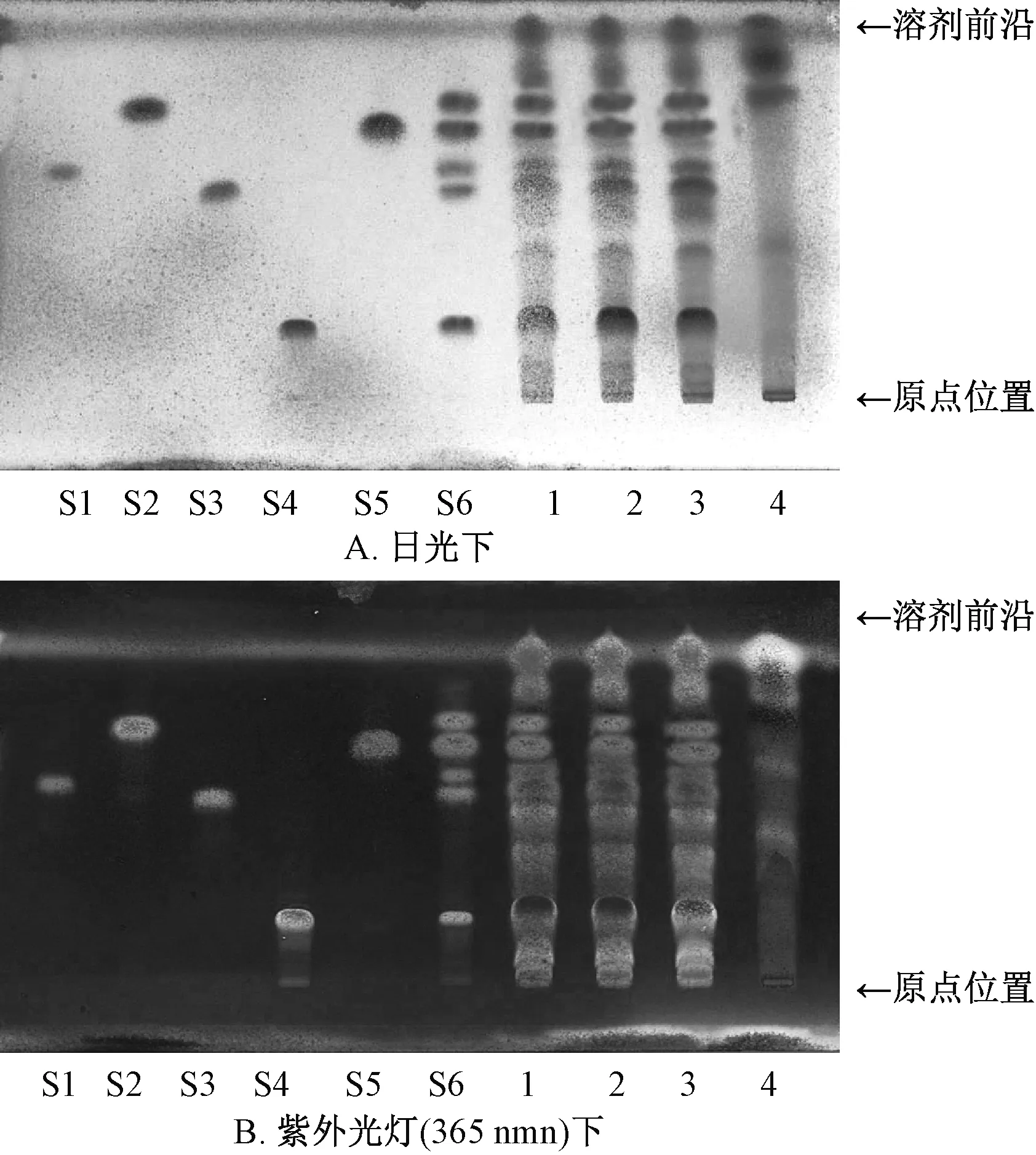
图5 三七、西洋参TLC色谱图Fig.5 TLC chromatograms of Notoginseng Radix et Rhizoma and Panacis quinquefolii Radix
2.3.2 溶液制备
2.3.2.1 对照品溶液 精密称取各对照品适量,置于25 mL量瓶中,甲醇溶解定容至刻度,摇匀,制成分别含三七皂苷R1、人参皂苷Rg1、人参皂苷Re、 人 参 皂 苷 Rb1317.12、 552.32、 646.72、561.28 μg/mL 的溶液, 即得。
2.3.2.2 供试品溶液 取质量差异项下本品内容物,研细,混匀,精密称取约0.5 g,置于具塞锥形瓶中,精密加入25 mL甲醇,称定质量,静置1 h,80℃水浴回流2 h,放冷,甲醇补足减失的质量,摇匀,滤过,取续滤液,即得。
2.3.3 线性关系考察 精密量取对照品溶液0.5、1、2、3、4、5、6 mL,置于10 mL量瓶中,甲醇稀释定容至刻度, 分别精密量取 10 μL[4], 在“2.3.1”项色谱条件下进样测定[10]。以溶液质量浓度为横坐标 (X), 峰面积为纵坐标 (Y)[16]进行回归,结果见表2,可知各成分在各自范围内线性关系良好。

图6 各成分HPLC色谱图Fig.6 HPLC chromatograms of various constituents

表2 各成分线性关系Tab.2 Linear relationships of various constituents
然后,甲醇多次稀释对照品溶液,以信噪比S/N=3为检测限,S/N=10为定量限。结果,三七皂苷R1检测限、 定量限分别为 2.448、 8.606 μg/mL,人参皂苷Rg1分别为0.628、 3.580 μg/mL, 人参皂苷 Re 分别为 3.720、 13.953 μg/mL、 人参皂苷Rb1分别为 0.102、 27.151 μg/mL。
2.3.4 精密度试验 精密吸取对照品溶液各10 μL, 在 “2.3.1” 项色谱条件下进样测定 6次[16], 测得三七皂苷 R1、 人参皂苷 Rg1、 人参皂苷Re、人参皂苷Rb1峰面积RSD[17]分别为1.4%、1.2%、1.2%、0.9%,表明仪器精密度良好。
2.3.5 稳定性试验 精密称取批号170502样品0.5 g,按 “2.3.2.2”项下方法制备供试品溶液,于0、 4、 8、 12、 24、 48 h在 “2.3.1” 项色谱条件下进样10 μL测定[18],测得三七皂苷R1、人参皂苷Rg1、人参皂苷Re、人参皂苷Rb1峰面积RSD分别为1.6%、1.5%、1.5%、0.9%,表明溶液在48 h内稳定性良好。
2.3.6 重复性试验 精密称取批号170502样品6份,每份0.5 g,按 “2.3.2”项下方法制备供试品溶液,在 “2.3.1” 项色谱条件下进样测定[19],测得三七皂苷R1、人参皂苷 Rg1、人参皂苷 Re、人参皂苷Rb1含有量RSD分别为1.4%、1.5%、13%、0.8%,表明该方法重复性较好。
2.3.7 加样回收率试验 精密称取批号170529样品6份,每份0.25 g,精密加入含三七皂苷 R1、人参皂苷Rg1、人参皂苷Re、人参皂苷Rb11 982、4 054、 3 564、 3 784 μg/mL 的对照品溶液 0.2 mL及甲醇24.8 mL,按 “2.3.2”项下方法制备供试品溶液,在 “2.3.1”项色谱条件下进样测定,计算回收率,结果见表3。

表3 各成分加样回收率试验结果 (n=6)Tab.3 Results of recovery tests for various constituents(n=6)
2.3.8 样品含有量测定 将 3批样品[13]按“2.3.2”项下方法制备供试品溶液,在 “2.3.1”项色谱条件下进样测定[9],计算含有量,结果见表4。然后,按三七皂苷R1、人参皂苷Rg1、人参皂苷Re、人参皂苷Rb1平均含有量的80%设限,分别为0.30、1.60、1.30、3.00 mg/粒,拟规定样品中[5,18]含西洋参、三七量以各成分总含有量计,不得少于6.0 mg/粒。

表4 各成分含有量测定结果 (n=3)Tab.4 Results of content determination of various constituents(n=3)
3 讨论
3.1 TLC条件筛选 川芎的TLC条件参照2015年版 《中国药典》,采用乙醚回流提取作为提取方法;比较了硅胶G预制薄层板、硅胶H预制薄层板、高效硅胶G预制薄层板 (青岛海洋化工厂)上,发现高效硅胶G板虽然斑点较清晰,但Rf值相对其他2种板稍逊,综合考虑选择硅胶G板作为点样薄层板;考察了不同展开系统,最终采用正己烷-乙酸乙酯 (3∶1),此时斑点清晰,分离度好,Rf值适宜; 比较了点样2、5、 8、10 μL, 发现点样5 μL时斑点清晰可见,分离度良好,无拖尾现象;样品放置24 h后再点样,发现斑点仍清晰可见,表明稳定性较好;温度、湿度对川芎TLC定性鉴别的影响不显著,两者分别在15~22℃、38%~65%范围内时薄层层析结果稳定,斑点清晰。
赤芍的TLC条件参照2015年版 《中国药典》,采用乙醇超声作为提取方法;比较了硅胶G预制薄层板 (青岛海洋化工厂、德国MN公司)、高效硅胶G预制薄层板 (青岛海洋化工厂),发现均能得到较好分离,主斑点清晰,其中MN硅胶G板的斑点清晰度优于青岛海洋硅胶G板,但Rf值较低,而后者虽然斑点略散,但Rf值较适中,故选择青岛海洋硅胶G板作为点样薄层板;比较了不同展开系统,最终采用三氯甲烷-乙酸乙酯-甲醇-甲酸(40∶5∶20∶0.5),此时斑点清晰,分离度好,Rf值适宜; 比较了点样2、5、8、10 μL, 发现点样8 μL斑点清晰可见,分离度良好,无拖尾现象;样品放置24 h后点样,发现斑点仍清晰可见,表明稳定性较好;温度、湿度对赤芍TLC定性鉴别的影响不显著,两者分别在15~22℃、38%~65%范围内时薄层层析结果稳定,斑点清晰。
西洋参、三七的TLC条件参考了2015年版《中国药典》,由于前者含有拟人参皂苷F11,为其特异性成分,同时2种药材中共有成分较多,以三七皂苷R1、人参皂苷Rg1、人参皂苷Re、人参皂苷Rb1相对含有量较高,故选择上述5种成分进行实验;考察了不同提取方法,最终采用甲醇回流蒸干→加水溶解→正丁醇萃取→水洗作为提取方法;比较了硅胶G预制薄层板、硅胶H预制薄层板、高效硅胶G预制薄层板 (青岛海洋化工厂),发现对照品在硅胶G、硅胶H板上均不能完全分离,而在高效硅胶G板上有较好分离,主斑点清晰,故选择其作为点样薄层板;比较了不同展开系统,最终采用三氯甲烷-无水乙醇-水 (20∶20∶2);比较了点样2、 5、 8、 10 μL, 发现点样 5 μL时斑点清晰可见,分离度良好,无拖尾现象;样品放置24 h后点样,发现斑点然清晰可见,表明稳定性较好。温度、湿度对人参皂苷类成分TLC定性鉴别的影响较大,两者分别在20℃以下、低于50%时薄层层析结果稳定,斑点清晰。
3.2 HPLC条件筛选 参考2015年版 《中国药典》,分别放置过夜、1 h后再回流提取,发现两者无明显区别,故确定提取方法为取样后加甲醇静置1 h,80℃水浴下回流2 h,此时供试品溶液提取充分,简便易行;以出峰数、相邻对照品色谱峰之间的分离度为主要指标,优化色谱柱、柱温、流动相、梯度洗脱程序、检测波长,最终确定“2.3.1” 项下色谱条件[20]。

