中西药合用治疗慢性乙型病毒性肝炎疗效观察
朱豫萌,朱丹燕,张国强
(郑州大学附属洛阳中心医院感染科,河南 洛阳 471003)
慢性乙肝指乙肝病毒检测为阳性,但病程超过半年或发病日期不明确且临床具有慢性肝炎表现[1]。临床多表现为失眠、多梦、腹胀、肝区疼痛等症状,病情迁延后可能会出现肝大、肝纤维化,质地变硬且痛感加剧等。慢性乙肝并发症较多,如脂肪肝、糖尿病、红素血症等,严重影响生活及健康[2-3]。本研究以中西药合用治疗慢性乙型病毒性肝炎取得较好效果,现报道如下。
1 临床资料
共126例,均为2016年12月至2018年12月我院收治的慢性乙型病毒性肝炎患者,按随机数表法分为对照组和观察组各63例。观察组男33例,女30例;年龄39~68岁,平均(54.33±7.62)岁;病情轻度28例,中度30例,重度5例。对照组男32例,女31例;年龄40~69岁,平均(55.07±8.01)岁;病情轻度27例,中度32例,重度4例。两组一般资料比较差异无统计学意义(P>0.05),具有可比性。
纳入标准:①符合西医2015版《慢性乙型肝炎防治指南》[4]中的慢性乙型病毒性肝炎诊断标准。②符合2018版《慢性乙型肝炎中医诊疗指南》[5]中的湿热内蕴证诊断标准,主症为热势缠绵,午后热高,身重疲乏,胸脘痞满,大便黏腻不爽,小便黄赤;次症为神志昏沉,胸脘痞满,不思饮食,小便不利,大便黏腻不爽;舌脉为舌质红,舌苔黄腻,脉沉弦。③了解本研究详情后患者本人及家属同意并签字确认。
排除标准:①恶性肿瘤及急性肝炎;②对本研究中使用药物过敏。
2 治疗方法
两组均给予常规护理,包括保持愉快、增强信心、合理饮食、适量运动等。恩替卡韦(长治市三宝生化药业有限公司生产,国药准字H20173327)口服,日1次,每次0.5mg;异甘草酸镁注射液(江苏正大天晴药业股份有限公司生产,国药准字H20140092)0.1g,溶于10%葡萄糖溶液250mL,静脉滴注,日1次,剂量根据病情遵医嘱调整为每次0.2g。
观察组加用参芪肝康片(江苏黄河药业股份有限公司,国药准字Z20080109)2.1g,口服,日3次,剂量可根据具体病情遵医嘱调整。
两组观察周期均为3个月。
3 观察指标
免疫功能:采用FACSCantoII流式细胞仪检测T细胞(亚群)指标,包括:CD3+、CD4+、CD8+。
肝纤维化:采用放射免疫检测法检测HA(透明质酸)、LN(层粘蛋白)、PCⅢ(血清Ⅲ型前胶原)。
肝功能及乙型肝炎标志物:采用放射免疫检测法测定治疗前后谷丙转氨酶(ALT)、谷草转氨酶(AST)、总胆红素(TBIL)、白/球(A/G)、白蛋白(ALB)及白细胞介素-2(IL-2)水平变化。
血常规:使用全自动血细胞分析仪(桂林优利特医疗电子有限公司,桂食药监械(准)字2009第2400166号)测定白细胞(WBC)、血小板(PLT)、红细胞计数(RBC)、血红蛋白(HB)、中性粒细胞计数(NEUT)水平变化。
肾功能:使用免疫层析法测定血肌酐(SCR)、尿素氮(BUN)、24h尿蛋白定量(24hUpro)水平变化。
HBsAg、HBeAg、HBV-DNA定量情况:选择乙型肝炎病毒(HBV)核酸(DNA)检测试剂盒[东北制药集团沈阳第一制药厂,国食药监械(准)字2013第3401853号]使用荧光探针法测定HBsAg、HBeAg、HBV-DNA定量变化。
肝脾变化:使用EK-7000系列影像工作站[徐州亿康电子科技有限公司生产,苏食药监械(准)字2011第2210551号]测定肝表面粗糙、边缘圆钝、肝实质颗粒、结节及脾肿大变化情况。
不良反应:包括过敏性休克、肺水肿、荨麻疹、胸闷气急。
4 疗效标准
显效:肝区疼痛、乏力等临床症状完全消失,肝功能检查示谷丙转氨酶及谷草转氨酶降至正常范围。有效:肝区疼痛、乏力等临床症状明显好转,肝功能检查示谷丙转氨酶及谷草转氨酶下降40%~85%,且谷草转氨酶小于谷丙转氨酶。无效:临床症状无改善,肝功能检查未变化甚至增加,病情加重。
5 治疗结果
两组临床疗效见表1。
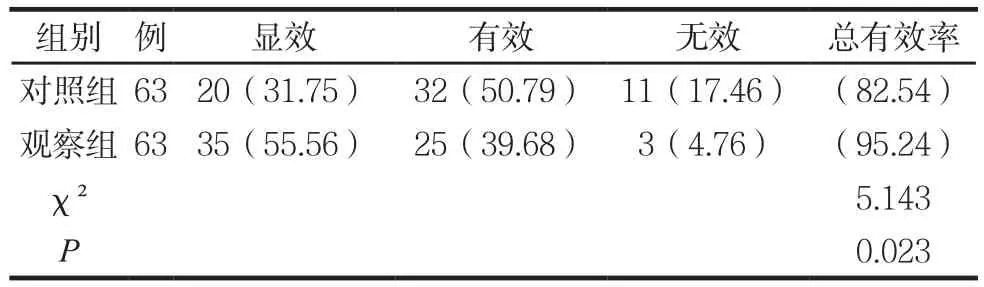
表1 两组临床疗效比较 例(%)
两组治疗前后免疫功能指标比较见表2。
表2 两组治疗前后免疫功能指标比较 (±s)
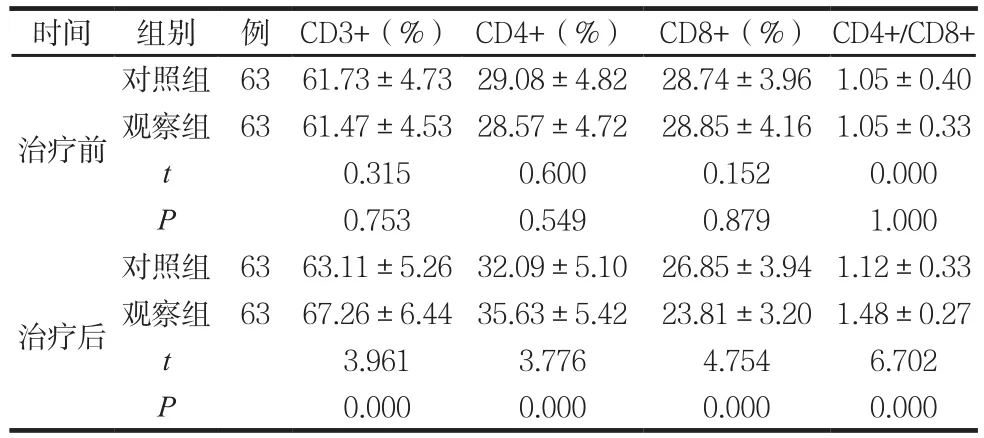
表2 两组治疗前后免疫功能指标比较 (±s)
两组治疗前后肝纤维化指标比较见表3。
时间 组别 例 CD3+(%) CD4+(%) CD8+(%) CD4+/CD8+治疗前对照组 63 61.73±4.73 29.08±4.82 28.74±3.96 1.05±0.40观察组 63 61.47±4.53 28.57±4.72 28.85±4.16 1.05±0.33 t 0.315 0.600 0.152 0.000 P 0.753 0.549 0.879 1.000治疗后对照组 63 63.11±5.26 32.09±5.10 26.85±3.94 1.12±0.33观察组 63 67.26±6.44 35.63±5.42 23.81±3.20 1.48±0.27 t 3.961 3.776 4.754 6.702 P 0.000 0.000 0.000 0.000
表3 两组治疗前后肝纤维化指标比较 (ng/mL,±s)
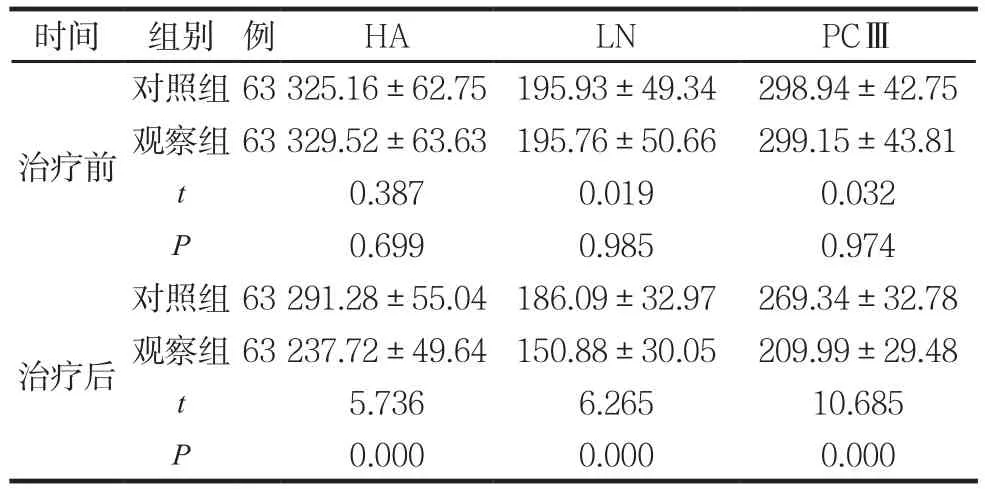
表3 两组治疗前后肝纤维化指标比较 (ng/mL,±s)
时间 组别 例 HA LN PCⅢ治疗前对照组 63 325.16±62.75 195.93±49.34 298.94±42.75观察组 63 329.52±63.63 195.76±50.66 299.15±43.81 t 0.387 0.019 0.032 P 0.699 0.985 0.974治疗后对照组 63 291.28±55.04 186.09±32.97 269.34±32.78观察组 63 237.72±49.64 150.88±30.05 209.99±29.48 t 5.736 6.265 10.685 P 0.000 0.000 0.000
两组治疗前后肝功能及乙型肝炎标志物指标比较见表4。
表4 两组治疗前后肝功能及乙型肝炎标志物指标比较 (±s)
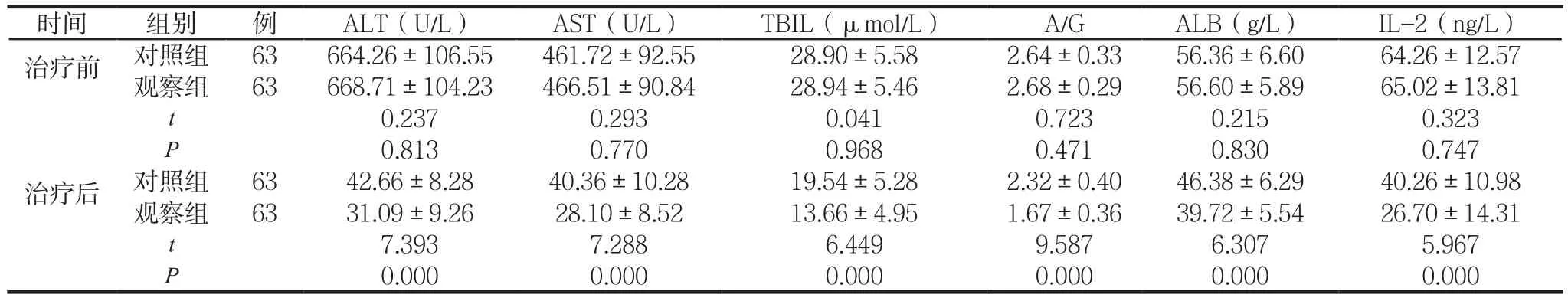
表4 两组治疗前后肝功能及乙型肝炎标志物指标比较 (±s)
时间 组别 例 ALT(U/L) AST(U/L) TBIL(μmol/L) A/G ALB(g/L) IL-2(ng/L)治疗前 对照组 63 664.26±106.55 461.72±92.55 28.90±5.58 2.64±0.33 56.36±6.60 64.26±12.57观察组 63 668.71±104.23 466.51±90.84 28.94±5.46 2.68±0.29 56.60±5.89 65.02±13.81 t 0.237 0.293 0.041 0.723 0.215 0.323 P 0.813 0.770 0.968 0.471 0.830 0.747治疗后 对照组 63 42.66±8.28 40.36±10.28 19.54±5.28 2.32±0.40 46.38±6.29 40.26±10.98观察组 63 31.09±9.26 28.10±8.52 13.66±4.95 1.67±0.36 39.72±5.54 26.70±14.31 t 7.393 7.288 6.449 9.587 6.307 5.967 P 0.000 0.000 0.000 0.000 0.000 0.000
两组治疗前后血常规指标比较见表5。
表5 两组治疗前后血常规指标比较 (109/L,±s)
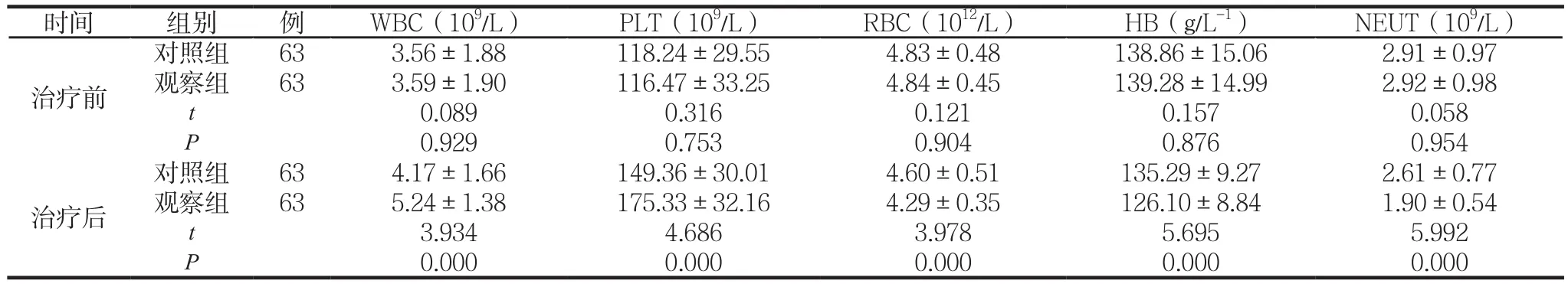
表5 两组治疗前后血常规指标比较 (109/L,±s)
时间 组别 例 WBC(109/L) PLT(109/L) RBC(1012/L) HB(g/L-1) NEUT(109/L)治疗前对照组 63 3.56±1.88 118.24±29.55 4.83±0.48 138.86±15.06 2.91±0.97观察组 63 3.59±1.90 116.47±33.25 4.84±0.45 139.28±14.99 2.92±0.98 t 0.089 0.316 0.121 0.157 0.058 P 0.929 0.753 0.904 0.876 0.954治疗后对照组 63 4.17±1.66 149.36±30.01 4.60±0.51 135.29±9.27 2.61±0.77观察组 63 5.24±1.38 175.33±32.16 4.29±0.35 126.10±8.84 1.90±0.54 t 3.934 4.686 3.978 5.695 5.992 P 0.000 0.000 0.000 0.000 0.000
两组治疗前后肾功能指标比较见表6。
表6 两组治疗前后肾功能指标比较 (±s)
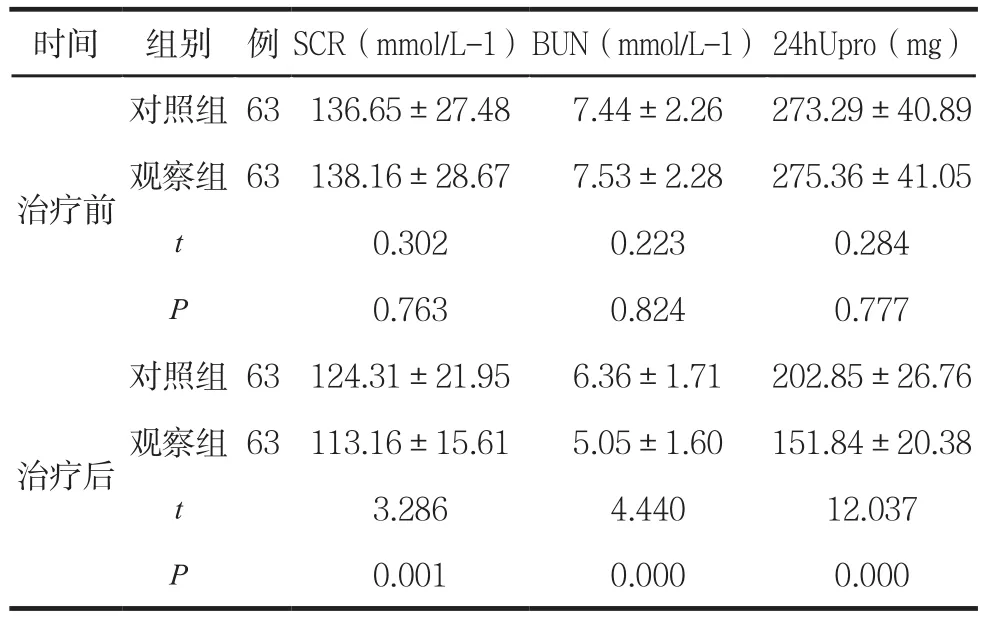
表6 两组治疗前后肾功能指标比较 (±s)
时间 组别 例 SCR(mmol/L-1)BUN(mmol/L-1)24hUpro(mg)治疗前对照组 63 136.65±27.48 7.44±2.26 273.29±40.89观察组 63 138.16±28.67 7.53±2.28 275.36±41.05 t 0.302 0.223 0.284 P 0.763 0.824 0.777治疗后对照组 63 124.31±21.95 6.36±1.71 202.85±26.76观察组 63 113.16±15.61 5.05±1.60 151.84±20.38 t 3.286 4.440 12.037 P 0.001 0.000 0.000
两组治疗前后HBsAg、HBeAg、HBV-DNA定量比较见表7。
表7 两组治疗前后HBsAg、HBeAg、HBV-DNA定量比较 (±s)
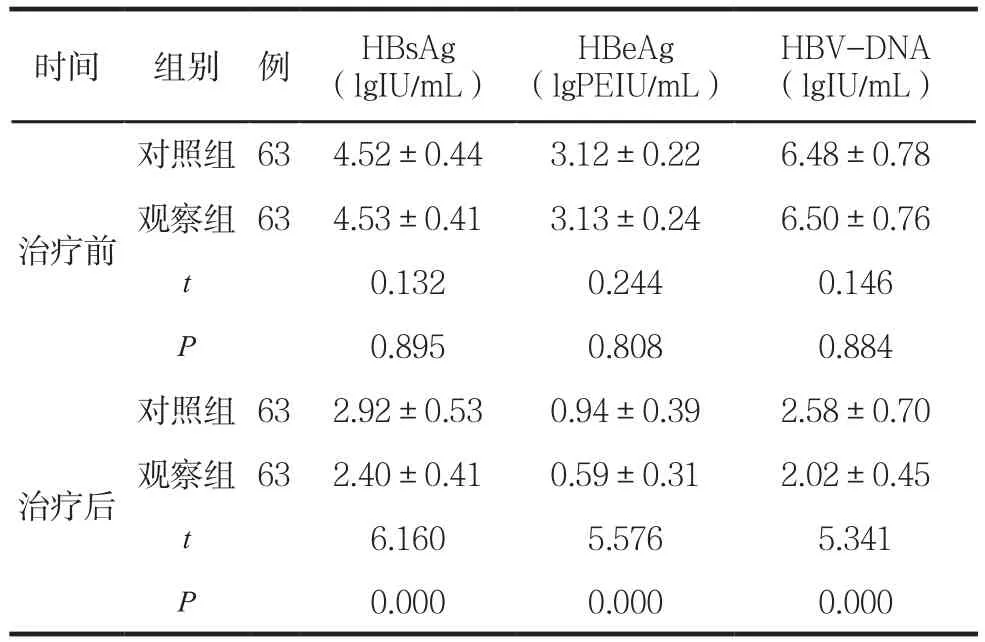
表7 两组治疗前后HBsAg、HBeAg、HBV-DNA定量比较 (±s)
时间 组别 例 HBsAg(lgIU/mL)HBeAg(lgPEIU/mL)HBV-DNA(lgIU/mL)治疗前对照组 63 4.52±0.44 3.12±0.22 6.48±0.78观察组 63 4.53±0.41 3.13±0.24 6.50±0.76 t 0.132 0.244 0.146 P 0.895 0.808 0.884治疗后对照组 63 2.92±0.53 0.94±0.39 2.58±0.70观察组 63 2.40±0.41 0.59±0.31 2.02±0.45 t 6.160 5.576 5.341 P 0.000 0.000 0.000
两组治疗后B超检查肝脾比较见表8。
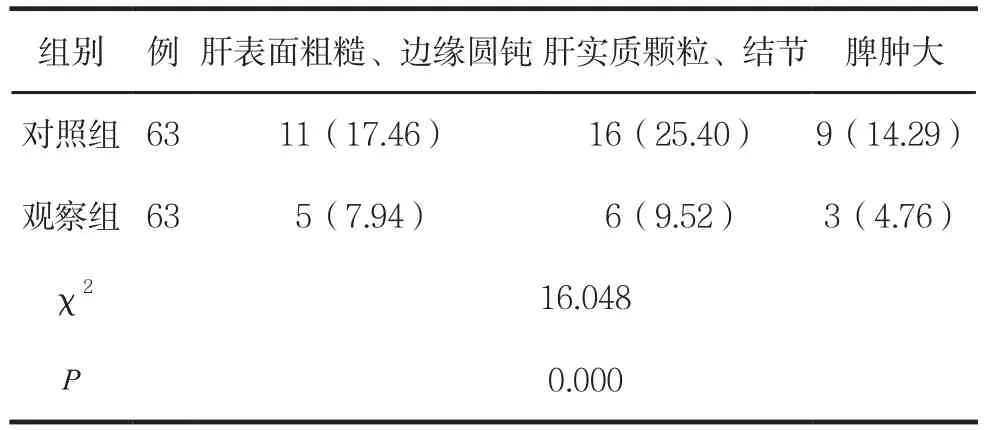
表8 两组治疗后B超检查肝脾比较 例(%)
两组不良反应比较见表9。
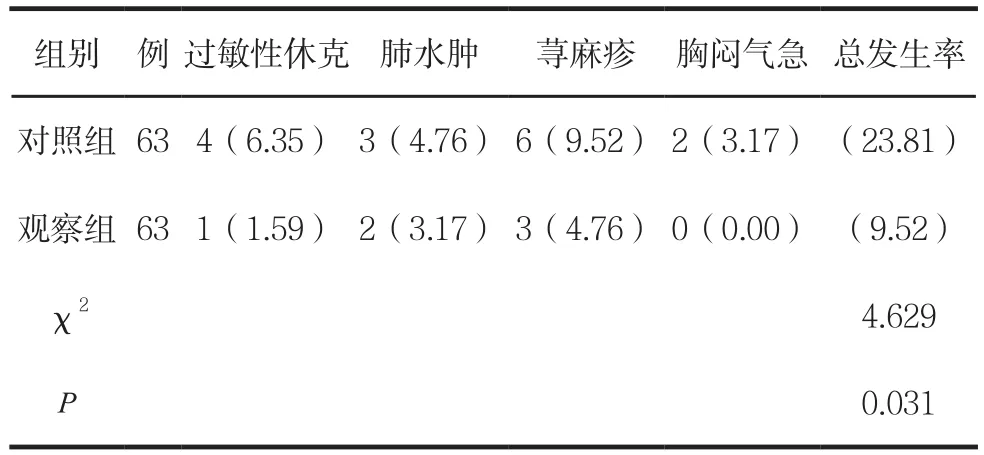
表9 两组不良反应比较 例(%)
6 讨 论
慢性乙型病毒性肝炎是由肝炎病毒传染所致,其传染性强弱由病毒DNA数值决定。发病后,肝脏细胞受到损伤,从而影响蛋白质及脂肪消化能力,降低胆汁分泌,促使血液中胆红素聚积,导致血流不畅,形成水肿、腹水。此外,肝脏解毒能力减弱,易受到毒素影响,诱发毒血症等疾病。HBV是引起肝硬化、重型肝炎及HCC的常见因素,病毒性肝炎较为典型的临床表现是抑制骨髓造血功能,因此,血常规检查中各项数据可以作为疾病诊断与疗效判定的参考指标。
临床常用恩替卡韦及异甘草酸镁治疗,其中恩替卡韦为鸟嘌呤核苷类似物,通过抑制乙肝病毒中逆转录酶的活性起到抗病毒作用。异甘草酸镁作为肝细胞保护剂,通过抑制血清转氨酶升高达到减轻肝细胞坏死程度,且异甘草酸镁可有效降低NO水平,避免纤维化加剧。但恩替卡韦及异甘草酸镁不良反应较多,且对免疫功能提高较小。
中医通过辨证论治,可改善慢性乙肝临床症状,提高体质,增强抗病能力,促进免疫系统清除病毒,从而达到治疗的目的[6-7]。慢性乙肝常见湿热内蕴证,湿热蕴于中焦脾胃及肝胆,导致气机运行受阻。治疗应祛湿清热,调和肝脾。本研究结果显示,观察组总有效率及CD3+、CD4+、CD4+/CD8+指标及WBC、PLT、HBeAg阴转率、抗-Hbe阳转率、HBV-DNA阴转率均高于对照组,不良反应总发生率、CD8+、HA、LN、PCⅢ、ALT、AST、TBIL、A/G、ALB、IL-2、RBC、HB、NEUT、SCR、BUN、24hUpro、肝表面粗糙、边缘圆钝、肝实质颗粒、结节脾肿大面积指标均低于对照组。与对照组相比,观察组治疗有效率高,不良反应发生率低,免疫系统及肝纤维化改善幅度大,表明在西药治疗基础上加用参芪肝康片治疗对改善免疫功能、肝功能等意义重大。参芪肝康片方中茵陈味苦辛性微寒,归脾、胃、肝、胆经,清利湿热,利胆退黄;党参味甘性平,归脾、肺经,补中益气,养血生津;五味子味甘性温,归肺、心、肾经,收敛固涩,益气生津;水飞蓟味苦性凉,归肝、胆经,清热利湿,疏肝利胆,可达保肝降脂之功效;当归味甘性温,归肝、心、脾经,补血活血,调经止痛;刺五加浸膏益气健脾,补肾安神。诸药共用,可达调肝祛湿、清热安神之功。药理研究发现,茵陈化学成分含有黄酮及香豆素,可有效抑制肝细胞损伤,此外茵陈还具有抗凝及促进纤维蛋白溶解作用,且具有一定解热、利胆、降压、抗菌功效。
综上所述,参芪肝康片联合西药治疗慢性乙型病毒性肝炎可提高治疗效果,增加用药安全性,改善免疫功能,抑制肝纤维化,有利于改善预后。

