L-鸟氨酸发酵液的脱色研究
吴 昊,焦志勇,郝 宁,许 晟
(1.南京工业大学生物与制药工程学院,江苏南京211800; 2.江苏先进生物与化学制造协同创新中心,江苏南京210009)
L-鸟氨酸又名α,δ-二氨基戊酸,分子式为C5H12N2O2,它是重要的碱性氨基酸,主要参与鸟氨酸循环(尿素循环),用于生物体内瓜氨酸、精氨酸、脯氨酸及多胺的生物合成,对于体内氨态氮的排出有重要作用[1]。L-鸟氨酸及其衍生物具有保肝护肝、健脑、解毒、抑制癌细胞、促进生长和减肥等多重医学与保健作用[2],L-鸟氨酸产品在医药、保健领域中的应用日益广泛。目前微生物发酵直接制备L-鸟氨酸已经逐渐成为L-鸟氨酸的主要生产方法[3-4],但是与传统的酶水解精氨酸法相比,L-鸟氨酸发酵液中含有大量的色素,高效脱除其中的色素对保证产品质量至关重要。
目前,L-鸟氨酸的提取过程中往往将超滤处理后的发酵液经过离子交换吸附其中的L-鸟氨酸,通过氨水解吸获得含有L-鸟氨酸的洗脱液,将其浓缩后进行酸化结晶,再对粗晶体溶解后加入粉末活性炭进行脱色,脱色液再次结晶获得色泽合格的产品[5-6]。在此过程中,由于离子交换树脂对色素具有明显的吸附作用,影响了树脂的分离效率,同时氨水解吸会将吸附的色素与L-鸟氨酸几乎同时洗脱,增加了后期的纯化压力和分离损失[7]。尽管有文献报道通过纳滤膜分离可将L-鸟氨酸发酵液中的大部分色素拦截[8],但膜污染也比较严重,导致通量迅速衰减,同时纳滤膜对L-鸟氨酸也具有一定的拦截损失。
针对以上问题,本文中,笔者以颗粒活性炭为脱色剂,开展L-鸟氨酸发酵液的脱色研究,考察多种因素对脱色效果的影响,在此基础上建立活性炭动态脱色与再生工艺。
1 材料与方法
1.1 实验仪器
DSHZ-300A型台式水浴恒温振荡器,江苏太仓市实验设备厂;BT01-100M型蠕动泵,保定兰格恒流泵有限公司;pHS-3C型精密pH计,上海雷磁仪器厂;Ultimate 3000型高效液相色谱仪,美国Dionex公司;紫外-可见光分光光度计,上海棱光技术有限公司;玻璃层析柱,晚晴化玻仪器有限公司。
1.2 原料与试剂
采用精氨酸缺陷型谷氨酸棒杆菌Corynebacteriumglutamicum1006(CGMCC No.3663)制备L-鸟氨酸发酵液,发酵液经过离心和超滤处理后为棕黄色透明液体,pH=6.7,其中含L-鸟氨酸34 g/L、L-谷氨酸0.22 g/L、L-丙氨酸0.67 g/L、L-甘氨酸0.79 g/L、葡萄糖0.5 g/L,南京工业大学郝宁课题组提供。
大孔非极性吸附树脂(HZ-802、HZ830)、大孔弱极性吸附树脂(HZ-818)、大孔中等极性吸附树脂(HZ-806),上海华震科技有限公司;大孔弱极性吸附树脂AB-8,南开大学化工厂。
颗粒活性炭JL、GH、ZS、ZX-N分别由苏州佳联、唐山光华晶科、溧阳竹溪等活性炭生产企业提供(均筛选至0.38~0.54 mm);H2SO4、NaOH、NaNO3均为分析纯,上海凌峰化学试剂有限公司;L-鸟氨酸标准品,Sigma试剂公司。检测中所使用的其他试剂均为色谱纯或分析纯,国药集团化学试剂有限公司,
1.3 实验方法
1.3.1 树脂吸附色素性能考察
将大孔吸附树脂用2倍体积的无水乙醇浸泡2 h,使其充分溶胀。过滤后,再用3~4倍体积的去离子水浸泡树脂,并不时搅动,通过多次过滤,将乙醇完全置换出即可使用。将经过超滤处理的L-鸟氨酸发酵液调节至pH 5.0,分别取30 mL,加入3 g吸附树脂,置于恒温水浴振荡器中,以150 r/min振荡吸附4 h。过滤后,根据样品检测结果,计算出大孔吸附树脂对色素的脱除率及L-鸟氨酸的脱色损失。
1.3.2 活性炭静态脱色试验
取经过超滤处理的L-鸟氨酸发酵液100 mL,调节至设定的pH,加入一定量的活性炭(0.38~0.54 mm),在一定温度下,置于恒温水浴振荡器中,以150 r/min振荡脱色一定时间,使其对色素的吸附达到平衡。过滤后根据样品检测结果,计算出活性炭对色素的吸附容量、脱色率及L-鸟氨酸的脱色损失。
1.3.3 活性炭动态脱色试验
在玻璃层析柱中填装16.5 g颗粒活性炭(0.38~0.54 mm),活性炭床层直径为1.52 cm,床层高度为27.5 cm,高径比为18,床层填充体积为50 mL,将其设定为1倍床层体积(1.0 BV),作为考察动态脱色流出曲线的体积计量单位。将L-鸟氨酸发酵液预热到70 ℃,按照一定的流速经蠕动泵通入活性炭层析柱,并自上而下流出层析柱,每间隔一定体积,对流出的脱色液进行取样分析,绘制出流出曲线。
1.3.4 检测方法
L-鸟氨酸的定量检测采用异硫氰酸苯酯(PITC)柱前衍生化法,用高效液相色谱法(HPLC)测定,具体方法见文献[9]。
料液中的色素含量采用分光光度法检测,以纯水作参比,黄色素在430 nm波长下有较好的吸收峰,故以超滤处理后的发酵液浓缩至1/3体积时的吸光值A430作为基准,设定该基准液的色素含量为ca=1.0 U/mL,在不同稀释倍数下,根据分光光度计的吸光值表征色素含量的高低,建立色素含量的函数关系,对发酵液中色素的含量进行相对定量测定[10]。根据绘制的色素标准曲线拟合得到回归方程为c=0.894 17A+0.003 24,R2=0.999 88,线性关系显著,可用于表征色素含量。
料液的透光率T430,在430 nm下采用分光光度计检测,以纯水为参比,标定为T430=100%。
活性炭比表面积及孔容孔径的测试,采用BET方程计算比表面积,t值法计算外表面积和孔容积,密度函数理论(DFT)计算样品的孔径分布。
活性炭零电荷点pHPZC(水溶液中固体表面净电荷为零时的pH)的检测采用质量滴定法[11]。首先将2 g经过去离子水洗至中性并干燥的活性炭加入50 mL的0.05 mol/L NaNO3溶液中(pH为7.0),用N2吹扫脱除其中的CO2,将瓶口密封后在25 ℃下振荡48 h后测定其pH作为pHPZC0,随后将多份50 mL的0.05 mol/L NaNO3溶液均调节至该pH,并分别加入0.05、0.25、0.5、1.0、2.5和5.0 g活性炭,按以上方法振荡48 h后检测pH,直至pH不变为止,将该pH作为pHPZC。
1.4 活性炭脱色性能与再生效果的计算
吸附容量的计算见式(1)。
Qi=(ci0V0-ci1V1)/m
(1)
式中:Qi为吸附剂对组分i的吸附容量,ci0、ci1为发酵液和脱色液中组分i的浓度,V0、V1为发酵液和脱色液的体积,m为活性炭的质量。
脱色率(损失率)的计算见式(2)。
脱色率(损失率)=(ci0V0-ci1V1)/(ci0V0)×100%
(2)
活性炭再生率的计算见式(3)。
活性炭再生率=Q1/Q0×100%
(3)
式中:Q1为再生后的活性炭对色素吸附容量,Q0为新活性炭对色素的吸附容量。
2 结果与讨论
2.1 吸附树脂对色素的吸附选择性及色素性质的确定
取预处理好的树脂各3.0 g,分别加入30 mL发酵液,在20 ℃、150 r/min的条件下振荡吸附4 h,考察其对色素的脱除效果,结果见图1。
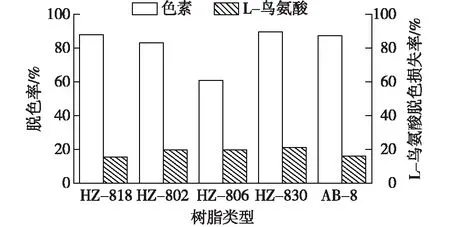
图1 不同树脂对色素的吸附性能比较Fig.1 Decoloration performance of different resins
由图1可见,非极性和弱极性吸附树脂对色素的吸附能力均强于中等极性吸附树脂HZ-806,这些现象说明L-鸟氨酸发酵液中的大部分色素可能属于非极性或弱极性分子[12]。由于大孔吸附树脂在吸附色素时,L-鸟氨酸的脱色损失较大,因此不适合用吸附树脂进行脱色处理。
2.2 脱色用颗粒活性炭的选择
向L-鸟氨酸发酵液中分别加入数种颗粒活性炭进行脱色性能的比较,脱色条件为 pH 6.5,活性炭添加量为5 g/L,在60 ℃、150 r/min条件下振荡脱色40 min,结果见图2。
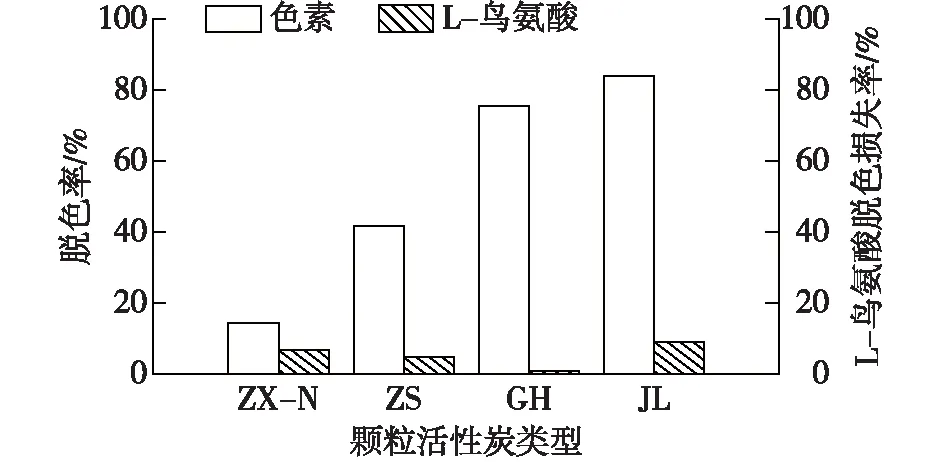
图2 活性炭脱色性能的比较Fig.2 Decolorization performance of different activated carbons
由图2可见,在pH 6.5下,颗粒活性炭JL与GH的脱色率明显高于其他颗粒活性炭活性炭。
为了分析相关颗粒活性炭脱色性能差异的原因,对各种颗粒活性炭的物理结构与零电荷点pHPZC进行了检测,结果见表1。
由表1可知:前3种颗粒活性炭的比表面积均明显高于脱色性能最弱的颗粒活性炭ZX-N,说明较大的比表面积有利于活性炭吸附色素,但比表面积最大的GH所具有的脱色性能不如JL,可见比表面积并非衡量活性炭脱色潜力的唯一因素。活性炭的脱色性能随着平均孔径和活性炭的比孔容的增加而提高。这可能是由于色素分子的吸附存在尺寸排斥效应,活性炭对色素的吸附选择性会受到孔径-孔容分布状况的影响[13]。当活性炭孔径与被吸附质分子直径的比值为1.7~3时最有利于吸附[14],大多数水溶性有机物的直径为1~3 nm[15],因此平均孔径为3.447 nm的JL活性炭吸附色素能力更强,但其脱色损失也最高。由于颗粒活性炭GH的脱色损失率仅为0.78%,故选择此活性炭进行后续脱色研究。
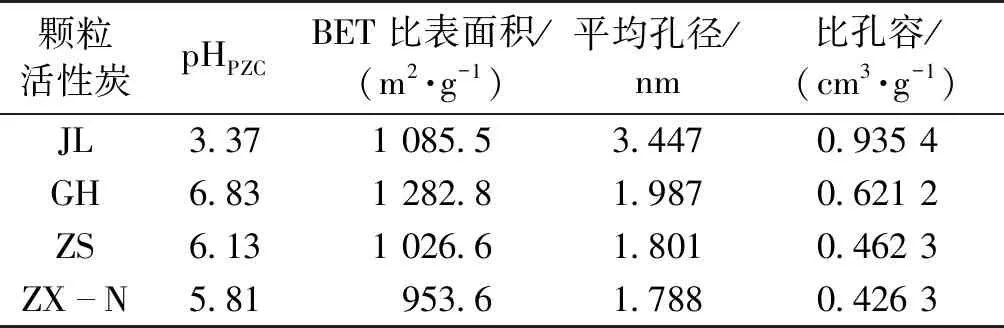
表1 活性炭的物理结构与零电荷点
2.3 pH对活性炭脱色性能的影响
为了避免酸性料液对管线设备的腐蚀,着重考察活性炭在较高pH下的脱色性能。分别将L-鸟氨酸发酵液调节至pH 6.0~7.0进行脱色,活性炭添加量为5 g/L,在60 ℃、150 r/min条件下,振荡脱色40 min,结果见图3。
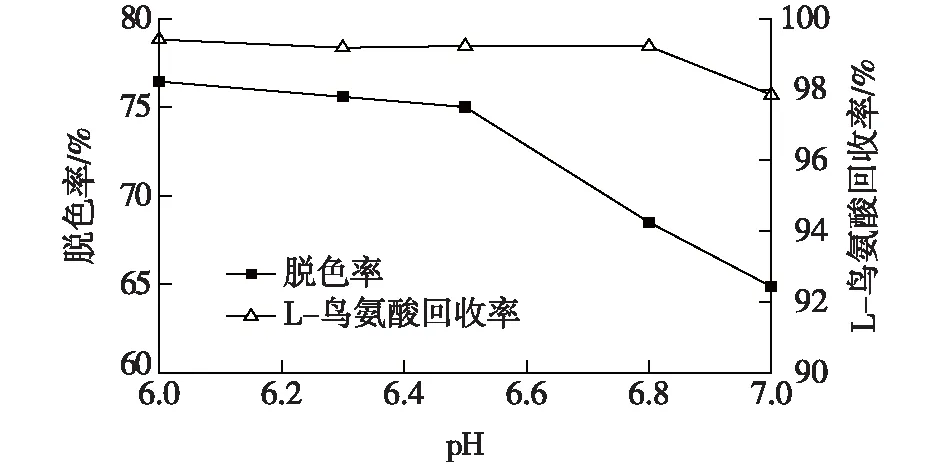
图3 pH对活性炭脱色性能的影响Fig.3 Effects of pH on decolorization of activated carbon
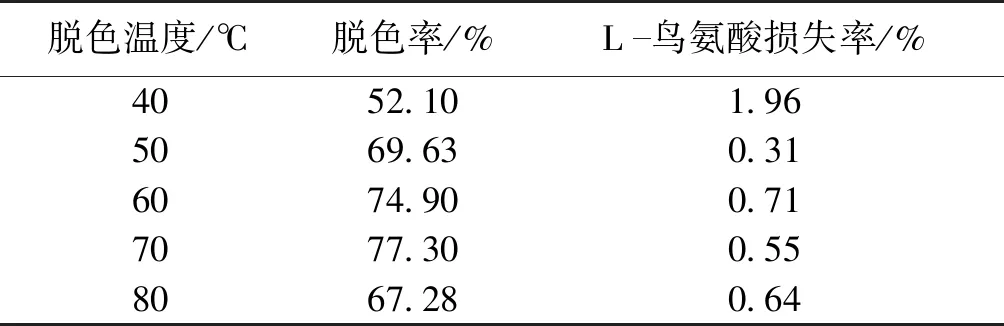
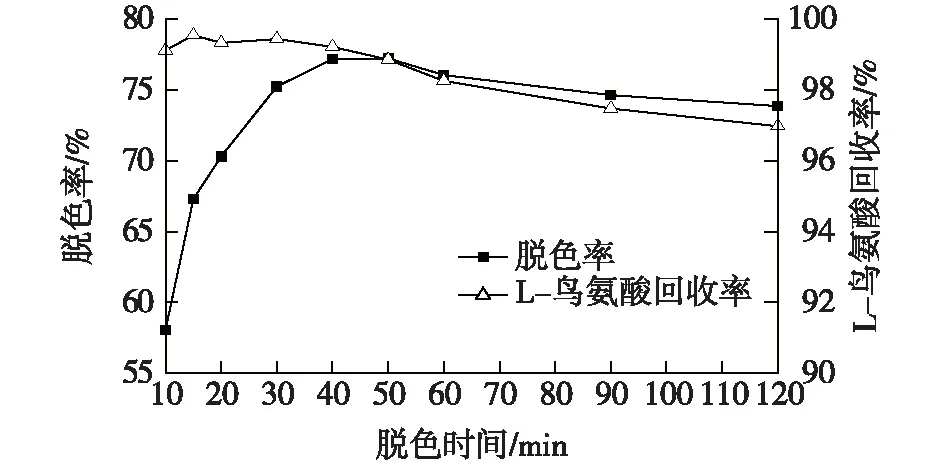
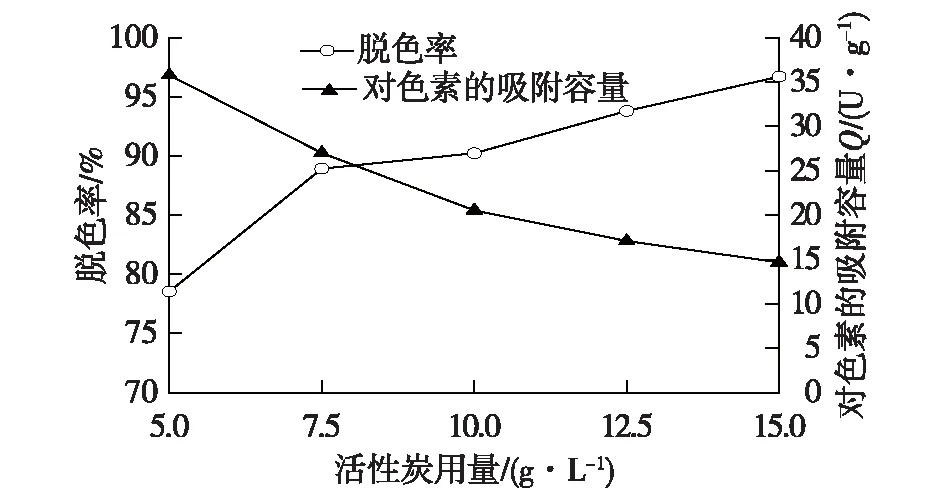
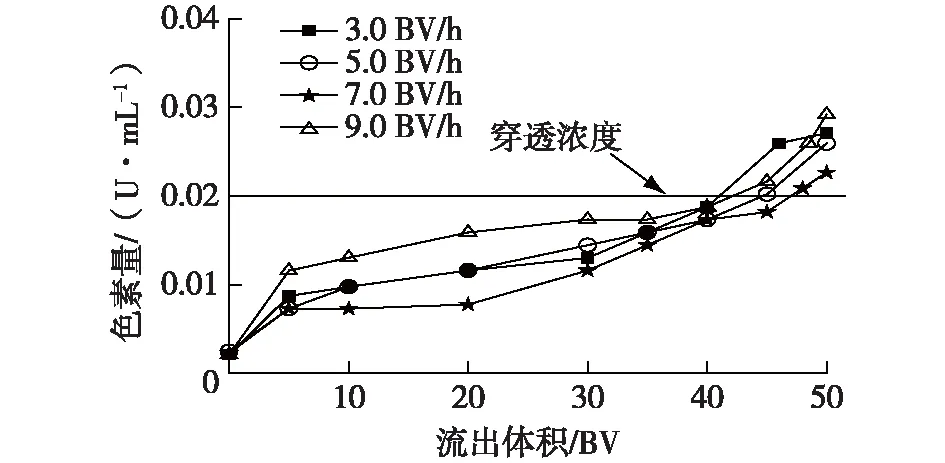
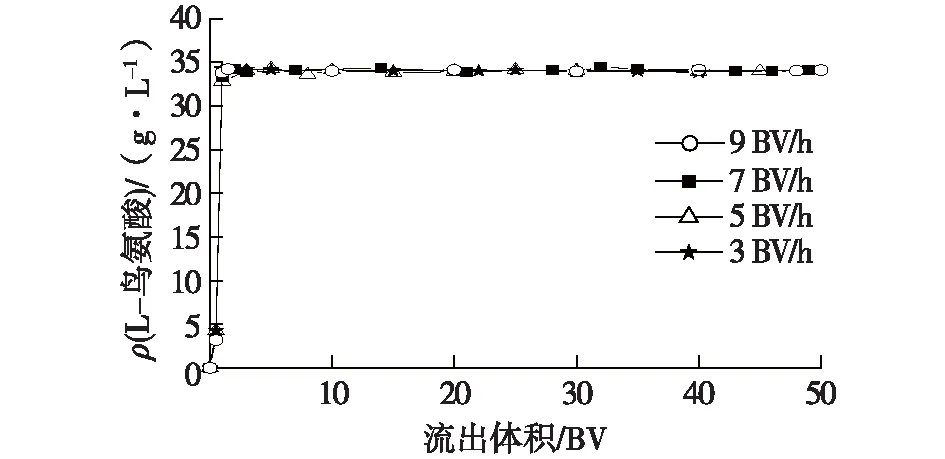
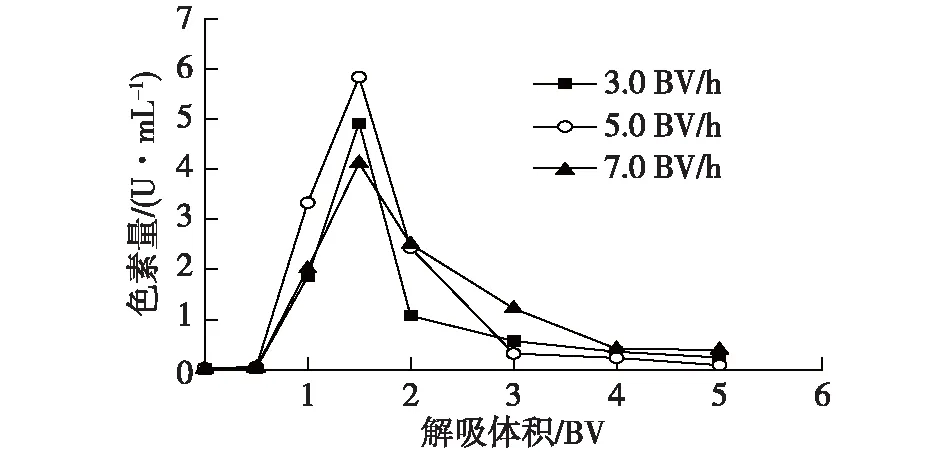
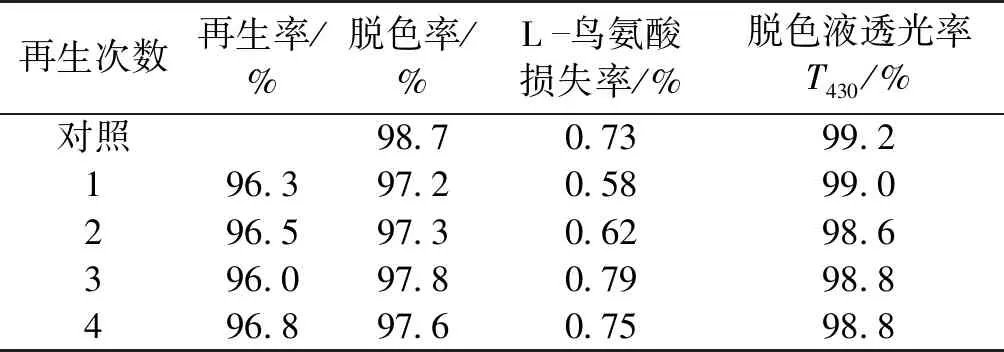
由图3可知:pH为6.0~6.8时,活性炭脱色损失较小,但当pH增至7.0时,L-鸟氨酸回收率明显下降。颗粒活性炭GH的零电荷点pHPZC为6.83(表1),而L-鸟氨酸的等电点pI约为9.73,根据文献[8]报道,在pH 6~6.5的范围内,绝大部分L-鸟氨酸分子携带一个正电荷,此时活性炭表面携带正电荷,与其存在一定的静电排斥,所以脱色损失小,这也是其他零电荷点pHPZC<6.5的颗粒活性炭在此pH下脱色损失大的原因(图2、表1)。继续增大pH,活性炭GH表面开始携带负电荷,而绝大部分L-鸟氨酸分子依然携带正电荷,导致脱色损失加大。pH对脱色效果的影响较为显著,较低的pH有利于脱色,但当pH>6.8时,脱色率显著降低,这与前人提出的pH 将L-鸟氨酸发酵液的pH调节为6.5,考察温度对活性炭脱色性能的影响,结果见表2。 表2 温度对活性炭脱色性能的影响 由表2可知:较高的脱色温度有利于减少L-鸟氨酸的脱色损失,同时脱色率随着温度的升高而逐渐增大,但当温度上升到80 ℃后,脱色率不升反降,说明发生了色素解吸。 以此确定脱色温度为70 ℃。在此温度下考察脱色时间对脱色性能的影响,结果见图4。 图4 脱色时间对活性炭脱色性能的影响Fig.4 Effects of time on decolorization of activated carbon 由图4可知:在脱色的前30 min,活性炭对色素的吸附迅速提高,至40 min时脱色率已达到77%,并维持了一段时间,说明色素吸附达到平衡;而脱色时间达到60 min后,脱色率略有下降,说明在长期高温环境中活性炭发生了色素解吸行为。同时,当色素吸附达到平衡,L-鸟氨酸的脱色回收率出现下降,说明颗粒活性炭优先吸附色素,之后才开始吸附L-鸟氨酸。由此可见,脱色时间40 min即可,不宜过长。 将L-鸟氨酸发酵液的pH调节为6.5,70 ℃脱色40 min,活性炭用量分别为5.0~15.0 g/L,考察活性炭用量对脱色性能的影响,结果见图5。 图5 活性炭用量对脱色性能的影响Fig.5 Effects of activated carbon dosage on the decolorization 由图5可知:随着活性炭用量的增加,脱色率提高,当活性炭用量为15.0 g/L时,脱色率已达95%以上,但单位质量活性炭对色素的吸附容量Q仅为14.68 U/g,比活性炭用量为5.0 g/L时下降59%。可见提高活性炭的利用效率需采用动态脱色技术。 L-鸟氨酸发酵液被调节至pH 6.5并预热至70 ℃,2.5 L发酵液(50 BV)分别以3.0~9.0 BV/h的进料流速上柱进行动态脱色处理,当流出的脱色液中的色素浓度为发酵液中含量的5%时,即可认为发生穿透,其流出曲线见图6。 图6 不同进料流速下的色素流出曲线Fig.6 Effluent curves of pigment at various flow rates 由图6可知:当进料流速从3 BV/h提高至7 BV/h,发生色素穿透的位置逐渐推后,说明活性炭的脱色效果显著改善,推测在此范围内液膜扩散为控速步骤,增加进料流速有利于减少活性炭表面液膜层的厚度,使色素被快速吸附。但当进料流速进一步提高至9 BV/h,色素穿透位置提前,表明脱色效果下降,这可能是由于此时发酵液在层析柱内停留时间过短,导致活性炭导致色素未能与活性炭发生充分的吸附作用。其中,进料流速为7 BV/h时的脱色率最高,连续处理45 BV发酵液才出现穿透,此时活性炭对色素吸附容量Q达到50.5 U/g,总脱色率达到98.71%,脱色液的透光率T430达99%,呈无色透明状。 考察相关进料流速下的L-鸟氨酸流出曲线,结果见图7。 图7 不同进料流速下的L-鸟氨酸流出曲线Fig.7 Effluent curves of L-ornithine at various flow rates 由图7可知:在动态脱色过程中活性炭对L-鸟氨酸的吸附极少,在3~9 BV/h的进料流速下,当流出体积为1.0 BV时均出现L-鸟氨酸完全穿透现象,产品脱色损失均在3%以内,故选择活性炭层析柱动态脱色的进料流速为7 BV/h。 通过颗粒活性炭再生预实验发现,热水可将活性炭吸附的少量L-鸟氨酸解吸,但几乎不能解吸色素,活性炭再生率只有8.5%,而1.0 mol/L的稀H2SO4对活性炭的再生率为74%,1.0 mol/L的NaOH溶液对活性炭的再生率为87%,因此确定采用热水与NaOH两步解吸法:第一步采用80 ℃热水解吸活性炭层析柱中残留的L-鸟氨酸。结果发现80 ℃热水可解吸回收丁二酸,在3.0 BV/h的解吸流速下,2.0 BV的热水可回收70%被活性炭吸附的L-鸟氨酸,使L-鸟氨酸的脱色率达到99%。第二步采用1.0 mol/L NaOH作为再生剂解吸色素,解吸温度为80 ℃,再生剂用量为5.0 BV,最后用去离子水将残留的碱液洗出,使流出液的pH降至7.5以下,3种解吸流速下的色素流出曲线见图8。 图8 不同解吸流速下的色素流出曲线Fig.8 Desorption curves of pigment at different elution rate 由图8可知:NaOH的解吸流速为5.0 BV/h时,3.0 BV的再生剂就可以解吸出绝大部分色素。以未使用过的活性炭作为对照,考察相关活性炭的再生效果,结果显示再生率均在93%以上,其中5.0 BV/h解吸速度下获得再生活性炭,活性炭再生率达到96.5%。 考察活性炭进行反复脱色及再生性能,结果见表3。 表3 再生次数对活性炭脱色性能的影响 由表3可知:活性炭层析柱再生后重复使用4次,其对同一批发酵液的脱色率均稳定在97%以上,脱色液的透光率T430均达98.5%以上,接近纯水的透光率,呈无色透明状。L-鸟氨酸的损失率均在1%以内,活性炭再生效果稳定。 1)L-鸟氨酸发酵液中的大部分色素可能属于非极性或弱极性分子,具有较高的零电荷点pHPZC、较大的平均孔径和比孔容积的活性炭GH在pH 6.5下对色素具有较好的吸附能力,而过高的脱色温度和过长的脱色时间不利于活性炭对色素的吸附。 2)确定了活性炭层析柱对L-鸟氨酸发酵液的动态脱色/再生工艺:进料流速为7.0 BV/h、脱色温度70 ℃,可连续处理45 BV的发酵液。采用两步解吸法再生活性炭,第一步采用80 ℃热水在3.0 BV/h的流速下解吸残留的L-鸟氨酸,处理量为2.0 BV;第二步在同样的温度下采用以1.0 mol/L NaOH以5.0 BV/h流速解吸色素,处理量为5.0 BV。在该条件下,脱色率保持在97%以上,而L-鸟氨酸的损失率低于1%,活性炭重复使用性能稳定。2.4 温度和时间对活性炭脱色性能的影响
2.5 活性炭用量对脱色性能的影响
2.6 进料流速对活性炭动态脱色性能的影响
2.7 活性炭层析柱的解吸与再生
3 结论

