术前新辅助治疗与根治性放化疗治疗ⅢA(N2)期NSCLC效果的Meta分析
井晓亮 张力为 宗亮 李德生 居来提·艾尼瓦尔 杨凡


[摘要] 目的 比較新辅助治疗联合手术与根治性放化疗治疗ⅢA(N2)期非小细胞肺癌(NSCLC)的效果。 方法 采用计算机检索PubMed、Medline、Ovid、CNKI、维普数据库及万方数据库,并辅以手工检索,收集建库至2018年4月已公开发表的比较新辅助治疗联合手术和根治性放化疗治疗ⅢA(N2)期NSCLC的有关研究,并根据治疗方式将样本分为新辅助治疗联合手术组和根治性放化疗治疗组。 结果 符合纳入标准的共14项研究,其中包括5项随机对照研究,9项回顾性病例对照研究,总样本量12 713例,其中新辅助治疗联合手术组1792例,根治性放化疗治疗组10 921例。随机对照研究中新辅助治疗联合手术组的3年生存率与根治性放化疗组比较,差异无统计学意义(OR = 0.93,95%CI:0.71~1.22,P = 0.61)。病例对照研究中,新辅助治疗联合手术组3年生存率优于放化疗组(OR = 0.63,95%CI:0.55~0.72,P < 0.00 001)。随机对照研究中新辅助治疗联合手术组的5年生存率与根治性放化疗组比较,差异无统计学意义(OR = 0.77,95%CI:0.52~1.12,P = 0.17)。而在病例对照研究中新辅助治疗联合手术组5年生存率优于根治性放化疗组(OR = 0.36,95%CI:0.25~0.51,P < 0.00 001)。 结论 新辅助治疗联合手术治疗可以使ⅢA(N2)期NSCLC患者获得更长的生存时间或达到治愈效果。新辅助治疗后行全肺切除也许是安全可行的,进一步开展有关新辅助治疗联合手术尤其是全肺切除术患者生存分析的随机对照研究具有重要意义。
[关键词] ⅢA(N2)期;NSCLC;新辅助治疗;根治性放化疗;Meta分析
[中图分类号] R734.2 [文献标识码] A [文章编号] 1673-7210(2019)02(b)-0108-06
[Abstract] Objective To compare the effects of preoperative neoadjuvant therapy combined surgery with radical chemoradiotherapy for stage ⅢA (N2) non-small cell lung cancer (NSCLC). Methods PubMed, Medline, Ovid, CNKI, VIP and Wanfang databases were retrieved by computer, and supplemented by manual search. The publicly published studies concerning the treatment of stage Ⅲ A (N2) NSCLC with neoadjuvant therapy combined surgery and radical chemotherapy were collected from building database to April 2018, and the samples were divided into neoadjuvant therapy combined surgery group and radical chemoradiotherapy group according to the treatment method. Results A total of 14 studies met the inclusion criteria, including 5 randomized controlled trials, 9 retrospective case-control studies, with a total sample size of 12 713 cases, including 1792 cases in neoadjuvant therapy combined surgery group and 10 921 cases in radical chemoradiotherapy group. The 3-year survival rate of the neoadjuvant therapy combination surgery group in the randomized controlled trial was not significantly different from the radical chemotherapy group (OR = 0.93, 95% CI: 0.71-1.22, P = 0.61). In the case-control study, the 3-year survival rate of the neoadjuvant combination surgery group was superior to that of the radical chemotherapy group (OR = 0.63, 95% CI: 0.55 - 0.72, P < 0.00 001). The 5-year survival rate of the neoadjuvant therapy combined surgery group in the randomized controlled trial was not significantly different from the radical chemoradiotherapy group (OR = 0.77, 95% CI: 0.52-1.12, P = 0.17). In the case-control study, the 5-year survival rate of the neoadjuvant combined surgery group was better than that of the radical chemo group (OR = 0.36, 95% CI: 0.25-0.51, P < 0.00 001). Conclusion Neoadjuvant therapy combined with surgical treatment can make patients with stage Ⅲ A (N2) NSCLC have longer survival time or achieve cure effect. Pneumonectomy after neoadjuvant therapy may be safe and feasible. Further randomized controlled studies on survival analysis of patients undergoing neoadjuvant therapy combined with surgery, especially pneumonectomy, are of great significance.
[Key words] Stage ⅢA(N2); Non-small cell lung cancer; Neoadjuvant Therapy; Radical chemoradiotherapy; Meta analysis
肺癌严重危害人類健康,已成为我国人口因恶性肿瘤死亡主要原因之一[1]。中国肺癌发病率为53.86/10万(男性70.10/10万,女性36.78/10万),肺癌死亡率43.41/10万(男性57.64/10万,女性28.45/10万)[2]。NSCLC患者中10%~20%在首诊时临床分期即为ⅢA(N2)期[3],5年生存率仅为19.0%~42.8%[4],在胸部肿瘤领域对于ⅢA(N2)NSCLC的治疗模式一直存在争议。ⅢA(N2)期非小细胞肺癌(NSCLC)是一组异质性非常明显的疾病,且对N2再分类没有统一的标准。尽管疾病相同,不同地区数据库中治疗策略的选择却大相径庭。北美的外科医师倾向于对该时期患者进行诱导治疗后,对淋巴结降期、病灶缩小的患者实行手术治疗,同时尽量避免行全肺切除术;而欧洲胸外科医师更希望通过手术切除病灶,即使需要行全肺切除术[5]。两种治疗模式是否存在差异,仍然未达成一致。本研究收集NSCLC治疗有关的文献,并借助Meta分析,探讨两种治疗模式对ⅢA(N2)期NSCLC远期生存率的影响。
1 资料与方法
1.1 文献检索策略
计算机检索PubMed、Medline、Ovid、CNKI、万方、维普等数据库,并辅以手工检索,检索时限均为建库至2018年4月。英文检索词为“neoadjuvant chemotherapy”“induction chemotherapy”“preoperative chemotherapy”“ⅢA(N2)NSCLC”;中文检索词为:“NSCLC”“ⅢA(N2)”“新辅助化疗”“新辅助放化疗”。最后筛查检索获得的相关文献。
1.2 纳入与排除标准
1.2.1 纳入标准 ①公开发表的可获得全文的随机对照研究及回顾性分析;②原始文献为有关术前新辅助化疗或新辅助放化疗对ⅢA(N2)期NSCLC生存期影响的相关研究,其手术组行新辅助治疗+手术治疗,放化疗组行根治性放化疗治疗;③原始文献包含至少3年以上随访生存数据;④新辅助治疗均未接受生物、免疫治疗,无严重内脏功能疾患。
1.2.2 排除标准 ①无法获取全文的文献;②新辅助治疗包括生物、免疫治疗,且这种治疗方案可能造成不同的预后;③合并有其他恶性肿瘤、重要脏器疾病的患者。
1.3 文献筛选与数据提取
分别由2名研究者单独阅读文章题目和摘要后进行初筛,对符合的文章精读全文以进行二次筛选,根据纳入与排标准判定是否纳入文献,意见不同时由第三名研究人员阅读后讨论决定。此外,根据治疗方式将所有纳入文献的样本分为新辅助治疗联合手术组和根治性放化疗治疗组。文献提取数据包括:①一般信息:发表年份、国家、样本量、放化疗方案(化疗方案和放疗量)、周期;②疗效指标:不同分组的远期生存率。
1.4 统计学方法
采用Review Manager 5.3软件对数据进行分析,对纳入的原始文献进行异质性分析,I2<50%为异质性较低,选择固定效应型;I2>50%为异质性较高,则选择随机效应模型;求其效应合并值,计算合并优势比(OR),结果用95%CI表示。以P < 0.05为差异有统计学意义。
2 结果
2.1 纳入文献的数据特征
共14项研究符合纳入标准[6-19],其中共包含5篇随机对照研究及9篇回顾性病例对照研究,总样本量12 713例,其中新辅助治疗联合手术组1792例,根治性放化疗组10 921例。纳入文献的特征见表1。
2.2 纳入文献的偏倚风险评价
2.2.1 随机对照研究偏倚风险评价 所纳入的随机对照试验中虽然描述了分组方法、随机化方法、分配隐藏等信息,因术前新辅助治疗时很难实现盲法,故纳入的研究均不得分。本研究采用Newcastle-Ottawa Scale(NOS)文献质量评价量表分析偏倚来源,其评分均≥4分,总体评价随机对照研究质量较高。见表2。
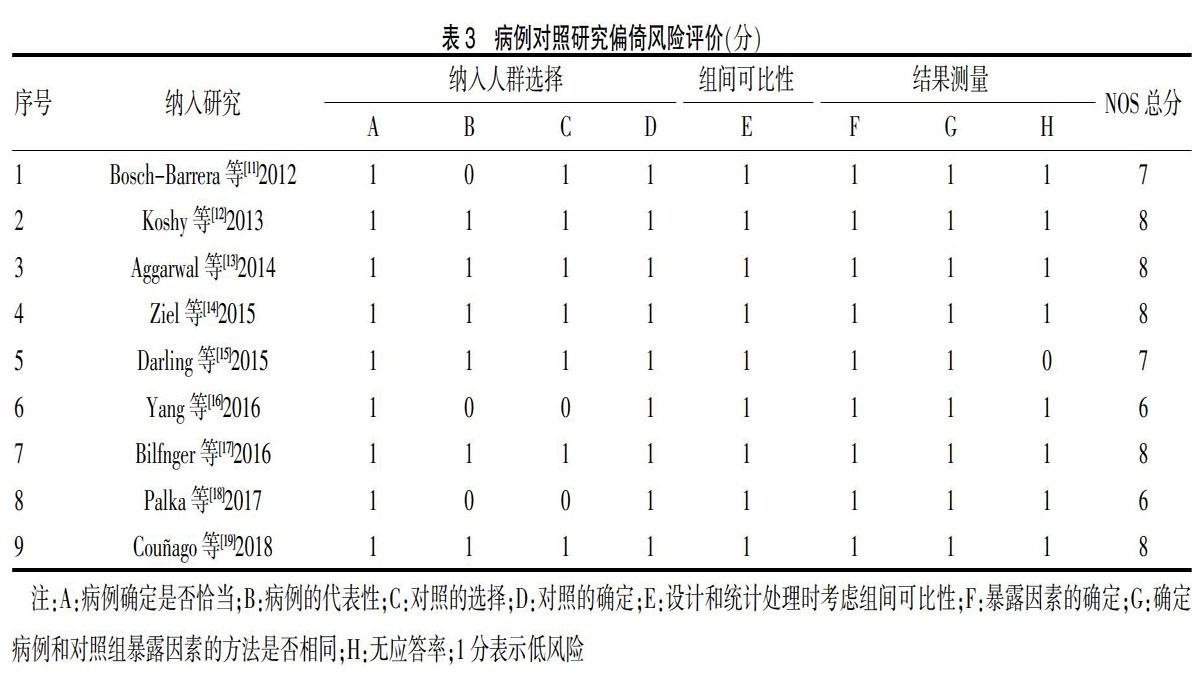
2.2.2 病例对照研究偏倚风险评价 所纳入病例对照研究采用NOS文献质量评价量表分析偏倚来源,部分研究对化疗或放化疗方案未进行详细描述、研究终点的不同等造成了一定的偏倚来源。本研究纳入文献的NOS总分均≥6分,总体质量较高。见表3。
2.3 疗效评价
2.3.1 3年总生存率 随机对照研究中共有5项[6-10]报道了3年生存率,经异质性检验(I2=0%,P = 0.64),选用固定效应模型分析,其新辅助治疗联合手术组与根治性放化疗组的3年生存率比较,差异无统计学意义(OR = 0.93,95%CI:0.71~1.22,P = 0.61)(图1)。共有5项研究[14-15,17-19]回顾性报道了3年生存率,经异质性检验(I2=48%,P = 0.10 ),其新辅助治疗联合手术组3年生存率优于根治性放化疗组(OR = 0.63, 95%CI:0.55~0.72,P < 0.00 001)(图2)。
2.3.2 5年总生存率 随机对照研究中共有3项[8-10]报道了5年生存率,经异质性检验(I2=0%,P = 0.63),选用固定效应模型分析,新辅助治疗联合手术组与根治性放化疗组的5年生存率比较,差异无统计学意义(OR = 0.77,95%CI:0.52~1.12,P = 0.17)(图3)。共有研究[11-17,19]回顾性报道了5年生存率,经异质性检验(I2=53%,P = 0.04 ),选用随机效应模型分析,其新辅助治疗联合手术组5年生存率优于根治性放化疗组(OR = 0.36,95%CI:0.25~0.51,P < 0.00 001)(图4)。

