饲料中铬的测定方法改进试验
马 川,李 宏,高勤叶,赵彩会,吉 辉,贺习文
(1.陕西秦云农产品检验检测有限公司,陕西 渭南 714000;2.农业部饲料质量监督测试中心,陕西 西安 710016)
铬(Cr)是人体必需的微量元素,在肌体的糖代谢和脂代谢中发挥特殊作用,常见的Cr有二价、三价和六价,三价的Cr是对人体有益的元素,而六价Cr是有毒的[1]。人体对无机Cr的吸收和利用效率很低,约1%,然而人体对有机Cr的利用率可达到10%~25%。Cr在天然食品中的含量较低、均以三价的形式存在。确切地说,Cr的生理功能是与其他控制代谢的物质配合才有作用,如激素、胰岛素、各种酶类、细胞的基因物质(DNA和RNA)等。Cr进入人体细胞后,对肝脏及DNA造成难以修复的损伤,因此对Cr的监测显得尤为重要[2]。
动物饲料中添加Cr的作用是调节免疫、抗应激和提高瘦肉率等,在饲料中的Cr只有极少部分会被动物吸收,在生物体内长期沉积,最终传递到食物链顶端[3-4]。Cr的化合物不会自然消解,其会造成畜禽黏膜充血以及内脏器官出血,并具有致癌性和引发基因突变的风险[5-6]。中国最新饲料卫生标准GB 13078-2017中限量值降至5 mg·kg-1,对铬元素有明确限制。GB/T 13088-2006中,样品干灰化后加硝酸消解,对样品的消解不彻底。因此,为了加强对饲料安全监督,必须进行一种高效、准确的检测方法,样品经高温灰化,加酸消解后,在波长359.4 nm处测定吸收值,试验验证结果具有较好的重复性。
1 材料与方法
1.1 试验原理
试验用样品:国产鱼粉。样品经高温灰化,加酸消解后,通过原子吸收测定吸收值,其吸收值与铬含量成正比,与标准系列比较定量。
1.2 仪器与试剂
原子吸收分光光度计(analytikena ZEEnit 700P);万分之一天平[奥豪斯仪器(常州)有限公司,CP224C];可控温电热板(北京中兴伟业仪器有限公司,SKML-1.54);马弗炉(天津市泰斯特仪器有限公司,SX-4-10);瓷坩埚。
铬标准溶液:国家有色金属及电子材料分析测试中心;盐酸(优级纯):北京化工厂;硝酸(优级纯):西陇化工股份有限公司;二级水。
1.3 试验方法
称样5 g(精确到0.0001 g),置于瓷坩埚中,在可控温电热板上完全碳化后,置于马弗炉内,由室温开始,逐渐升温至600℃灼烧5 h,直至试样呈白色或灰白色、无碳粒为止。取出放至室温,加5.0 mL 50%盐酸-50%硝酸溶液,在可控温电热板上缓慢加热,加热至溶液微沸,然后用水转移定容至50 mL容量瓶中,摇匀、待测。同时做样品空白。
1.4 仪器条件
光源:铬空心阴极灯;波长:359.4 nm;灯电流:4.5 mA;狭缝宽度:0.5 nm;火焰:空气-乙炔;助燃器压力:160 kPa(流速15.0 L·min-1);燃气压力:35 kPa(流速15.0 L·min-1);氘灯背景校正。
2 结果与讨论
2.1 标准曲线绘制
中间液(100 μg·mL-1):量取Cr(1 000 μg·mL-1)标准溶液10.0 mL于100 mL容量瓶中,加5%硝酸溶液稀释至刻度,此溶液每毫升相当于100 μg。
中间液(10 μg·mL-1):移取中间液(100 μg·mL-1)10.0 mL于100 mL容量瓶中,加5%硝酸溶液稀释至刻度,此溶液每毫升相当于10 μg。
工作液:吸取铬中间液(10 μg·mL-1)0.00、1.00、2.00、4.00、6.00和8.00 mL,分别置于100 mL容量瓶中,加5%硝酸溶液稀释至刻度,混匀,制成标准工作液。容量瓶中每毫升溶液分别相当于铬0、0.10、0.20、0.40、0.60、0.80 μg。
在波长359.4 nm处测定吸光值,做标准曲线(见表1),得到线性回归方程为:Y=0.076 057 2X+0.001 001 9,R2=0.999 5。
2.2 方法对比
GB/T 13088-2006方法中样品加酸后直接转移定容测定与本方法加酸消解后结果对比见表2。
测定结果对比发现,同样酸溶液的样品,消解与不消解结果有明显差异,消解后测定值明显大于不消解测定值。
2.3 不同酸对样品消解结果的影响
称取鱼粉样品4份,两份加入20%盐酸溶液,两份加入20%硝酸溶液,按照1.3的试验方法消解,所得结果见表3。

表1 标准曲线浓度及吸光度
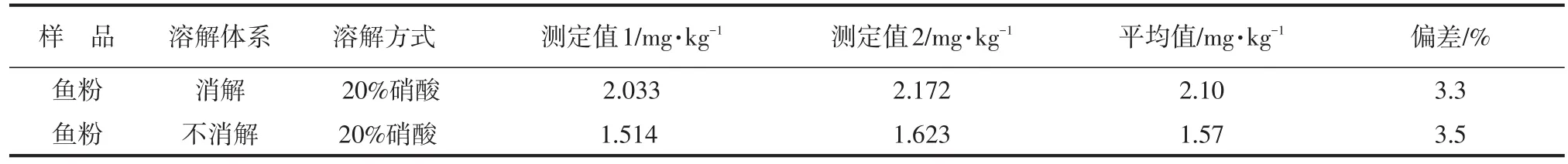
表2 消解与不消解结果对比

表3 20%盐酸与20%硝酸测定结果对比
20%盐酸与20%硝酸测定结果对比显示,20%盐酸消解测定值<20%硝酸消解测定值,20%硝酸消解情况更好。
2.4 不同浓度与酸度对消解结果影响
称取鱼粉样品6份,2份加入50%盐酸-50%硝酸溶液,2份加入20%硝酸溶液,2份加入硝酸,按照1.3部分中的试验方法消解,结果见表4。
单一硝酸无法完全消解出样品中的铬,50%盐酸-50%硝酸溶液与20%硝酸消解后结果对比表明,50%盐酸-50%硝酸溶液与20%硝酸结果有差异,50%盐酸-50%硝酸溶液比20%硝酸测定值大,消解效果优于20%硝酸。试验结果表明,试验中使用50%盐酸-50%硝酸溶液能更好地溶解出鱼粉中的Cr。
2.5 样品不同溶解系数测定值与试际值
通过不同浓度、酸度对鱼粉进行消解,得到两次测定结果的平均值与样品试际值的相对偏差,结果见表5。
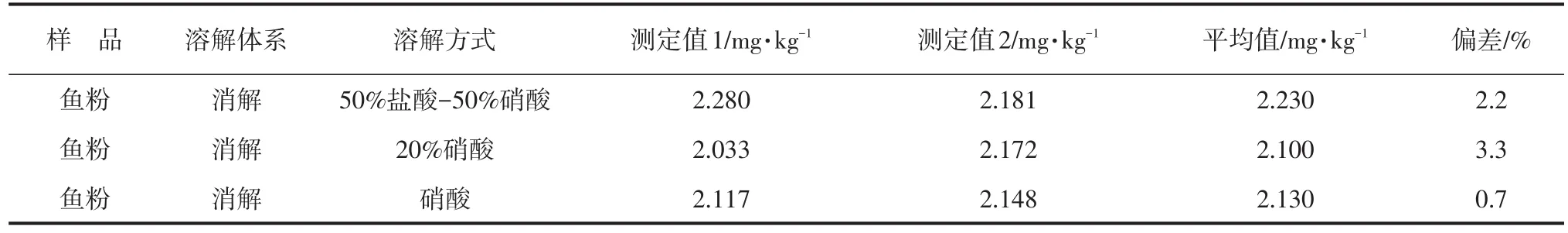
表4 50%盐酸-50%硝酸溶液与20%硝酸消解后结果对比

表5 与实际值相对偏差
试验结果表明,50%硝酸-50%盐酸溶液酸解样品的结果最接近试际值,其相对偏差为1.5%,相对偏差≤5%,结果在理想范围内。
2.6 加标回收
称取鱼粉样品2份,分别加入浓度为10 μg·mL-1中间液0.1、0.4 mL,加标浓度分别为1.0、4.0 mg·kg-1,所得回收率见表6。
由表6可知,通过对试样不同浓度加标,测得回收率在95%~106%,验证了本方法可行性。
2.7 重复性
称取6个鱼粉样品,按照1.3中的试验方法处理,所得结果的相对标准偏差RSD(n=6)见表7。
综合样品消解程度和偏差,50%硝酸-50%盐酸平行样相对偏差相对较小且消解最为彻底。
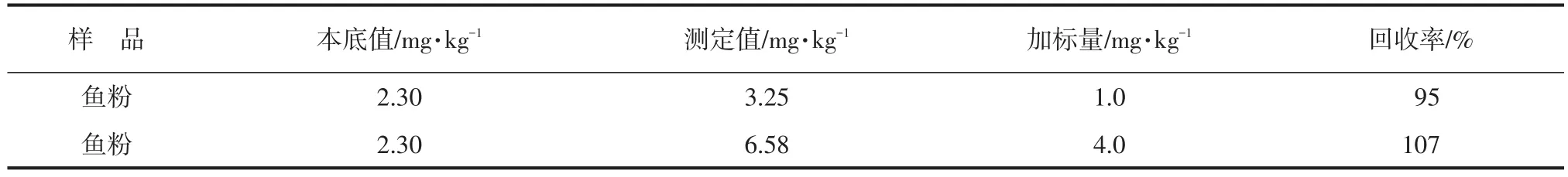
表6 50%盐酸-50%硝酸溶液加标回收率
2.8 结果计算
以水为清洗溶液调零,在原子吸收分光光度计(analytikena ZEEnit700P)在波长359.4 nm处测定吸收值,从所得标准曲线上查得铬的浓度。计算公式见式1。

式(1)中:A为测定用试样溶液中铬的含量(μg·mL-1);A0为试剂空白液中铬的含量(μg·mL-1);V为试样溶液的总体积(mL);m为试样的质量(g)。计算结果为同一试样两个平行样的算术平均值,精确到小数点后两位。
3 结论
目前中国饲料中铬的检测方法发布于2006年,饲料行业大部分的检测方法都是引用GB/T 13088-2006饲料中Cr的测定,然而GB/T 13088方法使用的20%硝酸溶液且不加热消解,根本无法完全消解样品,本方法与原方法区别是用50%盐酸-50%硝酸溶液代替20%硝酸溶液,加酸后加热消解测定,无论从溶出效率、测定值、回收率、精密度、稳定性上,都优于原方法。经上述试验验证,饲料中Cr测定,干灰化后加50%盐酸-50%硝酸溶液消解,能完全消解样品,有利于准确测定饲料中铬的含量。本试试验测定饲料中Cr的含量,改进易于操作,回收率为95%~106%,检测条件稳定,加标回收率高,平行样相对偏差较小。

