HPLC法同时测定半枝莲饮片中4种黄酮类成分的含量及主成分分析
夏云岭 张振凌 张洪坤 林钦贤 梁伟龙 路丽

中图分类号 R283 文献标志码 A 文章编号 1001-0408(2019)20-2839-06
DOI 10.6039/j.issn.1001-0408.2019.20.20
摘 要 目的:建立同时测定半枝莲饮片中野黄芩苷、野黄芩素、木犀草素、芹菜素等4种黄酮类成分含量的方法,并进行主成分分析。方法:采用高效液相色谱法。色谱柱为Agilent ZOXDB-C18,流动相为甲醇-乙腈(80 ∶ 20,V/V)-1%醋酸水溶液(梯度洗脱),流速为1.0 mL/min,检测波长为335 nm,柱温为30 ℃,进样量为10 μL。采用SPSS 20.0、SIMCA-P 13.0软件进行主成分分析。結果:野黄芩苷、野黄芩素、木犀草素、芹菜素进样量的线性范围分别为0.131~1.446 μg(r=0.999 0)、0.031~0.345 μg(r=0.999 7)、0.005~0.055 μg(r=0.999 2)、0.024~0.268 μg(r=0.999 2);定量限分别为1.178 8、0.602 9、0.744 1、1.079 1 ng,检测限分别为0.353 6、0.106 1、0.223 2、0.323 7 ng;精密度、稳定性、重复性试验的RSD均小于2%;加样回收率分别为99.38%~100.56%(RSD=0.44%,n=6)、91.01%~96.81%(RSD=2.43%,n=6)、91.44%~97.34%(RSD=2.59%,n=6)、96.21%~99.26%(RSD=1.23%,n=6)。主成分分析结果显示,主成分1和主成分2是影响样品质量评价的主要因子,2个主成分的累积方差贡献率为92.573%(>80%);S14-3样品综合评分最高,整体质量相对较好,S14-2、S14-1次之,这3批样品均系半枝莲种植基地药材加工产品,质量稳定。结论:本方法简单、快速,可用于同时测定半枝莲饮片中4种黄酮类成分的含量;主成分分析可为半枝莲饮片的质量控制提供参考。
关键词 半枝莲;野黄芩苷;野黄芩素;木犀草素;芹菜素;高效液相色谱法;含量测定;主成分分析
ABSTRACT OBJECTIVE: To establish the method for simultaneous determination of 4 kinds of flavones such as sutellarin, sutellarein, luteolin and apigenin in Scutellaria barbata decoction pieces, and to conduct principle component analysis. METHODS: HPLC method was adopted. The determination was performed on Agilent ZOXDB-C18 column with mobile phase consisted of methanol-acetonitrile (80 ∶ 20,V/V)-1% acetic acid solution (gradient elution) at the flow rate of 1.0 mL/min. The detection wavelength was set at 335 nm, and column temperature was 30 ℃. The sample size was 10 μL. Principal component analysis was carried out by SPSS 20.0 and SIMCA-P 13.0 software. RESULTS: The linear ranges of sutellarin, sutellarein, luteolin and apigenin were 0.131-1.446 μg(r=0.999 0), 0.031-0.345 μg(r=0.999 7), 0.005-0.055 μg(r=0.999 2), 0.024-0.268 μg(r=0.999 2), respectively. The limits of quantitation were 1.178 8, 0.602 9, 0.744 1, 1.079 1 ng; the limits of detection were 0.353 6, 0.106 1, 0.223 2, 0.323 7 ng;RSDs of precision, stability and reproducibility tests were all lower than 2%. The recoveries were 99.38%-100.56%(RSD=0.44%,n=6), 91.01%-96.81%(RSD=2.43%, n=6), 91.44%-97.34%(RSD=2.59%, n=6), 96.21%- 99.26%(RSD=1.23%,n=6), respectively. By principal component analysis, principal component 1 and prinicipal component 2 were main influential factors of sample, quality accumulative variance contribution rate of them was 92.573%(>80%). The comprehensive score of sample S14-3 was the highest, and the overall quality was relatively good; samples S14-2, S14-3 were the second. These 3 batches of sample were processed and produced in S. barbata planting base with stable quality. CONCLUSIONS: Established method is simple and rapid, and can be used for simultaneous determination of 4 kinds of flavones in S. barbata decoction pieces. Principle component analysis can provide reference for the quality control of S. barbata decoction pieces.
KEYWORDS Scutellaria barbata; Sutellarin; Sutellarein; Luteolin; Apigenin; HPLC; Content determination; Principle component analysis
半枝莲为唇形科黄芩属植物半枝莲(Scutellaria barbata D. Don)的干燥全草[1],主要含有黄酮类、二萜及二萜内酯类、多糖类等成分[2]。现代研究表明,半枝莲具有良好的抗肿瘤活性,临床上用于治疗胰腺癌、肝癌等多种癌症[3-5],而其抗癌的主要活性物质为黄酮类成分[6-7]。查阅历版《中国药典》及各省市炮制规范[8],发现半枝莲炮制方法较简单,且受采收期、产地和种植方式等多种因素影响,市场上半枝莲饮片质量参差不齐。现行2015年版《中国药典》(一部)对半枝莲以野黄芩苷和总黄酮为指标进行含量限定(野黄芩苷不得少于0.20%;总黄酮以野黄芩苷计,不得少于1.50%),采用索氏提取法进行样品制备[1],过程较为复杂且耗时较长。为建立半枝莲饮片中多种黄酮类成分同时测定的方法,同时简化样品制备方法、提高制备效率,本研究采用高效液相色谱法(HPLC)建立了同时测定半枝莲饮片中野黄芩苷、野黄芩素、木犀草素、芹菜素含量的方法,并采用主成分分析法对42批半枝莲饮片的质量进行评价,旨在为其质量控制及等级标准的建立提供参考。
1 材料
1.1 仪器
e2695型HPLC仪,包括四元泵洗脱系统、自动进样系统、柱温箱及紫外检测器(美国Waters公司);FW-200型高速万能粉碎机(北京中兴伟业仪器有限公司);UPT-Ⅱ-10T型优普系列超纯水器(成都超纯科技有限公司);DZKW-A型仪表恒温水浴锅(上海树立仪器仪表有限公司);GZX-9070 MBE型数显鼓风干燥箱(上海博讯实业有限公司医疗设备厂);BT25S型十万分之一天平、BSA224S-CW型万分之一天平[赛多利斯科技仪器(北京)有限公司]。
1.2 药品与试剂
野黄芩苷对照品(批号:121293-201404)、野黄芩素对照品(批号:170818-201612)、木犀草素对照品(批号:103200-201305)、芹菜素对照品(批号:100755-201236)均购自中国食品药品检定研究院,纯度均大于98%;甲醇、乙腈、冰醋酸为色谱纯,其他试剂均为分析纯,水为超纯水。
1.3 药材
半枝莲饮片经河南中医药大学药学院张振凌教授鉴定为唇形科植物半枝莲(Scutellaria barbata D. Don)干燥地上部分的加工炮制品,样品来源信息见表1。
2 方法与结果
2.1 含量測定
2.1.1 色谱条件 色谱柱:Agilent ZOXDB-C18(250 mm ×4.6 mm,5 µm);流动相:甲醇-乙腈(80 ∶ 20,V/V;流动相A)-1%醋酸水溶液(流动相B),梯度洗脱(0~20 min,28%A→35%A;20~30 min,35%A;30~50 min,35%A→70%A);检测波长:335 nm;流速:1.0 mL/min;柱温:30 ℃;进样量:10 µL。
2.1.2 混合对照品溶液的制备 分别精密称取野黄芩苷、野黄芩素、木犀草素、芹菜素对照品各适量,加甲醇制成含野黄芩苷313 μg/mL、野黄芩素305 μg/mL、木犀草素158 μg/mL、芹菜素244 μg/mL的单一对照品贮备液。分别精密吸取上述各单一对照品贮备液2.1、0.515、0.158、0.5 mL,置于同一5 mL量瓶中,加甲醇定容,摇匀,即得含野黄芩苷131.5 μg/mL、野黄芩素31.4 μg/mL、木犀草素5.0 μg/mL、芹菜素24.4 μg/mL的混合对照品溶液。
2.1.3 供试品溶液的制备 精密称取样品粉末(过3号筛)0.5 g,置于具塞锥形瓶中,加70%甲醇50 mL,称定质量,加热回流30 min,冷却至室温,用70%甲醇补足减失的质量,摇匀,经0.45 μm微孔滤膜滤过,取续滤液,即得。
2.1.4 阴性对照溶液的制备 精密量取70%甲醇50 mL,置于具塞锥形瓶中,称定质量,加热回流30 min,冷却至室温,用70%甲醇补足减失的质量,摇匀,经0.45 μm微孔滤膜滤过,取续滤液,即得。
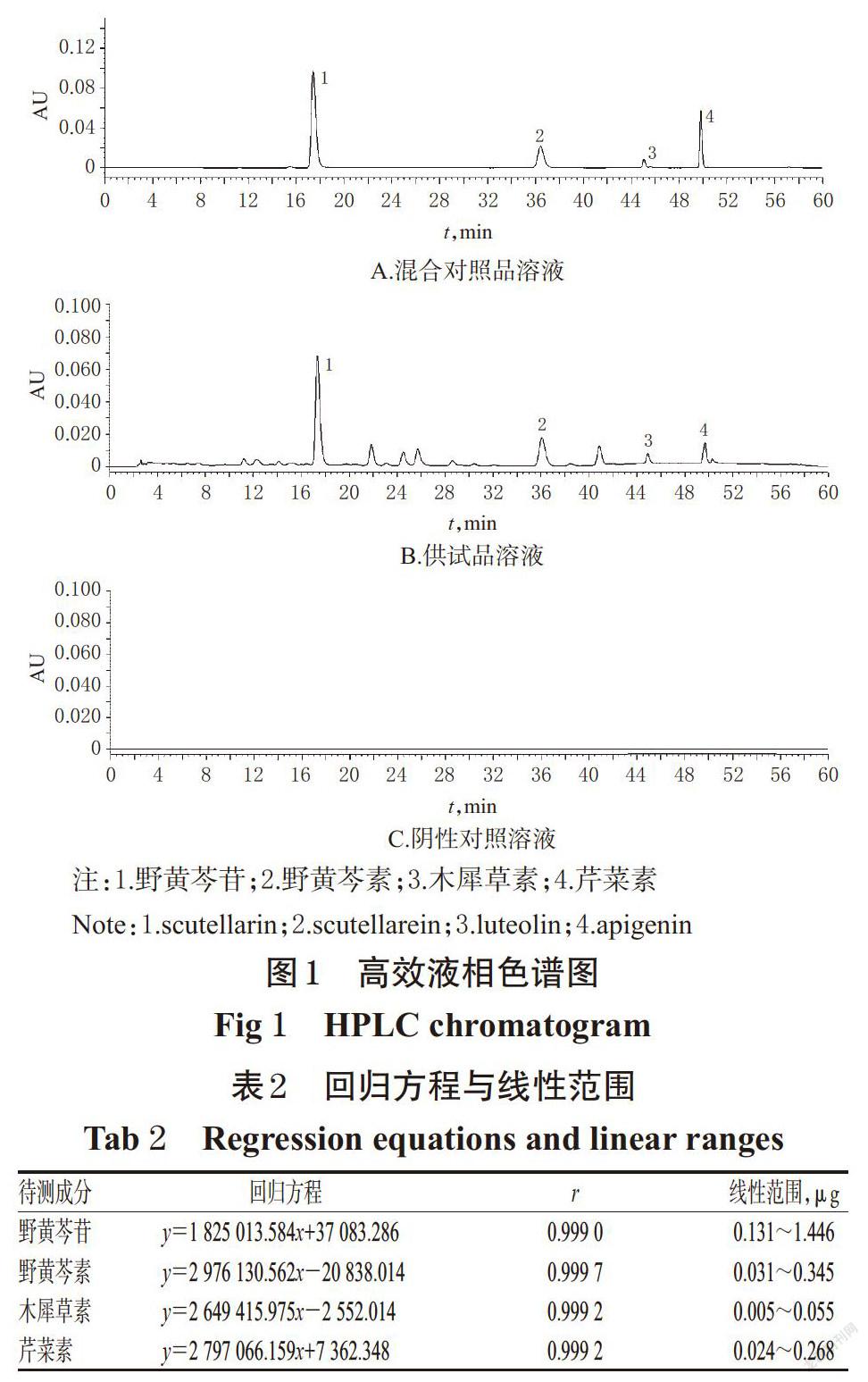
2.1.5 系统适用性试验 取上述混合对照品溶液、供试品溶液、阴性对照溶液各适量,按“2.1.1”项下色谱条件进样测定,记录色谱,详见图1。由图1可知,在该色谱条件下,野黄芩苷、野黄芩素、木犀草素分离度均大于1.5,芹菜素分离度大于1,且峰形对称、分离良好,理论板数均大于5 000;阴性对照溶液对测定无干扰。
2.1.6 线性关系考察 分别精密吸取“2.1.2”项下混合对照品溶液1、3、5、7、9、11 μL,按“2.1.1”项下色谱条件进样测定,记录峰面积。以各待测成分进样量(x,μg)为横坐标、峰面积(y)为纵坐标进行线性回归,得回归方程与线性范围见表2。
2.1.7 定量限与检测限考察 取“2.1.2”项下混合对照品溶液适量,用甲醇倍比稀释,按“2.1.1”项下色谱条件进样测定,以信噪比10 ∶ 1、3 ∶ 1分别计算定量限、检测限。结果,野黄芩苷、野黄芩素、木犀草素、芹菜素的定量限分别为1.178 8、0.602 9、0.744 1、1.079 1 ng,检测限分别为0.353 6、0.106 1、0.223 2、0.323 7 ng。
2.1.8 精密度试验 取“2.1.2”项下混合对照品溶液适量,按“2.1.1”项下色谱条件连续进样测定6次,记录峰面积。结果,野黄芩苷、野黄芩素、木犀草素、芹菜素峰面积的RSD分别为0.15%、0.31%、1.59%、0.39%(n=6),表明仪器精密度良好。
2.1.9 稳定性试验 取“2.1.3”项下供试品溶液(编号:S1-3)适量,分别于室温下放置0、2、4、8、12、24 h时按“2.1.1”项下色谱条件进样测定,记录峰面积。结果,野黄芩苷、野黄芩素、木犀草素、芹菜素峰面积的RSD分别为0.91%、0.46%、0.68%、0.82%(n=6),表明供试品溶液于室温下放置24 h内基本稳定。
2.1.10 重复性试验 精密称取样品(编号:S1-3)粉末,共6份,每份约0.5 g,按“2.1.3”项下方法制备供试品溶液,再按“2.1.1”项下色谱条件进样测定,记录峰面积并按标准曲线法计算4种待测成分的含量。结果,野黄芩苷、野黄芩素、木犀草素、芹菜素的平均含量分别为0.74%、0.06%、0.02%、0.03%,RSD分别为1.97%、0.56%、1.92%、1.76%(n=6),表明本方法重复性良好。
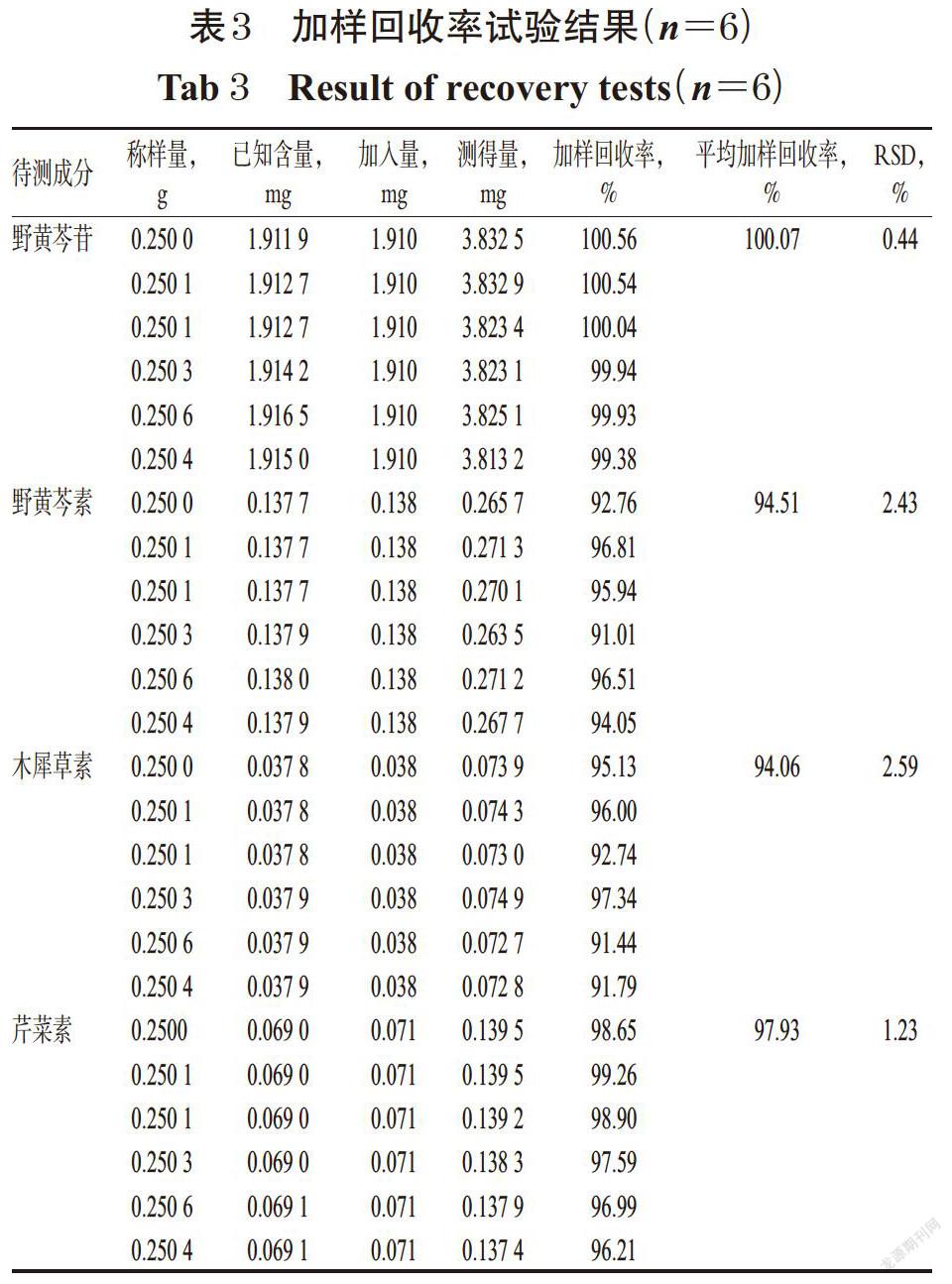
2.1.11 加样回收率试验 精密称取已知含量的样品(编号:S1-3)粉末,共6份,每份约0.25 g,精密加入混合对照品溶液(取野黄芩苷、野黄芩素、木犀草素、芹菜素对照品适量,加甲醇制成含野黄芩苷1.91 mg/mL、野黄芩素0.138 mg/mL、木犀草素0.038 mg/mL、芹菜素0.071 mg/mL的混合溶液)适量,按“2.1.3”项下方法制备供试品溶液,再按“2.1.1”项下色谱条件进样测定,记录峰面积并计算加样回收率,结果见表3。
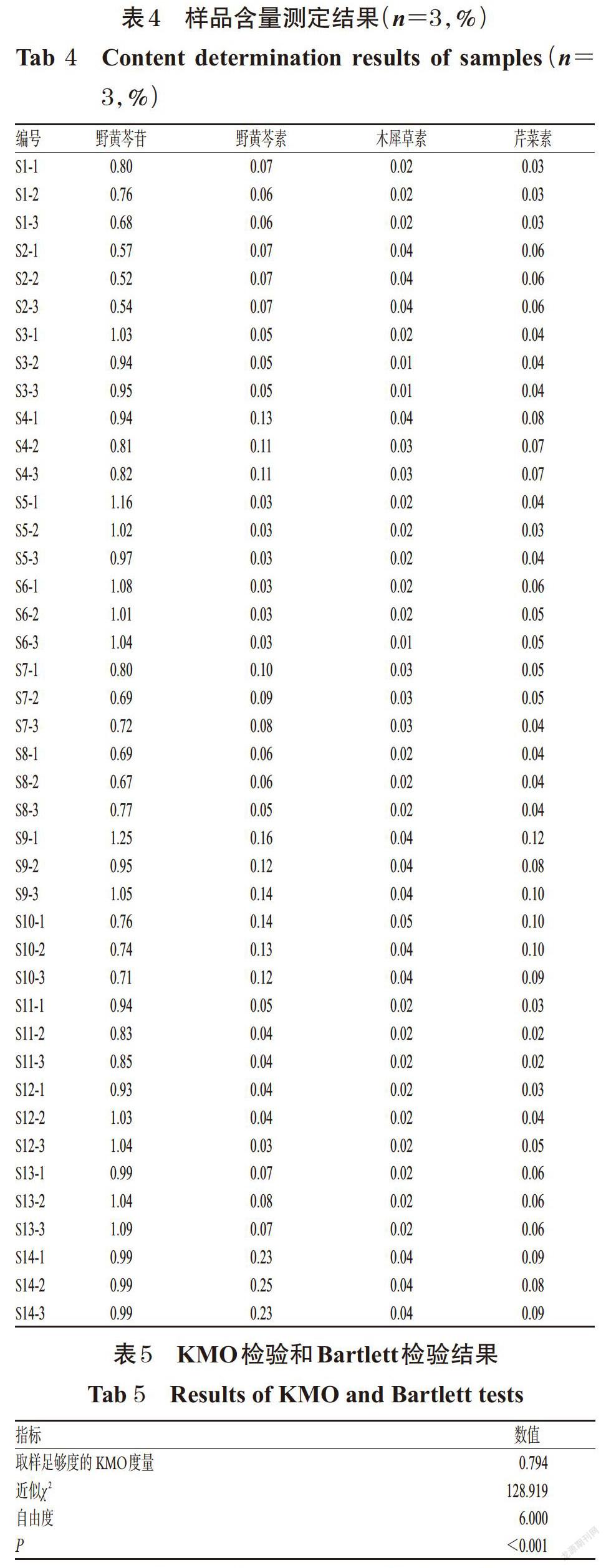
2.1.12 样品含量测定 取42批样品粉末各适量,按“2.1.3”项下方法制备供试品溶液,再按“2.1.1”项下色谱条件进样测定,记录峰面积并按标准曲线法计算样品中4种待测成分的含量,平行操作3次,结果见表4。
2.2 主成分分析
2.2.1 相关性 对4个指标成分进行主成分分析前先行KMO检验和Bartlett检验[9-11],得到KMO度量值为0.794,提示可以进行主成分分析。Bartlett检验法结果显示,P<0.001,提示各变量间存在显著的相关性,可进行因子分析以评价各变量间的共性,结果见表5。
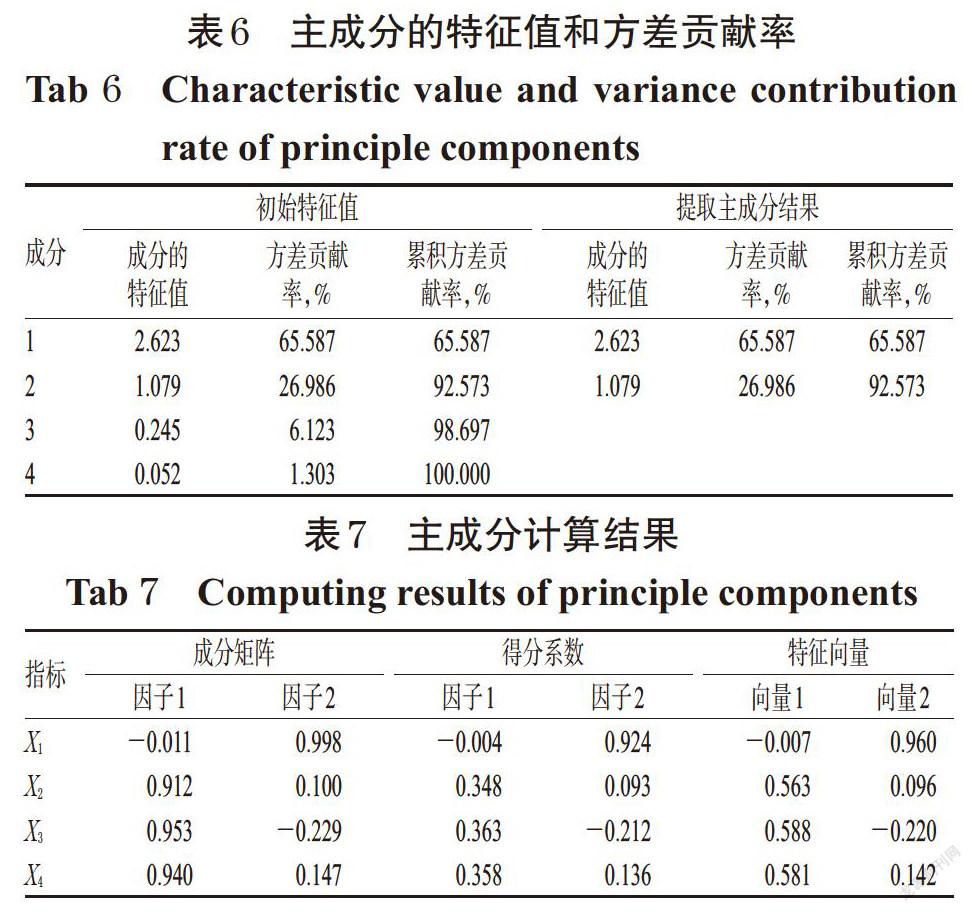
2.2.2 特征值和方差贡献率 由于4个指标成分含量差异较大,故先采用SPSS 20.0软件对数据进行标准化处理,结果见表6。由表6可知,前2个成分的特征值均大于1,且累积方差贡献率为92.573%(>80%),故此2个成分可反映半枝莲饮片中4个指标成分的大部分信息,因此可提取这两者为主成分对42批样品进行质量评价。
2.2.3 模型建立 采用SPSS 20.0软件,根據“成分矩阵”中各主成分对应的载荷,选择菜单中“转换”“计算变量”,得到特征向量,结果见表7。
采用SPSS 20.0软件,主成分“抽取方法”选择“相关性矩阵”,经最大方差法旋转,旋转因子显示设置“降序排列”,同时根据特征向量矩阵建立主成分分析模型[9]:
F=65.587%F1+26.986%F2
F1=-0.007X1+0.563X2+0.588X3+0.581X4
F2=0.960X1+0.096X2-0.220X3+0.142X4
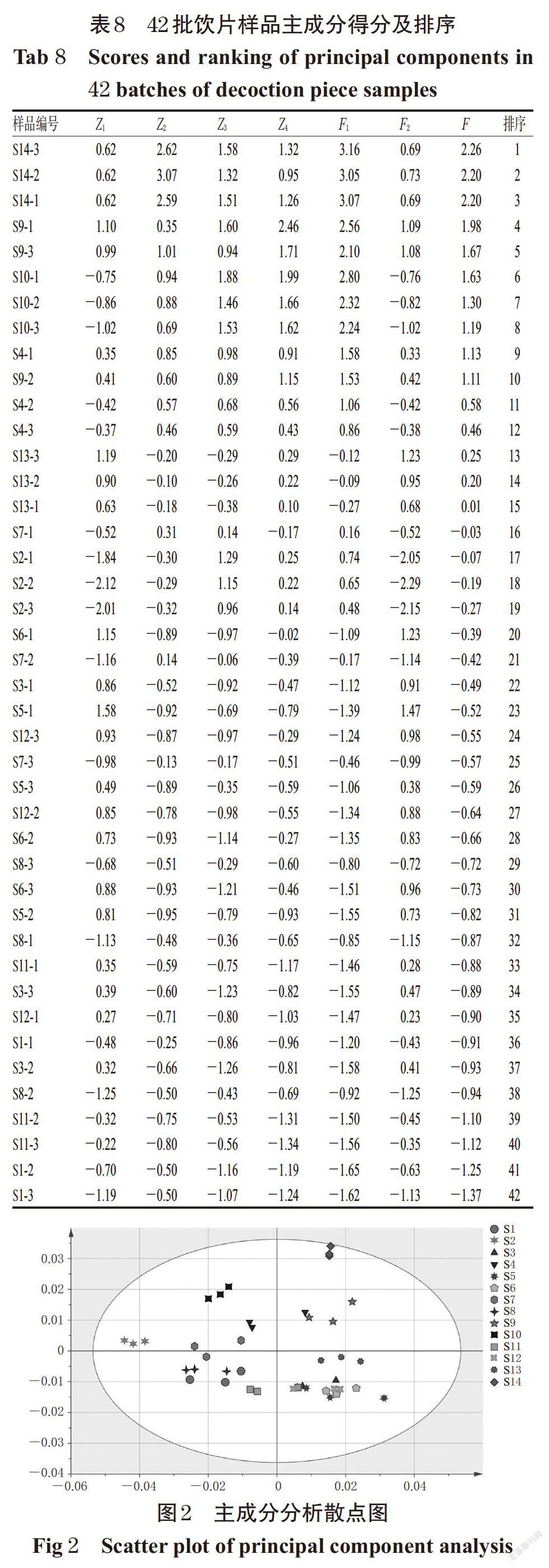
X1、X2、X3、X4分别为野黄芩苷、野黄芩素、木犀草素、芹菜素原始变量标准化后的变量,F1、F2为主成分1和主成分2得分,以各主成分的贡献率对主成分得分进行加权平均,得到综合得分(F),结果见表8。由表8可知,样品S14-3综合评分最高,整体质量相对较好,S14-2、S14-1次之,这3批样品均系半枝莲种植基地采收药材加工饮片(注:Zi表示各成分标准化数据)。
将42批样品含量测定结果的原始数据导入SIMCA-P 13.0软件进行标准化处理,数据标度方式选择“Pareto Scaling”,然后进行主成分分析。由于从4个指标成分中提取了2个指标成分为主成分,故选择生成二维散点图,详见图2。由图2可知,42批样品分布在4个象限,第一象限有7批样品,分别为S14-1、S14-2、S14-3、S9-1、S9-2、S9-3、S4-1;第二象限有10批样品,分别为S10-1、S10-2、S10-3、S7-2、S7-3、S4-2、S4-3、S2-1、S2-2、S2-3;第三象限有9批样品,分别为S11-2、S11-3、S8-1、S8-2、S8-3、S7-1、S1-1、S1-2、S1-3;第四象限有16批样品,分别为S13-1、S13-2、S13-3、S12-1、S12-2、S12-3、S11-1、S6-1、S6-2、S6-3、S5-1、S5-2、S5-3、S3-1、S3-2、S3-3。
3 讨论
本研究考察了甲醇-0.1%甲酸水溶液[5]、乙腈-1%冰醋酸水溶液[12]、甲醇-0.1%磷酸水溶液[13]、甲醇-1%醋酸水溶液等不同流动相系统的洗脱效果。结果发现,甲醇洗脱能力强,色谱峰分离度较高,色谱峰形在以1%醋酸水溶液为水相时较好,但以甲醇-1%醋酸水溶液为流动相进行洗脱时,存在野黄芩苷峰纯度及分离度不高的情况,故加入一定比例乙腈,以甲醇-乙腈(80 ∶ 20,V/V)-1%醋酸水溶液为流动相进行梯度洗脱。在此流动相系统下,野黄芩苷、野黄芩素、木犀草素与其相邻色谱峰的分离度均大于1.5,理论板数以野黄芩苷峰计大于10 000。
含量测定结果显示,野黄芩苷、野黄芩素、木犀草素、芹菜素含量分别为0.52%~1.25%、0.03%~0.25%、0.01%~0.05%、0.02%~0.12%。野黄芩苷含量最高,是半枝莲的代表成分,但仅以野黄芩苷为指标进行含量测定过于单一,不能全面反映半枝莲饮片的整体质量。虽然野黄芩素、木犀草素、芹菜素含量较低,但不同产地样品中这3种成分含量差异较大[14],故仍然有必要对其进行含量测定和主成分分析。
主成分分析主要是对样本的数据矩阵进行降维,取其主要成分进行投影分析和判别分析[15],该分析方法可从复杂的结果中筛选出主要影响因素,以突出主要问题,使复杂的问题简单化,得到观察结果中的一般聚类、趋势或异常值[16]。本研究的主成分分析结果显示,S14-3综合得分最高,S14-2、S14-1次之,S1-3为最低(-1.37分),提示42批样品质量存在较大差异。S14-1、S14-2、S14-3样品综合得分较高,均为半枝莲种植基地药材生产,可能与国家中药标准化项目实施后,企业通过对半枝莲进行科学化管理和规范化种植[17],采用传统产地加工方式(产地整枝晒干进行产地加工[18]),按照最佳炮制工艺切制,使得药材成分损失小,总黄酮、野黄芩苷、浸出物含量均较高,饮片质量更加稳定有关[19-21]。散点图结果显示,S14-1、S14-2、S14-3紧密聚集,表明该企业样品质量稳定,可与其他企业样品明显区分开。
半枝莲于1990年被收录入《中国药典》(一部)[22],入药部位为“唇形科植物半枝莲(Scutellaria barbate D. Don)的干燥全草”,但经产地走访、市场调研等发现,半枝莲每年可采收3~4次,几乎不存在全草入药的情况。究其原因,可能为半枝莲初入1990年版《中国药典》(一部)时为野生,采收多为连根拔起,故全草入药;近些年半枝莲被列入国家重点推荐发展的63种紧缺中药材之一,实现了农田规模种植,故采收时仅“割取地上部分”,以干燥地上部分入药。虽然半枝莲全草皆可入药,但结合市场实际流通情况,建议有关标准将其入药部分改为“唇形科植物半枝莲(Scutellaria barbate D. Don)的干燥全草或地上部分”。
参考文献
[ 1 ] 国家药典委员会.中华人民共和国药典:一部[S].2015年版.北京:中国医药科技出版社,2015:118.
[ 2 ] 林敬明,刘煜,罗荣城.半枝莲的化学成分及其抗肿瘤作用的研究现状[J].中药材,2006,29(4):407-410.
[ 3 ] 牛国晓,李洁.半枝莲抗肿瘤机制研究进展[J].肿瘤防治研究,2012,39(2):231-233.
[ 4 ] 胡晨骏,何菊,谢佳东,等.基于复杂网络的中药半枝莲系统生物学信息挖掘方法[J].世界科学技术:中医药现代化,2018,20(9):1506-1514.
[ 5 ] 蔡芸芸,高嵩,刘鲁明,等.半枝莲提取物通过Hippo/YAP通路抑制胰腺癌PANC-1细胞的增殖、侵袭转移和成瘤能力的研究[J].中华中医药杂志,2017,32(7):2947- 2951.
[ 6 ] 林靖怡,刘韶松,明艳林.半枝莲化学成分及药理活性研究进展[J].亚热带植物科学,2015,44(1):77-82.
[ 7 ] 吴晓龙,崔思远,王琰,等.中药半枝莲有效成分抗肿瘤作用机制研究进展[J].中华中医药杂志,2018,33(4):1459-1462.
[ 8 ] 于江泳,张村.全国中药饮片炮制规范辑要[M].北京:人民卫生出版社,2016:84.
[ 9 ] 张茹萍,石森林,范永升,等. HPLC指纹图谱结合主成分分析评价不同产地雷公藤药材质量[J].中国现代应用药学,2014,31(11):1338-1344.
[10] 刘爽,张振凌,李军,等.基于主成分分析法评价不同种类辅料对酒白芍饮片的影响[J].中药材,2019,42(1):78-82.
[11] 靳贝贝,裴香萍,梁惠珍.青皮药材的HPLC指纹图谱建立及聚类分析和主成分分析[J].中国药房,2018,29(24):29-32.
[12] 周溦,林敬明,王素麗,等. HPLC测定半枝莲中野黄芩苷、黄芩素、木犀草素和芹菜素的含量[J].食品工业科技,2017,38(12):27-30.
[13] 田新宇,范翠梅,渠田田,等.半枝莲总黄酮中7种成分的含量测定及抗肿瘤活性[J].中国实验方剂学杂志,2017,23(1):61-67.
[14] 王治阳,安华. HPLC同时测定不同产地半枝莲中8个黄酮类成分的含量[J].中国现代中药,2017,19(7):978- 982、1000.
[15] COMEAU AM,DOUGLAS GM,LANGILLE MG,et al. Microbiome helper:a custom and streamlined workflow for microbiome research[J]. mSystems,2017. DOI:10.1128/mSystems.00127-16.
[16] 周培,周颖.乡村旅游企业服务质量理论与实践[M].成都:西南交通大学出版社,2016:143.
[18] 范菊娣,覃容贵,李相陵,等.不同采收期半枝莲中黄酮含量比较[J].医药导报,2016,35(9):987-990.
[19] 张洪坤,王其丰,郭长达,等.半枝莲的产地加工方法研究[J].时珍国医国药,2018,29(10):2398-2400.
[20] 李洁. HPLC测定半枝莲不同药用部位野黄芩苷的含量[J].辽宁中医杂志,2008,35(3):427-428.
[21] 邹箴蕾,吴启南.半枝莲不同药用部位总黄酮含量测定[J].广西中医学院学报,2004,7(3):72-73.
[22] 国家药典委员会.中华人民共和国药典:一部[S]. 1990年版.北京:人民卫生出版社,1990:96.
(收稿日期:2019-04-13 修回日期:2019-07-22)
(编辑:陈 宏)

