基于原子力显微镜的细胞破损有限元模型建立与分析
杜美洁,王 立,王 彬, 3△,李志强,闫晓鹏
(1.太原理工大学机械与运载工程学院,太原 030024;2.太原理工大学生物医学工程学院,太原 030024; 3.College of Engineering, Design and Physical Sciences, Brunel University London, UK)
1 引 言
在基因转移尤其是基因治疗中,微注射和基因枪技术需要用物理方法穿透细胞膜[1],所以在进行相关实验研究时,若利用软件提前对实验进行模拟,将有助于实验设计以及参数设置,减少实验样本的浪费,因此需要对细胞膜力学性能尤其是破坏时的应力应变有所了解。原子力显微镜具有高分辨率和高灵敏度的特点,它能够对活细胞进行扫描,得到细胞的表面形貌以及细胞表面某点的力曲线,从而获得细胞的力学特性。Bremmell等人在活性条件下使用AFM研究了红细胞间的相互作用力及变形,测得了细胞膜的弹性常数范围,验证了细胞是粘弹性材料,其变形与弹性和粘附力有关[2];Garcia等人利用AFM探针对活Hela细胞施加较大的力,使AFM探针穿过细胞膜和细胞骨架结构令膜被破坏,通过观察力-位移曲线上明显的突变跳跃来识别细胞膜是否破裂,得到不同高度下,细胞破膜力不同[3];Atilla等人对分裂期和间期的Hela细胞进行AFM实验,比较两种细胞在破膜实验中的力-位移曲线,得到了分裂期细胞较于间期细胞,破膜力较大[4]。
国内外学者建立了一系列细胞的有限元模型,Chizari对悬浮活细胞的微注射实验进行了有限元模拟,将细胞膜假设为线弹性,细胞质假设为牛顿流体,利用流固耦合的方法得到细胞穿破时的应变值[5]。程琴建立了一个细胞膜是线弹性、细胞质与细胞核是粘弹性的三层复合结构细胞模型,研究了细胞受到1PN剪切力时的应力分布情况[6];Unnikrishnan等人分别对肌动蛋白皮质,细胞质和细胞核设置了不同的粘性参数,研究了不同粘度对三者的力-位移曲线的影响[7];王带领通过流固耦合的方法,将细胞膜设为超弹性材料,细胞质为水,模拟了红细胞在光镊拉伸过程中的变形情况,从而得到其剪切模量等力学参数[8]。
综上所述,目前细胞有限元模型未考虑细胞膜破损瞬间的情况,仅对细胞弹性阶段进行了分析。据此,本研究基于原子力显微镜,对Hela细胞膜进行力学性质的研究,将实验与有限元模型相结合,把细胞膜假设为弹塑性材料,得到细胞膜破坏时的应力应变值。为今后研究细胞膜受外载时的破损条件,以及使用有限元软件模拟AFM和微注射操作过程提供一种新方法。此外,可利用预建立细胞破损模型的方法,提前模拟基因枪实验过程,以便对实验进行设计与改进,从力学角度提高实验命中率,增加基因导入细胞的表达成功率。
2 原子力显微镜实验
2.1 材料与试剂
AFM(德国Bruker),型号:Bioscope Catalyst;MLCT悬臂(德国Bruker)见图1,F Triangular探针(氮化硅材料),弹性系数为0.6 N/m;细胞培养控温平台(自制);人宫颈癌细胞(Hela细胞)购自ATCC,美国;低糖DMEM培养基、胎牛血清购自Gibco公司;35 mm培养皿购自NEST公司。

图1 MLCT悬臂和氮化硅探针Fig.1 MLCT cantilever and silicon nitride probe
2.2 细胞培养与样品制备
将Hela细胞培养于10%胎牛血清和1%双抗(青、链霉素)的低糖DMEM培养液中,置于5% CO2、37℃条件下培养。
取细胞间期的Hela细胞接种于35 mm培养皿,贴壁24 h后用于实验。在开展AFM探针压陷实验时,培养基中加入10 mmol/L的HEPES用于保持培养基pH值。
2.3 实验过程与结果
将铺有单层Hela细胞的样本在室温条件下固定于工作台上,安装F Triangular探针于探针保持架,并设置扫描频率为1 Hz,让针尖逼近样品表面,设定扫描范围为50 μm×50 μm,对细胞表面进行扫描,选择密度适中、较为清晰的部分,扫描Hela细胞表面形貌,见图2。

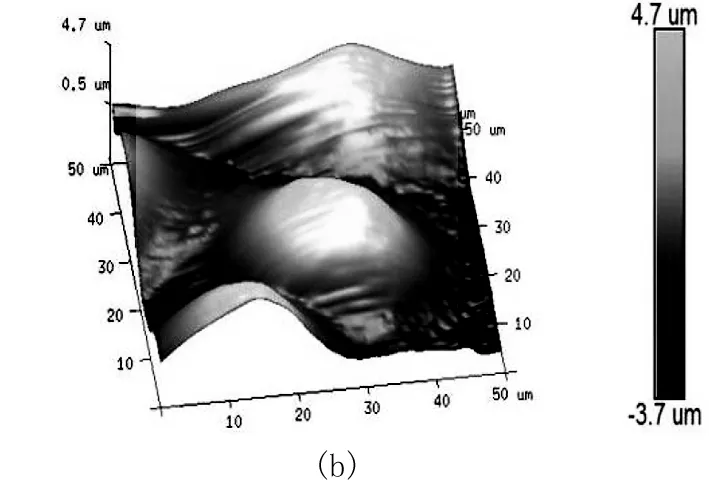
图2 细胞表面形貌 (a).细胞二维图; (b).细胞三维图Fig.2 Cell surface morphology(a).Two-dimensional cytogram;(b).Three-dimensional cytogram
实验利用原子力显微镜中的Contact模式,预先对探针的弹性系数及悬臂偏转灵敏度进行校正,设置针尖速度为1 μm/s,最大受力为55 nN,选择细胞高度约为3.5 μm的随机多组点进行实验,得到探针敲击细胞的力曲线,选择其中在均值范围内较为清晰的曲线进行分析,见图3。蓝色曲线为探针向下加载穿破细胞膜的力曲线,红色为探针达到最大力后卸载的力曲线,二者不重合的原因是细胞具有粘附力[3]。根据加载曲线在初始接触细胞时的弹性部分,可根据赫兹理论计算出细胞膜的表征弹性模量约为20 kPa,大于低加载力时的表面弹性模量。观察到加载曲线有明显突变跳跃点,根据Atilla等人研究结果[4]表明,探针在力曲线跳跃点处扎破细胞膜,此时探针距离初始接触细胞膜前进约2.35 μm,受力约为38.7 nN,且前期平缓,后期突变。
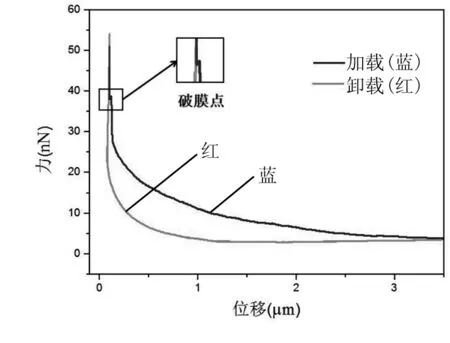
图3 力-位移曲线Fig.3 Force-displacement curve
3 有限元模拟
3.1 细胞本构模型
对Hela细胞模型作出基本假设[9-10]:
(1)实验位置位于细胞边缘,所以不考虑细胞核的影响;
(2)细胞整体表现为粘弹性,但细胞膜相对于细胞质而言厚度较薄,粘性可忽略不计;
Chizari[5]将细胞膜假设为线弹性,且实验表明探针穿破细胞膜后有不可恢复的残余变形,即将细胞膜假设为弹塑性,细胞质为粘弹性;
(3)细胞膜厚度均匀,不承受弯矩;
(4)细胞质和细胞膜为各向同性材料,在接触处有连续的速度场和位移场。
细胞膜假设为弹塑性材料,弹性阶段符合胡克定律,塑性阶段应用塑性非饱和模型Voce++模型[11]:
(1)
其中σs为屈服应力,εp为塑性应变,A、B、C、m均为需要拟合的参数。因实验数据十分有限,并不能从现有的数据中拟合到A、B、C、m四个参数,所以需要借助有限元软件,输入实验中已知数据,拟合出与实验对应的屈服应力、塑性应变等参数。
将细胞质设为粘弹性材料,使用Maxwell粘弹性模型[12],见图4。
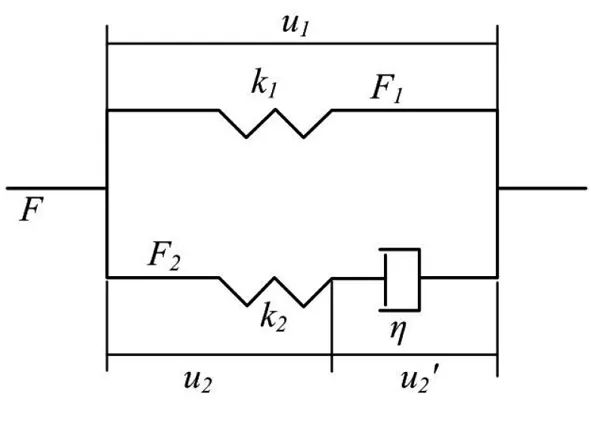
图4 Maxwell粘弹性模型Fig.4 Maxwell viscoelastic modelF=F1+F2
(2)
k1u1=F1
(3)
k2u2=ηu2′=F2
(4)
F为外力,u1、u2分别为分力F1、F2作用下弹簧产生的位移,u2′为阻尼的运动速度,k1、k2分别为弹簧的弹性系数,η为阻尼的粘性系数。
针尖即将穿破细胞膜造成局部破坏时,接触点应力超过屈服应力,产生塑性变形并在短时间内破坏,此时粘弹性细胞质只有纯弹性响应,考虑载荷继续作用期间细胞质粘性影响,根据余兴龙等人的研究结果[13],将细胞膜细胞质简化为弹-粘理想塑性半空间,可进行后续计算。
3.2 模型建立
采用ABAQUS对AFM实验过程进行有限元分析,将模拟结果与实验结果进行对比,相互验证,提高结论准确性。根据实验扫描得到的细胞形貌,并进行合理简化建立有限元模型。计算模型由基底、细胞膜、细胞质以及氮化硅探针四部分组成,其中基底、探针与细胞质采用SOLID单元,细胞膜采用细化的壳单元,见图5。
基底对实验和模拟的影响较小,所以假设为弹性模量较大的金属材料(如钢质板,弹性模量为206 GPa,泊松比为0.3);针尖为氮化硅材料(弹性模量为190 GPa,泊松比为0.28[12]);细胞膜采用弹塑性材料模型,利用最小误差修正法对塑性参数以及破坏参数进行拟合,根据实验曲线的弹性阶段测得表征模量为20 kPa,泊松比为0.3;细胞质采用粘弹性材料模型,根据原子力显微镜微切削加工实验结果,细胞质与细胞膜模量差为(0.288±0.08) kPa[14],泊松比为0.3,剪切松弛系数为0.6,松弛时间为25 s[15]。
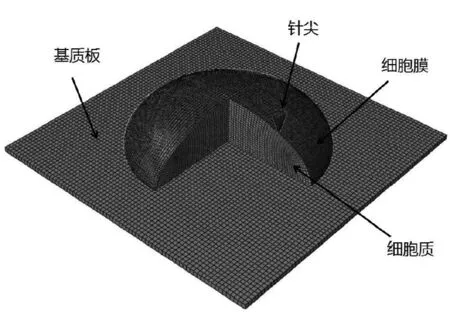
图5 三维计算模型Fig.5 3D computational model
研究中细胞为贴壁细胞,所以对基质板施加固定约束,根据实验对探针施加垂直细胞向下的恒定速度1 μm/s,并且当细胞膜破坏时停止运算。因破膜实验为准静态实验,故不考虑其应变率效应。
3.3 结果与分析
细胞膜受到探针冲击,最大接触力与最大位移均发生在针尖与细胞膜接触位置,通过对实验曲线的分析,拟合得到了细胞膜在被穿透前塑性穿透本构模型的屈服应力约为7 kPa,塑性应变为0.23。
当细胞膜破坏时,有限元计算显示此时接触点的位移为2.32 μm,力为39.3 nN,见图6、图7,与实验结果比较,误差范围在1.5%左右。图8为加载过程的细胞膜应力云图,随着针尖下移,应力逐渐增大为24.3 kPa,塑性应变为0.23,此时细胞膜破坏。

图6 破膜时轴向位移Fig.6 Axial displacement during membrane rupture
现选取细胞膜与探针接触点,对其应力与时间、应变与时间关系进行分析,见图9、图10。
图9为细胞膜与探针接触点应力随时间变化曲线,可以看出随着时间增加,应力也逐渐增加,直到细胞膜应力增大为最大应力24.3 kPa时,瞬时应力变为0,此时细胞膜被探针穿透;图10为细胞膜与探针接触点等效塑性应变随时间变化曲线,可以看出约0.7 s时进入塑性阶段,塑性应变随此时接触点塑性应变保持不变。随着时间增加而增大,直到约2.32 s时,探针位移达到2.32 μm细胞膜破坏,实验中探针位移为2.35 μm。

图7 破膜时受力图Fig.7 Force during membrane rupture
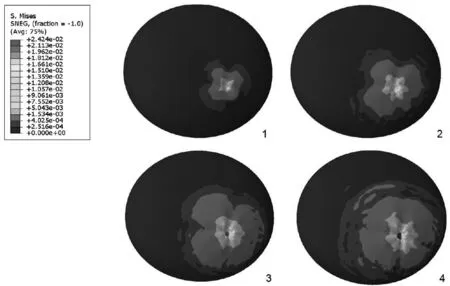
图8 破膜过程应力图Fig.8 Stress of the membrane breaking process

图9 应力-时间曲线Fig.9 Stress-time curve
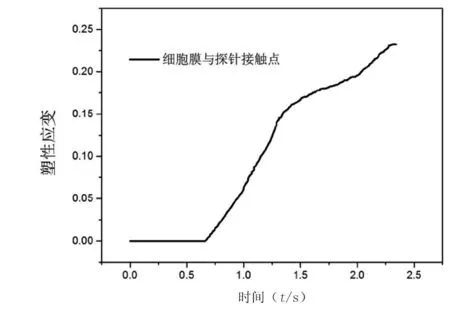
图10 塑性应变-时间曲线Fig.10 Plastic strain-time curve
4 结论与展望
通过原子力显微镜实验,得到Hela细胞破膜过程的力-位移曲线。从曲线中,不仅验证了细胞本质是粘弹性材料,受力随着针尖加载呈现非线性增加;而且从突变跳跃点得到了破膜力与破膜位移,即在细胞高度为3.5 μm处,破膜力为38.7 nN,破膜位移为2.35 μm,为未来研究细胞膜物理破坏提供实验依据。本研究将细胞膜设为弹塑性材料,细胞质设为粘弹性材料,通过实验数据与有限元模拟相结合的研究方法,拟合到了实验中无法得到的破坏参数,并确定了细胞膜破裂时受力为39.3 nN。验证了弹塑性模型可以很好地模拟Hela细胞膜破坏的整个过程,直观地显示细胞在受到针尖冲击时的形貌变化,为利用有限元模拟AFM、微注射、基因枪等实验过程提供了有效参数。
研究中有限元模拟结果与实验结果略有偏差,原因可能是:细胞骨架对细胞膜和细胞质的力学性能影响;加载速度和应变率效应的影响;卸载模型与加载模型不同,加载模型不能描述卸载(由于细胞具有粘附力)。将在今后的研究中进一步进行完善。

