细胞荧光断层图像的三维重建
唐伟健,付芸
(长春理工大学 光电工程学院,长春 130022)
随着观测技术的不断发展,单细胞水平的研究逐渐成为新的热点。细胞生物学通过观察细胞的形态结构、细胞器的运动和相互作用过程,揭示细胞生命活动的基本规律。因此,当研究一个生物系统时,可以通过观察单个细胞的生长与分化等生命过程,深入了解生物机体的结构。如果能够在分子水平上观察生物现象,将有助于更好地理解细胞表型细微的差异是如何诱导生物现象的,如学习和记忆,或细胞的特异性变化是如何导致功能障碍和诱发疾病的,例如癌症[1]。因此,对于细胞观测方法的研究,包括实现其三维可视化建模可以帮助理解癌症的形成机理,对分子动力学、生物仿生学、药物发现和遗传学的研究也具有重要意义。
本文采用共聚焦显微镜对已注入荧光探针的肿瘤细胞进行扫描,获取一系列轴向二维断层图像。激光共聚焦显微镜(CLSM)利用激光束经照明针孔后形成的点光源逐点扫描焦平面上的样本,样本上的被照射点经探测针孔后,成像在光电倍增管(PMT)或冷电耦器件(cCCD)上,并通过计算机屏幕输出荧光图像。照明针孔与探测针孔相对于物镜焦平面呈共轭关系,也就是说焦平面上的点同时聚焦于照明针孔和探测针孔处,而焦平面以外的点则无法通过探测针孔成像在探测器上,经过逐点扫描就得到样本上一个断层图像,再通过沿着轴向移动焦平面获得一组二维荧光断层图像。本文将数字图像处理技术,包括图像去噪、图像分割,以及三维重建等应用到细胞的荧光图像处理中,实现二维断层图像的三维可视化建模,从而更加直观地观测细胞的内部结构。
1 图像预处理
在共聚焦显微光学成像过程中,由于成像系统本身、光子转换过程、荧光组织结构和人为误差等因素的影响,采集的图像中必然包含噪声,特别是当利用强激发光进行厚组织断层成像时尤为明显,所以必须对图像进行预处理。
图像预处理是指在图像分割之前对细胞的荧光图像进行降噪与增强的过程。通过预处理可以提高二维荧光断层图像的质量,增强细胞膜和细胞器的局部与整体结构特征,改善细胞三维可视化的效果。本文采用数学形态学的降噪方法进行细胞荧光图像的预处理。
1.1 激光共聚焦显微镜图像采集
激光共聚焦显微镜(奥林巴斯FV-1000)最大分辨率4 096×4 096,每个通道4 096个灰度级(12-bit),配有 405 nm、458 nm、488 nm、515 nm、559 nm、623 nm的激光器,本实验选用405 nm氩离子和623 nm红色氦氖激光器,分别用于激发细胞核和细胞膜探针,读取细胞二维断层图像,通过沿Z轴移动焦点得到细胞的一系列二维断层图像。图1为共聚焦采集的一组二维断层图像。

图1 肝癌细胞荧光二维断层28层部分图像
1.2 数学形态学去噪算法
作为计算机数字图像处理技术的一个研究方向,数学形态学是基于集合理论和晶格理论的组合图像处理方法,用具有一定形态的结构元去度量和提取图像中的对应形状,以达到图像分析和识别的目的。形态学在处理复合运算时具有显著的优势,因而常用于图像处理中[2]。其优势在于采用并行处理算法,既能保留图像中原有信息又能有效地滤除噪声,与基于微分运算的边缘提取算法相比,基于数学形态学提取的边缘信息平滑、图像骨架连续,且断点少。
数学形态学包括腐蚀和膨胀两个基本运算。腐蚀用结构元与目标图像进行逻辑运算,可以消除二值图像中不相关的细节。腐蚀使图像的边界收缩,导致目标区域范围缩小,而区域内的孔洞变大。运算公式可表示为:
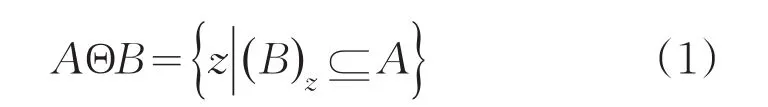
膨胀会扩大前景图像的边界,使得图像区域扩大,而区域内的孔洞变小。运算的表达式为:
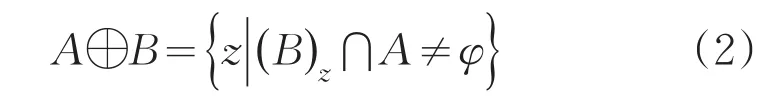
腐蚀与膨胀具有不同的处理目的。腐蚀运算可以消除图像中无意义的小物体。膨胀运算主要是为了弥补目标图像中的小空洞,因而具有去除内部噪声的作用。这两种算法通过结合形成开运算和闭运算。开运算是先腐蚀再膨胀,主要功能是对内边界点进行平滑处理,并保持图像边缘形状和位置不发生变化,其表达式为:

闭运算是膨胀之后再进行腐蚀,主要目的是对目标图像的细小空洞、外部边缘毛刺及小桥噪声点进行弥补,可表示为:

开运算和闭运算的用途不同。开运算处理外部细节对图像所产生的影响,而闭运算处理内部细节对图像的影响[3]。腐蚀运算可以消除一些小的空洞,膨胀运算通过边缘扩展来消除边缘毛刺。通过对细胞图像的研究和对形态学四种运算的不同组合进行滤波,发现通过对闭运算、膨胀组合运算和腐蚀、开运算组合进行串联组合运行能够得到较好的去噪结果,线性组合得到组合滤波器的表达式如下[4]:

下图为采用形态学算法的不同组合模式进行图像去噪的效果对比。

图2 形态学组合滤波器的处理效果对比图
从图2中看出,使用开运算和腐蚀结合形成的滤波器,不仅可以抑制毛刺和小桥噪声点,而且能够保护细胞边缘信息。通过闭运算和膨胀的组合运算能够抑制小孔噪声和小缝噪声,获得平滑的细胞外边缘信息[5]。还对细胞内部的小空洞进行弥补保持了完整且平滑的边缘信息,基本消除图像的噪声。
2 图像分割
在共聚焦显微镜采集的二维断层图像中,会同时出现多个细胞,甚至部分细胞黏连、重叠等复杂现象。因此,必须对目标图像进行图像分割以获取单个细胞,这是细胞三维重建的前提。由于细胞的边缘不规则而且具有非线性特征,如果采用线性分割算法会损失一部分边界轮廓,而且会使重构算法更加复杂。本文运用数学形态学中的分水岭算法进行图像分割。
分水岭算法是基于拓扑原理演变而成的图像分割算法,拓扑表面上的高密度区域代表波峰,低密度代表波谷。用不同颜色的水(标志物)分别充满各个波谷(即局部最低点),随着水面升高,来自不同波谷、具有不同颜色的水汇合到一起。这时在水汇合的地方修建水坝,以防止水的融合。持续注水与修建水坝,直至所有的波峰都处于水面之下。这些水坝就是图像分割的结果。这种方法已经用于血液和骨髓标本的图像处理中[6]。
令 M1,M2,…,MR表示图像g(x,y)的区域最小值点的坐标集合,C(Mi)表示与区域最小值Mi相关联的分水岭中的点坐标的集合,min和max分别表示g(x,y)的最小值和最大值。令T[n]表示满足g(s , t)<n的坐标集合,即:
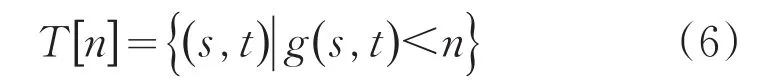
T[n]是g(x,y)中位于平面g(x,y)=n下方的点坐标的集合。
令Cn(Mi)表示集水盆地中与淹没阶段n的最小值Mi相关联的点坐标集,则Cn(Mi)可看成下式的二值图像:
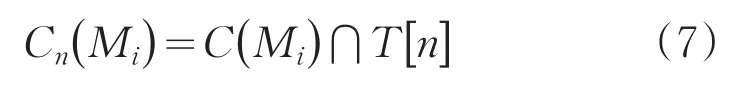
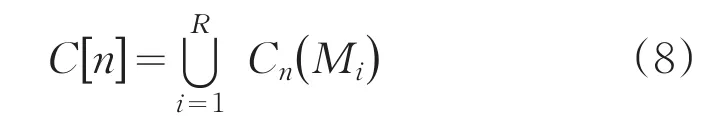
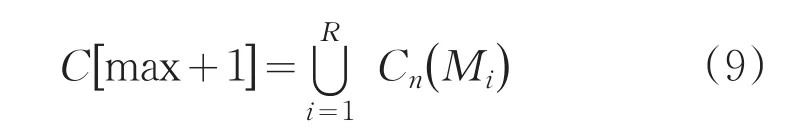
由公式(7)和(8)可知,C[n]是T[n]的子集,所以C[n -1]也为T[n]的子集,则C[n -1]中的每个连通分量都是T[n]的一个连通分量。
但是,由于细胞图像中的特殊性,图像边缘会存在很多的局部极值点,影响分水岭算法出现过度分割现象。首先,需要去除影响分割效果的区域极值点,然后将去除后的极值点的像素点在二值图像中用“1”表示。通过对图像中的前景和背景部分进行标记,分别为内部标记和外部标记。并且使内部标记指向背景,外部标记指向前景,通过标记的最小值可以确保分割线可以在内部标记和外部标记之间的区域,从而确保图像分割的合理性和精准性,降低了过度分割程度保持图像边缘完整并取得较好的效果。图3为分水岭算法分离出的细胞膜及细胞核。

图3 分水岭分割细胞核和细胞膜图像
3 三维重建
在细胞形态学研究中,主要使用共聚焦显微镜来观察细胞器的形态结构,而共聚焦显微镜只能获取细胞的二维图像,无法观测完整的三维结构,所以三维重建将有利于更好地认识细胞。
由于受荧光断层图像层间距的限制,为了提高数据分辨率,需要进行插值处理来改善细胞的三维可视化的效果。一般而言,断层图像的插值方法包括基于灰度的插值方法、基于形态学的插值方法和基于小波变换的插值方法[7-8]。基于形态学的插值算法是通过已知的断层图像的形状,直接构造出插值图像的轮廓[9]。由于细胞边缘不规则,且具有非线性的特征,所以本文选用形态学插值算法。
首先,创建起始对象和目标对象作为两个相邻的断层图像。然后提取各层的边缘轮廓,创建插值层。两个断层图像之间的插值表明两层之间的过渡信息,插值的目的是使两层平滑过渡。
为了比较形态学的差异,将两个断层图像重叠得到一个具有形态学差异的图像,见图4。Ⅲ是重叠区,Ⅰ和Ⅱ分别属于起始对象X1或目标对象X2,这两个区域表示断层图像之间的形态学差异。插值运算时,将Ⅱ和Ⅲ之间的边界向区域Ⅱ移动,从而使区域Ⅲ扩大。同样地,区域Ⅰ收缩直至最后消失。
为了简化运算,如图4,将结构元B的中心移动到x′。B0是在X1外法线方向一侧,Bi在内法线方向一侧。为了计算每一个插值,用Xn+1代替X2表示目标层,则在起始对象X1和目标对象Xn+1之间共有n-1个插值层,即X2,X3,…,Xn的计算公式:
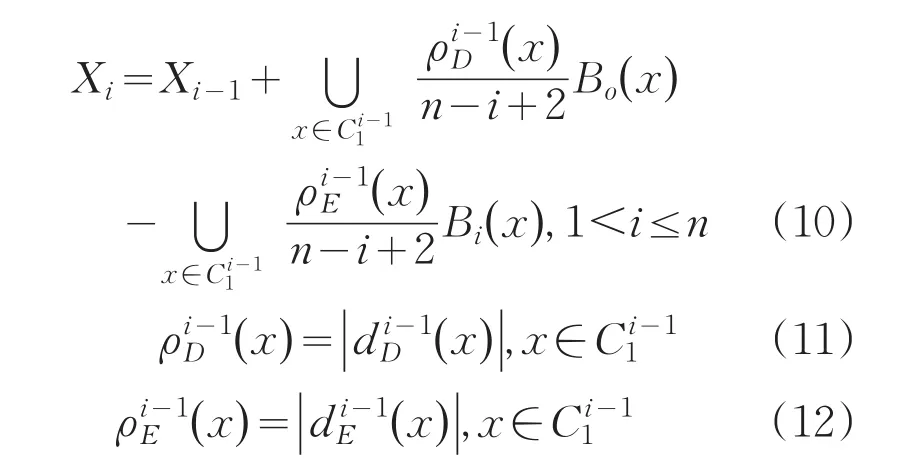
式中,n为层间距;为第(i-1)层的目标轮廓;为在第(i-1)层的位置x处分别进行膨胀与腐蚀的结构元的大小;和为形态学差异向量。
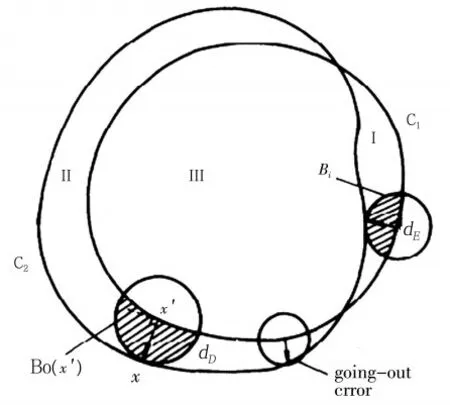
图4 算法原理图
采用八邻域方向链法跟踪起始对象的边缘轮廓,根据左手定则始终保持起始对象位于跟踪过程的左侧。然后,对于每个链单元,可以通过将单元顺时针旋转900定位外法线方向,因此,轮廓上每一点的外法线方向可以通过几个邻域链单元的外法线方向加权来计算[10]。
已知起始层与目标层的间隙为0.044 μm,采用4层插值,重构的细胞三维结构如图5所示。

图5 实验输出三维图像
由于细胞图像采集时,细胞培养液共聚焦皿中,所以只能采集出细胞为半封闭形态,重构结果可以看出符合细胞采集时的状态。相对于一般的插值法而言,对断层图像进行形态学插值三维重构,可以使两断层间创建的插值层图像从起始层图像不断接近于目标层图像,通过边缘方向的变化进行形态学补偿有效的使三维结构边缘平滑并且没有明显的层间阶梯感。但是由于插值层插入有限,可能会对图像的边缘结构进行破坏从而细胞三维结构的精准性还有待提高。
4 结论
目前,激光共聚焦显微镜是用于观察细胞形态的主要工具,但是它仅能获取细胞的二维断层图像,而无法得到三维结构。本文运用数字图像处理技术对采集的二维荧光断层图像进行三维重建,实现细胞的三维可视化。
本文通过图像预处理、图像分割和图像三维重建等方法完成细胞外形及内部结构的重构。首先采用数学形态学降噪算法对细胞荧光图像进行降噪处理。相对于常规算法,比如中值滤波、空间滤波和小波滤波等而言,形态学方法能够获得更好的降噪效果,同时还能保护图像边缘的非线性特征,取得更好的边缘平滑效果。本文通过对比腐蚀、膨胀、开运算和闭运算等几种形态学算法的处理结果,从中找出适合细胞的荧光图像处理的组合滤波器。其次,采用分水岭算法进行图像分割。由于细胞边缘具有非线性特征,常用的线性分割算法无法满足需要。因此,本文采用形态学中分水岭算法进行图像分割,通过构建水坝与分离集水盆的方式提高分割效果,保持细胞器边缘完整且不失真。最后,运用形态学插值的方法对相邻两幅图像进行层间插值实现三维重建,输出细胞的三维可视化结构。
本文的研究成果将为细胞生物学和生物动力学等方面的研究提供基础,活细胞的三维可视化技术将大大提高细胞实验的观测效果。

