芬顿法处理含酚废水的实验研究
苗秀荣,李同发
(太原工业学院 环境与安全工程系,山西 太原 030008)
伴随我国社会经济的日益发展,各个行业都在这一过程中获得了一定进步,但是,自古以来,发展和环境破坏就处于一个矛盾的状态,因此,在各行各业欣欣向荣的背景下,每年所产生的废水也越来越多,而水作为人类不可或缺的重要资源,若是受到污染,则会给人们的日常生活形成巨大影响,可以说是灾难性的。特别是含酚废水来源广泛,且危害性大,很多工厂的日常生产工作中,都会有含酚废水产生,进而影响到人们的日常生活,更是给植物、动物及人类的生命健康带去威胁。所以,关于水中的含酚浓度,我国进行了明确规定。当前,对于含酚废水中的酚类物质降解,主要采用的方法有生物法、化学法以及物理法。
H.J.H.Fenton[1]在一次苹果酸的研究实验中,因实验条件的pH为酸性,在过氧化氢的存在下,将亚铁离子加入进去后,发现会明显加快苹果酸的氧化速度,遂得出,在两者存在的前提下,会有一种促进氧化的物质产生,因此,他展开了深入研究,对芬顿试剂的发明形成了促进,在后续的相关研究中,芬顿试剂运用愈加广泛,被用来治理多种废水,如硝基苯废水、甘醇废水、除草剂废水、农药废水以及苯酚废水等,所收获的处理效率均较理想,应用前景十分广阔。
在本次研究中,重点改变了四种影响因素,即反应时间、pH值、Fe2+、H2O2投加量,对含酚废水模拟展开处理。然后在含酚废水经过各种影响因素处理后对吸光度进行测定,将相应的COD去除率和含量求出,确定出反应的最佳条件。
1 实验部分
1.1 实验药品
本次实验所采用的药品主要有如下:氯化铵(分析纯)、铁氰化钾(分析纯)、硫酸汞(分析纯)、重铬酸钾(分析纯)、硫酸银(分析纯)、4-氨基安替比林、邻苯二甲酸氢钾(分析纯)、FeSO4·7H2O(分析纯)、30% H2O2溶液、苯酚(分析纯)、硫酸溶液等。
1.2 实验仪器
本次实验所采用的仪器主要有752型紫外可见分光光度计、YHCOD-100型COD自动消解回流仪、pH计以及78-1型磁力加热搅拌器等。
1.3 实验方法
将一定浓度的苯酚溶液配好之后,在250 mL锥形瓶中倒入50 mL废水样,加入NaOH溶液或是稀硫酸将pH调节到指定值,后将30%的H2O2和一定质量的硫酸亚铁加入进去,在磁力加热搅拌器上放好,经过约20 min的反应时间后,将之取下来,用消解仪进行消解,消解时间为30 min,当结束消解后,要等待消解管冷却,温度降到60℃为宜,这时候就需要从装置上取下三角瓶,静置,冷却至室温,取上清液在600 nm处用分光光度计测其吸光度,将COD值求出,也就是反应完后水溶液中COD的浓度,COD的去除效率采用公式计算η为:
η=(C0﹣Ce)/C0×100%
式中,η:废水中COD的去除率,%;
C0: 废水 COD的初始浓度,mg/L;
Ce: 处理之后的COD浓度,mg/L。
2 结果与讨论
2.1 H2O2投加量对COD去除率的影响
分别取五份100 mL的含酚废水放到250 mL的锥形瓶内,初始浓度为100 mg/L,COD为2492 mg/L,采用盐酸将pH值调节为4,将FeSO4·7H2O 2.5 g加入后,进行不同体积的过氧化氢投加,反应1 h后,取上清液对其吸光度进行测定,结果见图1。
从图1中,我们能够看出,在氧化氢投加量较低的时候,COD的去除率也不高,这便说明一定范围内和投加量是呈正相关,去除率达到顶峰的时候为92.34%,这时候加入的氧化氢为4 mL,若仍进行投入量的加大,则不会使去除率出现变化,甚至还会有减少的情况出现。之所以如此,是由于羟基已经完全氧化分解了这时候废水中的有机物,形成了有着稳定化学性质的溶液,因此,就算投入更多的H2O2,也不能给芬顿试剂与废水中有机物的反应产生促进作用,并且,会因为H2O2的过量影响到COD的测量,而若投入较少的过氧化氢,这时候也不能把FeSO4·7H2O中的Fe2+完全氧化为Fe3+,产生的羟基自由基不足,也会给去除水中有机物产生影响,导致测出的吸光度偏大[2]。因此,H2O2的最佳投加量为4 mL。
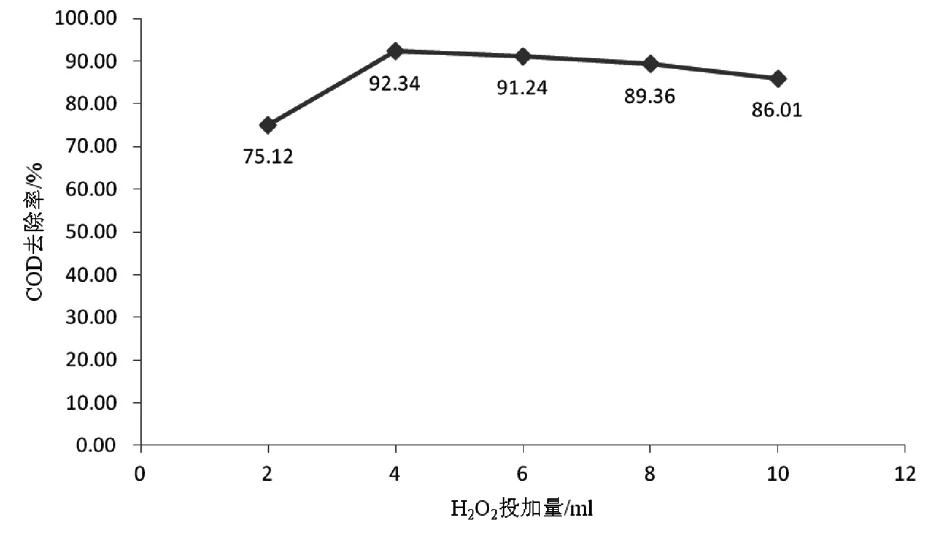
图1 H2O2投加量对COD去除率的影响
2.2 FeSO4·7H2O投加量对COD去除率的影响
分别取五份100 mL的含酚废水放到250 mL的锥形瓶内,初始浓度为100 mg/L,COD为2492 mg/L,使用盐酸对pH值进行调节使之为4,将4 mL H2O2加入进去,并加入质量不同的硫酸亚铁,反应1 h后,静置,取上清液测其吸光度,结果见图2。
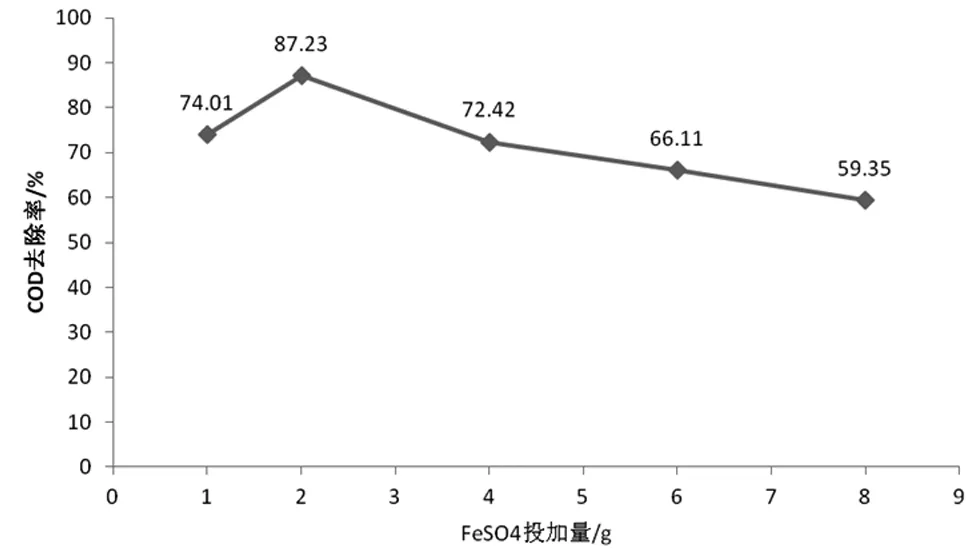
图2 FeSO4·7H2O投加量对COD去除率的影响
从图2中我们能够不难发现,COD去除率达到顶峰的时候为87.23%,投加量为2 g,随着不断加入,持续降低着去除率,之所以如此,是因为芬顿试剂中,FeSO4·7H2O中的亚铁离子是作为催化剂的,过多的投加量,会导致溶液中催化剂有着较高的含量,进而出现过多的·OH,但这时候水中的有机物基本已经反应完了,剩下的·OH不但无法起到任何的作用,还会出现·OH大量聚集的情况,同时,互相反应释放出氧气与水,给去除率形成直接影响;然而,若是投加量较少,伴随投加量的不断加大,COD去除率呈持续上升趋势,这是因为开始的时候,Fe2+比较少,不会产生较多的羟基,因而去除率也就不高,随着投加量的加大,羟基产生更多,也就提高了COD的去除率。所以,FeSO4·7H2O最佳投加量为2 g。
2.3 pH值对COD去除率的影响
分别取五份100 mL的含酚废水放到250 mL的锥形瓶内,初始浓度为100 mg/L,COD为2492 mg/L,采用NaOH或是盐酸对溶液进行调节,使之在2~10,然后分别加入FeSO4·7H2O 2 g,4 mL H2O2,反应1 h,取上清液对其吸光度进行测定,结果见图3。
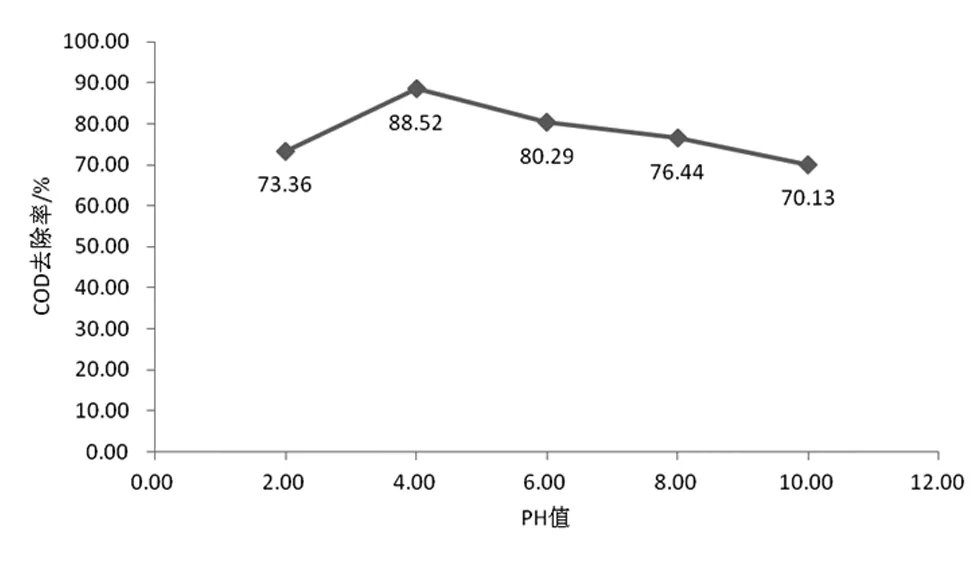
图3 pH值对COD去除率的影响
通过分析上图我们能够得知,COD去除率最高的时候,pH值调节为4,在pH过低的时候(强酸性),Fe3+不易被还原为二价铁离子,导致溶液中Fe2+不足,并且与过氧化氢所反应生产的羟基量也不够,这就使得不能完全将水中有机物进行氧化分解,使之成为水与二氧化碳,增大了吸光度,也相应降低了COD的去除率。在一定的范围内,去除率的增加是随pH增大一同变化的;但是,若pH值大于4的时候,不仅不能增加去除率,还会由于过高的pH,降低H2O2的活性,给其自身的分解形成抑制,由于无法产生足够的羟基自由基量,造成水中有较多的剩余有机物,进而增大了所测吸光度,也会相应降低COD去除率。总而言之,这项实验的最佳pH值初步确定为4[3]。
2.4 反应时间对COD去除率的影响
分别取五份100 mL的含酚废水放到250 mL的锥形瓶内,初始浓度为100 mg/L,COD为2492 mg/L,使用盐酸对pH值进行调节使之为4,然后分别将FeSO4·7H2O 2 g,4 mL H2O2,加入进去,不同反应时间,取上清液测其吸光度,结果见图4。
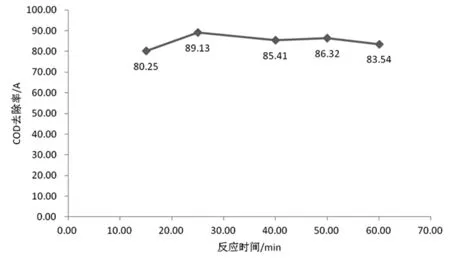
图4 反应时间对COD去除率的影响
通过分析上图,我们能够发现25 min的反应时间,去除率达到峰值为89.3%,去除率伴随时间的延长,不会减少反而会增加,但是变化范围不大,且均比89.13%小。之所以如此,是由于去除率在刚开始的时候会跟时间的推移呈正比关系,但反应到一定程度之后,基本去除完了有机物,这时候形成的溶液有着较为稳定的性质,因此,不会再较大受时间的影响,所以,25 min为最佳的反应时间。
3 结论
通过系统实验研究芬顿法处理含酚废水,得出的结论有如下:
(1)25 min的反应时间,温度为常温,pH值为4,H2O2投加量为4 mL,FeSO4·7H2O投加量为2 g,这时候COD去除率为峰值。因此,这是芬顿法处理苯酚溶液的最佳条件。
(2)在处理含酚废水的过程中,芬顿法的效果较为良好,并且反应条件相对简单,经济性较强,很容易就能够备齐药品。伴随人们对环境问题的愈加重视,芬顿法将会获得更为广泛的运用[4]。

