LIX63和Versatic10萃取体系中镍钴锰的协萃机制研究
吴 霞,朱 山,李 松
(六盘水师范学院 化学与材料工程学院,贵州 六盘水 553000)
红土镍矿中除含有镍、钴等有价金属外,也含有钙、锰、镁等杂质。酸浸过程中,这些杂质也会进入到浸出液中,使后续分离提纯工艺更加复杂,所以,需要对浸出液先进行预处理,除去钙、镁等大部分杂质[1]。从含钙、镁、锰等杂质的硫酸盐体系中萃取分离钴、镍,可以采用Versatic10(HA1)和LIX63(HA2)协萃体系[2-9]。该协萃体系对镍的萃取速率较慢,萃取10 min后萃取率仅为82%,反萃取速率也非常缓慢[2],不利于工业应用。从负载钴的LIX63有机相中反萃取时速率也非常慢,反萃取率仅49%,如果体系中鼓入空气,还会使LIX63中毒,造成钴反萃取率进一步下降;但Versatic10与LIX63协同萃取时,反萃取速率却非常快,即使鼓入空气76 h之后,反萃取率仍高达99%以上[2-3]。
Versatic10和LIX63协同萃取钴、镍的机制研究未见有报道。斜率法[10-15]可用以研究铜、钴、镍的萃取机制,得到萃合物的组成[12-14],因此,试验采用斜率法研究此协萃体系萃取钴、镍的机制。
1 试验部分
1.1 有机相和水相的配制
料液用分析纯硫酸锰、硫酸钴、硫酸镍和去离子水配制[11-15]。所有料液均采用0.5 mol/L硫酸钠作惰性电解质,离子强度μ=3 mol/L。试验用水均为去离子水。
Versatic10(HA1):Shell Chemicals公司产品,使用前未经纯化。
LIX63(HA2):由巴斯夫(BASF)上海公司提供,采用铜离子螯合法[16]进行纯化。取一定量LIX63,减压蒸馏除去其中的溶剂,剩余成分溶解在乙醚中,与铜氨溶液混合萃取,分相后,对含有铜螯合物的有机相进行蒸馏除去乙醚,然后过滤,并用丙酮多次洗涤,风干后将滤渣溶解于乙醚中,用1 mol/L硫酸溶液反萃取得到纯LIX63。
有机相:Versatic10+纯化LIX63+正己烷。
1.2 试验方法
为确定不同体系萃取Ni2+、Co2+、Mn2+时萃合物的组成,采用不同浓度、不同体系的萃取剂与不同pH、离子强度3 mol/L的NiSO4、MnSO4、CoSO4溶液于100 mL分液漏斗中混合萃取,料液体积20 mL,有机相体积20 mL,在(40±1) ℃恒温振荡器中振荡30 min,静置3 min后分液,得萃余液和负载有机相。
为确定Versatic10与LIX63协同萃取分配比随温度的变化情况,取20 mL浓度为0.5 mol/L的LIX63和Versatic10的混合有机相,与等体积初始pH=5、离子强度3 mol/L的NiSO4、MnSO4、CoSO4溶液于分液漏斗中混合萃取,分别在不同温度下恒温振荡30 min,静置3 min后分相,得萃余液和负载有机相。
1.3 分析和表征方法
用1H-NMR谱和FT-IR谱对纯化后萃取剂LIX63进行表征。
水相金属离子浓度用ICP-OES法测定,有机相中金属离子浓度用差减法计算求得,分配比D通过计算求得。
2 试验结果与讨论
2.1 纯化LIX63的表征
用铜离子螯合法提纯的LIX63的1H-NMR和FT-IR图谱分别如图1、2所示。
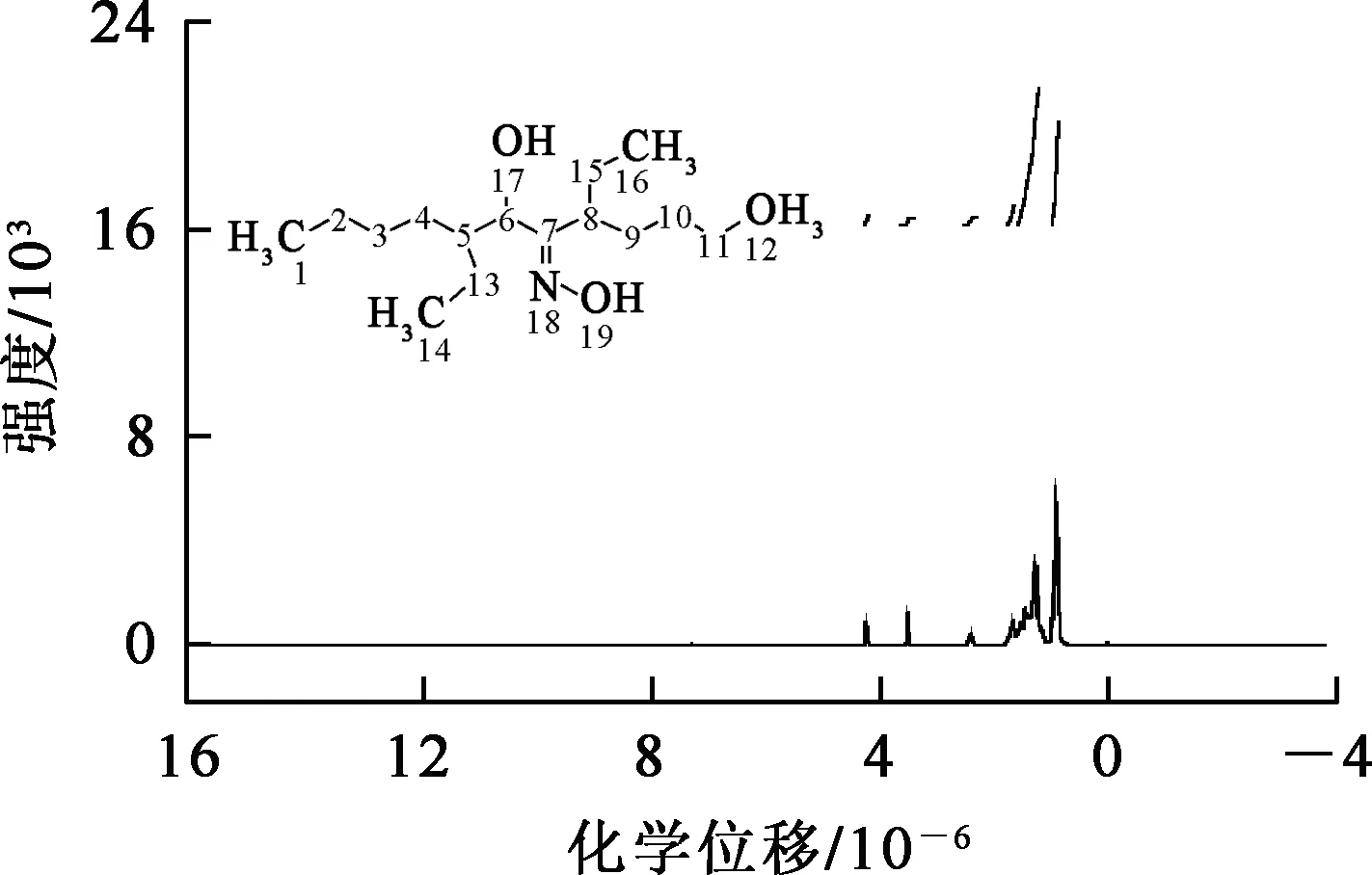
图1 LIX63的1H-NMR分析图谱

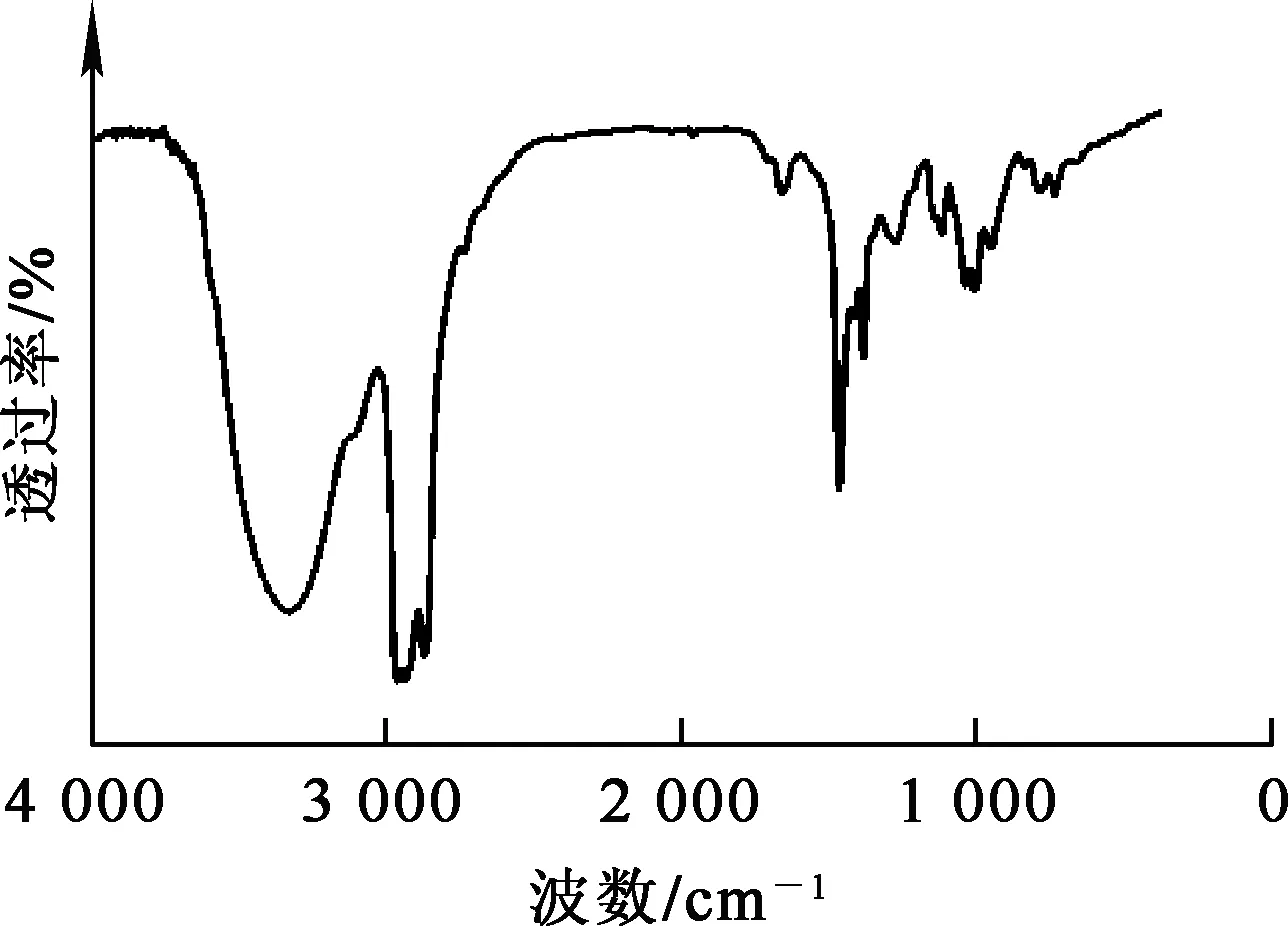
图2 LIX63的FT-IR分析图谱

2.2 LIX63和Versatic10配比对萃取分配比的影响
采用不同配比、不同浓度LIX63和Versatic10与pH=5、离子强度3 mol/L的Ni2+、Mn2+、Co2+溶液混合。混合萃取剂中,LIX63和Versatic10总浓度为0.1 mol/L,配比不同。2种萃取剂浓度与配比对萃取分配比的影响试验结果如图3所示。由图3(a)看出:分别用LIX63和Versatic10萃取,萃取分配比都很低,萃取剂浓度对分配比影响不大,表明2种萃取剂对Ni2+、Mn2+、Co2+的萃取率很低。由图3(b)看出:LIX63和Versatic10的物质的量比为2/3时,协萃体系对Ni2+、Co2+的萃取效果较好,对Mn2+的萃取效果较差,表明LIX63和Versatic10协萃体系在一定配比范围内对Ni2+、Mn2+、Co2+有协萃作用。
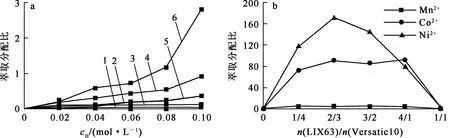
1—Versatic10(Mn2+);2—LIX63(Mn2+);3—Versatic10(Co2+);4—LIX63(Co2+);5—Versatic10(Ni2+);6—LIX63(Ni2+)。
2.3 萃合物的组成及相关热力学函数
2.3.1 Versatic10浓度、平衡pH对萃取分配比的影响
用Versatic10萃取金属离子,用0.5 mol/L的Na2SO4溶液调水相离子强度为3 mol/L。Versatic10浓度与平衡pH对萃取分配比的影响试验结果如图4所示。
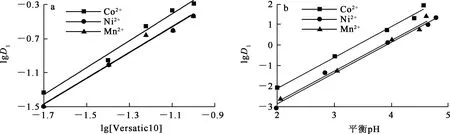
图4 Versatic10浓度与平衡pH对萃取分配比的影响
由图4(a)看出:lgD1与lg[Versatic10]呈线性变化,Versatic10萃取Co2+、Ni2+、Mn2+时的直线斜率分别为1.54、1.58和1.52,根据电中性原理[10]可规整为2,表明Versatic10萃取Co2+、Ni2+、Mn2+时每个萃合物分子中可能有2个Versatic10分子;由图4(b)看出:lgD1与平衡pH呈线性变化,萃取Co2+、Ni2+、Mn2+时的直线斜率分别为1.56、1.54和1.50,表明Versatic10萃取1分子金属离子时萃取剂失去2分子氢离子。根据图4结果,结合文献[19-20],可合理推断出Versatic10萃取Co2+、Ni2+、Mn2+时的萃合物组成为[M(A1)2],反应式可能为
式中,M代表Co2+、Ni2+和Mn2+。
2.3.2 LIX63浓度与平衡pH对萃取分配比的影响
用LIX63萃取金属离子,水相用0.5 mol/L Na2SO4调节离子强度为3 mol/L。LIX63浓度与平衡pH对萃取分配比的影响试验结果如图5所示。由图5(a)看出:lgD2与lg[LIX63]呈线性变化,LIX63萃取Ni2+时的直线斜率为1.54,可规整为2;LIX63萃取Co2+、Mn2+时的直线斜率分别为0.81和0.91,可规整为1。结果表明:单独用LIX63萃取Ni2+,复合分子中含有1个金属离子和2个LIX63分子;单独用LIX63萃取Co2+和Mn2+,复合分子中含有1个金属离子和1个LIX63分子。由图5(b)看出:lgD2与平衡pH呈线性关系;萃取Co2+、Ni2+、Mn2+时的直线斜率分别为1.61(可规整为2)、0.15和0.19(可规整为0),表明LIX63萃取1分子镍离子失去2分子氢离子,而LIX63萃取Co2+、Mn2+时不失去氢离子。因此,根据图5结果,结合文献[20-21]及电中性原理[10],合理地推断出:LIX63萃取Ni2+时,其萃合物组成可能为[Ni(A2)2];萃取Co2+、Mn2+时,其萃合物组成可能为[M(HA2)SO4]。因此,LIX63萃取镍时的反应式可表示为
LIX63萃取Co2+、Mn2+时的反应式可表示为
式中,M代表Co2+和Mn2+。

图5 LIX63浓度与平衡pH对萃取分配比的影响
2.3.3 萃取剂配比、平衡pH对萃取分配比的影响
水相用0.5 mol/L的Na2SO4溶液调离子强度为3 mol/L。有机相中LIX63与Versatic10的配比与平衡pH对萃取分配比的影响试验结果如图6所示。
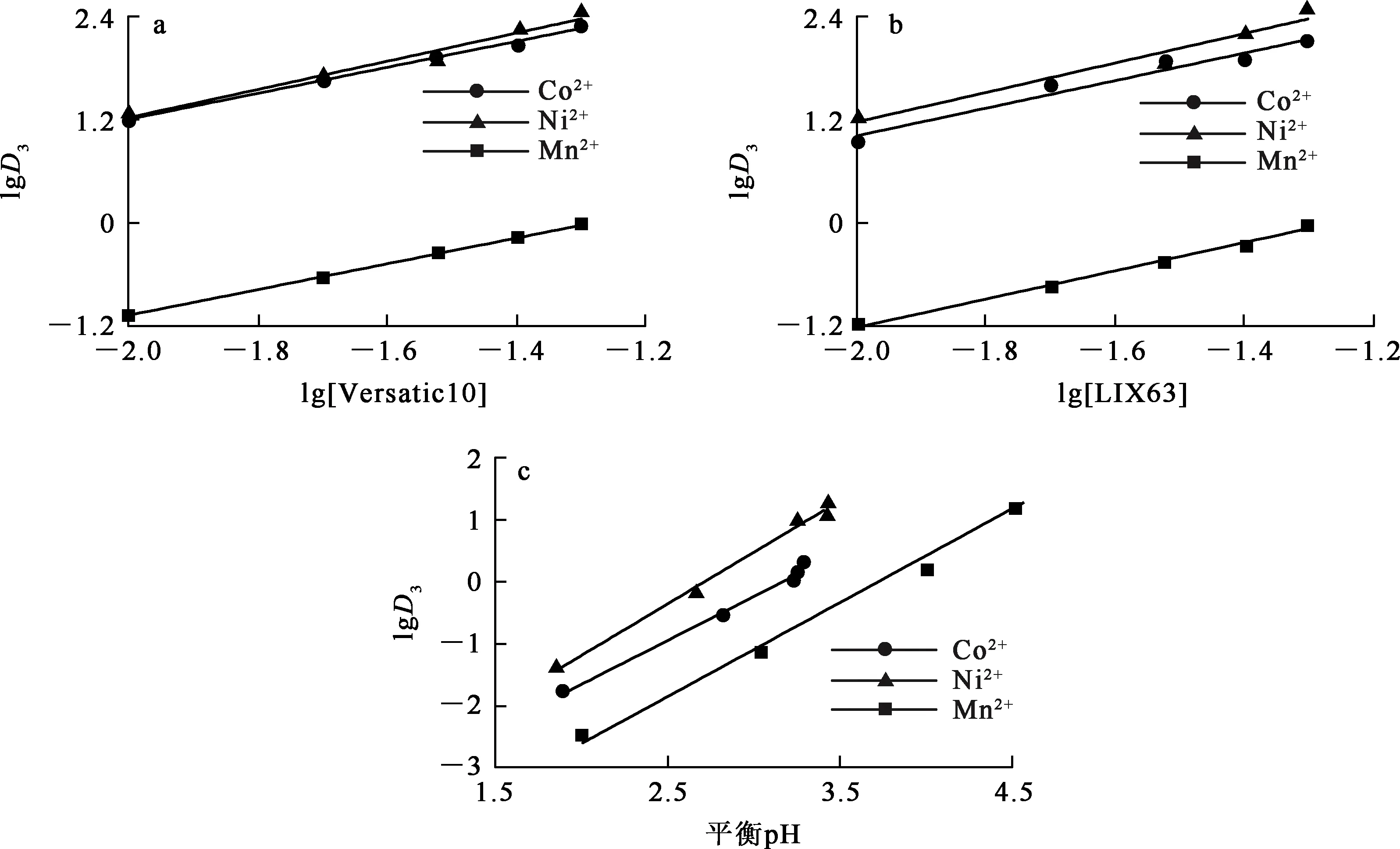
图6 萃取剂配比与平衡pH对萃取分配比的影响
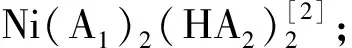

式中,M代表Co2+、Ni2+和Mn2+。
2.3.4 温度对协萃体系萃取分配比的影响
在不同温度条件下,用0.05 mol/L LIX63+0.05 mol/L Versatic10有机相协同萃取金属离子,水相离子强度为3 mol/L。温度对萃取分配比的影响试验结果如图7所示。
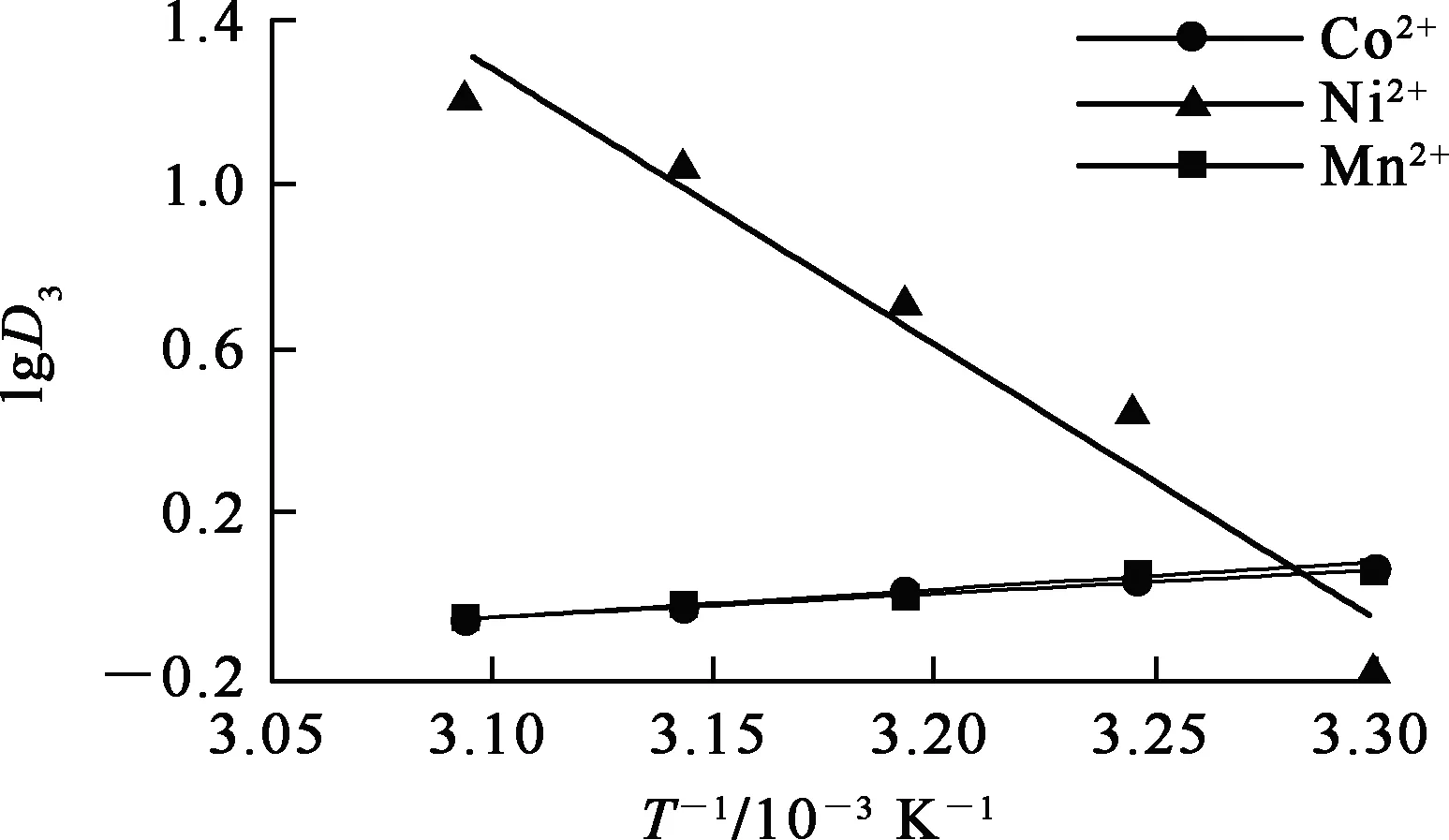
图7 温度对协萃体系萃取分配比的影响
由图7看出:萃取Ni2+、Co2+、Mn2+的直线斜率分别为-6 704.13、636.95和587.88,据此可计算出反应的ΔH[10,13]及40 ℃时的ΔG和ΔS。计算结果见表1。
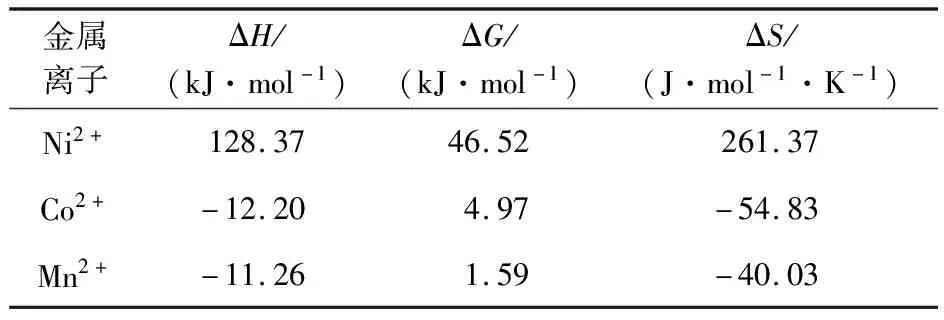
表1 协同萃取体系萃取Ni2+、Co2+、Mn2+过程中的相关热力学参数
由表1看出:协萃体系萃取过程中的ΔG均大于零,表明萃取过程不能自发进行;萃取Ni2+时ΔH>0,萃取Co2+和Mn2+时ΔH<0,表明Ni2+萃取过程中吸热,升高温度有利于萃取;而萃取Co2+和Mn2+过程放热,降温有利于反应进行。萃取Ni2+的ΔS>0,符合熵增原理,而萃取Co2+和Mn2+的ΔS<0,表明萃取过程中水相金属离子脱水过程引起的熵变要大于形成萃合物过程所引起的熵变[22],因此,萃合物分子中可能有水分子参与配位[19],使得Co2+、Mn2+萃取率下降,这很好地解释了图3中LIX63和Versatic10协同萃取体系对Ni2+的协同效应最强。
3 结论
采用斜率法研究LIX63和Versatic10协同萃取体系对Ni2+、Co2+、Mn2+的萃取行为,结论如下:
1)LIX63与Versatic10的物质的量比在1/4~4/1范围内,对Ni2+、Co2+有明显的协同萃取效应,对Mn2+基本没有协同萃取效应。
2)分别用Versatic10(A1)、LIX63(A2)及二者混合物协同萃取Ni2+、Co2+、Mn2+,形成的萃合物组成可能是Ni(A1)2、Co(A1)2、Mn(A1)2,[Ni(A2)2]、[Co(HA2)SO4]、[Mn(HA2)SO4]和[Ni(A1)2(HA2)2]、[Co(A1)2(HA2)2]、[Mn(A1)2(HA2)2]。
3)协同萃取过程中,ΔG>0,反应不能自发进行;协同萃取Ni2+时反应吸热,协同萃取Co2+、Mn2+时反应放热;协同萃取Ni2+时ΔS>0,协同萃取Co2+、Mn2+时ΔS<0,表明萃取过程中水相金属离子脱水过程引起的熵变要大于形成萃合物过程所引起的熵变。
斜率法可用于研究萃取机制,但适用于仅有一种萃合物生成的萃取过程,而且在实际应用中必须建立在许多近似处理前提条件下,如采用萃取剂总浓度代替达到萃取平衡时负载有机相中未参与反应的萃取剂浓度及萃取率不能太高等;对于协同萃取体系,萃取剂与萃合物分子间的相互作用、萃取剂分子间的聚合、萃取过程中不同化学计量比、多种萃合物的形成等因素都会影响试验结果。试验所得试验值与理论值存在一定偏差,可能是上述原因造成的,需进一步研究。

