g-C3N4-Ag3PO4/Fe3O4磁性光催化剂的制备及性能研究
朱鹏飞,王萍平,黄倩,熊贵霞,杨竞
(西南石油大学 化学化工学院 油气田应用化学四川省重点实验室,四川 成都 610500)
染料废水含大量有机污染物,采用常规方法难以有效治理[1]。光催化氧化法是能将有机污染物分解为简单无害物质的绿色氧化技术[2-3]。类石墨相氮化碳(g-C3N4)性质稳定,制备成本低,在光催化降解有机污染物方面潜力巨大[4]。但其可见光响应范围窄,比表面积较小,难分离回收[5-7]。将磁基体Fe3O4与g-C3N4复合,可增大其比表面积,实现催化剂的磁分离回收[6-8]。此外,将g-C3N4与适当的半导体复合,可以增强其可见光催化活性[2,8]。Ag3PO4半导体可见光响应能力强[9-10],且与g-C3N4存在导带电势差,将二者复合后,可提高催化剂的可见光响应范围和催化活性[2-3]。
采用超声混合法制备了g-C3N4-Ag3PO4/Fe3O4催化剂,对其进行了结构表征,并以光催化降解罗丹明B染料为探针,对光催化性能进行了评价。
1 实验部分
1.1 试剂与仪器
三聚氰胺、硝酸银、磷酸二氢钾、氨水、浓硝酸、三氯化铁、氯化亚铁、无水乙醇均为分析纯。
UV-1800紫外-可见分光光度计;PANalyticalX-射线粉末衍射仪(XRD);WQF-520傅里叶红外光谱仪(FTIR);Lambda 850紫外-可见漫反射光谱仪(UV-Vis-DRS );光催化反应仪,自制。
1.2 催化剂的制备
1.2.1 g-C3N4的制备 取适量三聚氰胺于密闭的坩埚中,置于马弗炉中,以5 ℃/min的升温速率升至530 ℃,保温4 h,待冷却后,研磨、装袋备用。
1.2.2 Ag3PO4的制备 取一定量AgNO3溶于 50 mL 纯水,搅拌20 min,滴加NH4·H2O调pH至7.0,滴加适量0.1 mol/L的KH2PO4溶液至黄色沉淀完全析出,继续搅拌2 h。洗涤2~3次,抽滤,80 ℃ 真空干燥12 h,研磨、装袋备用。
1.2.3 g-C3N4/Fe3O4复合物的制备 取制得的 g-C3N42.000 g 于30 mL无水乙醇和60 mL纯水的混合液中,超声分散2 h后加入0.140 g FeCl3和0.547 g FeCl2,80 ℃下搅拌30 min,滴加适量NH4·H2O至溶液完全变黑,继续搅拌30 min,待溶液冷却后,洗涤2~3次,抽滤,80 ℃真空干燥12 h,制得 g-C3N4/Fe3O4复合物。
1.2.4 g-C3N4-Ag3PO4/Fe3O4催化剂的制备 取制备好的g-C3N4/Fe3O4和Ag3PO4按质量比为1∶1分散于100 mL纯水中,避光搅拌30 min,再超声 30 min。洗涤2~3次,80 ℃真空干燥12 h,制得 g-C3N4-Ag3PO4/Fe3O4催化剂。
1.3 g-C3N4-Ag3PO4/Fe3O4对罗丹明B的光降解实验
配制5 mg/L罗丹明B溶液作为模拟染料废水,取30 mL废水于反应管,投加一定量的光催化剂,置于光催化反应器,从试管底部通入恒定流量空气,先暗反应 30 min,使催化剂与罗丹明B达到吸附-解析平衡,打开可见光源(65 W节能灯),光反应一段时间后取适量溶液离心,取上层清液,测得反应前后的吸光度A0和At,由公式D=[(A0-At)/A0]×100%计算降解率(D)。
2 结果与讨论
2.1 样品的XRD分析
g-C3N4、Ag3PO4、g-C3N4/Fe3O4和g-C3N4-Ag3PO4/Fe3O4的XRD谱图见图1。

图1 样品的XRD谱图Fig.1 XRD patterns of samples
由图1可知,g-C3N4在2θ为13.24°和27.65°处出现了典型的类石墨层晶体结构的特征衍射峰[3,8],表明所制备的g-C3N4确为类石墨相结构。纯Ag3PO4在20~80°范围内分别出现了立方晶相结构Ag3PO4不同晶面的特征衍射峰[9-10],表明Ag3PO4主要为立方晶体结构。在g-C3N4/Fe3O4的XRD谱图中,除了有g-C3N4的特征衍射峰出现,还在30.41,35.67,43.23,57.30,62.78°处出现了立方尖晶石型Fe3O4的特征衍射峰[6-7]。将Ag3PO4与 g-C3N4/Fe3O4复合后制得的g-C3N4-Ag3PO4/Fe3O4的三元催化剂中,g-C3N4、Fe3O4和Ag3PO4的特征衍射峰强度均发生了不同程度的减弱,这主要是复合后的三元催化剂中各组分含量相对降低引起的,但以上各组分特征峰的位置未发生明显变化,表明复合后的催化剂中g-C3N4、Fe3O4和Ag3PO4的晶体结构未发生明显改变。
2.2 样品的FTIR分析
g-C3N4、Ag3PO4、g-C3N4/Fe3O4和g-C3N4-Ag3PO4/Fe3O4的FTIR谱图见图2。

图2 样品的FTIR谱图Fig.2 FTIR patterns of samples
由图2可知,所有样品在3 125,1 636 cm-1附近均出现了很强的表面吸附O—H的伸缩振动和弯曲振动吸收峰。g-C3N4、g-C3N4/Fe3O4和g-C3N4-Ag3PO4/Fe3O4在1 563~1 234 cm-1和810 cm-1左右分别出现了g-C3N4的类石墨层结构的C—N六元杂环的系列振动吸收峰和g-C3N4中三嗪环弯曲振动吸收峰[2,8],并且二元和三元催化剂中的 g-C3N4吸收峰的峰型和位置与纯g-C3N4相比未发生明显变化,表明复合后的催化剂中的g-C3N4保持了完整的类石墨层结构,这与XRD表征结果一致。此外,与纯g-C3N4相比,g-C3N4/Fe3O4还在 560 cm-1左右出现了一宽散的Fe3O4中Fe—O特征吸收峰,且该样品中表面吸附O—H的吸收峰较g-C3N4显著增强,由此表明Fe3O4与g-C3N4的复合还增加了催化剂表面的羟基密度,这有利于催化剂吸附性能的提升[6],进一步观察g-C3N4/Fe3O4的谱图,发现该样品还在1 443 cm-1处产生了一个新的吸收峰,这可能是g-C3N4和Fe3O4在复合过程中通过分子间作用力发生了一定的相互作用引起的。对于纯Ag3PO4样品,其在1 007,550 cm-1处出现了P—O键的伸缩振动和弯曲振动吸收峰[10],将Ag3PO4与g-C3N4/Fe3O4通过超声混合法复合后,制得的g-C3N4-Ag3PO4/Fe3O4的表面吸附O—H吸收峰强度进一步增强。此外,该样品中P—O键吸收峰发生了一定程度红移,并在1 049 cm-1处出现了一个新的C—O键吸收峰,这可能是Ag3PO4在与g-C3N4/Fe3O4复合过程中Ag3PO4中的P—O与 g-C3N4发生了分子间的相互作用所致,由此也再次表明g-C3N4-Ag3PO4/Fe3O4中各组分不是简单的混合,而是通过分子间作用力发生了一定的相互作用。
2.3 样品的UV-Vis-DRS分析
g-C3N4、Ag3PO4和g-C3N4-Ag3PO4/Fe3O4的UV-Vis-DRS的谱图见图3。

图3 样品的UV-Vis-DRS谱图Fig.3 FTIR patterns of samples
由图3可知,纯g-C3N4和Ag3PO4在可见光区(400~800 nm)均表现出一定的可见光吸收能力,且纯Ag3PO4在可见光区的光吸收相对更宽更强,这与文献报道的一致[2-3]。与纯g-C3N4和Ag3PO4相比,g-C3N4-Ag3PO4/Fe3O4在可见光区的吸收能力进一步提升,且其吸收边红移程度更大,表明Ag3PO4和Fe3O4对g-C3N4的复合,有效缩短了其禁带宽度,使得g-C3N4-Ag3PO4/Fe3O4更易于被波长更长的可见光激发,产生光生电子-空穴对,从而促进光催化氧化反应的进行[8]。
2.4 催化剂用量对罗丹明B降解率的影响
分别取30 mL 5 mg/L的罗丹明溶液B于6支反应管中,不调pH(溶液初始pH在6.8左右),再分别加入不同用量的g-C3N4-Ag3PO4/Fe3O4,于可见光下反应120 min,实验结果见图4。

图4 催化剂投加量对罗丹明B降解率的影响Fig.4 Effect of catalyst dosage on the degradation rate of the Rhodamine B
由图4可知,当催化剂投加量较低时(0.33~0.83 g/L),随着催化剂质量浓度的增加,罗丹明B降解率逐渐升高,这是由于当催化剂用量较低时,催化剂与罗丹明B分子接触未达饱和,随着催化剂用量增多,光量子利用率增大,光生电子-空穴对数目增多,降解率显著提高。当催化剂投加量达到0.83~1.0 g/L时,其降解率趋于平缓,表明光生量子利用率趋于饱和,继续增加催化剂用量,由于反应体系浑浊度增加,影响反应体系对光的吸收,导致罗丹明B降解率略有下降,综合考虑经济性和光降解性能,催化剂投加量选取0.83 g/L。
2.5 反应时间对罗丹明B降解率的影响
取30 mL 5 mg/L罗丹明B于反应管中,不调pH,按0.83 g/L投加g-C3N4-Ag3PO4/Fe3O4催化剂(即催化剂加量为0.025 g),测不同反应时间下罗丹明B的降解率,实验结果见图5。
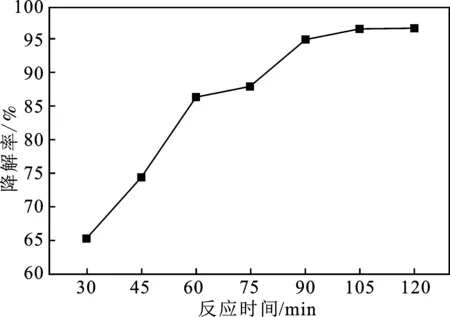
图5 反应时间对罗丹明B降解率的影响Fig.5 Effect of reaction time on the degradation rate of the Rhodamine B
由图5可知,随着反应时间不断增加,g-C3N4-Ag3PO4/Fe3O4对罗丹明B的降解率逐渐升高,当反应时间增至105 min时,其降解率趋于平缓,因此该反应体系反应时间可选取105 min。
2.6 溶液pH对罗丹明B降解率的影响
分别取30 mL 5 mg/L的罗丹明B于4支反应管中,调节溶液至不同pH值,按0.83 g/L投加 g-C3N4-Ag3PO4/Fe3O4催化剂,可见光下反应 105 min,实验结果见表1。

表1 溶液pH对罗丹明B降解率的影响Table 1 Effect of pH on the degradation rate of the Rhodamine B
由表1可知,g-C3N4-Ag3PO4/Fe3O4在溶液呈中性和弱碱性条件下对罗丹明B的降解活性优于酸性条件下的活性。导致该现象发生的原因可能是在酸性条件下催化剂表面带正电,而罗丹明B为阳离子型染料,不利于催化剂对罗丹明B的吸附催化,故光降解活性降低;其次,在酸性较大的条件下,还会影响·OH等光催化活性物种的产量,从而降低光催化效果[10],综合实验结果和废水排放要求,选择pH=7作为光催化反应的最佳条件。
2.7 光催化剂综合性能评价
在上述优选出的反应条件,分别投加g-C3N4和g-C3N4-Ag3PO4/Fe3O4光催化降解罗丹明B;此外,为考察催化剂处理其他染料废水能力,另配制 25 mg/L 的孔雀石绿、亚甲基蓝、龙胆紫溶液,按照优选出的处理罗丹明B的反应条件进行光催化降解实验,实验结果见图6。

图6 光催化剂普适性评价Fig.6 The universality of photocatalysts
由图6可知,在相同反应条件下,无论是对罗丹明B染料,还是对孔雀石绿等其他3种染料,g-C3N4-Ag3PO4/Fe3O4均表现出比纯g-C3N4更优的光催化降解能力,光催化活性和普适性良好。结合表征结果,该实验结果可归因于以下几个方面:①在g-C3N4-Ag3PO4/Fe3O4中,Ag3PO4和Fe3O4对g-C3N4的复合使g-C3N4-Ag3PO4/Fe3O4在可见光区的光吸收能力增强,且吸收边发生了一定程度红移,催化剂在可见光区的响应范围更宽,并表现出比纯g-C3N4更强的光吸收性能,使得催化剂活性得以提高;②g-C3N4、Fe3O4和Ag3PO4三者之间通过化学键成功复合,发生了一定的相互作用,并在催化剂表面引入了大量的吸附羟基,使得催化剂吸附性能得以提高;③g-C3N4与Ag3PO4存在电势差,二者的复合有效促进了催化剂光生电子-空穴的分离,延长了光生载流子寿命,提高了催化剂的活性和稳定性[2]。
此外,为评价催化剂的回用性能,采用磁分离技术对使用后的g-C3N4-Ag3PO4/Fe3O4进行回收。实验发现,在外加磁场的作用下,溶液中的g-C3N4-Ag3PO4/Fe3O4非常易于通过磁分离回收(见图6插图),且催化剂不易流失。将回收后的催化剂再次在上述优选出的反应条件下进行光催化降解罗丹明B,连续使用3次后,其降解率仍高于80%,表现出较好的稳定性。
3 结论
(1)通过超声混合法制备了一种可磁分离回收的g-C3N4-Ag3PO4/Fe3O4可见光催化剂。表征结果显示,催化剂中,g-C3N4呈现出典型的类石墨层状结构,Ag3PO4为立方晶相,Fe3O4为立方尖晶石型,g-C3N4、Fe3O4和Ag3PO4通过化学键成功复合,并拓宽了催化剂的可见光响应范围。
(2)光催化降解罗丹明B实验结果表明,在 g-C3N4-Ag3PO4/Fe3O4投加量为0.83 g/L,反应体系pH=7、可见光下反应105 min的反应条件下,该催化剂对5 mg/L的罗丹明B的降解率高达98.81%,且该催化剂易于通过磁分离回收再用,稳定性较好。此外,该催化剂对孔雀石绿等其他3种染料也表现出良好的光降解性能,普适性良好。

