1,2,4-苯并三嗪自由基的合成及应用研究进展
李淑昱, 林 渊, 张睿博
(西南民族大学 化学与环境学院 国家民委化学基础重点实验室,四川 成都 610041)
自由基是指含有未成对电子的原子、分子和离子,由于单电子的存在,化学性质比较活泼,具有独特的物理性质。稳定的自由基在电子器件、太阳能电池、锂离子电池、储能、电磁及生物应用材料的构建中占有重要的地位[1-12]。1900年,刚伯格发现了首例稳定的有机自由基[13]。此后,自由基化学得到了迅速的发展,大量稳定的有机自由基已被合成和分离,如氮氧自由基、三苯甲基自由基及其衍生物、噻唑自由基、主族较重元素自由基等[14-15]。而1,2,4-苯并三嗪自由基作为一种尤其稳定的自由基(Chart 1),自1968年Blatter首次合成以来,因其良好的热稳定性和化学稳定性、较低激发能等特性而受到人们的广泛关注[16-20]。

Chart 1
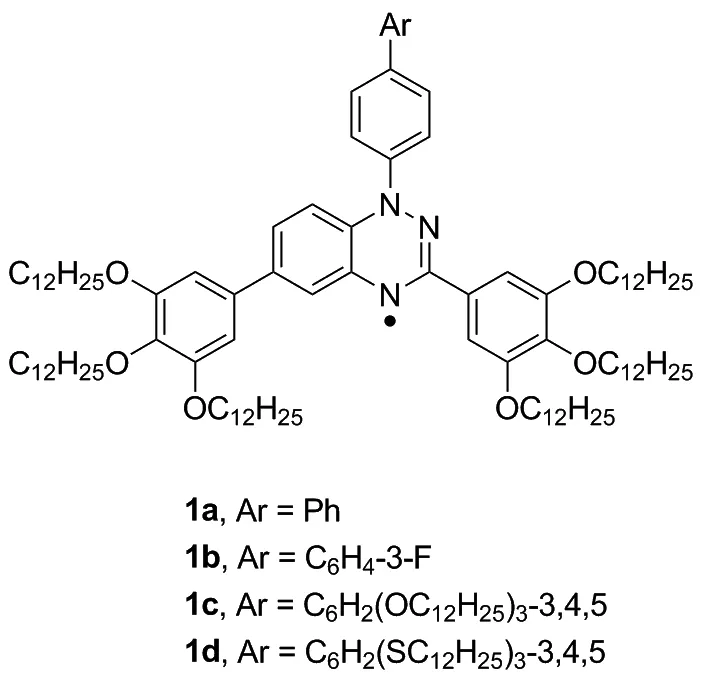
Chart 2
尽管1,2,4-苯并三嗪自由基发现较早,但是合成较为困难,多采用氧化苯三嗪的方式,产率较低[19,21]。2010年Koutentis课题组首次通过氧化腙胺化合物的方式合成了1,2,4-苯并三嗪自由基,极大提高了产率[22]。接着,研究者们通过不同的方法,如还原环化、增环反应、去氢氧化、氮杂Wittig反应法,制备了大量1,2,4-苯并三嗪自由基衍生物,并且发现其具有特殊的物理性质:很好的稳定性[19]、宽可见光吸收区域[23]、可逆的氧化还原电位[24-26]。这些独特的性质使1,2,4-苯并三嗪自由基衍生物在有机功能分子领域具有重要的应用。
本文综述了1,2,4-苯并三嗪自由基及其衍生物的合成方法,探讨了1,2,4-苯并三嗪自由基在各个领域的应用,同时对1,2,4-苯并三嗪自由基在功能材料开发中的应用前景进行了展望。
1,2,4-苯并三嗪自由基的合成方法大致分为五大类:氧化电环化(方法i)、还原环化(方法ii)、增环反应(方iii)、去氢氧化(方法iv)、氮杂Wittig反应(方法v)(Scheme 1)。
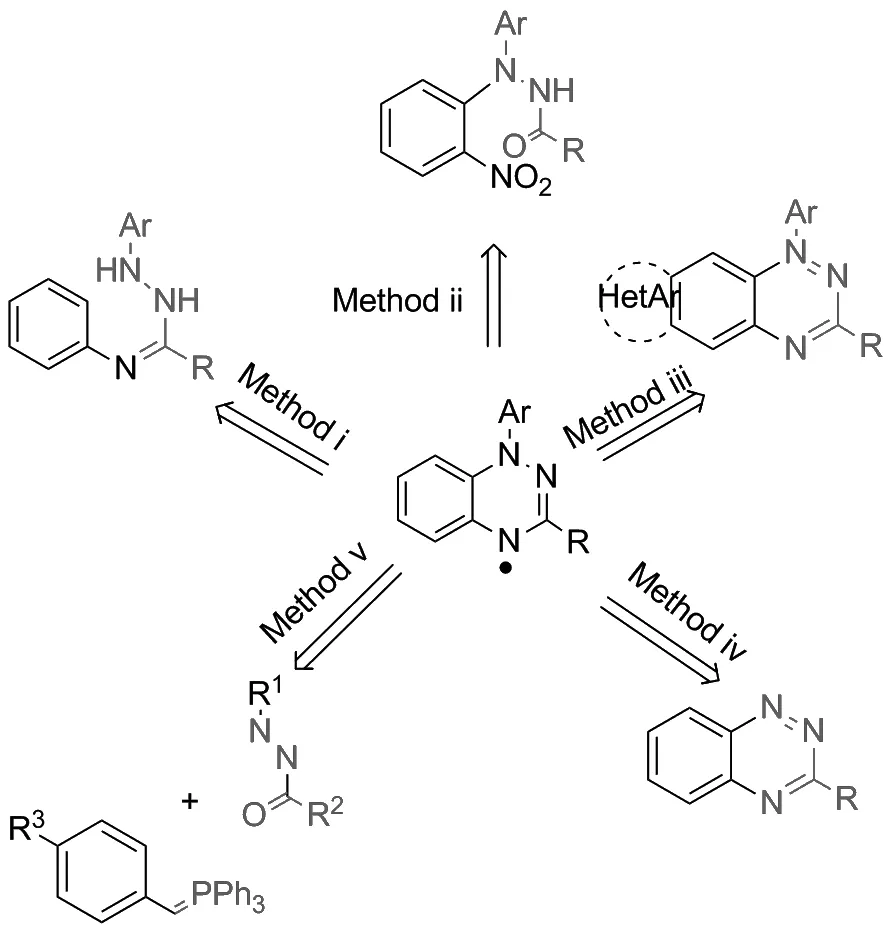
Scheme 1
1.1 氧化电环化
2010年,Koutentis课题组报道了1,2,4-苯并三嗪自由基及6个C-7(R=CF3, Cl,Br, I, Me, OMe)取代衍生物的合成;空气中,在Pd/C的催化下,1,8-二氮杂二环十一碳-7-烯(DBU)作为碱,于二氯甲烷溶剂中将相应的腙氨化合物环氧化生成1,2,4-苯并三嗪自由基,通过TLC检测分析反应是否完全;反应产物使用柱层析纯化,产率高达90%(Scheme 2)[22]。
2017年,Grant等用市售分析纯硝酸灵在乙腈中一步合成了1,2,4-苯并三嗪自由基,并进行了反应机理推测,水分子进攻硝酸灵的卡宾中心,发生裂解,伴随氧化环化反应(Scheme 3);通过此合成方式,将部分硝酸灵衍生物成功转化成了1,2,4-苯并三嗪自由基[27]。
1.2 还原环化
通过上述环氧化反应能够实现很高的产率,需要注意的是产率主要取决于腙胺化合物的纯度;但是此中间体不稳定,多数不能通过重结晶的方式提纯,为合成不同类型的1,2,4-苯并三嗪自由基衍生物带来了困难。
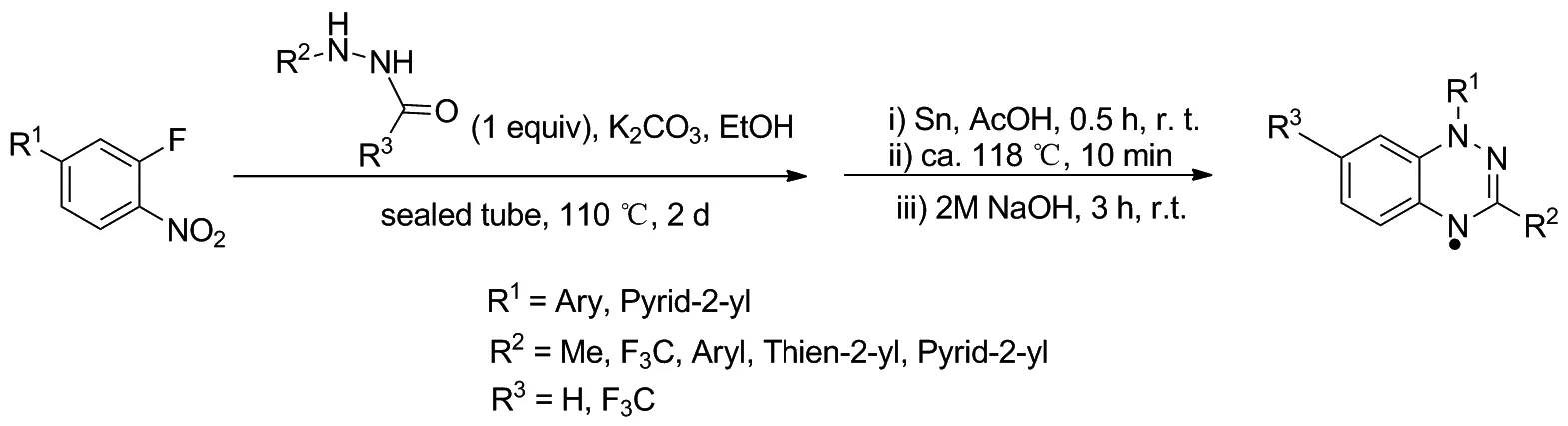
2014年Koutentis课题组通过还原环化反应合成了1,2,4-苯并三嗪自由基衍生物。首先通过多步反应制得酰肼化合物;室温下,将锡粉一次性加入到酰肼的醋酸溶液中加热回流反应,反应结束后冷却至室温,加入有机溶剂稀释;并用氢氧化钠溶液分解。此反应用锡粉作为还原剂还原得到胺,在冰醋酸作用下实现醛胺缩合,并成环;最后在苛性碱氢氧化钠溶液中分解得到1,2,4-苯并三嗪自由基衍生物。这种合成方法避免了不稳定中间体苯腙胺或其前体亚胺氯化物的合成,使反应更容易进行(Scheme 4)[26]。

Scheme 2

Scheme 3
Scheme 4
Scheme 5
Scheme 6
1.3 其他方法
(1)自由基参与的偶联反应
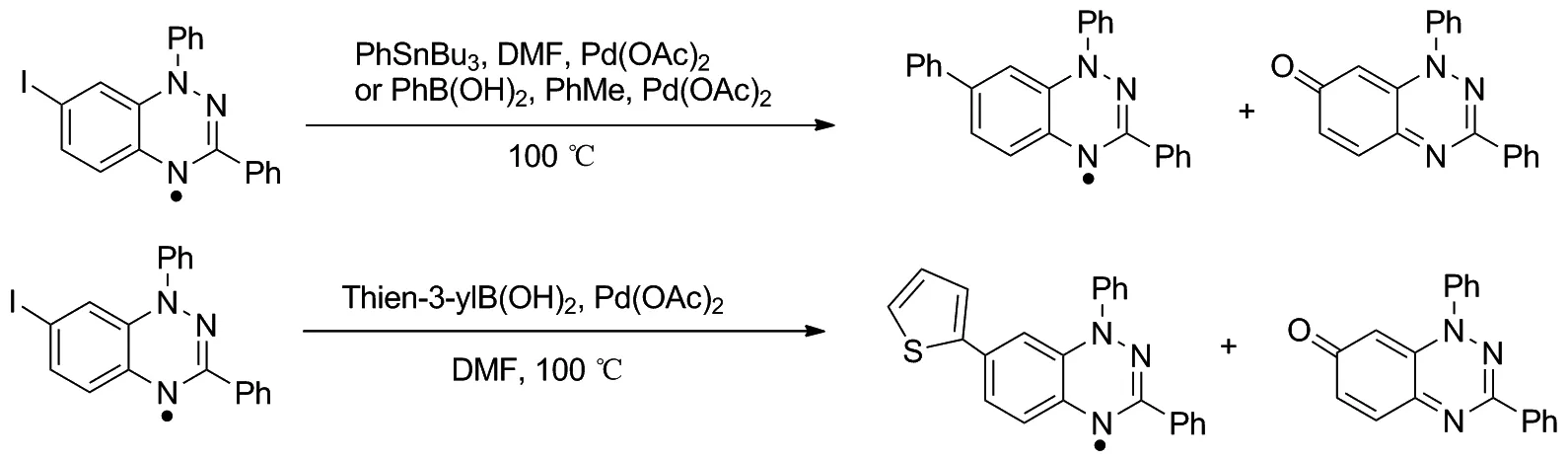
2011年,Koutentis课题组采用1,2,4-苯并三嗪自由基作为原料,进行Stille和Suzuki-Miyaura 偶联反应,可以得到一系列苯环、噻吩、呋喃、联苯取代的衍生物[28-31],是比较少见的稳定自由基参与偶联反应的例子(Scheme 5)。

Scheme 7

Scheme 8
Scheme 9

Scheme 10
将7-位碘代1,2,4-苯并三嗪自由基和苯基正丁基锡烷在醋酸钯催化下于干燥的DMF中发生Stille偶联,直到反应完全;或通过得到的碘代1,2,4-苯并三嗪自由基和苯取代硼酸在醋酸钯的催化下,碳酸钾提供碱性环境,于干燥的甲苯中发生Suzuki-Miyaura反应得到一系列7-位苯环及噻吩环取代1,2,4-苯并三嗪自由基衍生物。这两种反应均需要在惰性氛围中进行,反应产率都比较高,Stille偶联反应相对较快,但是Suzuki-Miyaura偶联反应得到的产物更加单一[28]。
(2)自由基官能团转换
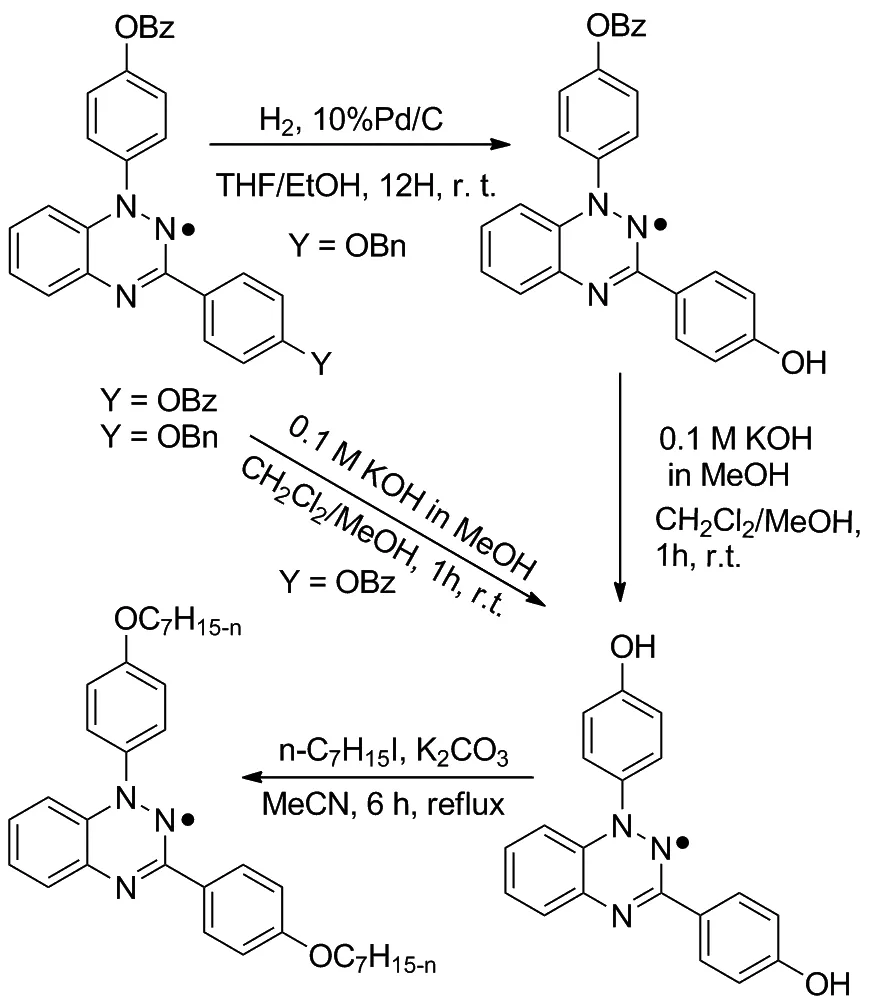
采用上述不同方法已经合成了部分1,2,4-苯并三嗪自由基,但是官能团的种类还比较少,并且多为7-位取代;2014年Kaszynński课题组合成了一系列OCOPh(OBz)、OCH2Ph(OBn)、NO2、CO2Me取代的1,2,4-苯并三嗪自由基衍生物,通过自由基的官能团转换来实现(Scheme 6)[20]。
取代羧酸经过酰化、氨化、氯代反应后,与取代水合肼反应得到腙胺化合物,进一步氧化环化得到1,2,4-苯并三嗪自由基衍生物。以OBz取代1,2,4-苯并三嗪自由基为例,通过与当量氢氧化钾在甲醇中反应可以实现苯甲酸酯的水解或通过催化加氢得到酚羟基取代产物,与碘庚烷发生取代反应实现羟基的官能团转换。
(3)环扩展
通过扩环反应引入杂原子S、N、O,增加自旋离域程度,能够使1,2,4-苯并三嗪自由基更加稳定,有利于对其结构和性质进行分析,而且会提高在固态的磁交换作用。增环反应可从苯环的C6和C7位置或者C7, C8位置进行。
2012年Koutentis课题组合成了噻唑环作为衍生环的1,2,4-苯并三嗪自由基衍生物。将1,2,4-苯并三嗪自由基用二氧化锰或高锰酸钾直接氧化得苯醌类似物,经过氨化、酰化后与五硫二磷反应成环(Scheme 7)[32]。
2013年,Koutentis课题组报道了咪唑作为拓展环的1,2,4-苯并三嗪自由基衍生物的合成与结构。以苯醌的类似物和酰胺为原料,于甲苯中,N,N-二异丙基乙基胺作为碱,反应即可得到中间体腙胺;将腙胺溶于冰醋酸,回流可得到咪唑环1,2,4-苯并三嗪自由基(Scheme 8)。其中苯醌类似物由二氧化锰或高锰酸钾直接氧化1,2,4-苯并三嗪自由基获得[25,33]。
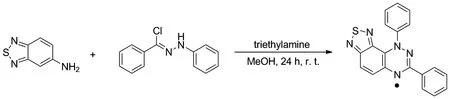
2015年,Yoshioka课题组通过苯胺与酰肼一步反应合成了噻唑重氮环合的1,2,4-苯并三嗪自由基,并从单晶结构中分析出分子间通过S—S键形成π堆积(Scheme 9)[34]。

Scheme 11
Scheme 12
1.4 去氢氧化
2016年,Kaszynński课题组报道了一锅煮合成1,2,4-苯并三嗪自由基的方法;由各类溴代芳烃和正丁基锂或叔丁基锂在低温反应获得芳基锂盐;芳基锂盐和1,2,4-苯并三嗪发生亲核反应后经空气氧化可得目标产物(Scheme 10)。此方法能够将杂环引入到N1的位置[35-37]。
2016年,Kaszynński课题组采用相似的方法合成了平面型1,2,4-苯并三嗪自由基(Scheme 11),使未成对电子离域程度增加,红外光谱向近红外区移动[38]。另外通过自由基环化反应实现了平面型自由基的官能团化,为自组装材料、分子电子器件的应用提供了可能性[39]。
1.5 氮杂Wittig反应
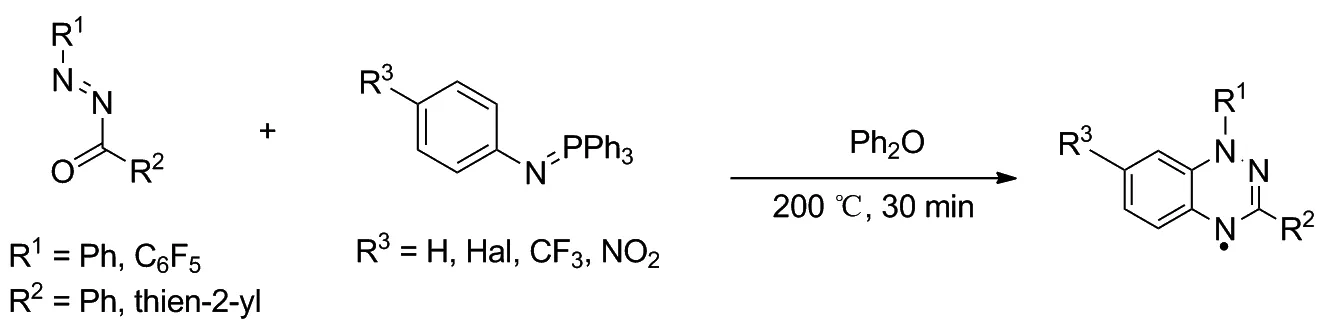
2017年,Koutentis课题组将氮杂磷叶立德和羰基化合物在二苯醚中进行加热合成了1,2,4-苯并三嗪自由基,此方法避免了腙胺等水氧敏感化合物的生成,为合成1,2,4-苯并三嗪自由基提供了便利(Scheme 12)[40]。
2 1,2,4-苯并三嗪自由基的应用
虽然1,2,4-苯并三嗪自由基含有单个电子,但是电子自旋离域程度较大,十分稳定,在各个领域均有应用。
2.1 液晶光电导体
液晶材料在有机发光二极管(OLED)、有机场效应晶体管(OFET)和太阳能电池器件中有广泛的应用。其中盘状液晶分子通常包括刚性的具有平面或近平面的芳香族内核和外面围绕着的6~8条柔性脂肪侧链两个基本组成部分;这样的盘状分子通过苯环之间的π-π键作用形成取向有序的向列相或位置有序的柱状相和层状相,拥有高的有序性和电荷传输速率。1,2,4-苯并三嗪自由基化合物多为平面化合物,且大π离域,当取代基为长链烷烃时,易形成盘状液晶材料。2016年,Jasiński课题组合成了长链取代的自由基分子1,分子间存在较强的自旋耦合,自组装形成柱状相;在液相中呈现反铁磁耦合,晶相中的作用与N1取代基有关(Chart 2);通过测试发现自由基1a和1c光引发载流子迁移速率为1.3×10-3cm2V-1s-1,并展示出不同的磁性,是很好的光导盘状液晶材料的结构单元[41-44]。
2.2 分子电子器件
自由基因为含有单电子可通过电荷转移的方式用作掺杂剂,例如有机自由基分子间作用可以形成自由基阴离子-自由基阳离子对,产生的电荷会在电场中发生离域,形成一种新的自掺杂半导体材料,用于制备有机场效应晶体管,且能够大幅度提高导电性[45]。2015年,Zheng课题组先后合成了双自由基2和3,经测试发现它们在室温具有导电性和磁性,且导电性通过温度控制可实现可逆调节,可用作分子电子器件(Chart 3);这种现象是由于分子自掺杂引起的,并且导电性有了极大的提高。分子自掺杂能有效控制且能极大挺高导电性的特性通过传统的化学掺杂很难实现,为先进光电器件的应用打开了新世界[46-47]。

Chart 3
2.3 光学探测器
近红外光电探测器在光纤通信、无人驾驶生物模式识别技术、光电耦合器等领域有重要应用。2015年,Zheng课题组合成的双自由基化合物3在紫外可见、近红外区域有宽的吸收峰,可用作光学探测器(Chart 3);当其和PCBM([6,6]-苯基C61丁酸甲酯)混合时,在300~1200 nm有较高的灵敏度和探测能力,和其他硅基、镓基有机光学探测器相比更具有优势[46]。
2.4 聚合物合成控制
在高分子化合物的合成过程中,不仅要实现高分子链分子量分布的控制,还要能够控制聚合物的组成和结构;控制自由基聚合的过程能够实现设定分子量和低离散度网状、枝状等聚合物结构的合成。2013年,Krasia-Christoforou等合成了一系列1,2,4-苯并三嗪自由基及其衍生物(4),首次用于稳定自由基调节苯乙烯聚合的过程,使多分散系数为1.05~1.27,并探究不同取代基对平均分子量、转化率的影响,为设计自由基用来控制聚合过程提供新思路(Chart 4)[48]。

Chart 4
2.5 电磁材料
1,2,4-苯并三嗪自由基是构筑高自旋分子体系和磁性材料很好的结构基元[17-18]。近几年,研究人员合成了基于1,2,4-苯并三嗪的高自旋双自由基及三自由基,发现它们在磁性材料中有潜在应用[46,49-52]。电磁材料不仅要求分子具有稳定性,并且要能够形成单层或薄膜用于电子设备中。2016年,Ciccullo课题组合成了自由基5并对其性质进行研究,发现自由基5能够在室温紫外光照射下以薄膜形式稳定存在,并通过EPR、XPS、原子力显微镜测试分析进行了验证;这类自由基化合物在无金属顺磁性薄膜材料中有潜在的应用(Chart 5)[52]。

Chart 5

Chart 6
2.6 传感器
三硝基苯酚是强有机酸,易爆炸、易溶于水,比TNT更危险,对人体健康有极大的影响,阻止三硝基苯酚在环境中的传播至关重要,各种各样的检测传感器已用来对硝基芳香化合物和三硝基苯酚进行检测。2014年,Zheng课题组合成了芘并三嗪自由基6,用于三硝基苯酚的检测;该自由基与三硝基苯酚反应灵敏,溶液颜色由粉色变为绿色,可视化,选择性好,检测限为10-6M(Chart 6)[53]。
虽然1,2,4-苯并三嗪自由基的合成研究取得了一定的进展,但是仍有困难存在,如取代基多位于C3及C7位,取代基种类较少,基于1,2,4-苯并三嗪的多自由基较难合成;另外可用于构筑功能材料的化合物还是少数,实现此分子在电磁材料领域的广泛应用是未来研究的重点,可以从高自旋1,2,4-苯并三嗪自由基的结构、性质等方面考虑,如构建不同骨架结构的多自由基、在分子中引入其他稳定自由基单元、与金属离子配位等。

