严家湖1号氧化塘底泥中氮的形态、分布及影响因素分析*
黎振兴 马 腾,2# 韩佳伟 雷 琨 陈 钰 郑波林
(1.中国地质大学(武汉)环境学院,湖北 武汉 430074; 2.中国地质大学(武汉)生物地质与环境地质国家重点实验室,湖北 武汉 430078)
氧化塘是一种依靠自身生物净化污水的处理技术,其原理是利用水体中的细菌来分解废水中的有机质并形成稳定的无机氮磷化合物和CO2,对有机污染物等有较好的去除效果[1]。然而氧化塘净化作用有限,普遍存在底泥淤积的问题,底泥中含有丰富的氮、磷、钾等养分[2],其主要来源于氧化塘进水中的悬浮物、塘水体中死亡生物体的沉积及天然或人为的外来物等。范晓军等[3]认为底泥由可生物降解和不可生物降解两部分组成,前者可通过厌氧分解过程转化为气体、可溶性有机物及生物残渣,后者只能在塘底不断累积。对积累的氧化塘底泥进行疏浚清淤并堆肥农用是一种有效的处置方式,欧美国家氧化塘底泥农用率在60%以上[4]。然而氧化塘底泥组成复杂,处理难度高,可能变为次生污染源,具有较高风险。
氮是水域生态系统中重要的生源要素之一,氧化塘底泥氮的赋存形态及空间分布对于氮循环过程具有重要意义。底泥中氮的赋存形态较为复杂,而不同赋存形态的氮具有不同的释放能力[5],可转化态氮(TTN)在水动力条件变化或生物扰动等情况下释放参与氮循环。王圣瑞等[6]采用分级连续浸取分离法将TTN分为离子交换态氮(IEF-N)、弱酸提取态氮(WAEF-N)、强碱提取态氮(SAEF-N)和强氧化剂提取态氮(SOEF-N)4种形态。研究氧化塘底泥中氮的赋存形态,判断各形态氮对水环境的潜在影响,将为氧化塘底泥的氮污染内源控制提供新的思路。
严家湖是我国第一批成功建立的氧化塘之一,按照厌氧/兼氧/好氧五塘串联方式运行,具有代表性[7]。该氧化塘运行历史长,处理的废水组成复杂,历史积累的底泥多,且堆放于人工堆积区,是周边环境的潜在污染源。长期以来围绕严家湖开展的研究大都针对多氯联苯、二噁英等有机污染与重金属污染,对氮污染的研究相对匮乏[8-10]。底泥是氧化塘中氮的重要源汇载体,氧化塘停用后氮的外源输入相对减少,底泥内源氮负荷对环境的影响逐渐显现。本研究选取严家湖1号氧化塘作为研究对象,采用分级连续浸取分离法分析氧化塘底泥中氮的形态及分布特征,以期为氧化塘清淤后的治理提供科学依据。
1 材料与方法
1.1 研究区概况
研究区严家湖作为鸭儿湖的子湖,位于武汉市东部,属于长江中下游富营养化浅水型湖泊[11],与五四湖相连。1978—1991年,严家湖被改造为氧化塘用于净化化工企业的工业废水,工业废水中主要污染物有二噁英、多氯联苯和六氯苯等[12]。1991年之后,废水经处理后改道排入长江,氧化塘失去原有的功能而处于闲置状态,周边村民抢占水面养鱼。严家湖氧化塘共有5口,废水首先进入1号塘,经过一段时间氧化后排入2号塘,再依次至5号塘,有害物质残留呈逐级递减趋势。2003年对氧化塘进行了清淤,在1号塘南北两边近 1/5 的地方各筑一道围堰,再将两道堰中间淤积物抽排到两边围堰内,然后在两边围堰的淤积物上覆盖黏土掩埋[13]。由于1号塘污染最为严重且底泥堆积于此,本研究的采样点设置于1号塘,该塘整体面积约0.304 km2,分为人工堆积区和氧化塘沉积区。人工堆积区有清理出的氧化塘底泥堆积并上覆约40 cm黏土,除少量农田外,遍布芦苇丛;氧化塘沉积区为原氧化塘水域,水流方向为西北—东南[14],底泥为氧化塘清淤后持续淤积形成。
1.2 样品采集与处理
本次研究共布设4个采样点(见图1),YJH1位于人工堆积区,其余沿氧化塘水流向布设,每个采样点使用柱状采样器采集3个柱状样品,混合均匀。现场按1 m前每5 cm切分,1 m后每10 cm切分,快速用铝箔包裹避光,装入自封袋密封,放入保温箱4 ℃低温保存,快速运回实验室-18 ℃冷冻保存。沉积物经冷冻干燥,去除大颗粒石块和植物残体,过筛装入自封袋待分析。
1.3 样品分析
pH采用电位法测定,含水率采用烘干称重法测定,总有机碳(TOC)采用元素分析仪(德国elementar)测定,总氮(TN)采用碱性过硫酸钾消解紫外分光光度法测定,TTN的各形态氮采用分级连续浸取分离法测定(见图2),提取液中氨氮采用纳氏试剂分光光度法测定,硝酸盐氮采用紫外分光光度法测定。非可转化态氮(NTN)为TN与TTN的差值。

图1 研究区与采样点分布Fig.1 Study area and distribution of sampling points
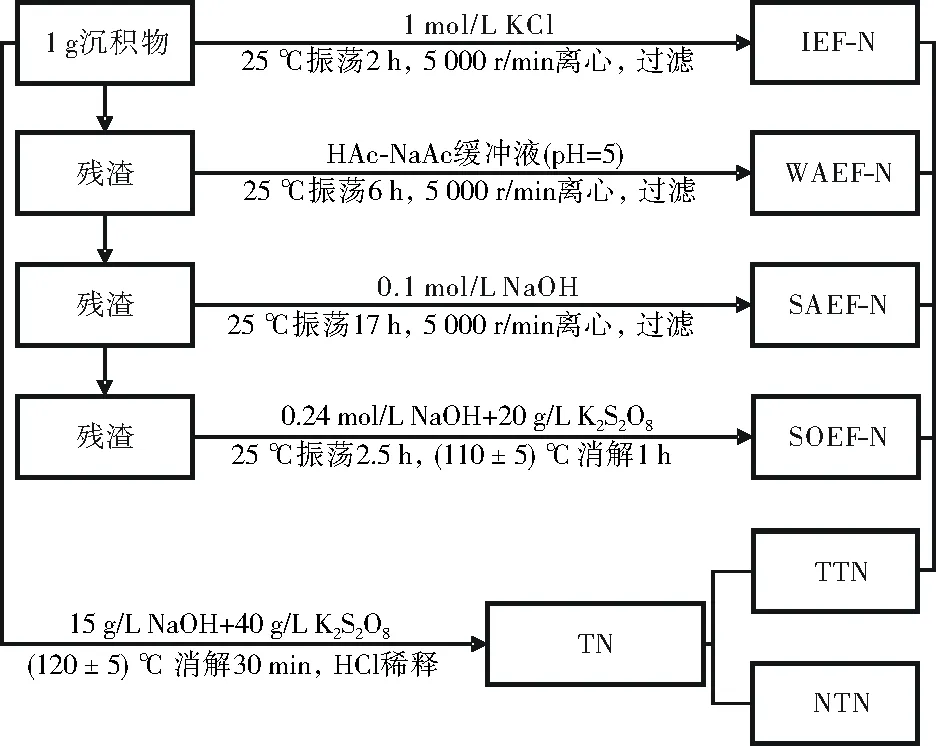
注:若部分样品出现黄褐色,则需要进行消解处理,即取2 mL上清液,加入5 mL H2O2,氧化15 min,加热煮沸至液体几乎完全消失,冷却后用超纯水定容至50 mL。HCl中浓盐酸与超纯水的体积比为1∶9。
2 结果与讨论
2.1 沉积物氮形态的表层分布特征
严家湖1号塘沉积物表层(0~5 cm)TN及TTN分布特征见图3。人工堆积区TN明显高于氧化塘沉积区,原因可能是后者长期淹水导致沉积物TN降低[15]。此外,人工堆积区采样点YJH1位于芦苇丛中,附近分布有农田,有研究表明,植被覆盖能显著提高土壤中TN含量[16],农田中氮肥的施用也造成TN的富集[17-18]。氧化塘沉积区中TN沿水流方向呈现升高的趋势,表明沉积物中的氮会随水流逐步沉积,与任凌霄等[19]研究结果一致,测定氧化塘水样TN为12.80 mg/L,是《地表水环境质量标准》(GB 3095—2012)Ⅴ类标准限值(2.0 mg/L)的6倍以上,污染严重。根据美国环境保护署(EPA)对沉积物TN污染的评价标准(TN小于1 000 mg/kg时为清洁;1 000~2 000 mg/kg时为轻度污染;大于2 000 mg/kg时为重度污染),氧化塘沉积区TN为轻度污染(1 193.20 mg/kg),人工堆积区则达到重度污染(2 245.22 mg/kg),表明清淤后人工堆积区可能成为氧化塘氮污染源头之一。TTN是TN中能参与氮循环的部分,不同赋存形态的氮反映了氮与沉积物的结合强度和转化能力[20]。TTN平均值为641.86 mg/kg,高于鄱阳湖(565 mg/kg)[21],低于洱海(1 808 mg/kg)[22],占TN的44.08%,各形态氮(平均值)占TTN比例的排序为SOEF-N(43.17%)>SAEF-N(25.91%)>WAEF-N(18.35%)>IEF-N(12.57%),其中SOEF-N为优势形态氮。
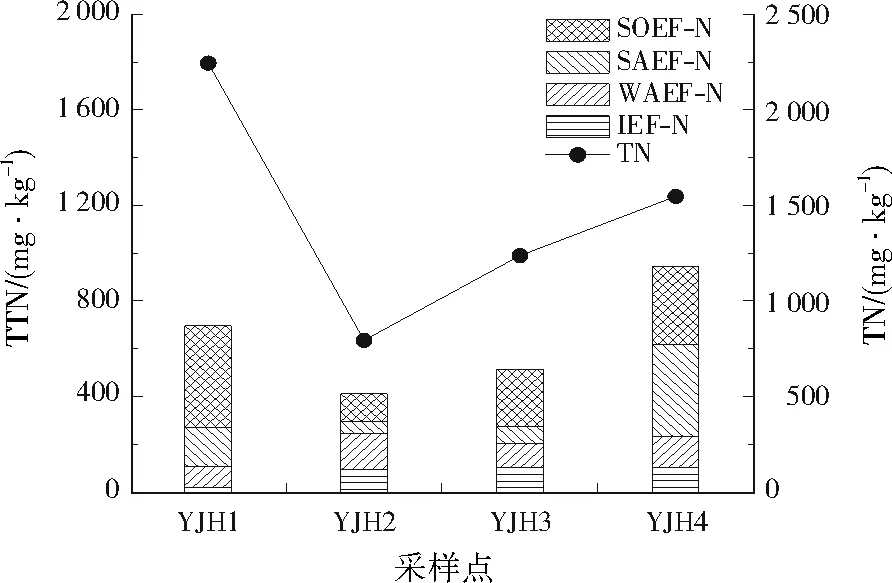
图3 TN、TTN的表层分布特征Fig.3 Surface distribution characteristics of TN and TTN
IEF-N与沉积物的结合能力最弱,容易被释放出来参与氮循环,环境温度、DO、盐度、有机质含量等都会影响其释放[23]453。人工堆积区的IEF-N含量最低,有机质含量也最低,沉积物吸附位点较少使得IEF-N较少被吸附[24],且该处长期受地表径流的冲刷影响,IEF-N不稳定,造成其释放[25]。氧化塘沉积区IEF-N含量沿水流方向小幅度上升,可能与水流流速减缓,对沉积物-水界面扰动减少,有利于其汇集有关[26]。WAEF-N与沉积物的结合能力稍强于IEF-N[27],其产生和分布主要取决于沉积物中碳酸盐含量及有机质矿化作用过程中pH的变化[28]。WAEF-N/TTN沿湖水流向从36.57%下降到13.96%,与沉积物pH逐渐降低相对应,表明碳酸盐含量沿湖水流向呈降低趋势,与文献[28]的研究结果一致。人工堆积区的WAEF-N含量最低,与其pH呈酸性(pH=6.19)密切相关。
SAEF-N的形成和分布主要受沉积物氧化还原环境的影响[29]。有研究表明,还原环境有利于SAEF-N的释放,氧化环境下利于保存[23]454。YJH4处SAEF-N含量最高,主要是由于岸边水浅、易受扰动,DO较高,SAEF-N不易释放。人工堆积区表层沉积物直接与空气接触,因此SAEF-N含量较高。SOEF-N是TTN中最难释放的氮形态[30],其主要来源于生物有关的各个过程,如植物消亡累积和农田有机氮肥施用等[31]3450,因此人工堆积区的SOEF-N含量最高。氧化塘沉积区沿水流方向SOEF-N含量呈递增趋势,与TTN和TN变化一致,进一步验证了氮沿水流方向逐步沉积的规律。
2.2 沉积物氮形态的垂向分布特征
柱状沉积物中氮形态的分布特征在一定程度上反映了不同时期氮的含量变化与其他环境演变相关的信息[31]3450,4个采样点柱状沉积物各形态氮的垂向分布特征见图4。人工堆积区0~40 cm为上覆土,40~140 cm为清淤底泥,140~290 cm为深层沉积物。表层TN含量最高;清淤底泥堆积形成的沉积物TN平均值(1 845.53 mg/kg)高于深层沉积物(1 419.73 mg/kg)和上覆土(1 713.17 mg/kg)。氧化塘沉积区内YJH2沉积物TN含量随深度增加大体呈升高趋势,越接近表层,与上覆水接触越密切,TN释放越多。靠近岸边 YJH4的TN含量随深度增加而总体降低,且氧化塘沉积区沉积物同深度处该点TN含量最高,原因是水流在此处汇集使得氮沉积。
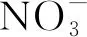

图4 柱状沉积物中TN与TTN的垂向分布Fig.4 Vertical distribution of TN and TTN in columnar sediments

表1 沉积物各形态氮与其理化性质的相关关系1)
SAEF-N可反映沉积环境的氧化还原条件,人工堆积区SAEF-N含量及SAEF-N/TTN总体呈缓慢下降趋势,在较深处偶有波动,这是由于随着沉积物深度增加,其环境越趋于还原环境,造成SAEF-N的释放增强。氧化塘沉积物SAEF-N垂直分布无明显趋势。SOEF-N在各点沉积物柱中总体为优势形态,在TTN中最难释放,在人工堆积区5~140 cm随深度增加大体呈上升趋势,140~290 cm总体呈下降趋势,与沉积柱TOC含量变化大体一致。氧化塘沉积区SOEF-N垂向分布存在差异,YJH2与YJH3呈波动式下降,变化不明显,YJH4则呈明显下降趋势,与TOC变化较为一致,SOEF-N与有机质含量关系密切。
2.3 沉积物理化性质对氮形态影响分析
沉积物中不同形态氮与沉积物的结合方式不同,其迁移扩散特征也存在差异,氮的迁移转化受到多种因素的共同影响[32]。本研究分析了TN与各形态氮之间的相关关系,以及pH、含水率、TOC与各氮形态含量的相关关系。由表1可知,TN与NTN存在极显著相关性,表明TN含量主要受到NTN的控制,而TTN更易于释放到环境中,与TN相关性较低。各形态氮与TTN均显著相关,相关性大小表现为SOEF-N>IEF-N>WAEF-N>SAEF-N,SOEF-N与TN相关性也最强,表明SOEF-N是优势形态,在一定程度上能代表TN和TTN的污染水平。
各采样点沉积柱TOC、pH和含水率随深度的变化见图5。人工堆积区TOC(质量分数)平均值为4.73%,上部TOC与上覆土以及植物腐败分解有关[33],中间部分主要由氧化塘底泥组成,有机质含量较高,深层TOC含量降低。氧化塘沉积区各点TOC整体上均随深度增加而波动下降,由于矿化作用随深度增加而减弱,使得TOC含量相对减少[34]。TOC与TN存在极显著正相关性,表明两者具有相似的来源,有机氮是TN的主要成分,有研究表明沉积物TOC含量对有机氮的分解有直接影响[35-36]。
pH可以影响沉积物的微生物活性、离子交换、吸附等过程[37]。人工堆积区pH随深度增加先升高后保持相对稳定,上覆土呈弱酸性,而氧化塘底泥呈弱碱性。氧化塘沉积区各采样点随深度的增加呈波动下降趋势,与WAEF-N含量的垂直变化较为一致。相关性分析中,pH与IEF-N、WAEF-N存在极显著正相关性,表明沉积物的酸碱性会影响易于释放的氮形态从而影响氮的迁移。
含水率表征沉积物中的孔隙水含量,而孔隙水是固-液界面间物质交换的桥梁和纽带[38]。人工堆积区YJH1中表层含水率在30%左右,0~170 cm随深度增加呈波动上升的趋势,最高达到60%左右,170~300 cm呈降低趋势,降到30%左右。氧化塘沉积区各采样点含水率整体呈随深度的增加而降低的趋势。含水率与大部分形态的氮、TN呈负相关关系,表明氮的迁移转化及沉淀成岩过程与含水率之间存在一定关系。
3 结 论
(1) 严家湖1号氧化塘表层沉积物氮含量差异明显,人工堆积区YJH1点TN含量高于氧化塘沉积区各采样点,且达到重度污染;氧化塘沉积区各点TN为轻度污染,沿水流方向呈递增趋势。氧化塘水体TN含量远高于GB 3095—2012 Ⅴ类标准限值,人工堆积区是可能的污染源头之一。
(2) 柱状沉积物垂向分布特征可以体现环境条件的变化,人工堆积区YJH1点原氧化塘清淤堆积底泥TN平均值(1 845.53 mg/kg)高于上覆土及深层沉积物;受不同环境水文因素影响,不同采样点各氮形态含量变化趋势亦不相同,SOEF-N为绝对优势形态。

图5 沉积物理化性质的垂向变化Fig.5 Vertical variation of major physicochemical properties of sediments
(3) 各区域氮形态含量的变化与沉积物理化性质密切相关,受到各参数的影响程度也不同。TOC与TN、WAEF-N等存在极显著相关性;pH与IEF-N、WAEF-N等存在极显著相关性;含水率与大部分形态氮、TN呈负相关关系。各形态氮与TN、TTN有不同程度的相关性,其中SOEF-N与TTN及TN相关性最强,贡献最大。

