镀铬板表面初始腐蚀机制的研究
李秀军,韦晓,薛彦鹏
(1.宝山钢铁股份有限公司冷轧厂,上海 201900;2.北京科技大学国家材料服役安全科学中心,北京 100083)
作为包装材料,金属包装材料以其密闭性高、质地坚硬、弹性好、阻光性佳、阻气性强等特点,在食品、饮料、气雾罐、化工罐等领域扮演着重要的角色。由于锡资源日趋紧张,在替代镀锡板做包装材料的无锡钢板产品中,镀铬板被认为是最为理想的材料[1]。镀铬板的生产流程较长且复杂,带钢经热轧、冷轧、退火、平整(或二次冷轧)后才镀铬。对于镀铬板来说,其镀层较薄且结构复杂。镀铬板包含了碳钢基板、金属铬层、氧化铬层和油膜4层。由于金属铬层直接沉积到二次冷轧板表面,二次冷轧板表面的物理化学特性(如氧化膜、表面活性、物理形貌等)均影响着金属铬的沉积与长大。另外,镀铬工艺段的电流效率一般为17% ~ 20%,80%左右的电量被消耗在析氢反应上,这导致金属铬段形成的孔隙较多。金属铬层的孔隙可被有序的三维网状结构的三价铬水合氧化铬层封闭,该膜层有很强的憎水性,从而提高了耐蚀性。
用途的特殊性要求镀铬板具有良好的耐蚀性,尤其是用于高温和碱性的饮料罐中时。二次冷轧板表面某些部位可能清洁度不足,使其导电能力受到影响,在电镀时出现漏镀,严重影响镀铬产品的性能,特别是耐腐蚀能力,镀层极易出现点锈缺陷[2]。另外,镀铬板产品从生产到用户使用,往往要经历2 ~ 3个月甚至半年以上的周转运输和存库,且各地的湿度和温度差异较大,拆包后镀铬板表面易存在一定的含水率和结露现象,很容易引起镀铬铁板表面“出汗”,最终导致产品表面产生点锈[3]。
目前国内对镀铬板生产过程中电解液浓度、温度和电流密度的影响[4],镀铬板的表面形貌和缺陷[5],镀铬板的腐蚀行为[3]等已有研究,但对镀铬板初始腐蚀机制的研究较少。基于此,本文通过浸泡模拟实验,利用扫描电子显微镜(SEM)、X射线能量色散谱仪(EDS)和X射线光电子能谱仪(XPS)研究了镀铬板短时间浸泡后的腐蚀形貌和化学成分,揭示了镀铬板的初始腐蚀行为和腐蚀机制,为解决镀铬板微点锈的发生提供依据。
1 实验
1.1 浸泡试验
为了研究镀铬板在不同工况下的初始腐蚀行为,将样品置于不同温度(25 °C和40 °C)的3.5% NaCl溶液中浸泡2、4、8或12 h。
1.2 形貌表征与成分分析
通过德国 Zeiss公司的扫描电子显微镜在不同放大倍数下观察镀铬板浸泡试验后的腐蚀形貌,并利用与扫描电镜相连的X射线能量色散谱仪分析腐蚀后样品表面的元素分布,电镜工作距离10 ~ 15 mm,加速电压20 kV。
1.3 X射线光电子能谱分析
采用英国ThermoFisher Scientific公司的ESCALAB Xi+型X射线光电子能谱仪,单色化Al靶,静电透镜模式,X射线束斑500 μm,分析室真空度优于0.1 Pa,宽扫通过能100 eV,窄扫通过能20 eV,3 kV的Ar离子枪溅射15 s(离子流0.5 μA)。
2 结果与讨论
2.1 镀铬板初始腐蚀表面形貌和成分分析
如图1所示,在低倍镜下可见镀铬板表面存在一些小坑,在高倍镜下可以观察到坑洼位置较粗糙。

图1 腐蚀前镀铬板的SEM照片Figure 1 SEM images of tin-free steel before corrosion
首先将镀铬板样品浸泡于25 °C的3.5% NaCl溶液中不同时间,结果如图2所示。

图2 镀铬板在25 °C的3.5% NaCl溶液中分别浸泡2 h(a, e)、4 h(b, f)、8 h(c, g)和12 h(d, h)后的SEM照片Figure 2 SEM images of tin-free steel after being immersed in 3.5% NaCl solution at 25 °C for 2 h (a, e), 4 h (b, f), 8 h (c, g), and 12 h (d, h), respectively
在较低的放大倍数下很难观察到腐蚀产物,可明显分辨出轧制痕[2];在较高的放大倍数下观察也没看到有宏观的腐蚀产物,但可以观察到一些缺陷部位较粗糙,这与基板的形貌(见图1)存在细微的差别。
从图3和表1可以看出,在浸泡前镀铬板表面较平滑和较粗糙处的元素成分差别不大,可以认为各元素均匀分布。
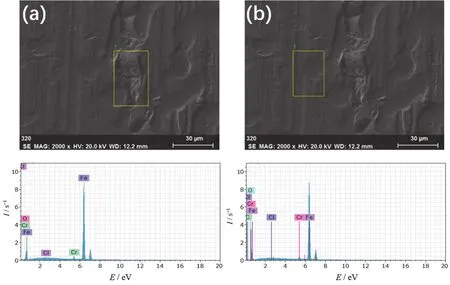
图3 腐蚀前镀铬板不同位置的能谱分析Figure 3 EDS analysis at different positions of tin-free steel before corrosion
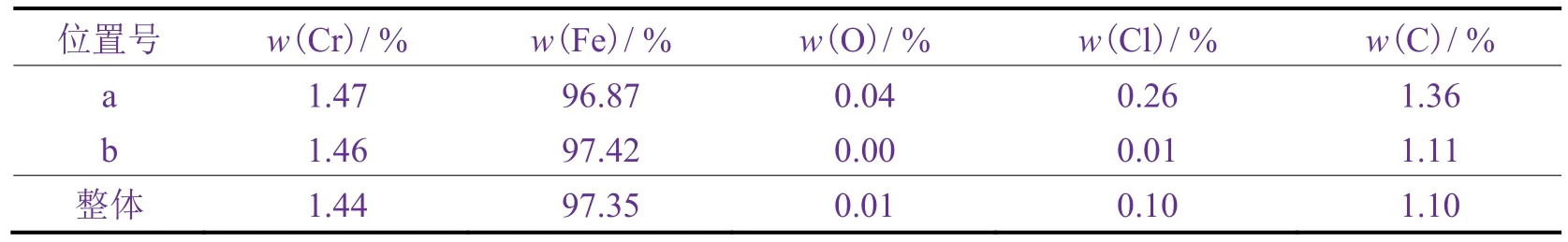
表1 腐蚀前镀铬板表面不同位置的元素组成Table 1 Elemental compositions at different positions of tin-free steel before corrosion
从图4和表2可知,镀铬板在25 °C的3.5% NaCl溶液中浸泡2 h后,在表面粗糙度比较大的位置(图4a和图4c标注的位置)其Cl元素质量分数较高,这说明在相同条件下,水溶液中的Cl−优先吸附在镀铬板表面较粗糙部位,这些部位可能会先发生腐蚀。

图4 镀铬板在25 °C的3.5% NaCl溶液中浸泡2 h后不同位置的能谱分析Figure 4 EDS analysis at different positions of tin-free steel after being immersed in 3.5% NaCl solution at 25 °C for 2 h
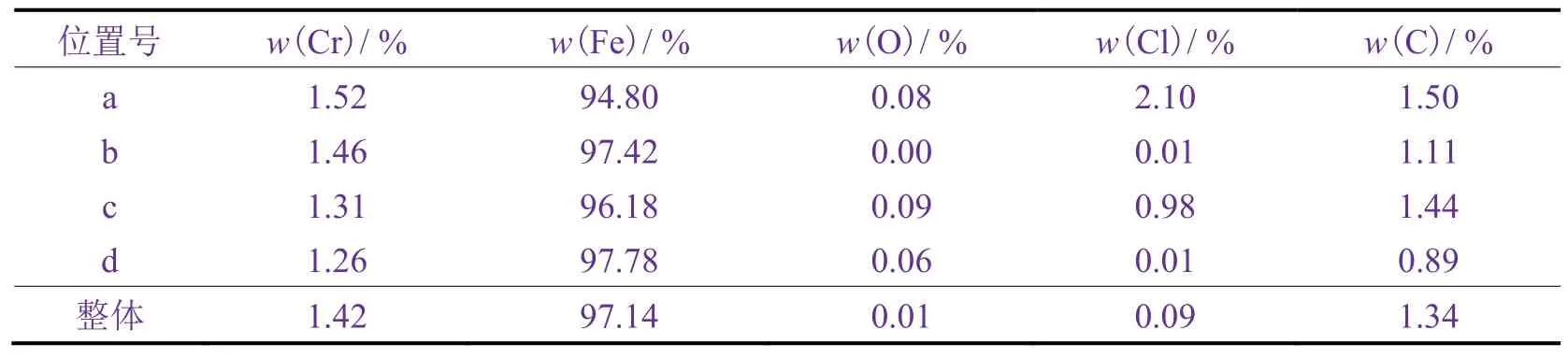
表2 镀铬板在25 °C的3.5% NaCl溶液中浸泡2 h后不同位置的元素组成Table 2 Elemental compositions at different positions of tin-free steel after being immersed in 3.5% NaCl solution at 25 °C for 2 h
镀铬板在25 °C下浸泡4 h后的能谱分析(见图5和表3)说明了同样的问题,即镀铬板表面粗糙度较大部位(见图5c标注的位置)的Cl质量分数比较高。再次说明在相同条件下,水溶液中的Cl−优先吸附在粗糙度比较大的位置,此位置可能先发生腐蚀。

图5 镀铬板在25 °C的3.5% NaCl溶液中浸泡4 h后不同位置的能谱分析Figure 5 EDS analysis at different positions of tin-free steel after being immersed in 3.5% NaCl solution at 25 °C for 4 h
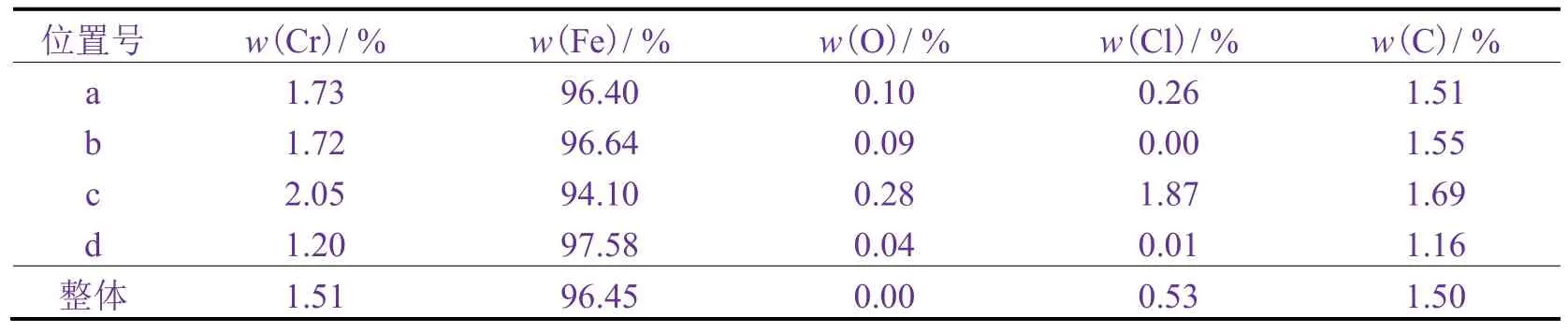
表3 镀铬板在25 °C的3.5% NaCl溶液中浸泡4 h后不同位置的元素组成Table 3 Elemental compositions at different positions of tin-free steel after being immersed in 3.5% NaCl solution at 25 °C for 4 h
图6展示了镀铬板在40 °C的3.5% NaCl溶液中浸泡不同时间后的腐蚀形貌。在较低倍数下可明显分辨出轧制痕;随着浸泡时间的延长,可以观察到样品表面粗糙度变化显著;在较高倍数下也没有出现明显的腐蚀产物,但可以看到样品的一些缺陷部位粗糙度明显较大。尤其是经过较长时间的浸泡后,可以观察到零散分布的白色区域,这与基板的形貌存在明显的差别,可以推断镀铬板腐蚀往往先发生于缺陷处。

图6 镀铬板在40 °C的3.5% NaCl溶液中浸泡2 h(a, e)、4 h(b, f)、8 h(c, g)和12 h(d, h)后的SEM照片Figure 6 SEM images of tin-free steel after being immersed in 3.5% NaCl solution at 40 °C for 2 h (a, e), 4 h (b, f), 8 h (c, g), and 12 h (d, h), respectively
从镀铬板在40 °C的3.5% NaCl溶液中浸泡12 h 的能谱分析(见图7和表4)看,镀铬板表面粗糙度比较大的位置吸附了大量Cl−,将优先发生腐蚀。
2.2 镀铬板初始腐蚀表面的XPS分析

图7 镀铬板在40 °C的3.5% NaCl溶液中浸泡12 h后不同位置的能谱分析Figure 7 EDS analysis at different positions of tin-free steel after being immersed in 3.5% NaCl solution at 40 °C for 12 h

表4 镀铬板在40 °C的3.5% NaCl溶液中浸泡12 h后不同位置的元素组成Table 4 Elemental compositions at different positions of tin-free steel after being immersed in 3.5% NaCl solution at 40 °C for 12 h
为研究镀铬板在初始腐蚀时的表面化学成分,利用XPS检测了浸泡于25 °C和40 °C的3.5% NaCl溶液中不同时间后的镀铬板。对在25 °C的3.5% NaCl溶液中浸泡不同时间的镀铬板进行XPS全谱扫描,结果如图8所示。由于不同试样表面碳含量不同,为统一比较镀铬板表面主要元素的含量,将C峰略去。观察图8,Cr、O、Fe三种元素的特征峰位置均有较强的响应信号,并且峰位置(经C1s吸附峰校正)与相应的标准谱相匹配,确定XPS可检测出此3种元素。

图8 镀铬板在25 °C的3.5% NaCl溶液中浸泡不同时间后的XPS分析Figure 8 XPS spectra for tin-free steel after being immersed in 3.5% NaCl solution at 25 °C for different time
分别对不同浸泡时间下镀铬板表面Cr元素的峰进行XPS窄谱扫描,结果如图9。采用Shirley方法消除背底,通过各峰面积与相应的灵敏度因子计算出Cr元素各价态的质量分数,结果列于表5。可见镀铬板钝化膜主要由Cr2O3、Cr(OH)3和少量金属铬组成。浸泡2 h后的镀铬板表面铬的主要组成为Cr2O3、Cr(OH)3和金属铬,其中金属铬的质量分数最高。随着浸泡时间的延长,金属Cr的质量分数逐渐降低,Cr2O3的质量分数逐渐增大,Cr(OH)3的质量分数变化不大。浸泡12 h后,表面Cr2O3、Cr(OH)3和金属铬的质量分数分别为44.63%、13.17%和42.19%。通过XPS分析可知,镀铬层同时含有Cr(III)的羟桥化合物Cr(OH)3和氧桥化合物Cr2O3,随着浸泡时间的延长,金属Cr含量逐渐降低,氧桥化合物Cr2O3含量逐渐增大,羟桥化合物 Cr(OH)3含量变化不大,这两种化合物均可对腐蚀介质和腐蚀性离子的渗透有着较强的阻挡作用,镀铬板在25 °C的3.5% NaCl溶液中浸泡12 h后依然未发生严重的腐蚀。

图9 镀铬板在25 °C的3.5% NaCl溶液中浸泡不同时间后Cr元素的XPS拟合结果Figure 9 Fitting results from XPS spectra of Cr in tin-free steel after being immersed in 3.5% NaCl solution at 25 °C for different time

表5 镀铬板在25 °C的3.5% NaCl溶液中浸泡不同时间后表面含Cr化合物的含量Table 5 Contents of chromium-containing compounds in tin-free steel after being immersed in 3.5% NaCl solution at 25 °C for different time
对经25 °C的3.5% NaCl溶液浸泡不同时间的样品Fe元素进行窄谱分析,采用XPS peak软件对Fe元素峰进行拟合,结果显示,镀铬板表面氧化膜均主要以FeO、Fe2O3为主(见图10)。通过计算峰面积,求得各种价态的Fe含量,见表6。随着浸泡时间的延长,零价Fe的质量分数逐渐降低,向FeO转化,经过一段时间后可能达到最高值。随着浸泡时间的延长,FeO逐渐向Fe2O3转化,后者的质量分数逐渐提高。浸泡初期腐蚀产物以FeO为主,随着浸泡时间的延长,二价Fe逐渐向三价Fe转化。
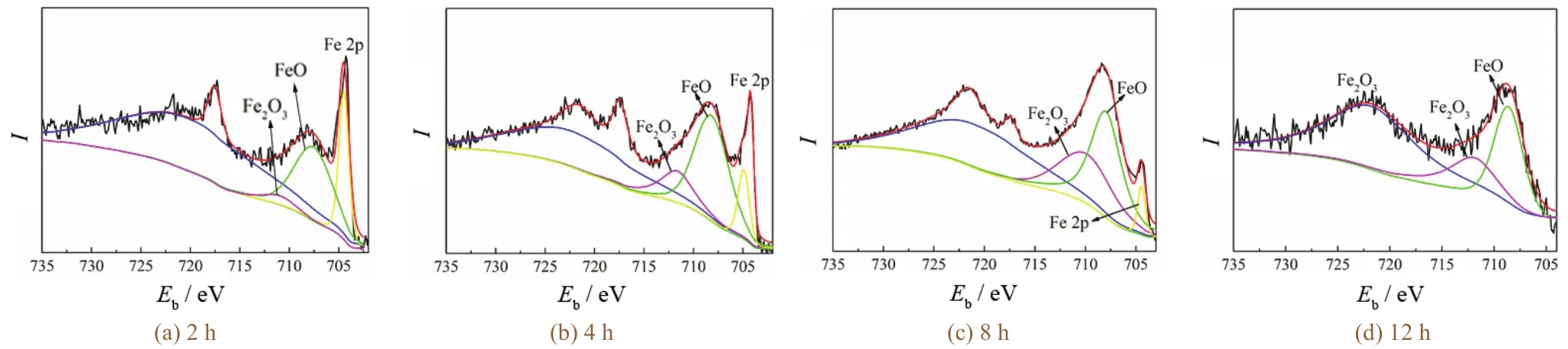
图10 镀铬板在25 °C的3.5% NaCl溶液中浸泡不同时间后Fe元素的XPS拟合结果Figure 10 Fitting results from XPS spectra of Fe in tin-free steel after being immersed in 3.5% NaCl solution at 25 °C for different time
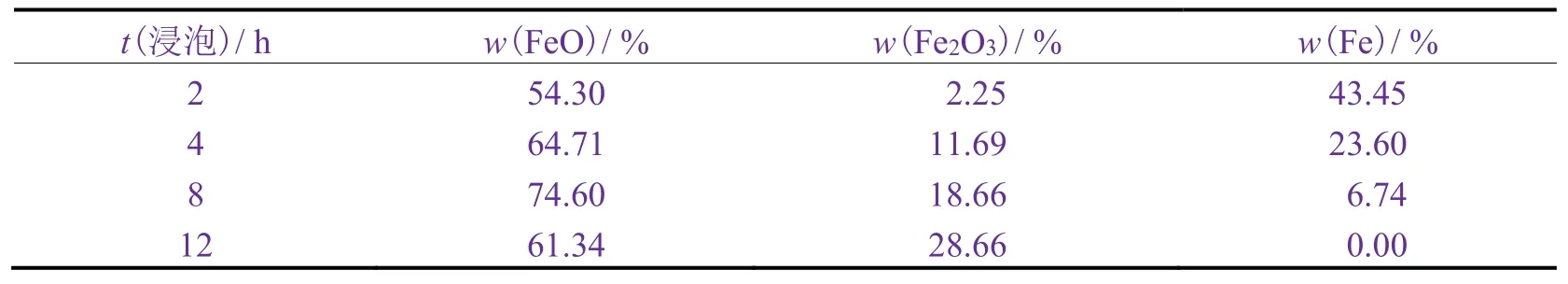
表6 镀铬板在25 °C的3.5% NaCl溶液中浸泡不同时间后表面含Fe化合物的含量Table 6 Contents of iron-containing compounds in tin-free steel after being immersed in 3.5% NaCl solution at 25 °C for different time
对在40 °C的3.5% NaCl溶液中浸泡不同时间的镀铬板进行XPS全谱扫描,结果如图11所示。经过不同浸泡时间后,镀铬板的XPS全谱扫描显示 Cr、O、Fe三种元素的特征峰位置也都有较强的响应信号,并且峰位置与相应的标准谱匹配。

图11 镀铬板在40 °C的3.5% NaCl溶液中浸泡不同时间后的XPS分析Figure 11 XPS spectra for tin-free steel after being immersed in 3.5% NaCl solution at 40 °C for different time
分别对不同浸泡时间下镀铬板表面Cr元素的峰进行XPS窄谱扫描,结果见图12。拟合结果表明,镀铬板钝化膜主要含有Cr2O3、Cr(OH)3和少量金属铬。可以看出:浸泡2 h后的镀铬板表面铬的组成主要为Cr2O3、Cr(OH)3、金属铬,其中Cr2O3和金属铬的质量分数相当,Cr(OH)3的质量分数比较低。随着浸泡时间的延长,Cr的质量分数逐渐降低,Cr2O3的质量分数逐渐增大,Cr(OH)3的质量分数变化不大。经过12 h浸泡,与25 °C下浸泡12 h样品相比,表面金属铬的质量分数降到最低,Cr2O3的质量分数最高,Cr(OH)3的质量分数升高。通过XPS分析可知,随着浸泡时间的延长,金属Cr含量逐渐降低,氧桥化合物Cr2O3含量增大,羟桥化合物Cr(OH)3略有增加,这两种化合物可以较有效地阻挡腐蚀介质和腐蚀性离子的渗透,因此镀铬板在40 °C的3.5% NaCl溶液中浸泡12 h后依然未发生严重的腐蚀。

图12 镀铬板在25 °C的3.5% NaCl溶液中浸泡不同时间后Cr元素的XPS拟合结果Figure 12 Fitting results from XPS spectra of Cr in tin-free steel after being immersed in 3.5% NaCl solution at 40 °C for different time

表7 镀铬板在40 °C的3.5% NaCl溶液中浸泡不同时间后表面含Cr化合物的含量Table 7 Contents of chromium-containing compounds in tin-free steel after being immersed in 3.5% NaCl solution at 40 °C for different time
对经40 °C的3.5% NaCl溶液浸泡的镀铬板进行Fe元素窄谱分析的结果(见图13)显示,镀铬板在40 °C下浸泡不同时间后,表面氧化膜主要以FeO、Fe2O3为主,虽有纯Fe的峰,但其含量很低。采用XPS peak软件对Fe元素峰进行拟合,求得各种价态的Fe含量如表8所示。经2 h浸泡后,FeO的质量分数达到最高,随着浸泡时间的延长,腐蚀产物由FeO逐渐向Fe2O3转化,前者的质量分数逐渐降低,后者的质量分数逐渐提高。

图13 镀铬板在40 °C的3.5% NaCl溶液中浸泡不同时间后Fe元素的XPS拟合结果Figure 13 Fitting results from XPS spectra of Fe in tin-free steel after being immersed in 3.5% NaCl solution at 40 °C for different time
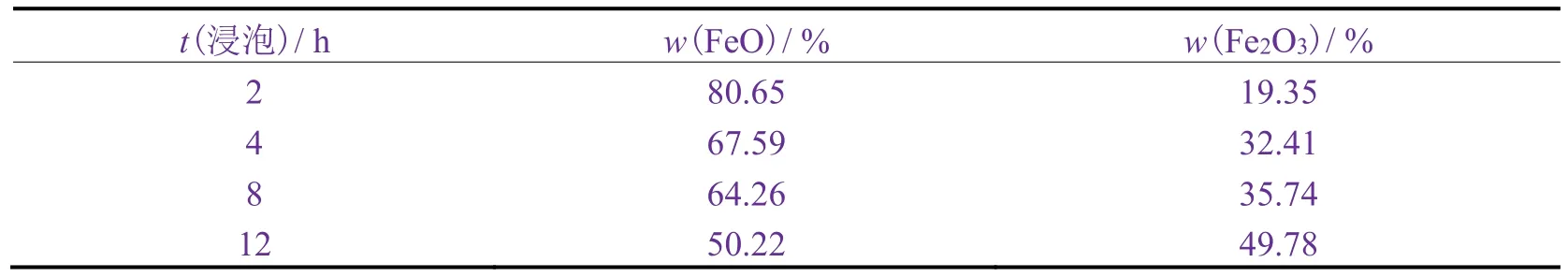
表8 镀铬板在40 °C的3.5% NaCl溶液中浸泡不同时间后表面含Fe化合物的含量Table 8 Contents of iron-containing compounds in tin-free steel after being immersed in 3.5% NaCl solution at 40 °C for different time
3 结论
利用SEM、EDS和XPS研究了镀铬板在3.5% NaCl溶液中的初始腐蚀行为。结果表明:镀铬板缺陷处较粗糙,容易吸附氯离子,从而先发生腐蚀。 XPS分析结果表明,镀铬板表面钝化膜主要由Cr2O3、Cr(OH)3和金属铬组成,随着浸泡时间的延长,表面钝化膜发生细微的变化。经过 3.5% NaCl溶液浸泡后,镀铬板表面腐蚀产物以FeO和Fe2O3为主。 不同浸泡温度下腐蚀产物的含量不同。低温(25 °C)下,随着浸泡时间的延长,零价Fe的含量逐渐降低,向FeO转化,Fe2O3含量逐渐增大;高温(40 °C)下,零价Fe的含量很低,FeO含量较高,随着浸泡时间的延长,FeO也逐渐转化为Fe2O3。

