硼中子俘获治疗人脑胶质瘤的研究进展
马 彭,董啟珊,陈业高,王丽琼
(云南师范大学化学化工学院,云南 昆明 650500)
1 人脑胶质瘤的治疗现状和BNCT的概念
人脑恶性神经胶质瘤是人体颅内常见的肿瘤之一,目前的治疗方式主要有化疗、放疗、手术和基因治疗等,但效果均不理想。特别是,恶性程度较高的多形性型脑胶质瘤(Giloblastoma Mutiforme,GBM),由于其浸润性较高,没有可以凭借肉眼观察到的清晰的边缘,很难通过传统的方法切除治疗,容易复发,中位生存期只有13~17月。因此,从20个世纪50年代开始,BNCT作为一种新的化疗方法开始成为人们探索治疗癌症的新方向。
2020年5月,在经过最新21例BNCT临床试验后,一年无进展生存率为71%,效果很好,副作用较低,日本南东北医院(Southern Tohuku Hospital Group)宣布使用BNCT接收治疗头颈部恶性肿瘤患者进行Ⅱ期临床试验,对治疗的有效性和治疗范围进行深度研究。这一治疗成果使BNCT作为一种新的化疗方式又引起了广泛关注[1]。
BNCT是基于在癌细胞的10B原子核反应,利用裂变中产生的高能线密度α粒子(4He),使之能够摧毁癌细胞的治疗方法。第一步是给病人注射足量的含有10B药物,使有选择性的10B大量进入癌细胞中。当癌细胞摄取了含有10B的药物之后,从外部用能量为0.0253eV的热中子(1n)照射病变部位,在癌细胞内发生裂变反应,产生了11B和α粒子以及锂原子。α粒子具有较高的辐射能量,可以杀死癌细胞,同时由于α粒子射程仅10 μm,小于一个细胞的直径,所以只能杀死癌细胞而不会影响周围健康的细胞。因着这一原理,BNCT成为一种温和高效的化疗方式(图1)。
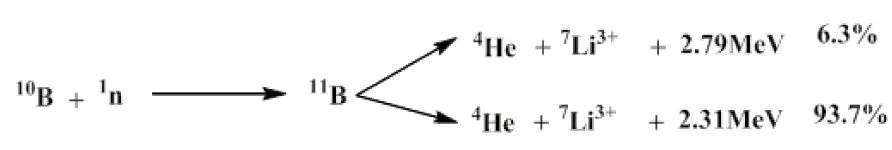
图1 硼中子俘获原理
2 BNCT治疗的人脑恶性胶质瘤病例研究进展
自20世纪50年代,美国就开始了BNCT的临床治疗实验,第一例恶性脑瘤患者用Brookhaven Graphite Research Reactor 进行了治疗,这是最初采用的中子发射器,后续有数名脑瘤患者参与了治疗试验。当时用于治疗的中子源对脑部肿瘤细胞的穿透能力非常弱,而且选用了一些无机硼酸作为注射药物,非靶向硼化合物不仅在肿瘤细胞中聚集,也在正常细胞中聚集[2-3]。治疗后的患者因此产生了强烈的副作用,包括辐射引发的皮肤病、脑水肿、脑梗以及脑细胞坏死等,实验以失败告终。1961年,美国停止了BNCT的临床试验。
在美国开展这项研究的Hiroshi Hatanaka教授在试验失败后回到了日本,并在日本接着开展此项试验。改进后的试验直接用中子对颅内肿瘤细胞进行照射,此次试验让10%的患者能够达到5年生存率[4],10年生存率达到了5.7%。这项研究再次引起了广泛关注[5-6]。
美国布鲁克哈文实验室在1994—1999年间共治疗53例多形性胶质母细胞瘤患者,平均年龄56.5岁,肿瘤大小平均为20.5 cm3,KPS评定为80,总生存期为12.8月。在2005年以后,该实验室陆续收治了46名脑瘤患者,虽然所有的患者在经过BNCT治疗以后都发现肿瘤萎缩变小了,但很多患者最后还是发生了癌细胞转移至未经辐射的部位。治疗效果最好的一个患者预后良好, BNCT治疗之后,每两周用贝伐珠单抗治疗,在84月后发现肿瘤完全消失。贝斯以色列医学中心共收治26例患者,总生存期为11月。
2005年,德国杜伊斯堡-埃森大学[7]试验了26例患者,总生存期为10.4~13.2月。2011年,芬兰赫尔辛基中心医院报导[8]该院共收治复发性脑瘤患者50例,总生存期达到了21.9月。瑞典尼雪平医院试验了31例患者,总生存期最高为17.7月。
在1999年至2007年间,日本筑波大学(Yamamoto, Nakai et al.2009, Kageji, Mizobuchi et al.)、德岛大学和大版医科大学[9]共进行了90例恶性脑胶质肿瘤的临床试验,其中有多形性胶质母细胞瘤(glioblastoma multiforme),渐变性星型细胞瘤(anaplastic astrocytoma), 间变性少突-星形细胞瘤(anaplastic oligoastrocytoma),中位生存期从10.8月到27.1月,两年生存率平均达到了24.1%。
Minoru Suzuki 组[10]用BNCT在2001年到2007年间治疗了62例复发头颈部肿瘤的病例,疗效稳定,一年生存率达到41%。Heikki Joensuu 组在赫尔辛基大学医院对79例之前接受分次放疗又复发的患者进行了治疗,其中38%的患者可以达到两年无进展生存期,总生存率为21%。
在中国,Wang Lingwei 组在台北荣民总医院对17例患者进行了同样的治疗后发现一年生存率达到56%,两年局部控制率为28%,两年生存率为47%[11]。
Iara S.Santa Cruz用RA-6作为中子源对5只患头颈部肿瘤的宠物狗进行治疗,生存寿命延长了8.5月至13.5月,超出了预计的生存时间,取得较好的效果。治疗后的结果显示,所有的病例都有明显的部分缓解,其中1例肿瘤减小50%。这一结果对人头颈部肿瘤的治疗有重要的借鉴意义。当然,值得注意的是,中子进入脑部的深度只达到了1 cm左右,这是一个让治疗不能充分进行的关键因素,其中两例发现了癌细胞转移至肺[12]。
日本南东北医院的近期试验结果(2019年公布)显示,全部21例患者中,完全缓解(CR)为5例(23.8%),部分缓解(PR)为10例(47.8%),稳定未发展(SD)5例(23.8%),出现新病灶的为0例,有1例(4.8%)无法评估[13]。
从这些治疗的结果来看,日本在头颈部肿瘤的治疗方面取得了重要的进展,而头颈部肿瘤用BNCT治疗的效果总体比脑胶质瘤好。目前脑胶质瘤的临床Ⅰ、Ⅱ期试验仍然困难重重,主要的原因还是与药物无法有效聚集在脑肿瘤细胞和中子未能够精准到达肿瘤位置有关系。
3 BNCT诱发肿瘤细胞凋亡机理
肿瘤细胞凋亡的机理对于肿瘤治疗有着非常重要的意义,对肿瘤细胞的抗凋亡蛋白研究能够很好地诠释肿瘤细胞的耐药性和肿瘤复发。然而,也有观点认为,没有证据表明抗肿瘤治疗与肿瘤细胞凋亡之间有必然联系。目前,细胞凋亡机理仍然是研究者关注的热点之一。本文综述了部分关于BNCT治疗中肿瘤细胞凋亡的研究观点。
大部分射线进入生物体内都有化学辐射反应,中子也不例外,直接的离子射线靶点是DNA。除此以外,研究表明在照射中产生的自由基和离子碎片可以破坏一些生物大分子如核酸、蛋白质、脂类和多糖等[14]。这些大分子的改变对于BNCT作用于肿瘤细胞的机理也产生了不同的影响。在治疗过程中发现,肿瘤细胞中的染色体异常比传统的化疗方式更多,致死率更高。同时发现BNCT能通过Bcl-2/Bax途径和线粒体调控细胞色素C的释放和Caspase-9的激活来加速脑肿瘤细胞凋亡[15]。超热中子能够让50%的DNA发生链断裂,同时随着10B在细胞内浓度的增加,DNA单链或者双链断裂的倾向更大。后续研究发现,在BNCT的治疗中,自噬内吞作用是由变异基因Beclin1,PARK2和PINK1引发的[16]。从目前的研究来看,用BNCT治疗以后的细胞凋亡机理仍然处于探索阶段。
4 硼中子俘获治疗的药物研究进展
在开展BNCT 的研究过程中,含硼药物的选择非常重要,基于半个世纪的研究结果与数据,很多的含硼药物被研究者合成出来。从治疗的过程来看,BNCT对含硼药物需要达到一下基本要求:
1)含硼药物一般通过滴注的方式进入患者体内,要求10B在肿瘤上的聚集达到10~30 μg/g,并且有一定的停留时间,能够使中子充分到达肿瘤内部发挥作用。
2)含硼药物必须对肿瘤细胞有较高的选择性,也就是10B在肿瘤细胞和正常组织、血液中的分配比例(T/N值,T/B值)至少要达到3以上。
3)高水溶性和低毒性。
从1990年开始,用于临床试验的有效的含硼药物主要是BSH(polyhedral boron anion, sodium mercaptoundecahydro-closododecaborate,Na2B12H11SH)和BPA((l)-4-dihydroxyborylphenylalanine)两种(图2)。BSH不能透过血脑屏障,当血脑屏障被破坏的时候,BSH可以进入并有效地聚集在脑肿瘤部位。而BPA则可以顺利通过血脑屏障进入颅内,但是有小部分BPA停留在正常细胞中,多余的BPA在患者尿液中代谢出来并结晶引起发烧,后来用增加给水的方式来预防[17]。虽然后续有很多含硼药物被设计合成出来,然而现在进入临床试验的还是这两种较早开发的药物。
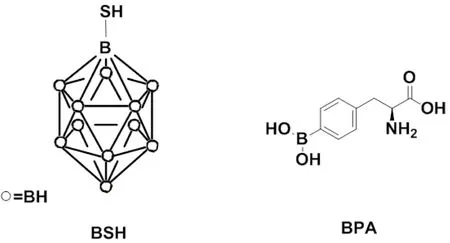
图2 BSH 与 BPA 的化学结构式
日本南东北医院使用的含硼试剂为Steboronine(9 000 mg/300 mL静脉注射),分子结构为(S)-2-amino-3-[4-(10B)dihydroxyboranyl phenyl]propanoic acid(S-BPA)。主要的副作用为脱发症90.5%(19/21例)、淀粉酶增加85.7%(18/21例)、恶心81.0%(17/21例)、味觉异常71.4%(15/21例)、腮腺炎以及食欲减退66.7%(14/21例)、口腔炎61.9%(13/21例)。
现在有很多研究者都致力于开发新型的含硼试剂,并将其应用于BNCT中。如硼代卟啉[18-20],H2OCP对人喉癌HEp2细胞不敏感,但是能够聚集在人脑胶质瘤细胞T98G中,在3 h内细胞摄取率达到了0.03 μmol/1 000细胞[19](图3,H2OCP,Octa-anionic 5,10,15,20-tetra[3,5-(nidocarboranylmethyl) phenyl]porphyrin)。铵盐基团的引入是化合物能够进入细胞内并快速聚集的关键(图3,卟啉铵盐),后续研究发现卟啉主要通过内吞作用集中在溶酶体中。
很多新的硼代葡萄糖[21],硼代多糖[22],硼代核酸[23],硼代抗体[24],硼代磷脂和硼代氨基酸[25]等都被合成并探索了它们的药物活性(图3)。
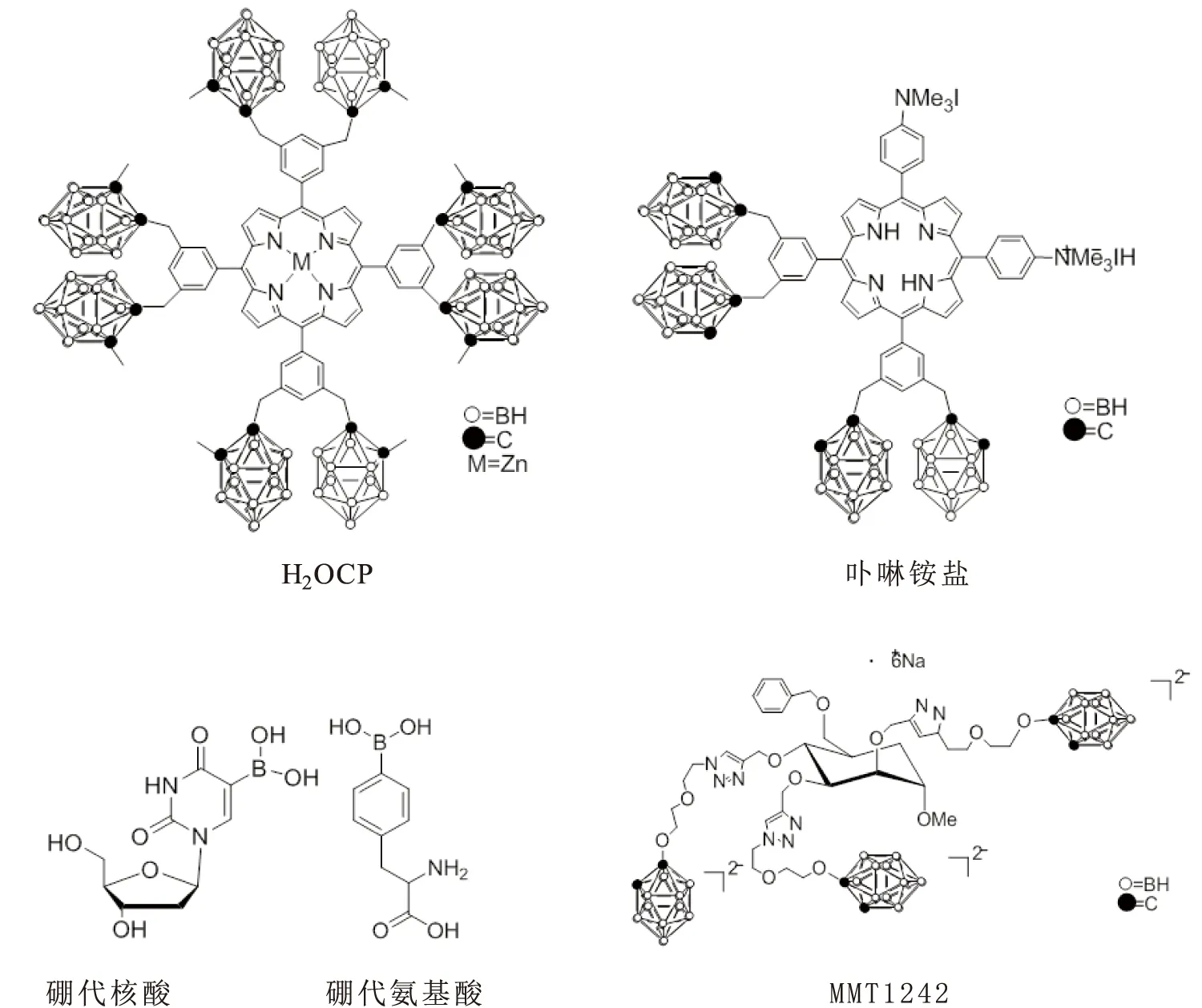
图3 BNCT含硼化合物
如以表皮生长因子(EGFR)介导的单克隆抗体(mAbs),cetuximab(IMC-C225),和EGFRvIII的L8A4抗体,实际操作中使用PAMAM聚酰胺胺型树枝状高分子聚合物作为载体,将网状硼烷Na(CH3)3NB10H8NCO和单抗偶联在一起,能够通过识别肿瘤细胞中过度表达的EGFR或者变异的EGFRvIII蛋白来达到输送硼试剂的目的,检测发现T/N比例为9.9,硼的聚集浓度达到了24.4μg /g(药物/肿瘤),达到含硼试剂的基本要求[26]。
2020年Takao Tsurubuchi组上报导了一个新的BNCT候选药物,结构如图3中的MMT1242。该化合物在CT26小鼠结肠癌细胞、B6-F10小鼠皮肤黑色素瘤和C6大鼠胶质瘤细胞中都有较高的摄取率,是BPA的两倍以上。同时,小鼠试验显示,此药物在肿瘤上的停留时间在60 min以上,具备了BNCT治疗的理想条件。同时发现,在化合物进入肿瘤细胞24 h之后,此化合物已经表现出中等抗癌活性,对BNCT的治疗更添助力[27]。
5 目前治疗中存在的问题
1)从使用量来看,一次治疗的剂量为静脉注射 9 000 mg,这是一个很大的量,因此引发的副作用也不可小觑。从日本南东北医院的治疗方案来看,21例患者全部都有不同类型,不同程度的副作用出现。因此改进含硼药物的结构,提高治疗效率,减少治疗用量,减少副作用仍然是一个具有挑战性的课题。
2)虽然基于不同靶点和机理的含硼化合物都被设计出来,但是在初期生物活性试验或后期的动物试验中的结果都不理想,因此,这些药物前体结构都有待进一步改进和提高。
3)含硼化合物进入脑肿瘤之前必须通过血脑屏障(BBB),而BBB的存在使很多药物的进入都非常困难。虽然,有研究者发现甘露醇[28]和Cereport[29]可以破环血脑屏障,协助药物进入肿瘤细胞。然而,甘露醇的操作有一定的副作用,而Cereport虽然增加了BBB的渗透性,却没能提高BPA在肿瘤细胞上的聚集率。后续没有看到此类报告,因此,提高含硼化合物的血脑屏障渗透性仍然是一个重要的研究方向。
6 总结与展望
作为一个新的化疗体系,每一个环节都决定着最后的疗效以及患者预后状态。因此,除了前面提到的有效含硼药物的研究开发问题,建立BNCT需要的条件设备如中子产生装置和治疗中硼浓度的检测等问题都是需要设计考虑的。
在BNCT的治疗过程中,国际原子能机构对中子源有较高的要求。在1 h内,超热(0.5 eV~10 keV)中子流必须以大于1×109n/cm2/s的量进入肿瘤细胞内,才能达到有效治疗的目的。最初在布鲁克哈文实验室使用的铀反应堆是中子源的提供装置,我国于 2009 年末建成了世界首座专为 BNCT 应用且可 建在医院内,由医疗人员自行操控的微型核反应堆中子源 ——医院中子照射器(IHNI)。目前,中子发生器已经从铀反应堆发展成为利用质子加速器射出质子与其他原子产生中子的加速器(accelerator-based neutron sources,ABNS),目前日本南东北医院的中子产生装置是由京都大学和住有重工联合研发的装置,而这个装置在提高BNCT的治疗方面起着至关重要的作用。这个装置主要是为了适应临床诊断和治疗的需要,达到了安全、紧凑、稳定和经济的要求。
除了开发高效的含硼药物和中子加速器之外,一个很紧迫的临床治疗需求就是含硼药物进入人体后的实时检测方法。含硼药物进入人体后到达肿瘤组织的时间、浓度和T/N比例等因素在临床治疗中非常重要。从1980年以来,人们一直用BPA-F(18F boronophenylalnine)标记药物并联合PET(Postiron Emission Tomography,正电子发射计算机断层显像)仪器使治疗过程中人体内硼浓度得以监测。但是这个过程需要一定时间才能完成,无法及时准确地指导对肿瘤部位进行照射。因此,实时检测方法也是亟待解决地问题之一。
在这些化合物的开发研究中,大部分研究者把DNA作为目标靶点来进行设计。本课题组在研究中发现,线粒体作为人体的能量中心,它的作用并不只是产生ATP作为能量,它是生命活动控制中心,不仅是是细胞呼吸链和氧化磷酸化的中心,而且在诱发细胞凋亡的信号转导中有至关重要的中枢调控作用。当凋亡信号被发出时,线粒体外膜通透性增强,一些凋亡因子如细胞色素等由线粒体膜间隙释放到胞浆中,启动凋亡进程,死亡受体途径一旦被打通,这个进程是不可逆转的。当研究的焦点是把一些代谢产物作为药物靶点时,线粒体的真正功能也被忽视了。实际上随着线粒体机制的研究深入发现,几乎所有导致细胞凋亡的因素都使线粒体结构被破坏,发生功能障碍。究竟是哪个过程发生在前面,还是同步进行,现在的研究还未能给出答案。因此我们致力于开发以线粒体为靶点的BNCT药物开发研究。目前已经发现并合成了几类能够进入线粒体并产生抗癌效应的小分子硼代化合物,为研究BNCT的先导化合物开辟一个新的方向。后续研究正在进行中。

