ZSM-5 分子筛协同脱硫脱硝脱汞的分子模拟
刘红芳,周瑞生,姚贵佳,李奇超
(江西华赣瑞林稀贵金属科技有限公司,江西宜春 331100)
目前联合脱除烟气中SO2、NO、Hg 污染物是国内外研究的热点。其主要的方法有吸附法、 电子束法、低温等离子体放电、光催化氧化、烟气循环流化床和微波辐射脱除法等[1]。例如,袁媛等[2]采用TiO2-硅酸铝纤维纳米复合材料通过光催化作用进行脱硫脱硝脱汞实验。结果表明,纳米复合材料的脱硫脱硝脱汞效率均随着反应温度的升高而降低。李兰廷等[3]探索了活性焦脱硫脱硝脱汞一体化技术的可行性。刘松涛等[4]通过实验研究了富氧型高活性吸收剂脱硫脱硝脱汞性能。
由于分子筛具有良好的吸附性能,关于分子筛吸附的研究不断涌现,且主要以分子模拟的方法为主。分子模拟的方法可以直接分析界面的分子模型,获得通过实验难以得到的信息[5]。目前,已有一些关于分子筛吸附的分子模拟研究,如曾晓放等[7]研究了NaY 分子筛模拟吸附油中噻吩;刘艳杰等[8]采用分子模拟的方法研究了H-STI 分子筛对氨分子的吸附;黄孟凯[7]探索了稠环芳烃在Y 分子筛中吸附规律等,但分子筛在脱硫脱硝脱汞方面的分子模拟却很少。ZSM-5 是一种沸石分子筛,微孔孔径在0.5~0.6 nm,热稳定性好,能够实现循环使用。其主要结构式由8 个五元环组成的结构单元构成,具有两种相互交叉的孔道体系[9-10]。由纯SiO2合成的ZSM-5分子筛价格低廉,在环保领域应用十分广泛。本文采用分子模拟方法从微观角度探讨ZSM-5 分子筛脱除烟气中SO2、NO、Hg 污染物的机制。
1 ZSM-5 吸附情况的分子模拟
1.1 ZSM-5 分子筛模型构建
本文在Materials Studio(以下简称“MS”)软件包中构建ZSM-5 分子筛模型。晶胞参数a=2.007 nm,b=1.992 nm,c=1.342 nm,α=β=γ=90°。选取 8 个(2×2×2)晶胞作为基本计算单元,由 96 个 SiO2分子组成,密度为 1.782 45 g/cm3。应用 MS 中的 Forcite 模块对新的ZSM-5 分子筛进行几何结构优化,Forcite模块条件设置如下:1)计算任务为几何优化(Geom etry Opti-mization);2)精度控制为精确(Fine);3)力场为Universal;4) 加和方法中的静电相互作用选择原子截断(Atom based)。优化后的 ZSM-5 分子筛骨架结构如图1 所示。

图1 ZSM-5 分子筛骨架结构
对优化后的 ZSM-5 分子筛模型用 MS 中的Reflex 模块 Powder Diffraction 做 XRD 衍射,得到构建的ZSM-5 型分子筛模型的XRD 谱,如图2 所示。将该XRD 谱与国际沸石协会结构委员会数据库中的标准XRD 谱进行对比,发现两个图谱的XRD 峰位置一致。由此说明,所构建的分子筛模型可以正确表征实际分子筛结构。

图2 ZSM-5 分子筛模型的XRD 谱
1.2 吸附模块的参数设置
采用MS 软件包中的Sorption 模块来模拟SO2、NO、Hg 在ZSM-5 分子筛上的吸附情况。模拟过程中,使用的是蒙特卡洛法(GCMC),采用属于分子力学范畴的巨正则系综进行诠释。预测SO2、NO、Hg 的吸附等温线,定量分析温度及压强对体系的影响,研究纯组分或混合组分体系在分子筛中的性质,从原子级别来理解吸附机制,通过图形表示法分析、解释模拟结果。Sorption 模块的模拟条件设置如下:计算方法为 Metropolis,计算精度为精确(Fine),吸附质选择需要模拟吸附质后缀为.xsd 的文件,性质勾选能量分布(Energy distribution)、态密度场(Density field)、能量场(Energy field)。平衡步数设为 104,生产步数设为105,温度根据需要来设置。吸附分子的运动中各分配系数采用默认设置。静电势能和van de Waals 势能设为 Ewald & Group 和 Atom based,吸附反应的压强设置在0.01~101 kPa。
2 结果与讨论
2.1 吸附等温线
2.1.1 纯组分吸附等温线
温度对吸附性能产生重要的影响,且不同物质对温度的敏感性不同。为研究不同温度对ZSM-5 分子筛吸附 SO2、NO 和 Hg 的影响,本文选取了 298 K、373 K、473 K、573 K 和 673 K 分别进行模拟,得到等温吸附曲线如图3~图5。

图3 ZSM-5吸附SO2 等温线
从图3 可以看出,常温下ZSM-5 分子筛吸附SO2的能力较强。在 373 K 范围内,SO2的吸附量受温度的影响较小。随着压强的增大,吸附量先呈现快速增加;当压强超过10 kPa 后,吸附量几乎趋于平衡。当温度高于 373 K 后,ZSM-5 分子筛对 SO2的吸附量急剧下降,在温度趋近673 K 时,吸附量几乎为0。在温度低于473 K 时,符合BDDT 分类中的第Ⅰ型等温线特点,能用Langmuir 吸附模型来描述,即吸附量在较低相对压力时迅速增加,达到一定的吸附量后,趋于吸附平衡,达到极限吸附。由于ZSM-5 分子筛的孔径在0.5~0.6 nm 左右,属于微孔,达到极限吸附时,吸附质填满了微孔。当温度高于573 K时,吸附量与压力成正比,吸附等温线为通过原点的直线,吸附等温线属于第Ⅱ型,且温度越高,曲线越缓,吸附量越低,这便于其在ZSM-5 分子筛的脱附。在298 K 时的吸附量的模拟结果与文献[11]的实验结果相吻合。

图4 ZSM-5 吸附 NO 等温线
从图4 可以看出,NO 在ZSM-5 分子筛上的吸附量随着温度的升高而急剧下降。在473 K 时,平衡吸附量趋向于0。NO 总吸附量不大,符合第Ⅱ型吸附等温线。

图5 ZSM-5 吸附Hg 的吸附等温线
从图5 可以看出,ZSM-5 分子筛对Hg 的吸附量并不大,符合第Ⅱ型吸附等温线,与NO 的吸附情况类似。吸附量随着温度的升高而降低,随着压力的增大而增大。当温度达到673 K 时,吸附量接近于0,这有利于ZSM-5 分子筛脱附。
对比 SO2、NO 和 Hg 在 ZSM-5 分子筛上的吸附现象,SO2的吸附量较大可能与ZSM-5 分子筛的酸性位点有关,SO2呈现酸性,能较稳定地吸附在酸性位点上,而NO 和Hg 都近乎呈中性,只存在普通的微孔吸附。
2.1.2 混合组分吸附等温线
为探索ZSM-5 分子筛同时吸附混合物的相互影响,模拟了Hg、SO2和NO 两两混合或三者同时存在相互之间的影响。模拟温度均298 K,模拟结果如图6 所示。

图6 Hg、SO2 和NO 两两混合或三者同时存在的影响模拟等温线对比(298 K)
从图6(a)看出,Hg 与 SO2联合脱除,ZSM-5 分子筛对SO2吸附量几乎无影响,吸附量和吸附模型均未改变;而对Hg 的吸附影响显著。此时,Hg 的吸附量几乎为0,说明SO2的存在抑制了Hg 的吸附。图6(b)显示出Hg、NO 联合脱除具有较好的效果,两者吸附量有微小程度地降低,但总吸附量还是有所增加。这可能是由于Hg 和NO 在ZSM-5 分子筛中竞争吸附力相近。图6(c)是SO2和 NO 联合脱除的吸附等温线,从中看出,SO2的吸附量依然没有受到影响,而NO 的吸附量近乎为0,说明SO2抑制了NO在 ZSM-5 分子筛上的吸附。图4(d)是 298 K 温度下,ZSM-5 分子筛联合脱除 SO2、NO 和 Hg 的吸附等温线。从中看出,SO2的吸附量没有改变,而Hg 的吸附量较Hg 与SO2共存时的吸附量略有增加。
综合分析以上联合脱除模拟结果,由于SO2、NO和Hg 在ZSM-5 分子筛中要相互竞争吸附位或者相互发生反应,因此SO2、NO 和Hg 的多组分吸附将与纯组分吸附不同:1)当 Hg 与 SO2共存时,ZSM-5 分子筛的酸性是催化反应的活性中心,对反应效果起着关键性影响,能使ZSM-5 优先吸附SO2[12]。2)当Hg和NO 共存时,NO 几乎呈现中性,对酸性位的争夺很弱,几乎能与汞同等概率地吸附于ZSM-5 分子筛孔道中。3)当 SO2、NO 共存时,SO2和 NO 相互竞争吸附位,由于SO2的分子极性强于NO,且分子直径、临界体积分子偶极矩均比NO 的大,导致SO2优先吸附[13]。4)当 SO2、NO 和 Hg 同时存在于混合气中时,分子筛优先吸附SO2的同时,吸附的NO 被氧化成NO2;NO2将带着电子转移到吸附态的SO2上,使得SO2的吸附更容易。当 NO2存在时,少量的 NO2与Hg发生氧化还原反应,汞以氧化态形式吸附在ZSM-5 分子筛上,于是出现了当SO2、NO 和 Hg 同时存在于混合气中时比仅Hg 与SO2共同存在时汞的脱除效率更高的现象。
2.2 能量分布图
其他设置与吸附等温线的设置一样,温度设置为 298 K,模拟得到SO2、NO、Hg 的吸附能量分布,见图7。

图7 SO2、NO、Hg 的吸附能量分布(298 K)
从图7 中看出,SO2吸附能量分布在较低区间,NO 和 Hg 则分布在能量相对较高的区间,SO2与Hg、NO 吸附能量分布区间不存在重叠,而Hg 与NO的吸附能量分布区间却存在重叠。NO 存在1 个很强的吸附峰,SO2与Hg 各自存在多个吸附峰,且能量分布区间较宽。结合SO2、NO、Hg 联合脱除的等温吸附曲线,推测三者联合脱除时,NO 先吸附在ZSM-5分子筛上而被氧化为NO2; 由于NO2具有强氧化性,NO2被还原成 NO,NO 则从 ZSM-5 分子筛脱附,而 Hg则以氧化态的形式吸附在ZSM-5 分子筛上。于是,出现了NO 存在强吸附峰,结果吸附量却很小的现象。
2.3 密度场分布规律
其他设置与吸附等温线的设置一样,只改变Sorption Calculation 中 Task/Adsorption isotherm 为Task/Fixed pressure。温度设置为298 K,压强设置为101 kPa 时,每50 步记录1 次相关分子质量中心的位置,并在该位置记为1 个点,模拟得到吸附SO2、NO、Hg 的密度场分布规律,如图8 所示。

图8 吸附空间概率密度场
图8 中3 种物质均有出现,但SO2分布的空间最广,Hg 次之,NO 出现的概率最低。
2.4 吸附热
吸附热的大小可以衡量吸附能力强弱,吸附热越大,吸附能力越强。为研究不同温度对SO2、NO 和Hg 在ZSM-5 分子筛中的吸附热的影响,本文选取了 298 K、373 K、473 K、573 K 和673 K 分别进行模拟,得到吸附热曲线如图9~图11。
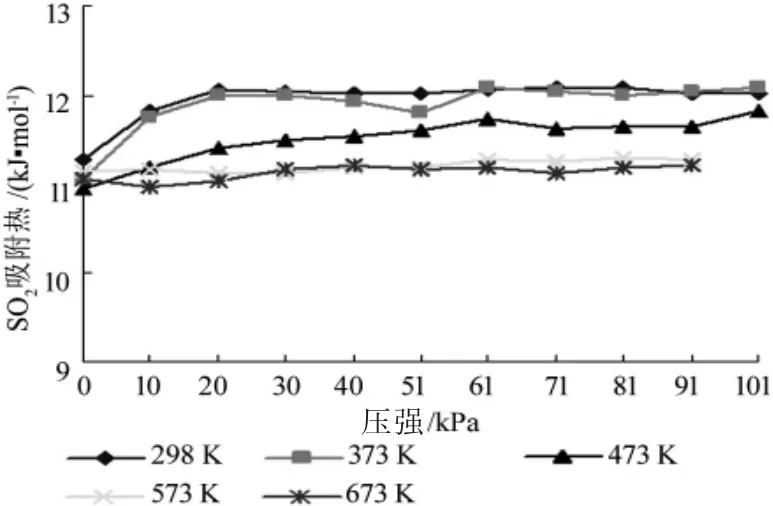
图9 SO2吸附热曲线

图10 NO 吸附热曲线

图11 Hg 吸附热曲线
一般来讲,一种物质在另一种物质中的吸附热,受反应条件影响而产生的吸附热变化值并不大。但从图9~图11 可以看出,SO2在 ZSM-5 分子筛中吸附热随反应温度升高而减小,NO、Hg 在ZSM-5 分子筛中的吸附热均随着反应温度的升高而增大。
图12 是在温度为 298 K 时,SO2、NO、Hg 三者混合组分的吸附热曲线。

图12 SO2、NO、Hg 吸附热曲线(298 K)
从图8 得知,SO2在 ZSM-5 分子筛中的平均吸附热最大,为 12 kJ/mol 左右,与文献[11]的实验值12.5 kJ/mol 接近。NO 的吸附热近似为 5.4 kJ/mol,Hg的吸附热近似为4.4 kJ/mol。
3 结 论
1)从吸附等温线得出,混合组分吸附,SO2吸附量受其他组分的影响很小,NO 促进了Hg 的吸附。2)能量分布图看出,处于低能量分布区的SO2更容易被吸附,Hg 与NO 的能量分布图存在重叠区。3)3种气体在ZSM-5 分子筛中出现多个吸附位点,且能量分布区间越宽,越容易被吸附;SO2概率密度分布空间最广,Hg 次 之 ,NO 出现 的 概 率 最 低 ;SO2在ZSM-5 分子筛中的平均吸附热最大,约为12 kJ/mol,NO 近 似 为 5.4 kJ/mol,Hg 在 4.4 kJ/mol 附 近 。4)ZSM-5 分子筛对 SO2、NO、Hg 都具有一定的吸附能力,且受温度的影响程度存在较大差异,通过升温能顺利实现脱附分离,使得吸附质能回收,吸附剂能够循环使用。

