二元非贵金属Co-Mo基催化剂制备及催化活性研究
王书航,吴明羽,曹安童,邹铠潞,王艳
(沈阳师范大学 化学化工学院,辽宁 沈阳 110034)
氢能是新能源[1]之一。然而,怎样制氢?靠什么来制氢?这些问题一直是广大科研工作者极为关注的研究领域。在众多的储氢材料中,硼氢化钠(NaBH4)以其高质量储氢密度、室温稳定性好被人们所发现。同时氢是一种碳中性[2]的能源载体,可以替代逐渐减少的化石燃料,但实现氢经济将需要高效的氢生产。硼氢化钠[3]潜力广阔无垠,特别是在无人机、燃料电池制氢、便携式制氢机方面具有较强的市场需求和广泛的应用前景。化工行业当中,大部分氢气用于加氢处理、加氢裂化和脱硫。由于优质低硫燃料的需求激增,以及轻质低硫燃油的减少,氢的需求量在不断增长。过去氢气本身是化工的副产品之一,然而现在需量增加,导致供需失衡,石化工业目前也在采取天然气为原料进行氢气的制备。根据现在情况假设,估计到2030年,与2005年相比,炼油行业氢气使用量将翻倍。除去传统燃料精炼之外,第二代的生物质燃料生产中需要相当数量的氢气进行加氢脱氧。
因此,无论对于在精炼过程中减少常规燃料的使用,还是在生物燃料的碳足迹改善中,氢燃料都扮演者重要的角色,尤其氢的脱碳具有显著的影响。通过管道进行氢气的输送已经有大量的实践经验。即使是最乐观的估计,在氢能源需量激增的未来,仍然需要高能量密度液体燃料方便运输。到2050年,石油基燃料仍可占全球运输燃料总需求的60%,包括生物燃料在内的所有液体燃料的市场份额约为80%。这样的份额主要是由于在公路货运,航空和航运中需要高能量液体燃料,并且还反映了使用氢气或电力的替代车辆具有更高效率的事实,从而降低了它们在总运输能量使用中的份额。由于所有液体燃料在生产过程中都需要氢气,因此脱碳可以产生显著的碳减排效应。用低碳氢代替化石氢,到2050年每年可减少约100 MtCO2的二氧化碳排放量。
NaBH4可以通过水解的方式释放其中的氢气,在室温且无催化的情况下不反应。贵金属在一般情况下不易发生化学反应,性质相对来说非常稳定,常温下不易被氧化,高温下也不会自燃,一般酸碱无法腐蚀它,所以用贵金属催化剂制备以后,比一些普通金属催化剂要稳定,容易储存。所以对于贵金属基催化剂,其高昂的成本和有限的存储极大程度的抑制了硼氢化钠制氢的实用化进程。因此,开发不仅价格低廉、储量丰富、具有较高活性[4]的非贵金属催化剂对人类能源改革[5]十分有效。制备二元非贵金属(CoM)[6]基催化材料,并将其应用于NaBH4水解制氢体系。考察制备工艺条件、材料组成等对其催化活性的影响,研究了 NaBH4催化水解制氢的动力学性质。为 NaBH4制氢的进一步应用提供技术支持[7]。对比与非贵金属单质,双金属CoM由于其不同元素之间的协同效应影响,有助于增加材料的表面缺陷,增加表面吸附能力,有助于提高材料催化的相关活性[8]。
1 实验部分
1.1 前处理部分
将泡沫铜金属片切成方形2 cm×2 cm,然后在水浴加热至60 ℃的氢氧化钠溶液中连续浸泡3 min。然后在铜腐蚀溶液中连续浸泡3 min。取出后,将泡沫铜片同时用蒸馏水和无水乙醇涮洗3次,待泡沫铜片不潮湿且干燥有轻微发黑后加入敏化液浸泡3 min和活化液中浸泡2 min,再次上述润洗,烘干,完全干燥后冷却至室温进行称重,质量记作m1。
1.2 镀液的制取
准备3个有40 mL蒸馏水的小烧杯依次加有合适量3份1.1897 g CoCl2·6H2O溶解,待CoCl2·6H2O完全溶解后再称取3份质量分别为计划量钼酸钠溶于上述3份溶液中,边搅拌边向以上3种混合溶液中量取加入有适量甘氨酸,并且无气泡。准备适当浓度的NaOH溶液加入另一个小烧杯里。对上述溶液的pH值滴定调整到预定值,重复水浴加热到25 ℃。最后称取0.151 3 g NaBH43份,分别慢慢加入上述溶液中。配制完镀液后,进行恒温加热。
1.3 化学积淀
将Co/Mo的摩尔比分别为1∶0.6、1∶1、1∶1.2的3份镀液同时放入温度为25 ℃的恒温水浴锅中,待到渡液温度达到25 ℃且稳定不变后。分别放入先前准备好的2 cm×2 cm泡沫铜片。计时3 min后用镊子捞出后依次分别上述洗涤、烘干操作后得到的黑色薄片即为制备的沉积在泡沫铜片上的Co-Mo基催化剂,再次用分析天平对其称量,用质量标记为m2表示。则所制备Co-Mo基催化剂的质量为m3=m2-m1。
1.4 NaBH4放氢过程
将铜片切成1 cm×1 cm备用的小片,以3个完全干燥10 mL圆底烧瓶加入0.106 2 g NaOH和10 mL蒸馏水,再加入 0.500 2 g NaBH4制备氢,恒温水浴温度25 ℃,与所有的圆底烧瓶的解决方案所需的温度,在加入之前的实验准备了小块的金属(Co-Mo基催化剂),采用实验室常用、方便的排水收集法装置对NaBH4放氢性能进行测量,每20 s记录不同组放氢体积(mL)。根据所得到放氢数据绘制出不同Co/Mo摩尔比条件下的放氢动力学曲线,然后利用软件对不同组放氢速率进行拟合计算,得出实验结论。
2 结果与讨论
正如图1、图2、图3所示,硼氢化钠的析氢体积(mL)与镀液时Co/Mo摩尔比存在一种数学函数关系。
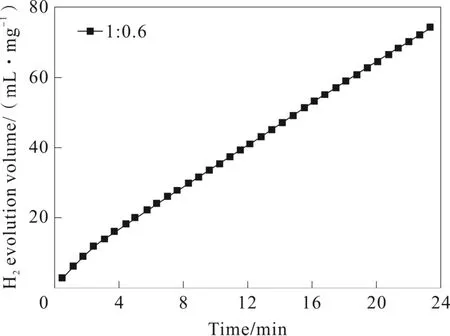
图1 Co/Mo摩尔比为1∶0.6时制备的催化 NaBH4放氢动力学曲线

图2 Co/Mo摩尔比为1∶1时制备的催化 NaBH4放氢动力学曲线
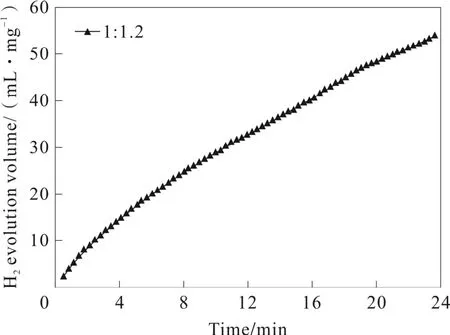
图3 Co/Mo摩尔比为1∶1.2时制备的催化 NaBH4放氢动力学曲线
当实验仅改变镀液中Co/Mo摩尔比时,即当Co∶Mo的摩尔比为1∶0.6、1∶1和1∶1.2其对应析氢的速率是4 434.6、8 938.5和4 108.7 mL·min-1·g-1。可见,当镀液Co/Mo摩尔比为1∶1时,实验中在泡沫铜片上的制备Co-Mo基催化剂对硼氢化钠放氢效果是最为良好的,其产氢速率达到8 938.5 mL·min-1·g-1,该值明显高于Co@C(1 680 mL·min-1·g-1)[9]29和Cu-Co(1 000 mL·min-1·g-1)[10]催化剂。
3 结论
本3组实验借助了一步化学沉积法制备了不同Co/Mo摩尔比的制氢催化剂,研究了泡沫铜片上的生成Co-Mo基催化剂对NaBH4水解制氢能力的影响因素。通过数据结果可以得出:当温度为25 ℃,且镀液浸泡时间为3 min,镀液中Co/Mo摩尔比为1∶1时,较好的催化活性被泡沫铜上制备的Co-Mo基催化剂表达出来了,NaBH4催化水解的产氢速率达到8 938.5 mL·min-1·g-1。
——庆祝中国共产党成立一百周年贵金属纪念币展

