基于流动注射化学发光的两种Luminol体系对重楼药材中总皂苷的分析检测研究
王仕宝,李霞,李会宁,杨培君,张慧
(1.汉中职业技术学院药学院,陕西 汉中 723000;2.汉中职业技术学院秦巴山区药(食)用植物研究所,陕西 汉中 723000;3.汉中职业技术学院农林技术与生物工程学院,陕西 汉中 723000;4.陕西理工大学生物科学与工程学院,陕西 汉中 723000)
中药材重楼为百合科(Liliaceae)重楼属(Paris)植物,主要分布于我国云贵地区、四川南部及西藏南部等地.作为稀有药材,具有抗肿瘤、消肿止痛、止血等功效,对治疗癌症、毒蛇咬伤、跌打损伤、咽喉肿痛等方面有显著疗效[1-3].2015年版《中国药典》收载的重楼(rhizoma Paridis)为百合科重楼属植物云南重楼ParispolyphyllaSmith var.yunnanensis(Franch.)Hand-Maz.或七叶一枝花Parispoly-phyllaSmith var.chinensis(Franch.)Hara 的干燥根茎[4].目前,流动注射与化学发光联用产生的流动注射化学发光分析法,在医药卫生、食品检测方面已有一些应用.本试验研究基于鲁米诺(Luminol)构建了2种化学发光体系,在适当的条件下,重楼皂苷对体系的化学发光反应均具有一定的抑制作用,其检测方法表现出线性范围较广、灵敏度较高的优点.因此,本文对重楼皂苷成分开展分析检测,以期建立重楼药材中对重楼皂苷的流动注射-化学发光检测方法.
1 材料与方法
1.1 试验材料
供试样品来源于七叶一枝花Parispolyphyllavar.chinensis(Franch.)Hara的根茎,于2015年8月采集于陕西省汉中市镇巴县简池镇.从所采药材中选取大小适中的根茎作为供试材料,50 ℃干燥,粉碎,过粒径0.45 mm筛,备用.
1.2 试剂与仪器
所用主要试剂包括重楼皂苷Ⅶ(111593-200402,HPLC≥98%)购自上海源叶生物科技有限公司;Na2CO3,H2O2等均为分析纯试剂;Luminol试剂为化学纯,水为纯水.
主要仪器有流动注射化学发光分析仪(IFFM-E,西安瑞迈分析仪器有限公司)、多功能化学发光检测器(IFFM-A,西安瑞迈分析仪器有限公司);高效液相色谱仪(E2695,美国Waters公司);超声波清洗器(KQ3200DB,江苏昆山超声仪器有限公司);电子天平(梅特勒AL204,精密度0.000 01 g);优普超纯水机(UPH-40,成都超纯科技有限公司);旋转蒸发仪(RV10,德国IKA公司);循环水式多用真空泵(SKD-Ш,郑州长城科工贸有限公司)等.
1.3 试验方法
1.3.1 主要试剂配制 重楼皂苷Ⅶ标准溶液(3.05×10-2mg/mL);Luminol储备液(0.1 mg/mL)按照试验要求,称量、溶解、置于冰箱保存,备用.其他储备液:Cu2+溶液(1×10-2mg/mL);H2O2溶液(质量浓度30%H2O2溶液),KMnO4溶液(1.0 mol/L),H2SO4溶液(1.0 mol/L),HCl溶液(1.0 mol/L),H3PO4溶液(1.0 mol/L),HNO3溶液(1.0 mol/L)等现用现配或提前配制后,置于冰箱保存.
1.3.2 供试样品液制备 准确称取重楼样品20.00 g,置于1 000 mL烧瓶中,用70%乙醇、液料比30∶1(mL∶g)浸泡90 min,之后在水浴锅中加热提取1 h(60 min/次),连续回流提取2次,合并提取液;回收乙醇,浓缩至浸膏后用甲醇溶解定容;在此基础上,采用D-101大孔树脂纯化重楼总皂苷,保存备用.
1.3.3 重楼皂苷 CL-FIA 分析检测设计 参照文献[5-6],准确移取重楼皂苷Ⅶ标准溶液5份,分别稀释至不同浓度,备用.按照流动注射化学发光分析仪的操作流程,以加入重楼皂苷Ⅶ标准浓度为横坐标,空白体系的发光强度和加入重楼皂苷Ⅶ对照品溶液后发光强度的差值为纵坐标,绘制标准曲线.从而计算样品溶液中重楼皂苷得率.取重楼样品溶液50 mL,按上述条件进行检测.根据公式计算重楼样品溶液中重楼总皂苷含量.

(1)
式中:C为样品溶液中重楼总皂苷浓度(μg/mL);V为供试样品的体积(mL);W为称取重楼样品的质量(μg);ρ为供试溶液稀释倍数.
1.3.4 方法学考察 检出限的计算:按照国际纯粹与应用化学联合会(IUPAC)相关规定,以3倍的空白标准偏差(δ)和标准曲线的斜率(k)之比作为检出限,计算公式如下:

(2)
精密度试验:对重楼皂苷Ⅶ标准溶液(3.05×10-3mg/mL),平行测定11组,计算相对标准偏差(RSD).
加标回收率试验:准确吸取3份已知浓度的样品溶液1.0 mL于10 mL容量瓶中,分别加入1.0,2.0、3.0 mL经稀释的重楼皂苷Ⅶ标准液.按照标准曲线建立的方法测定发光强度,并计算回收率.

(3)
2 结果与分析
2.1 Luminol-H2O2体系
Luminol-H2O2体系的化学发光动力学曲线表明,体系反应的化学发光强度呈先升高至最大值,之后开始衰减的趋势(图1-a).在体系中将超纯水换作重楼皂苷Ⅶ标准液后,变化趋势未变,但化学发光信号明显减弱(图1-b).

图1 化学发光动力学曲线
2.1.1 流路及仪器参数的选择 试验比较了不同流路对化学发光的影响[5].研究发现,当流动注射化学发光分析仪的4条通路(a,b,c,d)分别进行如下流路时:a为纯水,b为H2O2溶液,c为金属离子,d为Luminol溶液时,Luminol-H2O2-Cu2+体系的化学发光信号最强,且信号稳定.多次试验结果比较,体系的发光强度随着光电倍增管加载负高压的增大而增大,同时仪器的噪音也增大.为了综合考虑仪器的灵敏度和试验结果的稳定性,选择该仪器负高压为600V,同时确定增益值为1.经过多次对泵速的测试及比较,最终确定了理想的泵速条件,即主泵2.01 mL/min(30转),副泵2.68 mL/min(40转)[5].
2.1.2 反应条件的优化 分别以0.1 mol/L Na2CO3,NaHCO3,NaOH和H2O为反应介质,考察各介质对化学发光强度的影响.结果表明,在纯水介质中发光强度最大,且信号稳定,故选纯水为反应介质.
在其他条件不变的情况下,通过多次比较优化,确定Luminol浓度为2×10-5mg/mL(图2),H2O2的最佳浓度为0.03%(图3).另外,试验考察了等量相同浓度的Mg2+,Mn2+和Cu2+标准溶液,对化学发光体系的增敏作用,结果发现Cu2+对发光强度的影响最大,故选择Cu2+作为该体系的增敏剂,其最佳浓度为1.0×10-3mg/mL(图4).
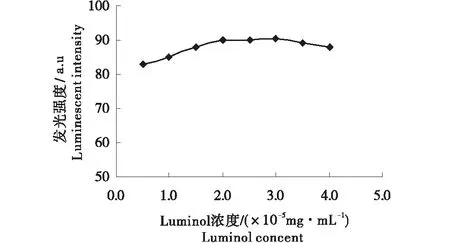
图2 Luminol浓度对体系发光强度的影响

图3 H2O2体积分数对体系发光强度的影响
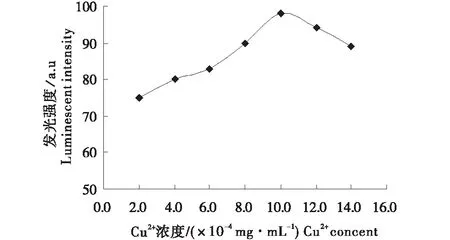
图4 Cu2+浓度对体系发光强度的影响
2.2 KMnO4-Luminol-H+体系
发光动力学曲线表明,在KMnO4-Luminol-H+体系中,化学发光是一个快速反应,发光强度呈先快速升高至最大值,然后开始迅速衰减的趋势(图5-a).将超纯水依次换为重楼皂苷Ⅶ后,化学发光信号分别表现出较大程度的减弱(图5-b).

图5 化学发光动力学曲线
2.2.1 流路及仪器参数的选择 同2.1.1.
2.2.2 反应条件的优化 同2.1.2.确定该体系可选用H2SO4溶液0.30 mol/L(图6)作为反应介质的最佳浓度,选择Luminol浓度为2.0×10-5mg/mL(图7),KMnO4浓度为0.8×10-4mol/L(图8)时较为适宜.

图6 H2SO4浓度对体系发光强度的影响
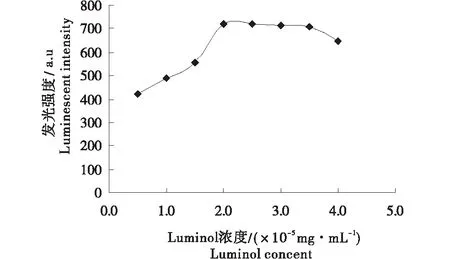
图7 Luminol浓度对体系发光强度的影响
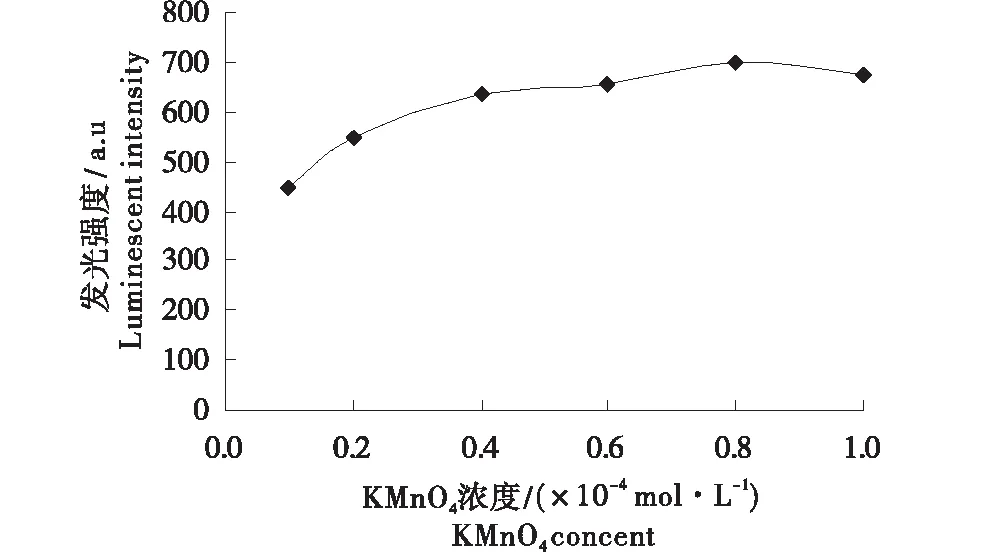
图8 KMnO4浓度对体系发光强度的影响
2.3 标准曲线、精密度和检出限
2.3.1 标准曲线的建立 准确分别移取重楼皂苷Ⅶ标准液,配成梯度溶液.在优化的最佳试验条件下,以加入重楼皂苷Ⅶ标准液的浓度为横坐标,空白体系的发光强度和加入重楼皂苷Ⅶ标准液后体系发光强度的差值为纵坐标,绘制标准曲线[5].试验结果表明:在Luminol-H2O2体系中,重楼皂苷Ⅶ浓度在0.305~3.050 μg/mL范围内,与体系的相对发光强度呈线性关系,线性方程为ΔI=23.453c+8.98,R2=0.998 3(图9).

图9 Luminol-H2O2体系的标准曲线
在KMnO4-Luminol-H+体系中,重楼皂苷Ⅶ浓度在0.140~2.330 μg/mL范围内与体系的相对发光强度呈线性关系,线性方程为ΔI= 174.871c+350.23,R2=0.997 7(图10).

图10 KMnO4-Luminol-H+体系的标准曲线
2.3.2 精密度和检出限试验 在Luminol-H2O2体系中,对2.330 μg/mL的重楼皂苷Ⅶ对照品溶液依次平行检测11次,RSD为2.86%(表1,图11);在KMnO4-Luminol-H+体系中,对1.220 μg/mL的重楼皂苷Ⅶ对照品溶液依次平行检测11次,RSD为2.31%(表1,图12).上述结果表明,仪器精密度较好.

图11 重楼皂苷Ⅶ(2.330 μg/m)检测溶液的化学光谱图

图12 重楼皂苷Ⅶ(1.220 μg/mL)检测溶液的化学光谱图
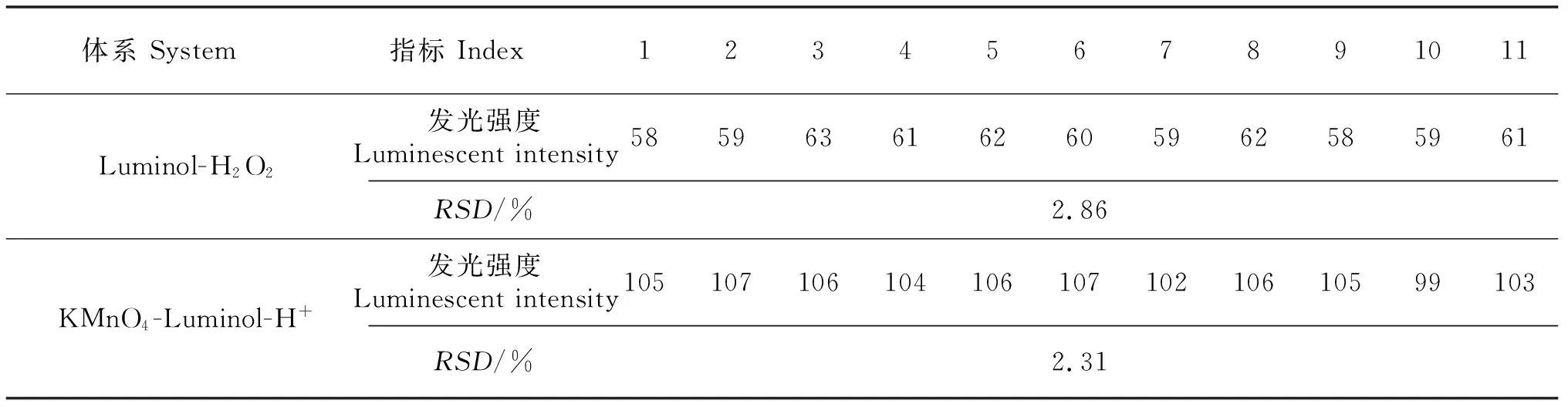
表1 两种体系中精密度试验
根据公式(2)计算,在Luminol-H2O2体系和KMnO4-Luminol-H+体系中,检出限分别为0.201 5 μg/mL和0.102 1 μg/mL.
2.4 干扰试验
结合文献[5-7]对试验方法的选择性评价,在优化最佳条件下,发光强度相对误差绝对值≤5%作为参照值,对2种发光体系中标准溶液的干扰性进行考察.结果表明,外加多个因素均不产生干扰,从而说明本试验中,所构建的化学发光体系抗干扰能力较强;干扰试验设计见表2.

表2 干扰试验结果
2.5 样品分析
按照1.3方法所制备的重楼皂苷类样品溶液,用纯水稀释后并定容至容量瓶中,存冰箱备用;在上述优化条件下分别检测样品,计算重楼皂苷的含量,两种体系检测结果分别为21.138 mg/g和21.317 mg/g.
为验证方法的可靠性,在试验中对重楼皂苷样品测定时采用加标回收方法.方法是将经过稀释的重楼皂苷对照品,分别加入已知浓度的样品溶液中,制成供试品溶液(n=9).分别检测样品中重楼皂苷含量,并据(公式3)计算加样回收率.对2种体系的样品检测,重楼皂苷平均回收率99.96%和97.23%,RSD为2.55%和2.73%.HPLC,UV及CL-FIA不同仪器检测方法检测结果见表3.

表3 不同方法测定重楼总皂苷含量
3 讨论
1) 目前,流动注射与化学发光联用产生的流动注射化学分析法,在医药卫生、食品安全、环境检测等领域得到了广泛的应用[8-11],在Luminol-H2O2体系中,通常情况下鲁米诺与H2O2的化学反应较为缓慢,但当金属离子如Fe2+、Mn2+(反应催化剂)存在时,反应速度变得非常迅速;而且在适当的浓度范围内,化学发光强度与金属离子的浓度呈正比线性关系,从而为金属离子含量的测定与化学发光强度的关系提供检测依据[12].研究表明,Luminol和H2O2溶液发生氧化,当Cu2+存在时,化学发光信号相比空白体系的发光反应强度呈现很强的增敏作用.在本研究Luminol-H2O2体系的溶液中,加入重楼皂苷类物质后,试验结果显示发光强度有较大程度的减弱(约减少40%).究其原因,可能是重楼皂苷与未反应完全的H2O2发生了氧化还原反应,导致Luminol氧化产物(激发状态的发光体,3-氨基邻苯二甲酸盐)的浓度降低,因此返回基态时发光强度表现为一定程度的减小.在KMnO4-Luminol-H+体系中,在酸性环境中,加入重楼皂苷后能极大地抑制发光强度的信号(约减少500%左右).分析原因,可能是重楼皂苷类物质与该反应体系中相关成分反应生成了新的络合产物,从而使得KMnO4与Luminol反应产物的激发态物质量减少,最终导致该体系化学发光反应受到了抑制.有文献报道[13],山奈酚对KMnO4-Luminol体系的化学发光也存在增敏作用.
2) 由于重楼药材中皂苷类成分较多,在前期试验中,选择重楼皂苷Ⅰ、重楼皂苷Ⅶ和薯蓣皂苷分别对两种体系的发光抑制程度进行比较,其3种标品的测定结果的偏差均小于5%,但当重楼皂苷Ⅶ作为标品时,其标准曲线的线性方程的R2相对较大,检测限较低,故在该试验中,选择重楼皂苷Ⅶ作为标品进行重楼总皂苷的检测设计较为合理.在Luminol-H2O2中,标品建立的标准曲线对重楼样品中总皂苷的含量测定为21.138 mg/g,RSD为1.05%,平均回收率为99.96%.在KMnO4-Luminol-H+体系中,总皂苷的平均含量测定为21.317 mg/g,RSD为1.09%,平均回收率为97.23%.在Luminol-H2O2和KMnO4-Luminol-H+2种体系中,在适当的条件下,重楼皂苷对上述体系的发光反应均具有抑制作用,2种检测方法表现出线性范围较广、灵敏度较高的优点,因此构建的检测重楼皂苷类物质的CL-FIA方法,检测结果较为理想.结合表3比较表明,CL-FIA,HPLC或UV对重楼总皂苷检测结果略有差异;CL-FIA检测皂苷类平均含量略低于UV,而回收率略高于UV;但CL-FIA检测相对UV方法体现出很宽的线性范围和较低的检出限.Luminol作为化学发光试剂,可以组合多种化学发光体系,可广泛用于药物的含量测定[14-15].此外,通过综合比较2种发光检测体系,KMnO4-Luminol-H+体系的检测范围较宽、检出限更低、灵敏度较高,故在实际应用中可用于重楼皂苷类化合物的检测和含量控制.

