虾青素聚集体的研究进展
赵英源,王昭萱,薛文杰,舒澳,王高伟,张胜梦,贾慧慧,李瑞芳
(河南工业大学生物工程学院,河南郑州 450001)
虾青素(Astaxanthin)化学名称为3,3'-二羟基-4,4'-二酮基-β,β′-胡萝卜素,是一种酮式类胡萝卜素。常见虾青素为紫红色晶体,不溶于水,易溶于氨仿、丙酮、苯和二硫化碳等有机溶剂[1]。它广泛存在于生物界中,如藻类、虾类、蟹、鱼和鸟类的羽毛。
虾青素的分子结构中根据与碳碳双键连接的基团排列方式的不同,分为顺式结构和反式结构。自然界中的虾青素大部分以全反式(all-trans)结构存在,但在加热、光照或其他环境因素的影响下,会异构化变为顺式异构体[2]。常见的虾青素几何异构体有全反式(all-trans)、9-顺式(9-cis)、13-顺式(13-cis)、15-顺式(15-cis)等见图1,其中全反式结构最不稳定[3]。

图1 虾青素的几何异构体[3]Fig.1 Geometric isomer of astaxanthin[3]
虾青素的分子结构中有两个手性中心(如图2a中标注C-3和C-3'的位置处所示),它可以形成左旋、右旋、内消旋三种结构,因而虾青素存在三种光学异构体(图2)[3]。

图2 虾青素的光学异构体[3]Fig.2 Optical isomer of astaxanthin[3]
虾青素为紫红色晶体,其熔点在216 ℃至218 ℃之间,沸点为774 ℃,密度为1.07 g/mL,不溶于水,可溶于有机溶剂如二氯甲烷(30 g/L)、氯仿(10 g/L)、二甲基亚砜(0.5 g/L)、丙酮(0.2 g/L)等[4]。由于虾青素的分子结构中含有共轭不饱和双键链,因此稳定性差,容易受光、热、酸和氧等破坏而发生异构化和降解。在虾青素分子末端的两个β-紫罗兰酮环中各有一个羟基,可与脂肪酸形成酯(虾青素单酯或虾青素双酯)[5]。
虾青素具有多种重要而独特的保健功能特性,在医药、食品、生物、化妆品等行业都有重要应用。在医药方面,虾青素可有效清除肌细胞中因运动产生的自由基,强化需氧代谢,具有显著的抗疲劳和延缓衰老的作用,能显著提高人体免疫力,因而在抗氧化、抗肿瘤、防癌症、光保护、视力保护、中枢神经的保护、抗炎症、预防心血管疾病等多方面起到重要作用[6];在食品方面,虾青素作为食品着色剂、抗氧化剂等,提升食品品质,增强食品的观感[7];在生物领域,虾青素有色素沉着作用,作为饲料可提高观赏鱼的价值,增加鱼的观赏性[8];在化妆品行业,虾青素能够有效淬灭单线态氧、清除氧自由基、防紫外线辐射,例如日本的高丝面膜有很好的抗皱功效[9]。
1 虾青素的H聚集体和J聚集体
Lu等[10]的研究发现,疏水性的虾青素单体分子在水合溶剂中可以发生分子聚集,产生两种显著不同的聚集体。一种是卡包(Card-packed)构型的H聚集体[11],由虾青素单体分子以“面对面”平行的共轭链堆叠而成,相对于虾青素游离单体的最大吸收波长发生蓝移。另一种是头包尾(Head-to-tail)构型的J聚集体[11],以松散的虾青素单体分子错位平行堆叠组成,相对于虾青素游离单体的最大吸收波长发生红移(图3)。

图3 H和J聚合体的模型[11]Fig.3 H and J aggregates models[11]
2 研究方法
虾青素在水合极性溶剂溶液(Hydrate Polar Solvents)中自组装形成H聚集体或J聚集体,从而引发其构型、光学性质和生理功能的巨大变化,因而对虾青素聚集体的研究是必不可少的。现有常见的研究方法有紫外可见光光谱(UV-vis)、电镜观察样貌(TEM)、圆二色性光谱(CD)、拉曼光谱图(Raman)、荧光光谱图(Fluorescence Spectra)和分子模拟法(Molecular Simulation),从分子水平上对虾青素聚集体进行更深入的研究。
2.1 紫外可见光光谱法
不饱和有机物的π成键轨道跃迁到π反键轨道所吸收的光子正好落在紫外区[12],所以紫外光谱主要用于测定带有双键、三键以及共轭结构的不饱和有机物。虾青素分子结构为含C=C双键的不饱和长链,利用紫外光谱法以对虾青素单体及其聚集体的组成、含量和结构进行分析。
Polivka等[13]将虾青素溶于水合二甲亚砜(DMSO)中形成聚集体,发现虾青素有3种颜色的变化,即黄色(Yellow)H聚集体、橘色(Orange)M单体、粉紫色(Pink-purple)J聚集体。Giovannetti等[14]发现25 ℃下的虾青素与水合丙酮或甲醇溶液中形成卡包(Card-packed)构型的H聚集体,升温至30 ℃时则形成稳定的头包尾(Head-to-tail)构型的J聚集体。不同构型的虾青素在200~800 nm紫外波长范围扫描下,有明显的不同特征吸收峰λmax:虾青素H聚集体的λmax为375~390 nm;虾青素M单体的吸收峰为475~495 nm;虾青素J聚集体的吸收峰为521~533 nm,并伴随着550~565 nm的肩峰。Marcel等[15]将虾青素溶于水合DMSO溶剂时,两个蓝移的H聚集体被分为H1和H2型,λmax分别在386 nm和460 nm处,而红移的J聚集体在570 nm处有最大吸收峰,且发现狭窄的峰是由大量分子组成的H聚集物,而宽频带是由小聚集物组成的。
Lu等[10]分别用乙醇与水比例为1:3、1:5、1:7和1:9的乙醇水溶液和虾青素混合,并立即检测到聚集体形成后的光谱(图4a)和1 h后的测量结果(图4b)。将虾青素与1:3乙醇水溶液混合后,立即检测到的即为H聚集体,其最大蓝移为31 nm,且同样条件下1 h后转变为了J聚集体。此外,在乙醇与水体积为1:1的样品中没有足够的水分子参与聚集体的形成,所以没有任何聚集体。在387 nm处,H聚集物的吸收光谱显示出一个狭窄的吸收峰,而在右边则是一个从400 nm到600 nm的宽频带。基于弗伦克尔激子模型(Frenkel Exciton Model)和线性谱理论(Linear Spectral Theory),该研究计算了这些聚集体的线性吸收和发射光谱来描述溶液中的聚集体结构(分子模拟详见本文2.6)。实验又结合高斯函数(Gaussian Function)模拟计算出了虾青素H聚集体的紫外吸收光谱,研究表明实验测得的H聚集体紫外光谱与由模型计算所得的结果吻合一致。

图4 不同乙醇-水溶剂比例下虾青素的实验吸收光谱[10]Fig.4 The experimental absorption spectra of astaxanthin atdifferent ratios of ethanol-water solvent[10]
2.2 透射电镜观察样貌
透射电子显微镜(Transmission Electron Microscope,TEM)可以看到在光学显微镜下无法看清的小于0.2 μm的超微结构。虾青素的H聚集体和J聚集体尺寸均在100~200 nm之间,因此透射电子显微镜能很好的展现聚集体的外观形态。
根据Giovannetti等[14]的研究,虾青素在一定比例的乙醇/水溶液中形成的H和J聚集体聚合物是不稳定的且难以长期存储。笔者团队[12,16]前期采用乳化-旋蒸和聚电解质大分子自组装技术,将虾青素H聚集体和J聚集体包裹在所构建的DNA和壳聚糖纳米载体的疏水微区中,成功制备了稳定的H型和J型的虾青素/DNA/壳聚糖纳米复合物(H-ADC和J-ADC)。Dai等[17]也成功制备H-ADC和J-ADC纳米颗粒,并通过紫外光谱法确定了虾青素的聚集形式(图5a)。Dai等[17]通过TEM观察到H-ADC和J-ADC为结合紧密的中心为黑色的实心球状物,外部呈灰色且结构较为疏松。H-ADC相比于J-ADC的直径较小,尺寸的差异可能是紧密堆积的H聚集体和松散堆积的J聚集体的空间差异造成的(如本文2.1所述)。且H-ADC和J-ADC在水或脱水状态下均稳定(图5b)。此外,笔者团队[12,16]研究发现H-ADC和J-ADC纳米粒子均带有正电荷,有望表现出非凡的细胞亲和力。

图5 (a)AST、H-ADC纳米复合物和J-ADC纳米复合物;(b)H-ADC和J-ADC纳米悬浮液、纳米粉体的图片及其透射电镜(TEM)图[17]Fig.5 (a) Ultraviolet and visible spectrophotometry (UV-Vis)spectra of astaxanthin (AST), AST H-aggregates/DNA/chitosan nanocomplex (H-ADC) and ASTJ-aggregates/DNA/chitosan nanocomplex (J-ADC); (b) Pictures of H -ADC and J-ADC nano-suspensions, nano-powders and their transmission electron microscopy (TEM) photos[17]
Wang等[16]制备了虾青素J聚集体复合物,并用被H2O2预处理的Caco-2细胞处理该复合物,结果发现该复合物对细胞有很强的保护作用,细胞的存活率明显提高。此外,Dai等[17]在体外对1,1-二苯基-2苦肼基(DPPH·)和羟基自由基(HO·)的清除研究证实,H聚集物的清除效率高于J聚集物或虾青素单体,推测是由于虾青素聚集体的分子间氢键更有助于H聚集体间的电子传递。这些实验结果均为精确设计类胡萝卜素聚集体提供了研究基础。
2.3 圆二色性光谱
根据光学活性分子对左、右偏振光的吸收不同,可以测定分子的手性,其光吸收的差值称为该物质的圆二色性(CD)[18]。通过分析CD光谱的波长,即可得出虾青素H聚集体和J聚集体的取向信息和结构差异。
虾青素在丙酮-水混合物中可以形成不同类型的聚集体,当混合物中水含量较高时(丙酮与水的体积比为1:9)会形成H聚集体,而在水含量较低的混合物(丙酮与水的体积比为3:7)中可以形成两种不同类型的J聚集体,即J1和J2[19]。
KöPsel[20]发现在丙酮与水的体积比为1:9中,虾青素的CD光谱分别在450 nm和475 nm处表现出两种正负科顿效应(Cotton Effect)(图6a)。在波长小于436 nm的波长范围内存在正的圆二色性,在436~650 nm范围内存在负的圆二色性。对偶分子的符号反转发生的波长与最大吸光度一致,证明所研究的聚合体由两个以上的分子组成。最大椭圆度和最小椭圆度在CD光谱上的不同绝对值进一步表明,单体分子在H聚集体中的取向不是严格平行的。此外,由Kuhn[21]首先提出的耦合振荡器模型(Coupled Oscillator Model)观察到的圆二向色性序列及其符号的反转指的是虾青素H聚集体的左螺旋结构。在丙酮与水的体积比为3:7的混合物中存在两种不同的J聚集体,每种不同的部分光谱同样表现出两种有不同的迹象的正负科顿效应(Cotton Effect)(图6b)。J聚集体的圆二色性记录的电子跃迁具有较高的能量,与H聚集体的符号反转情况是相同的,因此该左旋螺旋结构可以归结为J聚集体。另一方面,在低能量吸收带范围内检测到的椭圆度变化与前面两个虾青素聚集体记录的椭圆度变化相反,这表明有两种J聚集体且螺旋的旋转方向明显相反[20]。

图6 (a)虚线:H聚集体CD谱(椭圆度E相对波长);固体线:H聚集体吸收光谱;(b)虚线:J聚集体CD谱(椭圆度E相对波长);固体线:J聚集体吸收光谱[20]Fig.6 (a): Dashed line: H aggregates CD (ovality E relative to wavelength); Solid line: H-aggregates absorption spectrum (b):Dashed line: J aggregates CD spectrum (ovality E relative to wavelength); Solid line: J- aggregates absorption spectrum[20]
2.4 拉曼光谱法
拉曼光谱法是一种通过用激发光照射目标物,收集其内部分子对激发光的散射光谱,从而判断目标物内分子结构及含量的方法,因而该方法可以提供类胡萝卜素聚集体的高能振动信息,进而通过测定多烯中共轭C=C键的变化来判断虾青素的H聚集体和J聚集体[19]。
Subramanian等[19]对反式虾青素聚集体的研究结果表明,在丙酮与水的体积比为10%的虾青素溶液中,2 h后形成卡包结构(Card-packed)聚集体,24 h后形成头尾聚集体(Head-to-tail),且拉曼光谱能有效的区分虾青素聚集体的两种构型。其中,卡包(Card-packed)结构的虾青素的拉曼光谱中C-C和C=C伸缩模式对应的峰值位置分别红移了3 cm-1和9 cm-1(如图7a(ii)),而头尾(Head-tail)排列的虾青素的拉曼光谱中C-C和C=C拉伸模式对应的峰与单体谱相比分别发生了3 cm-1和1.5 cm-1的蓝移(图7a(iii))。反式虾青素的卡包结构(Card-packed)聚集体和头尾(Head-to-tail)聚集体的冷场扫描电镜(FESEM)图像如图7所示。这两种聚集体都是在丙酮-水溶液中产生,并以薄膜的形式转移到玻璃载玻片上,卡包堆积呈片状且呈现出分层特征的结构为H聚集体(图7b),头尾相连呈纤维状且交接处相互重叠或融合的结构为J聚集体(图7c)。

图7 虾青素H和J聚集体的拉曼光谱和FESEM图像[19]Fig.7 Raman spectra and FESEM images of astaxanthin H and J aggregates[19]
Dai等[17]根据虾青素聚集体的拉曼光谱,由于C-C键和C=C键的伸缩振动,1157 cm-l和1515 cm-l处分别有一个峰值。在J-ADC频谱中,C=C拉伸模式(1512 cm-1)较虾青素单体(1515 cm-1)红移约3 cm-1,C-C拉伸频率较虾青素单体(1157 cm-1)下降1155 cm-1。而对于H-ADC,其C=C拉伸模式和C-C拉伸频率较虾青素单体分别蓝移1 cm-1和红移3 cm-1。结果表明,拉曼技术可以有效地区分这两种虾青素聚集体。
2.5 荧光光谱法
虾青素的H和J聚集体经过较短波长的光照,把能量储存起来再缓慢放出较长波长的光,放出的这种光叫荧光。H聚集体、J聚集体和M单体得荧光光谱均不相同,由此即可准确分辩虾青素的两种聚集体。
Lu等[10]选择用于测量的聚集体为1 h后形成的在乙醇和水比例为1:3和1:5溶液中形成的J聚集体和H聚集体。在500~600 nm范围内,单体的不同荧光光谱是由激发态S2的最低波段到基态S0的不同振动波段的发射引起的(图8a);在乙醇和水的比例为1:3溶液中形成的J聚集体的发射光谱与M单体呈现出相似的形状(图8b);在乙醇和水的比例为1:5溶液中形成的H聚集体的发射光谱在540~600 nm范围内最大,且与J聚集体相比有明显的红移(图9a)。

图8 不同激发条件下虾青素单体(a)和J聚集体(b)的发射光谱[10]Fig.8 Emission spectra of astaxanthin monomer (a) and J-aggregate (b) at different excitation. The experimental spectra are shown by solid lines and simulated emission spectrum is shown by dashed line[10]
由于分子间的强烈相互作用,在室温条件下,虾青素单体在乙醇水溶液中形成H聚集体时会产生较大的协同效应,导致激发态分裂成几个子带,子带的数量由聚合系统中的分子数量决定。初始激发后,激子从上向下发生弛豫。Lu等[10]推测是这种能量弛豫机制导致了斯托克位移(Stoker Displacement),即H聚集体的荧光吸收光谱红移。该研究假设J聚集体激发后在子带内没有发生能量弛豫,即松散的J聚集体具有更短的荧光发射时间;而在紧密堆积的H聚集体中,强激子耦合诱导子带发生了能量弛豫。基于假设,Lu等[10]模拟了虾青素M单体和H聚集体的荧光光谱(图8a和图9b),发现得出的峰值与实验值吻合较好。由此可判断两种聚集体的显著差异来自于强激子耦合和弱激子耦合,进而能够准确区分H聚集体和J聚集体。

图9 H聚集体的实验发射光谱(a)和模拟发射光谱(b);实验发射光谱(平方)减去基线并归一化[10]Fig.9 Experimental emission spectra (a) and simulated emission spectrum (b) of H-aggregate. The experimental spectrum(square) is subtract baseline and normalized[10]
2.6 分子模拟法
分子模拟(Molecular Simulation)利用计算机以原子水平的分子模型来模拟分子结构与行为,进而模拟分子体系的各种物理、化学性质的方法。Lu等[10]模拟了H和J聚集体的分子结构并计算了该结构的紫外光谱,发现理论模拟预测值与实验结果吻合,因而分子模拟是一种有效的研究方法。
根据一些天然结构,如蜂巢、雪花、玄武岩柱等稳定的构象,Lu等人[10]假设H聚集体模型是由紧密排列的单个分子堆叠成的,包括二聚体、三聚体和六聚体,J聚集体是由六个分子组成的松散的头尾结构(图10),H聚集体(图10a,b,c)为的正相互作用,而J聚集体(图10d)为负相互作用。

图10 虾青素H聚集物的结构,包括六聚体(a)、三聚体(b)、二聚体(c)和J聚集体(d)[10]Fig.10 Structures of astaxanthin H-aggregates including hexamer (a), trimer (b), dimmer (c) and J-aggregate (d)[10]
H和J聚集体分子结构模型中,耦合作用由距离r决定H聚集体和J聚集与r的函数关系(图11)。对于六个分子组成的聚合体,通过耦合作用分析,得到了各种聚集体中分子间的距离r。H型聚集体的计算值为0.475 nm,J型聚集体的计算值为0.668 nm,这些数值与其他文献中的一致[20,22]。当水的浓度为90%时,平行二聚体和较大的六聚体是主要成分。不同团聚体的混合料需要在不同条件下进行转化。该实验通过对H和J聚集体的分子模拟结合高斯函数模拟出的紫外吸收光谱与实验值的相似情况十分理想,证明该分子模拟模型科学合理。
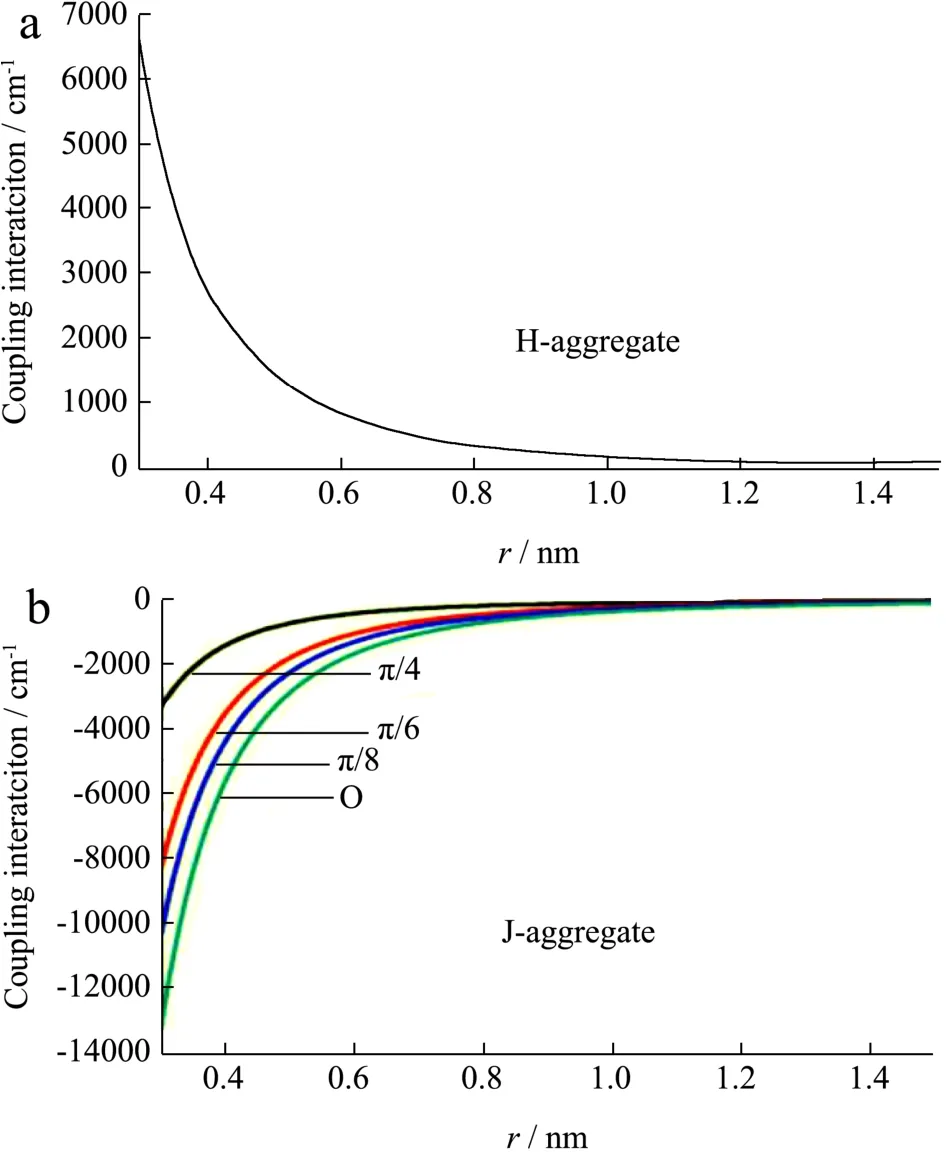
图11 H和J聚体分子间作用力与r的关系[10]Fig.11 Dependence of the intermolecular interactions for H-aggregate and J-aggregate[10]
2.7 其他研究方法
以上研究方法均可以区分虾青素的H和J聚集体,但根据现有的技术,推测有一些研究方法暂时无法详细区分两者,例如红外光谱法。物质由不断振动的状态的原子构成,这些原子振动频率与红外光的振动频率相当。用红外光照射有机物时,分子吸收红外光会发生振动能级跃迁,不同的化学键或官能团吸收频率不同,每个有机物分子只吸收与其分子振动、转动频率相一致的红外光谱,所得到的吸收光谱通常称为红外吸收光谱[23]。Jiang等[24]成功制备了虾青素/玉米蛋白复合物和虾青素/玉米蛋白-壳寡糖配合物,并通过红外光谱证实了虾青素的包覆。在虾青素和虾青素/玉米蛋白复合物和虾青素/玉米蛋白-寡聚糖配合物中的1548 cm-1(C=C的伸缩振动芳环)和970 cm-1(碳氢键中C=C共轭系统)显然在很大程度上削弱了,这表明虾青素结构中的芳环主要是被包埋在玉米蛋白构建的纳米载体中。但目前关于虾青素卡包堆积的H聚集体或头尾连接的J聚集体,通过红外光谱法暂无法明显区分。
虾青素属于类胡萝卜素的一种,有众多对人体有利的理化性质,以上我们对虾青素聚集体的形成机理、影响因素、功能性质和检测方法这四个方面进行了阐述。此外其他类胡萝卜素,与虾青素具有类似的结构,但是性质又有些许不同,因此对其相关的研究也很有必要。
3 展望
虾青素具有超强的抗氧化能力及多种生理功效,且虾青素存在多种光学异构体、顺反异构体、聚集体等不同种形式,不同的虾青素分子构型具有不同的光学特性及生理活性。本文对以虾青素为代表的类胡萝卜素类脂溶性小分子在水合有机溶剂中聚集体的类型、结构、形成机理、影响因素、研究方法等进行了详细的阐述。对后续虾青素及其他类胡萝卜素的生理活性和生物利用度的进一步研究和应用有重要的作用,对今后虾青素在食品、医药、生物学等领域中的应用都具有十分重要的意义。

