反溶剂法制备玉米醇溶蛋白-海藻酸钠复合微粒研究
安丰豪,曹煜婕,姜珊珊,刘佶轩,李 明
(通化师范学院食品科学与工程学院,吉林通化 134001)
玉米醇溶蛋白是存在于玉米胚乳中的一种醇溶性蛋白,约占玉米蛋白总量的60%[1-2]。虽然玉米醇溶蛋白不溶于水,但由于其含有50%以上的疏水性氨基酸,因此该蛋白质可溶解于乙醇溶液、高浓度尿素、碱性pH 值(>11)缓冲剂和阴离子表面活性剂中[3],并且可以通过自组装转化为具有两亲性的微/纳米颗粒,用于运载疏水性活性物质,提高其稳定性和生物利用率[4-8]。然而,玉米醇溶蛋白单独作为载体使用时,其稳定性并不理想,对pH、离子强度和温度的变化敏感。多糖作为天然材料已被广泛用于食品工业,具有高度的稳定性、生物相容性和生物可降解性。由于多糖在分子链上带有天然电荷(离子或非离子)和各种基团(羟基、羧基、氨基等),因此多糖可以通过化学交联、物理交联、多离子复合物和自组装等方式与蛋白质一起参与微/纳米载体的制备[9-10]。因此,玉米醇溶蛋白常与多糖反应制备复合微粒以提高其稳定性。
玉米醇溶蛋白-多糖复合微粒的制备多采用反溶剂法(anti-solvent),也称为液-液分散法(liquid-liquid dispersion)。目前,在玉米醇溶蛋白-多糖复合微粒的研究中,多集中于稳定性及生物活性物质的运载方面,对制备方法则鲜有报道。Joye 等[11]提出,反溶剂法制备微/纳米颗粒的过程中,混合技术(搅拌或超声波)、添加顺序(溶剂向反溶剂中加入或反溶剂向溶剂中加入)、添加方式(滴加或倒入)、反溶剂与溶剂的比例、化合物浓度、温度和稳定剂等都可能会对产品特性产生影响。因此,本研究重点考察了不同制备技术对玉米醇溶蛋白-海藻酸钠复合微粒特性的影响,以期促进蛋白质-多糖复合微/纳米颗粒技术的深入研究和推广应用。
1 材料与方法
1.1 材料与试剂
玉米醇溶蛋白,Z3625,西格玛奥德里奇(上海)贸易有限公司;海藻酸钠、无水乙醇、氯化钠、磷酸氢二钠、磷酸二氢钠、盐酸、氢氧化钠,分析纯,均购自国药集团化学试剂有限公司。
1.2 仪器与设备
水浴锅,DK-S24,上海精宏实验设备有限公司;旋转蒸发仪,RE-3000A,上海亚荣生化仪器厂;分光光度计,722N,上海仪电分析仪器有限公司;高速分散均质机,FJ-200S,杭州齐威仪器科技有限公司;真空冷冻干燥机,LGJ-12,北就松源华兴科技发展有限公司;傅立叶红外光谱分析仪,Nicolet iS20,赛默飞世尔科技(中国)有限公司。
1.3 方法
1.3.1 复合微粒制备
方法一(F1):将玉米醇溶蛋白溶于80%乙醇后得到玉米醇溶蛋白乙醇溶液,将其滴入海藻酸钠水溶液中,边滴边搅拌,搅拌速率为10 000 r/min,混合后继续搅拌5 min,然后旋转蒸发除去乙醇,用蒸馏水定容至原体积,得复合微粒溶液,进行稳定性检测。
方法二(F2):将海藻酸钠溶液滴入玉米醇溶蛋白乙醇溶液中,其他操作同方法一。
方法三(F3):将玉米醇溶蛋白乙醇溶液缓慢倒入海藻酸钠溶液中,其他操作同方法一。
方法四(F4):将海藻酸钠溶液缓慢倒入玉米醇溶蛋白乙醇溶液中,其他操作同方法一。
方法五(F5-分阶段制备):将玉米醇溶蛋白乙醇溶液滴入蒸馏水中,边滴边搅拌,搅拌速率为10 000 r/min,混合后继续搅拌5 min,然后旋转蒸发除去乙醇,用蒸馏水定容至原体积,得玉米醇溶蛋白微粒悬浮液,然后将玉米醇溶蛋白微粒溶液与等体积海藻酸钠溶液混合,得复合微粒溶液,进行稳定性检测。
1.3.2 红外光谱检测
复合微粒溶液经冷冻干燥后得固体样品,取一定量固体样品进行ATR-FTIR 检测,检测所得各样品红外光谱数据经标准化处理后进行对比分析。
1.3.3 稳定性检测
复合微粒的稳定性主要表现在当环境发生变化时,微粒是否易于发生聚集甚至沉淀。复合微粒聚集时,粒度增加,粒度变化可由样品的透光度反映出来[12]。在一定条件下,当样品的透光度降低,说明复合微粒发生聚集,粒度增加,溶液浑浊度增加。因此,复合微粒溶液的透光度可反映样品微粒的聚集状态,从而判断复合微粒的稳定性。
(1)pH 稳定性
吸取1 mL 复合微粒溶液,加入19 mL 磷酸盐缓冲溶液(pH 3~8),混匀,在波长500 nm 条件下测定溶液的透光度。
(2)离子强度稳定性
NaCl溶液浓度分别为200、400、600、800、1 000 mol/L。吸取1 mL 复合微粒溶液,加入1 mL、200 mol/L NaCl 溶液,混匀,取1 mL 混合溶液,再加入19 mL、100 mol/L NaCl 溶液稀释,在波长500 nm 条件下测定溶液透光度。其它不同NaCl 浓度条件下的离子强度稳定性检测方法同上。
(3)热处理稳定性
吸取1 mL 复合微粒溶液,加入19 mL 水,混匀,分别置于45、55、65、75、85、95、100 ℃水浴中,加热15 min,在波长500 nm 下测定溶液透光度。
1.4 数据处理与分析
每组实验均至少重复3 次,结果表示为平均值±标准差。应用Origin 8.5 进行数据处理,并采用最小显著差数法(LSD)进行显著性分析。
2 结果与分析
2.1 制备方法对复合微粒稳定性的影响
2.1.1 制备方法对复合微粒pH 稳定性的影响
由图1 可知,pH 变化对F1 的稳定性影响不显著,但对F2~F5 具有显著性影响(P<0.05)。说明F1 对pH 变化的稳定性相对较好。除F1 和F4 的透光度比较接近外,其它方法制备所得样品的透光度在数值上相差较大,其中F3 的透光度最高,其次是F1、F4、F2 和F5,说明F3 制备的微粒粒度最小,其次是F1、F4、F2 和F5。由以上结果可得,F1 的pH 稳定性最好,F2 的稳定性最差;F3的粒度最小,F5 的粒度最大。因此,在复合微粒制备过程中,玉米醇溶蛋白与多糖溶液的添加顺序、混合方式(滴入、倒入)以及复合方式(F5)对pH 变化的敏感度不同,所得微粒的粒度也不同,是在微粒制备时需要重点考察的因素。

图1 制备方法对复合微粒pH 稳定性的影响Fig.1 Effect of preparation method on pH stability of composite microparticles
2.1.2 制备方法对复合微粒离子强度稳定性的影响
由图2 可知,离子强度的变化对复合微粒的稳定性有显著影响(P<0.05)。其中,F1 在200 mmol/L NaCl 条件下透光度最高,在300~500 mmol/L NaCl 范围内变化不显著;F2 在100~300 mmol/L NaCl 范围内变化不显著,但在300~500 mmol/L NaCl 范围内先下降后上升;F3 在100~300 mmol/L NaCl 范围透光度逐渐下降,在300~500 mmol/L NaCl 时透光度先上升后下降;F4 在100~500 mmol/L NaCl 范围内先上升后下降,300 mmol/L NaCl时透光度最高;F5 在100~500 mmol/L NaCl 范围内变化显著(P<0.05),在400 mmol/L NaCl 时透光度最低。通过以上分析可得,5 种制备方法对离子强度的变化都较敏感,透光度随离子强度的变化呈现不同的变化趋势。由极差比较可得,在100~500 mmol/L NaCl 范围内,F1 的透光度变化相对最小,F2 的透光度变化相对最大,因此,各制备方法对离子强度的相对稳定性由大到小依次是F1>F5>F3>F4>F2。
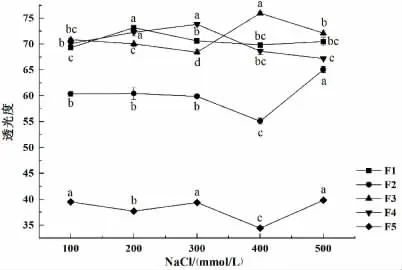
图2 制备方法对复合微粒离子强度稳定性的影响Fig.2 Effect of preparation method on ionic strength stability of composite microparticles
2.1.3 制备方法对复合微粒热处理稳定性的影响
透光度可通过检测样品的混浊度而得,反映了样品微粒聚集程度的大小或微粒粒度的大小[12]。由图3 可知,在45~100 ℃范围内,不同制备方法所得复合微粒的透光度对温度的变化比较敏感(P<0.05),说明热处理对复合微粒稳定性的影响显著。5 种制备方法所得的复合微粒中,F1 对热处理的稳定性相对较好,F5 对热处理的稳定性相对最低。

图3 制备方法对复合微粒热处理稳定性的影响Fig.3 Effect of preparation method on thermo stability of composite microparticles
综上所述,在复合微粒制备过程中,不同的制备方法对所得微粒的透光度有显著影响,说明不同方法所得微粒的粒度大小差异明显,同时,不同制备方法所得微粒的稳定性也不同。因此,在利用玉米醇溶蛋白和多糖制备复合微粒时,添加顺序、混合方式及复合方式等制备参数都是需要重点考察的因素。
2.2 不同制备方法所得复合微粒的红外光谱分析
傅立叶变换红外光谱技术常用于研究蛋白质与多糖的相互作用,有效地识别功能团。蛋白质重复单元的振动产生一些特征性的红外吸收带,如酰胺A、B 和I~VII 等[13]。
由图4 可知,在玉米醇溶蛋白的红外光谱中,1 644 cm-1和1 531 cm-1分别属于酰胺I 带(1 700~1 600 cm-1区域,主要是C═O 拉伸)和酰胺II 带(1 600~1 500 cm-1区域,主要是C—N 拉伸加上N—H 弯曲模式),3 100~3 500 cm-1是由于羟基的O—H 拉伸振动,CH2反对称和对称拉伸振动的光谱在3 000~2 800 cm-1范围内。在海藻酸钠的红外光谱中,O—H 和C—H 的伸缩振动分别表现在3 242 cm-1和2 925 cm-1[14],而1 590 cm-1和1 409 cm-1分别来源于COO—和C═O 的伸缩振动[15],C—O—C 的伸缩振动表现在1 082 cm-1[16]。

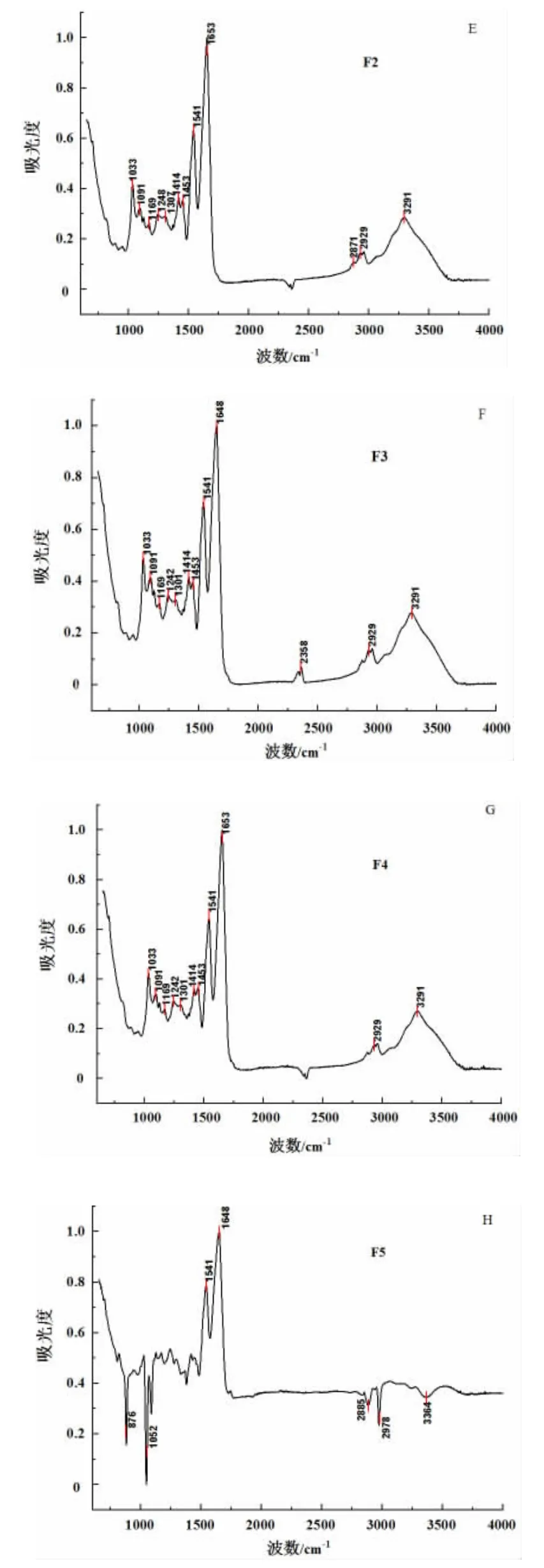
图4 玉米醇溶蛋白(A)、海藻酸钠(B)、玉米醇溶蛋白和海藻酸钠的物理混合物(C)、方法1~5(D~H)所得微粒的红外光谱Fig.4 The infrared spectroscopy of Zein (A),sodium alginate(B),zein-alginate physical mixture (C),microparticles obtained from F1~F5 (D~H)
由图4 可知,玉米醇溶蛋白和海藻酸钠粉末混合样品的红外光谱(图4C)与F1~F4 的光谱有显著的区别,说明玉米醇溶蛋白与海藻酸钠的相互作用不是简单的物质混合,而是发生了某些化学反应。有研究显示,蛋白质与多糖之间的相互作用包括离子键、氢键和疏水作用力[10]。由F1~F4 的光谱结果可知(图4 D~G),不同制备方法对样品红外光谱的影响不显著,说明玉米醇溶蛋白与海藻酸钠的作用机制是相同的,不受溶液的添加顺序和混合方式(滴入、倒入)的影响。但是,由图4H 可知,F5 的红外光谱与前4 种样品的红外光谱有显著区别,说明F5 与F1~F4 的反应机制不同。
3 结论
由稳定性研究结果可得,在玉米醇溶蛋白与海藻酸钠复合微粒的制备过程中,添加顺序和混合方式(滴入、倒入)对微粒的稳定性有显著影响,其中,F1 对pH 和热处理的稳定性相对较好。同时,不同制备方法所得复合微粒的粒度不同,由小到大依次是F3<F1<F4<F2<F5。由红外光谱结果可得,分阶段制备法(F5)与其它方法在微粒的形成机制上有本质的区别,需要进一步深入的研究。

