基于深度学习的术后医疗相关感染风险预测模型
孙 琛,裴丽坚,张越伦,黄宇光
中国医学科学院 北京协和医学院 北京协和医院麻醉科,北京 100730
医疗相关感染(healthcare-associated infection,HAI)是外科手术后常见且严重的并发症,是指由某种感染性物质或其产生的毒素介导的局部或全身感染状态,而在治疗前并无感染证据[1],与二次手术、二次入院、永久性残疾甚至死亡等不良预后密切相关[2]。HAI一直以来都是影响患者健康的重要问题,各种预测模型层出不穷。目前大多数预测模型主要基于术前和术中危险因素进行构建,主要包括患者自身因素(如基础疾病、一般状态)和手术因素(如手术时间、手术种类),采用的模型包括多因素Logistic回归模型[3- 6]、随机森林[7]、人工神经网络[8]等。然而这些预测模型往往较为单一,预测能力有限。近年来,越来越多的学者开始关注基本生命体征(心率、血压、核心体温等)对术后HAI的影响,采用长短期记忆网络(long short-term memory,LSTM)模型等机器学习模型,充分利用生命体征随时间变化的时序性特点[9],取得了一定的预测效果。LSTM是一种时间循环神经网络,其独特的设计结构适合处理时序性数据,以及预测时间序列中的重要事件。但这类模型只考虑了生命体征的影响,并未很好地融合其他传统危险因素,不能全面预测术后HAI的发生。因此,本研究拟融合传统术前、术中危险因素和术中基本生命体征(心率、血压、核心体温),基于深度学习方法构建术后HAI预测模型。希望利用深度学习方法,对多种可能危险因素进行深入分析,提高模型表现力,增强其临床实用性,改善患者预后。
资料和方法
资料来源基于2项随机对照试验(randomized controlled trial,RCT)(NCT02715076[10]和ChiCTR-IPR- 17011099 http://www.chictr.org.cn/showproj.aspx?proj=18892),回顾性分析2016年2月1日至2019年1月31日在北京协和医院行择期根治性切除术的进展期消化系统肿瘤患者的临床资料。纳入和排除标准参照2项RCT。体重指数(body mass index,BMI)>30 kg/m2、术前4 d内存在严重感染或腋下温度>37.5 ℃、存在难以控制的胰岛素依赖型糖尿病(术前血糖>250 mg/dl,1 mg/dl=1/18 mmol/L)、存在出凝血功能障碍性疾病、术前系统性应用糖皮质激素>6个月的患者均不纳入本研究。
数据收集患者基线资料包括可能与术后HAI相关的术前和术中因素。术前因素包括:性别、年龄、BMI、吸烟史、美国麻醉医师学会(American Society of Anesthesiologists,ASA)分级、合并基础疾病史、新辅助放化疗史、是否接受肠外营养和术前最近一次实验室指标。术中因素包括:手术入路、手术类别、术中失血量、术中异体红细胞输注情况、麻醉时间和术中间隔10 s的生命体征监测值(心率、血压、核心体温)。因所有患者均采用全身麻醉,术中呼吸频率和脉搏血氧饱和度几乎保持不变,故不纳入分析。患者均随访至术后30 d,观察记录结局指标的发生情况。
结局指标主要结局指标:术后30 d内首次出现HAI。HAI诊断依据2008年美国疾病控制与预防中心(Centers for Disease Control and Prevention,CDC)提出的诊断标准[1]进行判断,出现该标准中规定的任意一种HAI均认为出现主要转归。存疑病例由麻醉科、重症医学科、外科和感染科的高级职称医生组成的专家组讨论后确定。次要结局指标:非计划二次手术、非计划二次入院和住院天数。非计划二次手术定义为患者术后30 d内因各种原因导致的计划外二次手术。非计划二次入院定义为患者术后30 d内因各种原因导致的出院后急诊入院。
特征筛选传统的术前、术中危险因素采用单因素Logistic回归分析进行筛选,以术后HAI作为因变量,术前、术中因素作为自变量,选出其中P<0.1的变量。进一步结合临床经验、既往研究、共线性诊断结果等,筛选出最终的危险因素。共线性诊断采用相关系数、方差膨胀因子及特征根系统3种方法。术中基本生命体征采用基于迭代遮挡输入的LSTM模型进行筛选[11]。首先使用术中基本生命体征数据集训练LSTM预测模型,再分别对术中整个时段的各项生命体征(心率、血压、核心体温)进行迭代遮挡,比较遮挡前后模型预测术后HAI的差别,计算出每个特征的显著性分数,并在所有患者中求平均值。显著性分数以|Sy-Sy’|表示, Sy代表遮挡前LSTM模型预测术后HAI的概率,Sy’代表遮挡后LSTM模型预测术后HAI的概率。
模型构建与评估构建融合术前、术中危险因素和术中基本生命体征的术后HAI深度学习预测模型(简称融合的术后HAI深度学习预测模型)。首先利用LSTM模型将术中基本生命体征(心率、血压、核心体温)序列进行编码,进而将筛选出的术前、术中危险因素和编码后的术中基本生命体征融合在一起,使用全连接层对术后HAI进行预测。受实际临床数据集样本量的限制,为了尽量减少划分数据集时对样本分布造成的影响,采用5折交叉验证[12],在每次验证中,以8∶1∶1划分训练集、验证集和测试集。模型训练时采用Cross-Entropy损失函数[13],每个交叉验证中共进行20个迭代训练。
同时,分别构建仅纳入术前、术中危险因素的多因素Logistic回归模型和随机森林模型[14],仅纳入术中基本生命体征的LSTM模型。多因素Logistic回归模型:将上述筛选得到的术前、术中危险因素以向后选择法(似然比检验)纳入多因素Logistic回归模型。随机森林模型:采用上述筛选得到的术前、术中危险因素,以100个树构成,使用基尼系数计算分叉标准[16]。LSTM模型:采用术中基本生命体征变化序列进行模型训练,在LSTM最后一个输出位置接全连接层,以输出HAI发生率。模型训练采用Cross-Entropy损失函数,每个交叉验证中共进行20个迭代训练。将上述各种模型性能进行评估,评估指标包括准确率(accuracy,ACC)、F1值、受试者工作特征曲线下面积(area under the receiver operating characteristic curve,AU-ROC)[15]。ACC是指所有预测正确的样本数(包含阳性与阴性)与总样本数之比;F1值是用来综合评价精确率(precision,P)和召回率(recall,R)指标,2/F1=1/P+1/R,P为正确预测为阳性的样本数与全部预测为阳性的样本数之比,R为正确预测为阳性的样本数与全部实际为阳性的样本数之比。
术中基本生命体征模拟调整采用模拟退火算法在基本生命体征数值上添加一个最优干预,在有效范围内合理调整生命体征,使HAI发生率最大程度地降低。模拟退火算法关键评价函数采用融合的术后HAI深度学习预测模型计算术后HAI发生率。提取术后发生HAI患者的数据,分别设定3种不同模拟条件:不降低退火初始温度且取手术进程后10%、降低退火初始温度且取手术进程后10%、降低退火初始温度且取手术进程后20%。采用术后HAI发生率降低比例的平均值对调节效果进行评价。
结 果
研究对象特征描述本研究共纳入839例行择期根治性切除术的进展期消化系统肿瘤患者,其中男性575例(68.5%),女性264例(31.5%),平均年龄(62.9±10.8)岁(表1)。术后30 d内出现HAI的患者112例(13.3%),非计划二次手术19例(2.3%),非计划二次入院13例(1.5%),住院天数14(12,19)d。
HAI特征筛选结果术前、术中危险因素的单因素Logistic回归分析结果显示,新辅助化疗(OR=0.35,95%CI=0.11~1.15,P=0.083)、肠外营养(OR=2.34,95%CI=1.32~4.13,P=0.003)、术前最近一次血红蛋白(haemoglobin,Hb)(OR=0.99,95%CI=0.97~1.00,P=0.043)和血细胞比容(haematocrit,Hct)(OR=0.94,95%CI=0.89~0.99,P=0.024)、手术部位[食管(OR=0.11,95%CI=0.02~0.82,P=0.031)、胃(OR=1.77,95%CI=0.80~3.90,P=0.098)、结直肠(OR=1.56,95%CI=0.87~2.82,P=0.087)、胰十二指肠(OR=3.51,95%CI=1.92~6.41,P<0.001)、肝脏(OR=0.30,95%CI=0.13~0.71,P=0.006)]、术中失血量>500 ml(OR=2.55,95%CI=1.33~4.87,P=0.005)、术中输入异体红细胞>2 U(OR=1.92,95%CI=0.90~4.10,P=0.090)以及麻醉时间>4 h(OR=2.08,95%CI=1.15~3.80,P=0.016)会增加术后HAI的发生风险。结合临床经验,考虑到术前Hb和Hct值绝大多数在正常范围内,对术后HAI影响的临床意义有限,因而剔除。共线性诊断发现术中失血量和术中输入异体红细胞之间存在较明显的共线性,考虑患者术中输血是大量失血后的主要治疗措施,因此剔除术中输入异体红细胞>2 U。最终筛选得到9个术前、术中危险因素,即新辅助化疗、肠外营养、手术部位(涉及食管、胃、结直肠、胰十二指肠、肝脏)、术中失血量>500 ml和麻醉时间>4 h。采用基于迭代遮挡输入的LSTM模型对术中基本生命体征(心率、血压、核心体温)进行筛选,计算得到心率、收缩压、舒张压和核心体温的显著性分数分别是2.4891、0.0002、0.0000、0.0003,可见显著性程度:心率>核心体温>收缩压>舒张压。

HAI预测模型构建与评估结果根据上述LSTM模型中各项基本生命体征的显著性程度对其进行排序编码,进而将其与9个术前、术中危险因素融合,构建融合的术后HAI深度学习预测模型。同时,将9个术前、术中危险因素纳入多因素Logistic回归模型和随机森林模型,将时序性的术中基本生命体征(心率、血压、核心体温)数据纳入LSTM模型。4种模型性能评估比较结果显示,融合的术后HAI深度学习预测模型表现最佳,拥有更好的区分度和校准度(ACC=0.733,F1=0.237,AUC=0.728)(表2)。
术中基本生命体征模拟调整结果对发生HAI患者采用模拟退火算法进行模拟调整,调整前HAI发生率为0.518,3种不同模拟条件(不降低退火初始温度且取手术进程后10%、降低退火初始温度且取手术进程后10%、降低退火初始温度且取手术进程后20%)调整后的HAI发生率分别是0.467、0.464、0.447,分别降低了0.051、0.054、0.071。3种模拟条件下模拟退火算法均可一定程度上降低术后HAI发生率。与不降低退火初始温度相比,降低退火初始温度可以更好地降低术后HAI发生率;与取手术进程后10%相比,取手术进程后20%可以更好地降低术后HAI发生率。
讨 论
HAI是术后常见且严重的并发症,每年有近百万患者因HAI而死亡,造成的经济损失高达350亿美元[18]。为了降低术后HAI的发生率,越来越多的研究者们开始探索HAI危险因素及预测模型。已报道的危险因素包括:高龄、糖尿病/围手术期高血糖、肥胖、吸烟、术前低白蛋白(<35 g/L)、免疫抑制状态等患者因素,以及急诊手术、切口分级、手术时间过长、大量输血等手术因素,并基于这些危险因素构建了相应的预测模型[3- 6]。然而这些研究大多采用Logistic回归分析,虽简单易行,但模型较为单一,对于更复杂的临床数据分析存在局限性。另一方面,针对术中因素,既往研究较少关注基本生命体征的影响,未能引起医护人员对术中生命体征管理的足够重视。针对这一问题,部分研究者开展了术中基本生命体征相关研究,发现术中核心体温、血压等与术后感染存在相关性[19- 23]。但是这些研究并未充分利用生命体征随时间变化的特点,多将其进行简单的统计学计算与分析,难以充分挖掘这些时序性变化数据的潜在信息。随着数字化数据的获取和人工智能在医疗领域的发展,研究者开始将机器学习、深度学习方法用于疾病预测模型的建立,尝试如何更有效地利用时序性生命体征的数据信息,例如基于支持向量机(support vector machine,SVM)[24]和LSTM[9]的败血症及感染性休克预测模型,基于梯度提升决策树(gradient boosting decision tree,GBDT)的心力衰竭预测模型[25]。然而这些模型的预测能力较为有限,模型准确性不高,可能与仅仅纳入时序性生命体征数据,而没有结合传统的围手术期危险因素有关。
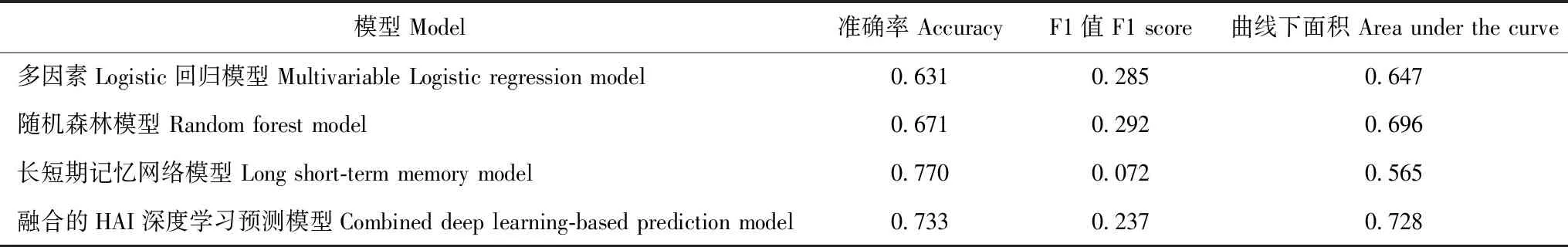
表2 4种模型性能评估比较
本研究针对术后HAI这一重要问题,首先将术中基本生命体征作为模型预测的主要纳入变量,这在术后HAI预测模型研究中并不多见,强调了术中生命体征管理对术后HAI的重要性。同时预测模型并不局限于生命体征,而是充分融合了传统的术前、术中危险因素和术中基本生命体征2类特征,并利用深度学习方法充分提取和分析纳入变量的数据信息,既保证纳入特征的全面性与模型预测的有效性,也提高了模型的临床可干预性。
本研究构建了融合的术后HAI深度学习预测模型、多因素Logistic回归模型、随机森林模型和LSTM模型,并对4种模型进行了评估比较。多因素Logistic回归模型是目前此类研究中最常用的预测模型,只纳入传统围手术期危险因素进行建模;随机森林模型是近几年在医学领域被广泛应用的早期机器学习模型,通常也只纳入传统围手术期危险因素进行建模;LSTM模型是适用于处理时序性数据的一类模型,近年来逐渐应用在生命体征与疾病预测的研究中。本研究结果发现,综合ACC、F1值和AUC,融合的术后HAI深度学习预测模型表现最佳,模型性能最好;单纯纳入术前、术中危险因素建模,机器学习模型(随机森林)比多因素Logistic回归模型在一定程度上表现出更强的拟合能力;单纯纳入术前、术中危险因素建模比单纯纳入术中基本生命体征建模效果更好,提示在预测HAI方面,术前、术中危险因素可能起着主导性作用,而在此基础上融入时序性生命体征数据,可以提升模型的预测能力。
本研究结果显示,术后30 d内HAI发生率达13.3%,与既往研究一致[26]。术前、术中危险因素中最终筛选出9个显著性因素,即新辅助化疗、肠外营养、手术部位(涉及食管、胃、结直肠、胰十二指肠、肝脏)、术中失血量>500 ml和麻醉时间>4 h。术中基本生命体征显著性排序表明,心率对术后HAI的影响较其他指标更大。这些危险因素筛选结果提示,除了患者自身的基础疾病、营养状态等情况,手术创伤以及术中组织灌注对于术后HAI的发生也有着不可忽视的影响。多项研究表明,术中失血和输血是HAI的独立危险因素[27- 28],事实上,大多数术中输血是作为大量失血后的一种治疗手段,用于补充血容量、维持组织灌注,尽管异体输血本身可造成输血相关感染等不良后果[29],但更重要的是大量失血后的低血容量、低灌注、低氧供状态,造成机体免疫防御能力下降[30]。心率升高是低血容量的早期临床征象之一,心率较其他生命体征对HAI影响更大也提示维持血容量、保证组织灌注对于降低术后HAI起着重要作用。
以往的HAI预测模型相关研究大多停留在建模,并未进一步应用建模结果改进临床方案和临床转归。本研究充分利用术中基本生命体征干预性强这一优势,对其进行模拟调整,尝试探索了基于模拟退火算法的自动调节系统,通过模拟退火算法寻找添加在基本生命体征上的最优数值扰动,在有效范围内合理调整生命体征,使得HAI发生率有一定程度的下降,初步形成了一个覆盖特征筛选、预测、调整的完整系统。
本研究存在以下局限性:(1)数据来源于单中心RCT,样本量有限,阳性病例偏少,在一定程度上限制了模型的预测能力,未来还需要更大样本量的数据以提升预测模型的准确性,并在更广泛的人群中对模型进行外部验证。(2)术中基本生命体征只纳入了心率、血压(收缩压和舒张压)和核心体温,维度较低,对模型预测能力的提升有限,未来可以挖掘更多可干预性强的时序性数据,丰富数据包含的信息,提高预测的准确性和预测模型的可干预性。(3)由于模拟退火算法本身是一种基于随机迭代的启发性算法,波动较大,在临床实际情境中的应用性较差,未来需要选取更适合真实临床情境的自动调节系统,生成更符合临床实践的调整策略。
综上,本研究针对HAI这一外科手术后常见且严重的并发症,基于深度学习方法,构建了融合术前、术中危险因素和术中基本生命体征的术后HAI预测模型,模型性能表现较好,并采用模拟退火算法探索术中基本生命体征的模拟调整,在一定程度上降低了术后HAI的发生率,为预防术后HAI提供了新思路,为围手术期管理方案提供了参考。

