醋酸铅暴露对PC12细胞凋亡与自噬的影响及可能机制
张 谊,王立晖,陈月芳,李永金,柳浦青
(1.南通大学附属丹阳医院,江苏省丹阳市人民医院,江苏 丹阳 212300;2.江苏大学医学院药理学教研室,江苏 镇江 212013;3.浙江中医药大学附属第二医院,浙江 杭州 310005)
铅是一种普遍存在于环境中的重金属。长期接触铅可使神经系统发生不可逆损伤,导致学习和记忆功能减退[1]。在模拟阿尔茨海默病研究中,抑制神经细胞凋亡可改善大鼠行为和认知功能[2];而抑制自噬对小鼠神经元具有保护作用[3],表明神经系统损伤过程中存在细胞凋亡与自噬。
沉默信息调节因子1(sirtuin1,Sirt1)是一种脱乙酰酶,可通过激活下游底物——叉头框蛋白转录因子3a(forkhead box O3a,FoxO3a)介导神经细胞的生成、凋亡与自噬[4-5]。重金属锰暴露可导致神经细胞中Sirt1 蛋白降解,促使FoxO3a 蛋白表达上调及乙酰化水平增加,诱导细胞损伤[6]。在H2O2诱导的神经毒性反应中,阻断Sirt1/FoxO3a 信号途径可抑制细胞促凋亡蛋白和自噬蛋白的表达,减轻神经细胞损伤[7],表明Sirt1/FoxO3a 信号通路参与了细胞凋亡和自噬。本实验室前期研究发现,神经细胞的损伤伴随氧化应激与细胞凋亡[8],但目前仍不清楚铅暴露是否可诱导神经细胞自噬。
本研究选用大鼠肾上腺嗜铬细胞瘤PC12 细胞作为实验对象,建立醋酸铅〔Pb(Ac)2〕暴露细胞模型,探讨铅暴露对PC12 细胞凋亡与自噬的作用及其与Sirt1/FoxO3a信号通路之间的关系,为研究及预防铅神经毒性相关性疾病提供实验支持与理论依据。
1 材料与方法
1.1 细胞、试剂和仪器
大鼠肾上腺嗜铬细胞瘤PC12 细胞株,中国科学院上海细胞库。DMEM 培养基、胰蛋白酶、单丹磺酰尸胺(monodansylcadaverine,MDC)试剂盒,美国Gibco公司;新生牛血清,杭州四季青生物工程材料有限公司;Pb(Ac)2,美国Sigma 公司;MTT,美国Amresco 公司;乳酸脱氢酶(lactate dehydrogenase,LDH)试剂盒,碧云天生物技术研究所;吖啶橙/溴化乙锭(acridine orange/ethidium bromide,AO/EB)试剂盒,北京Solarbio 公司;Annexin V/PI凋亡检测试剂盒,美国Molecular Probes 公司。兔抗人Sirt1、FoxO3a、叉头蛋白M1(forkhead box protein M1,FoxM1)和P62 蛋白多克隆抗体,美国ImmunoWay 公司;兔抗大鼠Bcl-2 相互作用蛋白1(Bcl-2 interacting coiled-coil protein 1,Beclin1)多克隆抗体,武汉ABclonal 公司;兔抗小鼠微管相关蛋白1 轻链3(microtubule-associated protein 1 light chain 3,LC3)多克隆抗体,美国Proteintech公司;小鼠抗人GAPDH 单克隆抗体、山羊抗兔IgG二抗、山羊抗鼠IgG 二抗,美国GeneTex 公司;显影剂,美国Millipore 公司。其余试剂均为市售国产分析纯。
SW-CJ-2G 型超净台,苏州净化设备总厂;CO2细胞培养箱,上海Heal Force 公司;CKX53 型倒置显微镜,日本Olympus 公司;UPK-I-10T 型超纯水机,成都超纯科技有限公司;CP124S型电子分析天平,德国赛多利斯公司;680型酶标仪和1658001 型电泳仪,美国Bio-Rad公司;凝胶成像系统,南京麦高德生物科技公司;X1R 型冷冻离心机,美国Thermo Fisher 公司;Axio Scope A1 型荧光显微镜,德国Carl Zeiss公司;2400F超声波粉碎机,新芝生物科技公司;FACS CantoⅡ型流式细胞仪,美国BD公司。
1.2 细胞培养和分组处理
PC12 细胞置高糖DMEM 培养基中,置于含5%的CO2和95%空气的37 ℃培养箱中孵育,取对数生长期细胞进行实验。细胞分为细胞对照组(空白培养基)和Pb(Ac)2100,200 和400 μmol·L-1组,给予Pb(Ac)2暴露24 h后,收集细胞进行实验。
1.3 MTT 法和比色法检测细胞存活率和细胞外液LDH含量
取对数生长期的PC12 细胞接种于96 孔板中,按1.2 分组处理后,弃去上清,每孔加入10 μL MTT 0.5 g·L-1,于37 ℃继续培养4 h 后弃去培养液,加入100 μL DMSO,振匀后于490 nm 处测定各孔吸光度(A490nm)值。细胞存活率(%)=(1-处理组A490nm/细胞对照组A490nm)×100%。
按照试剂盒说明书进行操作,收集1.2 分组细胞上清液,在波长450 nm 处检测各孔吸光度(A450nm)值,计算各组LDH含量。
1.4 AO/EB染色观察细胞凋亡
取对数生长期PC12 细胞接种于6 孔板中,按1.2 分组处理后,弃培养液并用PBS 洗涤2 次,在各孔加入2 mL 按比例配制好的AO/EB 混合染液,4 ℃避光反应10 min,将6 孔板置于荧光显微镜下,每组随机挑选10 个视野,观察各组细胞染色情况,核染色质呈橙红色荧光的为凋亡细胞。
1.5 流式细胞仪检测细胞凋亡率
取1.2 分组处理的细胞,用预冷的PBS 洗2 遍后加入400 μL 缓冲液,轻轻混匀细胞,再加入5 μL Annexin V-FITC 和5 μL PI 溶液,避光孵育15 min,用流式细胞仪检测细胞凋亡率。
1.6 MDC染色法观察细胞自噬
取对数生长期PC12 细胞接种于装有玻璃片的6 孔板中,按1.2 分组处理后,弃去培养基,用PBS洗涤,加入MDC 染料室温避光染色30 min。吸去染料后,加入4%多聚甲醛固定10 min,待玻璃片晾干后置于荧光显微镜下观察。自噬细胞出现绿色自噬空泡,以绿色荧光强度表示细胞自噬程度。
1.7 免疫荧光法检测细胞内Beclin1的表达
取1.2收集的细胞,用0.3% Triton X-100透化,羊血清封闭后,滴加抗Beclin-1 抗体(1∶300),4 ℃摇床反应过夜;用PBS 洗涤后加入山羊抗兔IgG二抗(1∶600),37 ℃避光反应1 h,甘油封片后置荧光显微镜下观察。当细胞自噬时,Beclin1蛋白呈点状聚集,以荧光强度反映Beclin1的表达水平。
1.8 Western 印迹法检测细胞Sirt1,FoxO3a,FoxM1,Beclin1,LC3和P62蛋白表达水平
取1.2 收集的细胞,加入裂解液裂解提取总蛋白,并用试剂盒测定蛋白浓度。总蛋白经电泳分离并转印至PVDF膜上,用脱脂奶粉封闭,继而与一抗(Sirt1,FoxO3a,FoxM1,Beclin1,LC3 和P62 均1∶1000;GAPDH,1∶7000)于4 ℃摇床反应过夜。洗涤数次后,将膜和相应山羊抗兔、山羊抗鼠IgG二抗(1∶5000)在室温下反应1 h,加入显影剂,在凝胶成像系统上进行扫描并拍照,Image J 软件分析各条带积分吸光度值。以目标蛋白与GAPDH 的积分吸光度值比值表示目标蛋白的相对表达量,LC3-Ⅱ与LC3-Ⅰ蛋白表达比值表示细胞自噬水平。
1.9 统计学分析
2 结果
2.1 Pb(Ac)2对PC12 细胞存活率和细胞外液LDH含量的影响
MTT 法检测结果如图1A所示,与细胞对照组相比,处理24 h 后,Pb(Ac)2100,200 和400 μmol·L-1组PC12 细胞存活率均显著降低(P<0.05,P<0.01)。如图1B所示,Pb(Ac)2可引起PC12细胞外液LDH 含量增加。与细胞对照组相比,Pb(Ac)2100,200 和400 μmol·L-1组细胞外液LDH 含量均显著增加(P<0.05,P<0.01),表明Pb(Ac)2诱导PC12细胞损伤。
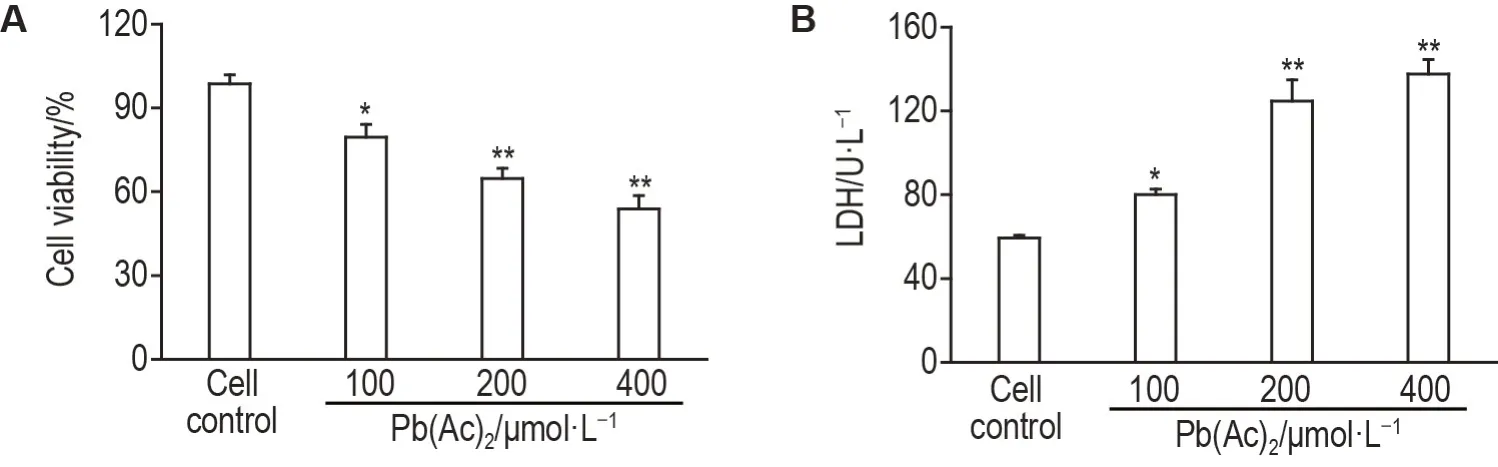
Fig.1 Effect of lead acetate(Pb(Ac)2)on cell viability(A)and lactate dehydrogenase(LDH)content(B)in extracellular fluid of PC12 cells by MTT and colorimetry. After exposure to Pb(Ac)2 0(cell control),100,200 and 400 μmol·L-1 at 37 ℃for 24 h,cell viability and LDH content in extracellular fluid were determined. Cell viability(%)=(1-A490 nm of treatment group/A490 nm of cell control group)×100%.±s,n=5.*P<0.05,**P<0.01,compared with cell control group.
2.2 Pb(Ac)2对PC12细胞凋亡的影响
PC12 细胞经Pb(Ac)2处理24 h 后经AO/EB双染色,凋亡的细胞表现出AO/EB 染色双阳性,荧光叠加后呈现出均匀一致的橙红色圆形;而对照组细胞AO 染色均匀,且几乎无EB 染色阳性,表明无明显凋亡(图2)。
流式检测结果如图3 所示,与细胞对照组相比,Pb(Ac)2100,200 和400 μmol·L-1组细胞凋亡率均显著升高(P<0.01),表明Pb(Ac)2可诱导PC12细胞凋亡。
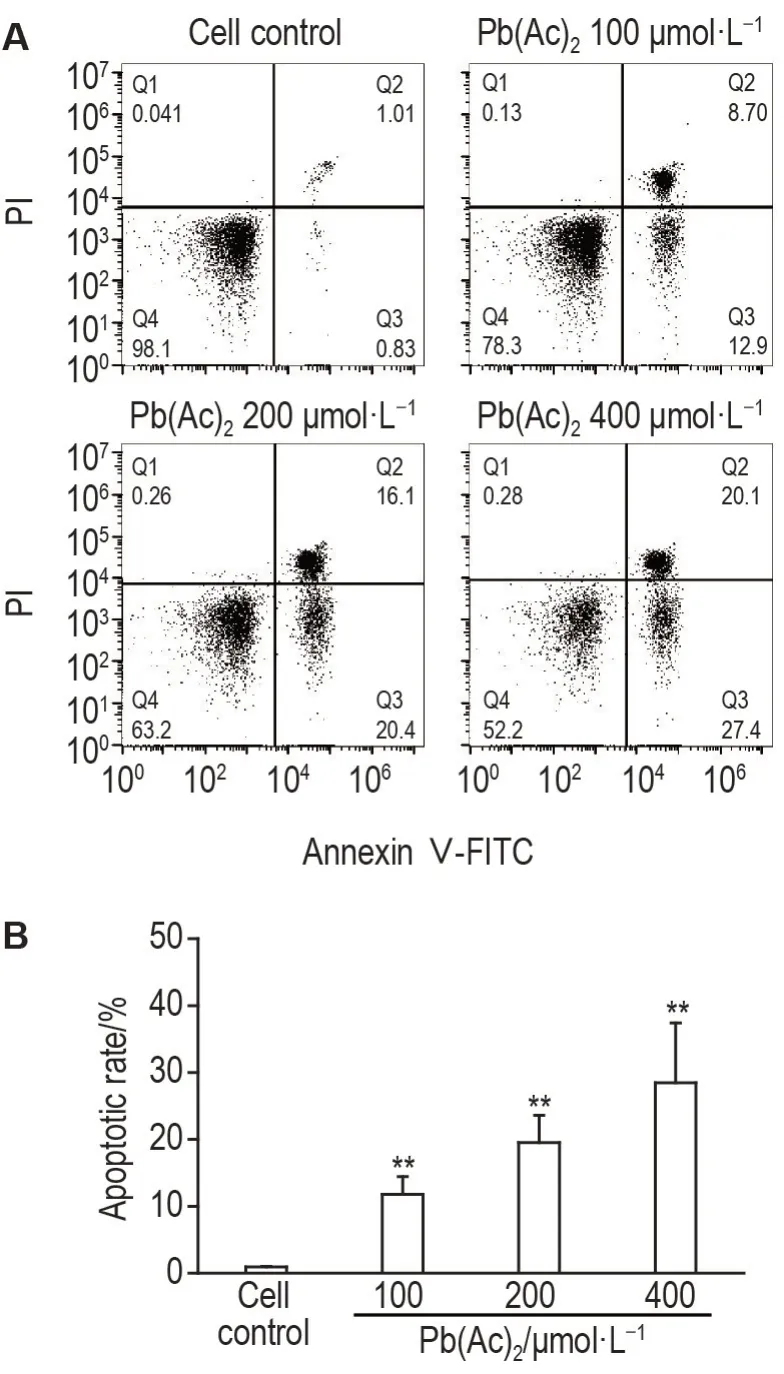
Fig.3 Effect of Pb(Ac)2 on apoptotic rate of PC12 cells detected by flow cytometry. See Fig.1 for the cell treatment. B was the quantitative result of A. ±s,n=3.**P<0.01,compared with cell control group.
2.3 Pb(Ac)2对PC12细胞自噬的影响
如图4A 所示,细胞对照组细胞几乎未见荧光和自噬泡,Pb(Ac)2100 μmol·L-1组细胞内荧光虽弱但自噬泡已开始出现,Pb(Ac)2200 μmol·L-1组MDC点状荧光信号显著增强,Pb(Ac)2400 μmol·L-1组细胞周围呈强烈绿色荧光,提示细胞内出现大量自噬空泡。定量结果(图4B)表明,与细胞对照组相比,Pb(Ac)2各浓度组荧光强度显著增强(P<0.01),表明Pb(Ac)2染毒后PC12细胞自噬增强。
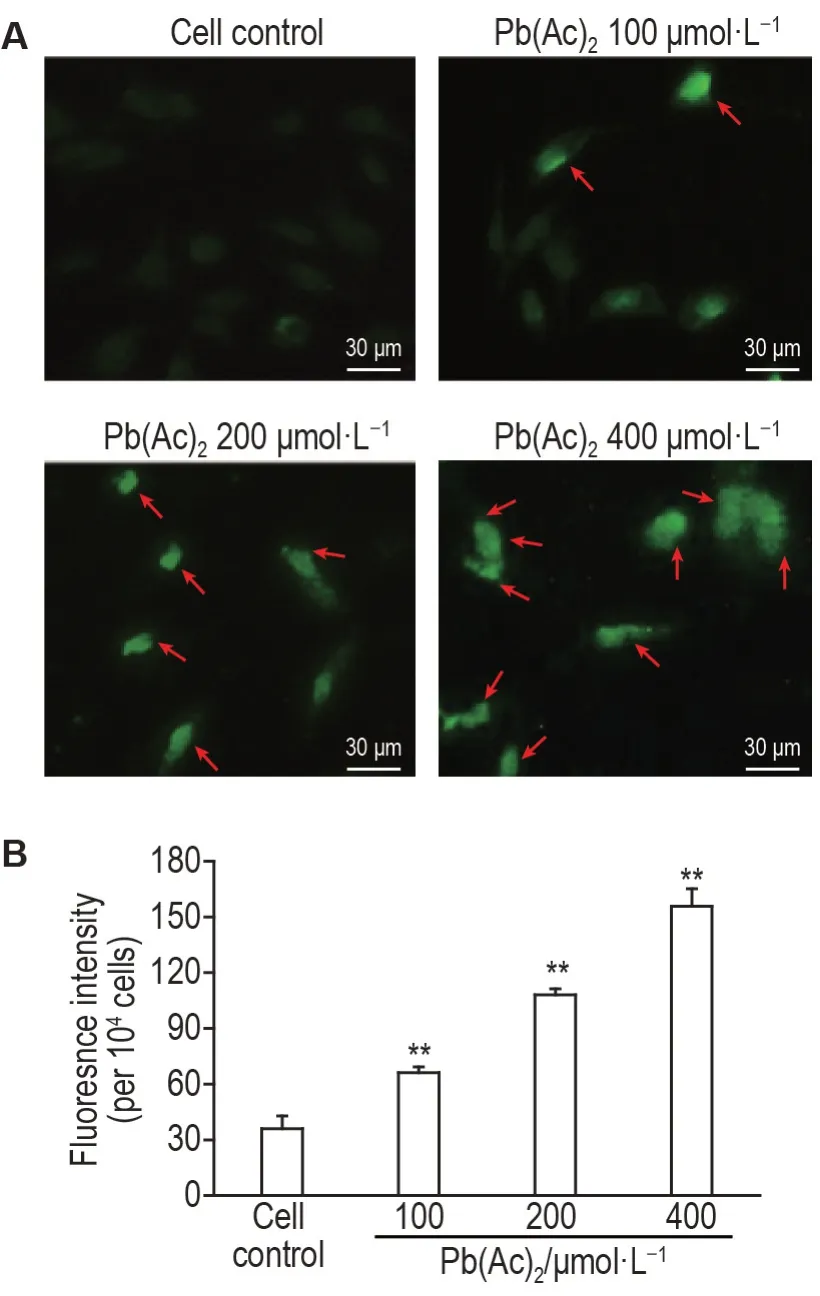
Fig.4 Effect of Pb(Ac)2 on autophagy of PC12 cells determined by monodansylcadaverine staining. See Fig.1 for the cell treatment. B was the quantitative result of A. ±s,n=3. **P<0.01,compared with cell control group. The arrows indicate autophagic bubbles.
2.4 Pb(Ac)2对PC12细胞Beclin1定位的影响
图5所示,细胞对照组Beclin1在细胞质微弱表达,Pb(Ac)2200 μmol·L-1组细胞细胞质中Beclin1表达明显增强,Pb(Ac)2400 μmol·L-1组细胞质内Beclin1 呈现大量点状聚集且荧光强度加强。表明细胞发生了明显自噬,细胞内自噬体数量增多。
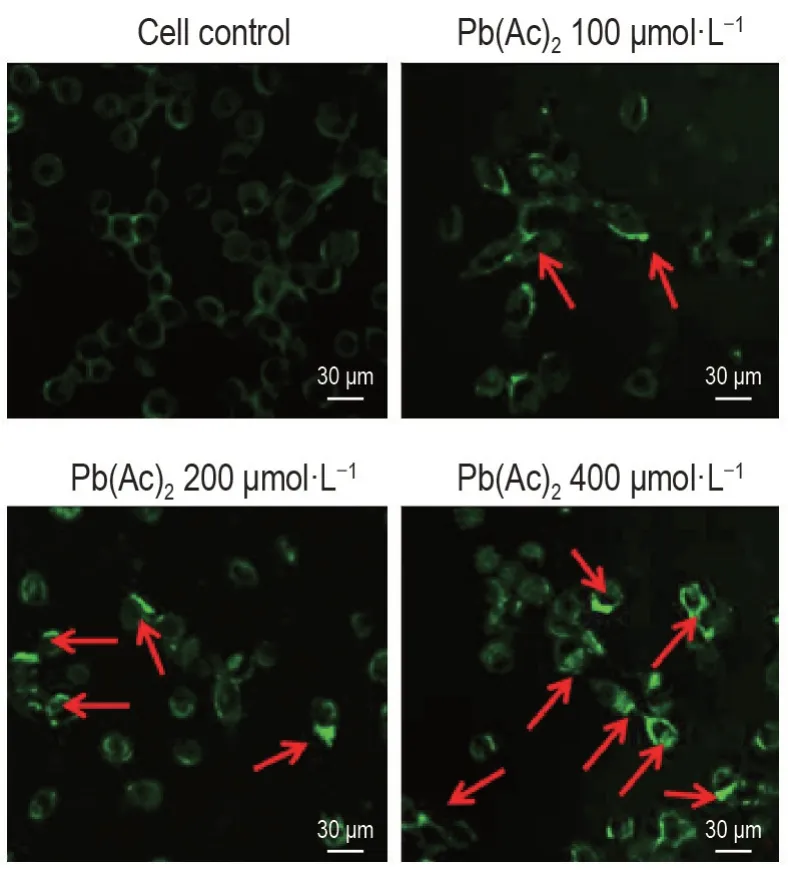
Fig.5 Effect of Pb(Ac)2 on nucleic accumulation of Bcl-2 interacting coiled-coil protein(Beclin1)in the PC12 cells by immunofluorescence. See Fig.1 for the cell treatment. Arrows show the representative Beclin1 accumulation.
2.5 Pb(Ac)2对细胞自噬相关蛋白Sirt1,FoxO3a,FoxM1,Beclin1,LC3和P62表达的影响
Western 印迹法结果(图6)显示,与细胞对照组相比,Pb(Ac)2100,200 和400 μmol·L-1组细胞内Sirt1(P<0.01)和FoxO3a蛋白(P<0.05,P<0.01)表达明显上调,同时自噬相关蛋白Beclin1 蛋白表达(P<0.05,P<0.01)和LC3-Ⅱ/LC3-Ⅰ比值(P<0.01)也明显增加,P62 蛋白表达降低(P<0.05,P<0.01);Pb(Ac)2200 和400 μmol·L-1组细胞FoxM1蛋白表达显著降低(P<0.05,P<0.01)。
3 讨论
本研究采用Pb(Ac)2暴露诱导PC12 细胞损伤模型,发现Pb(Ac)2可显著诱导细胞凋亡,且细胞内自噬程度明显增加,自噬相关蛋白表达显著增多,提示细胞自噬参与了Pb(Ac)2诱导的细胞凋亡过程。
自噬是一种细胞程序性死亡的机制,常由多种应激反应引起。大量研究表明,抑制细胞自噬可减少神经细胞的死亡,反之可促进细胞死亡[9-11]。本研究中,随着Pb(Ac)2浓度的增加,PC12 细胞内自噬泡增多,且Beclin1在PC12 细胞中的荧光强度明显增强,表明Pb(Ac)2促进PC12 细胞发生自噬。Beclin1,LC3 和P62 都是细胞自噬的重要标志物。其中,Beclin1 水平和LC3-Ⅱ/LC3-Ⅰ比值与自噬呈正相关,P62 蛋白表达水平与细胞自噬呈负相关[12-14]。本研究通过Western印记法检测Beclin1,LC3 和P62 蛋白的表达,发现Pb(Ac)2暴露诱导PC12 细胞自噬相关蛋白Beclin1 表达和LC3-Ⅱ/LC3-Ⅰ比值升高,P62蛋白表达降低,进一步证实细胞发生了自噬。
细胞自噬与凋亡之间存在交联,但两者的互作关系尚不明确[15]。有研究发现,抑制新生大鼠神经元自噬后,脑神经元凋亡增加[16];另有研究发现,抑制大鼠海马体中神经元自噬后,大鼠脑损伤及神经元凋亡率明显降低[17],表明细胞自噬与凋亡参与了细胞的死亡过程。本实验室前期研究也发现,用荧光染料Hoechst33342 对Pb(Ac)2处理的PC12 细胞染色后,显微镜下可观察到细胞核明显皱缩且蓝色荧光增强[18],提示细胞出现了凋亡。本研究中,用AO/EB 染色后,随Pb(Ac)2浓度增加,细胞橙色荧光增强,绿色荧光逐渐减弱,表明细胞损伤中发生自噬的同时伴有细胞凋亡,同时,流式细胞检测结果表明,Pb(Ac)2可诱导细胞发生明显凋亡,与之前实验结果相一致。
Sirt1 在调节血管稳态、细胞自噬和凋亡中发挥重要作用[4]。FoxO3a是Sirt1 的下游靶基因,Sirt1可通过去乙酰化调节FoxO3a 的表达,参与调控细胞氧化应激、凋亡和增殖等过程[19]。而FoxM1 是FoxO3a 的下游基因,也是FoxO3a 的直接转录靶点,但关于FoxO3a 和FoxM1 的表达相关性报道不一[20-21]。本研究中,不同浓度Pb(Ac)2作用细胞后,可使细胞内Sirt1 和FoxO3a 蛋白表达明显上调,而FoxM1 表达下调,表明在PC12 细胞损伤的过程中可能有Sirt1/FoxO3a相关信号通路的参与,并存在FoxO3a负向调节下游效应基因FoxM1的可能。
综上所述,本研究发现Pb(Ac)2可显著诱导PC12细胞损伤,且细胞自噬及Sirt1/FoxO3a信号通路可能参与该损伤过程。在后续研究中,将使用自噬抑制剂加以干预,进一步证实细胞凋亡和自噬及Sirt1/FoxO3a信号通路在铅诱导PC12细胞损伤中确切机制。

