双氧水脱硫工艺在铜冶炼烟气制酸中的应用研究
王 宝,白宏伟
(易门铜业有限公司,云南 玉溪 651100)
0 引言
二氧化硫(SO2)属于一种无色气体,有强烈刺激性气味,是大气主要污染物之一。在最近几年里,虽然我国有加强了为其污染方面的治理,并且取得了相应的成果,但是从根本上解决大其污染问题难度较大。随着我国制定一系列环保政策后,大气污染的治理力度也在不断增加,对含硫尾气的治理成为现阶段人们亟需解决的问题。在铜冶炼生产时,由于所燃用的材料中含有大量的硫元素,使得冶炼过程中产生大量高浓度的SO2尾气,在将其排放至空气中后,将会对大气环境造成严重污染[1]。针对此种情况,部分分铜冶炼企业结合自身的情况,纷纷引入先进的技术,不断优化冶炼工艺,以此来降低SO2浓度。因此,对双氧水脱硫工艺在铜冶炼烟气制酸中的研究具有一定的现实意义。
1 工艺简述
某413kt/a 铜冶炼项目主要通过底吹熔池熔炼+转炉吹炼进行铜冶炼,冶炼过程中产生的烟气通过余热回收和电收尘后,通过动力波进行洗涤,并将其制成相应的酸,然后再采用氨酸法脱硫进行脱硫。在非正常的情况下,持续高浓度脱硫会导致排放口存在冒白烟现象,同时产物容易造成设施的堵塞,严重影响SO2去除效率。针对此种情况,该项目采用双氧水脱硫工艺代替氨酸法处理制酸尾气,在一定程度上降低了制酸尾气中的SO2浓度,使其达到ρ(SO2)≤50mg/m3的标准。此外,由于制酸尾气的清洁度得到有效提升,副产物稀硫酸可代替补充水的作用,具有较高的经济价值。
2 双氧水法脱硫原理
双氧水也叫做过氧化氢(H2O2)具有较强的氧化性。对于双氧水脱硫而言,其主要是在脱硫塔中加入一定量的H2O2溶液,通过H2O2溶液与二氧化硫反应,将其转换为氧化为硫酸,使其进入循环液中,将烟气中的二氧化硫分离,进而实现脱硫,其中所涉及的化学反应如下:H2O2+SO2→H2SO。
双氧水脱硫主要是借助过氧化氢强氧化性的特点,将铜冶炼制酸尾气中残余的SO2氧化,并将其循环吸收[2]。从理论上来说,可通过改变过氧化氢的用量来实现不同浓度SO2的脱硫,过氧化氢的用量与脱硫的程度成正相关。在实际脱硫过程中,需严格控制过氧化氢的用量,使其保持在较为稳定的状态,但是由于反应速度相对较快,制酸尾气中硫含量较低,在将过氧化氢的用量增加后,脱硫的效果不明显,在一定程度生增加了脱硫的成本。因此,在制酸尾气脱硫的过程中,需满足以下4 个条件:①SO2吸收率需达到要求。②稀硫酸回收率需高,防止环境受到污染。③在尾气处理过程中不会产生废液、废弃等。④脱硫方法具有一定的经济效益。
3 双氧水脱硫工艺流程
3.1 过程控制
在通过“两转两吸”工艺对烟气进行相应的处理后,将其通入净化塔中,完成烟气的水洗处理。在此过程中,烟气中的大部分烟尘将被洗涤水吸收,确保环境不会受到污染[3]。在洗涤塔中,对烟气的通入温度有一定要求,通常不能超过60~90℃,在洗涤过程中,需定期补充相应的蒸发洗涤液,确保洗涤塔中水分充足,在通常情况下,若系统中水量不足,系统便会自动补水,每次补水量大约为3m3。此外,在洗涤持续较长时间后,烟气中大部分烟尘、杂质将进入洗涤水中,为了避免洗涤效果不受到影响,循环液净化系统需及时更换系统中的洗涤水,每天大约为7~10m3,这样才能有效降低洗涤水中的烟尘与杂质浓度,提升洗涤效果。
在尾气经过相应的洗涤后,将其通入脱硫塔中,此时尾气将与循环液发生化学反应,从而将尾气中的二氧化硫吸收,反应过后的产物硫酸便会进入至循环吸收液中,反应越强烈,循环吸收液中的硫酸浓度越高,在循环吸收液中的硫酸浓度达到30%时,循环罐中少部分吸收液便会进入稀酸罐中,为了确保循环槽中的液为平衡,需过程补水控制,让硫酸塔吸收水分[4]。
3.2 尾气脱硫指标设定
在使用双氧水法脱硫的过程中,需严格控制器运行指标,尾气脱硫指标如表1 所示。

表1 尾气脱硫指标
3.3 系统装置
对于双氧水脱硫系统装置而言,其主要有尾气排放系统、SO2吸收系统、稀酸存贮系统等部分构成,尾气进入吸收塔时,需借助增压风机进行输送。
对于吸收塔而言,其材质主要为玻璃钢,并且在塔身中装有塑料填料,可保证过氧化氢与二氧化硫全面接触。在对二氧化硫氧化后,将氧化过程中产生的稀硫酸输送至制酸系统中,此时便可形成一定浓度的吸收酸[5]。此外,由于过氧化氢需向外采购,为方便存储,在系统中增设了相应的存储罐,并且配套计量泵,确保双氧水在未被氧化的情况下能够持续供应,使脱硫塔中具有充足的过氧化氢含量。双氧水脱硫系统的运行指标如表2 所示。
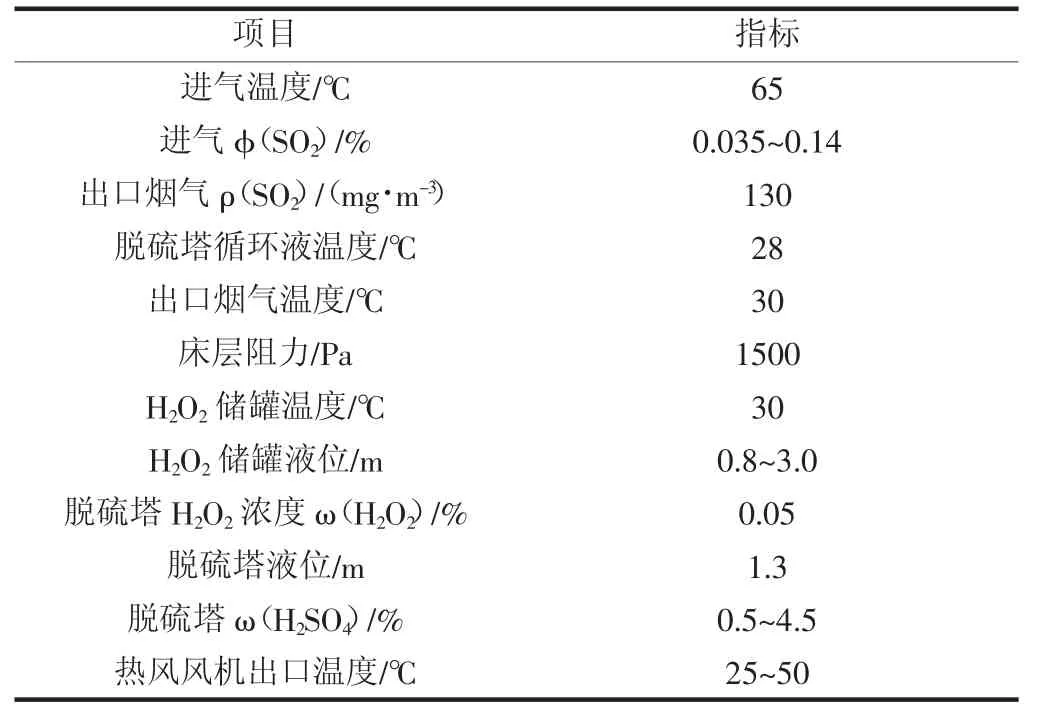
表2 双氧水脱硫系统运行指标
3.4 工艺流程
(1)外购过氧化氢,并将其存储至存储罐中,然后向硫酸塔中通过经过洗涤的铜冶炼制酸尾气,并使其与喷射至塔内的循环液全面接触,进行填料内的氧化反应,SO2经过氧化后产生的硫酸在进入循环液中。
(2)通过存储罐中的计量泵,时刻控制H2O2的浓度,保证吸收率稳定;而副产物稀硫酸则自动加入干吸系统中,并持续加水,使其能够连续吸收,连续排除稀硫酸[6]。对于尾气中的部分二氧化硫而言,其主要是通过脱硫塔上方的除雾装置除去,最后再通过烟囱排放。
(3)通过双氧水泵将双氧水送入循环槽的循环泵中,在生成相应的稀硫酸后,需将其运输至稀硫酸储罐中,然后再将储罐中的稀硫酸输送至配酸系统中。
(4)对于二氧化硫而言,其主要是将硫酸的转化率与尾气的吸收率作为衡量指标。一般来说,酸性转化率与双氧水的吸收率均在99%以上,在过氧化氢将尾气中的二氧化硫吸收后,其尾气中的二氧化硫浓度明显低于排放标准。而硫酸酸雾的含量主要是通过吸收液面的硫酸、三氧化硫以及蒸汽压力来进行衡量,由于硫酸具有较强的氧化性,其表面会产生大量的水蒸气,因此在此过程中不会产生硫酸雾。对于尾气颗粒指数而言,其主要是受到气溶胶影响,由于吸收液属于熔化液,在此过程中并不会产生相应的固体成分。此外,在生产过程中,干吸系统中使用的配酸均为生成的稀硫酸,由于在生产时稀硫酸中杂质被除去,故配酸的质量不会受到影响[7]。
4 双氧水脱硫装置运行情况
4.1 适应制酸系统能力强,脱硫效率高
在413kt/a 铜冶炼项采用双氧水脱硫工艺处理铜冶炼制酸尾气后,尾气的吸收效率较高。实践表明:双氧水脱硫技术在制酸尾气的处理中具有一定的适应性,二氧化硫的排放量达到了排放标准,2021 年脱硫系统的运行数据如表3 所示。

表3 2021 年脱硫系统运行数据
综合来看,该系统的脱硫能力较强,并且具有较高的脱硫效率,脱硫效率可达96.00%~98.00%。
4.2 运行成本低
表4 为双氧水脱硫系统主要技术和经济指标。通过分析该系统装置运行期间的数据得知,ω(H2O2)控制为0.3%~0.5%时,尾气中的二氧化硫浓度达到排放标准。同时,当ω(H2O2)27.5%双氧水消耗量为0.9~1.2kg时,可生产硫酸1t。由此可以看出,此种工艺装置的运行成本较低。
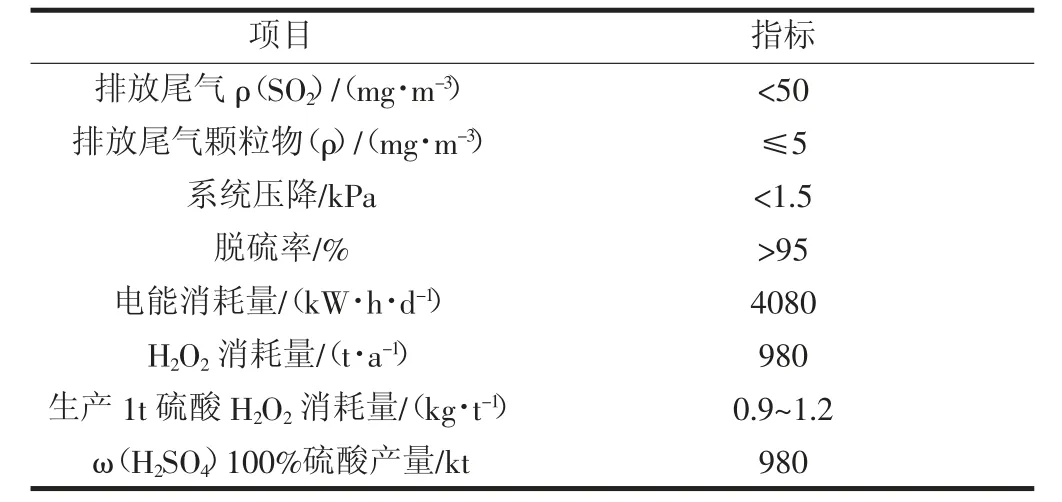
表4 双氧水脱硫系统主要技术和经济指标
4.3 副产品可全部回收再利用
表5 为稀硫酸产品质量数据。通过分析该装置在运行过程中的数据得知,通过双氧水工艺进行脱硫后,可生产ω(H2SO4)为20%~25%的稀硫酸。由于制酸尾气较为清洁,尾吸液产生的稀硫酸可直接将其作为生产补水,不影响成品酸质量,为尾吸双氧水脱硫产生的副产物稀硫酸提供了出路。
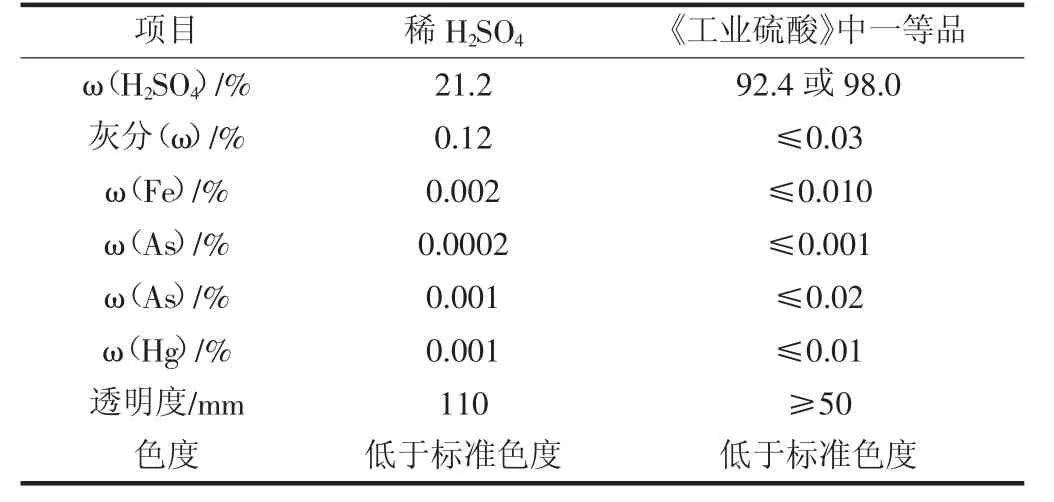
表5 稀硫酸产品质量数据
从表5 中可明确看出,在此种脱硫系统的作用下,除灰分外,Fe、As(0.0002)、As(0.001)、Hg 等杂质的含量、透明度、色度均达到《工业硫酸》(GB/T 534—2014)一等品的标准。
4.4 清洁生产
对于制酸尾气中的二氧化硫浓度而言,其与二氧化硫的转化率、双氧水的吸收率有着直接联系。在实际生产过程中,二转二吸的制酸工艺总转化率均>99%,排放尾气中的二氧化硫含量低于100mg/m3,满足《铜、镍、钴工业污染物排放标准》(GB 25467—2010)要求[8]。
对于酸雾指标而言,其与吸收液表面H2SO4和SO3的饱和蒸汽压有关,由于在生产过程中大部分稀硫酸表面的蒸汽为水蒸气,因此在生产过程中不会产生新酸雾。对于颗粒物指标而言,其与气相是否产生结晶体、气溶胶等有关,由于所使用的吸收液为液体,故生产过程中不会产生相应的固相成分。同时,生产过程中得到的稀硫酸可作为生产补水,在实现资源利用的同时不会对环境造成相应的污染,其清洁度较高。
5 结语
综上所述,双氧水脱硫装置稳定相对较高,排放尾气中的二氧化硫含量低于100mg/m3,在一定程度上满足了《铜、镍、钴工业污染物排放标准》要求。该工艺具备的优点如下。
(1)双氧水脱硫技术在制酸尾气的处理中具有一定的适应性,尾气的排放较为稳定,并且具有吸收率高、生产弹性大、调整及时有效的优点。
(2)工艺简单,运行过程中不会产生较高的成本,并且还具自动化程度高,无须专人操作,安全风险小。
(3)在生产过程中,硫酸与水可以任意比例混合,并且不会出现结晶、堵塞等情况;装置的阻力较小,在一定程度上节省了能耗,经济效益较高。
(4)可实现副产物的回收利用,并且不会对环境造成污染,属于目前较为清洁、先进的脱硫技术。实践表明,双氧水脱硫工艺具有较高的经济价值,对提升环境整体效益有着十分重要的作用。

